Do you worry about what is going to kill you? Heart disease, cancer, a car accident? Most of us worry about things we can't control, like war, terrorism, the tragic earthquake that just occurred in Haiti. But what really threatens humanity? A few years ago, Professor Vaclav Smil tried to calculate the probability of sudden disasters large enough to change history. He called these, "massively fatal discontinuities," meaning that they could kill up to 100 million people in the next 50 years. He looked at the odds of another world war, of a massive volcanic eruption, even of an asteroid hitting the Earth. But he placed the likelihood of one such event above all others at close to 100 percent, and that is a severe flu pandemic. Now, you might think of flu as just a really bad cold, but it can be a death sentence. Every year, 36,000 people in the United States die of seasonal flu. In the developing world, the data is much sketchier but the death toll is almost certainly higher. You know, the problem is if this virus occasionally mutates so dramatically, it essentially is a new virus and then we get a pandemic.
Опасаетесь ли вы того, что может убить вас? Болезней сердца, рака, автомобильной аварии? Большинство из нас опасается того, что не может контролировать, например, войны, терроризма, трагического землетрясения, что только что произошло на Гаити. Но что действительно угрожает человечеству? Несколько лет назад профессор Вацлав Смил пытался вычислить вероятность внезапных бедствий достаточно крупных, чтобы изменить ход истории. Он назвал их "массово фатальными разрывами". Это означает, что они могут убить до 100 млн. человек в ближайшие 50 лет. Он вычислял вероятность новой мировой войны, массивного извержения вулкана, даже столкновения астероида с Землей. Но вероятность одного из таких событий оказалась выше всех – почти 100 процентов, и это событие – жестокая пандемия гриппа. Можно воспринимать грипп просто как сильную простуду, но он может стать смертельным приговором. Каждый год 36 000 человек в Соединенных Штатах умирают от сезонного гриппа. В развивающихся странах точных данных нет, но число погибших почти наверняка выше. Вы знаете, проблема в том, что этот вирус иногда мутирует так сильно, что по сути получается новый вирус. И тогда мы получаем пандемию.
In 1918, a new virus appeared that killed some 50 to 100 million people. It spread like wildfire and some died within hours of developing symptoms. Are we safer today? Well, we seem to have dodged the deadly pandemic this year that most of us feared, but this threat could reappear at any time. The good news is that we're at a moment in time when science, technology, globalization is converging to create an unprecedented possibility: the possibility to make history by preventing infectious diseases that still account for one-fifth of all deaths and countless misery on Earth. We can do this. We're already preventing millions of deaths with existing vaccines, and if we get these to more people, we can certainly save more lives. But with new or better vaccines for malaria, TB, HIV, pneumonia, diarrhea, flu, we could end suffering that has been on the Earth since the beginning of time.
В 1918 году появился новый вирус, который убил от 50 до 100 миллионов человек. Он распространялся как лесной пожар. Некоторые умерли в течение нескольких часов после появления симптомов. Разве сегодня мы в большей безопасности? Ну, в этом году мы, кажется, смогли увернуться от смертельной пандемии, которой многие из нас боялись, но эта угроза может вернуться в любое время. К счастью для нас, в данный момент наука, технологии, глобализация совместно работают, чтобы создать беспрецедентную возможность, возможность войти в историю, предотвратив инфекционные заболевания, которые до сих пор ответственны за одну пятую часть всех смертей и бесчисленных страданий на Земле. Мы можем сделать это. Мы уже предотвращаем миллионы смертей при помощи существующих вакцин. И если мы дадим их большему количеству людей, мы, безусловно, спасём больше жизней. Но с новыми или лучшими вакцинами против малярии, туберкулеза, ВИЧ, пневмонии, диареи, гриппа, мы могли бы положить конец страданиям, которые царили на Земле с начала времён.
So, I'm here to trumpet vaccines for you. But first, I have to explain why they're important because vaccines, the power of them, is really like a whisper. When they work, they can make history, but after a while you can barely hear them. Now, some of us are old enough to have a small, circular scar on our arms from an inoculation we received as children. But when was the last time you worried about smallpox, a disease that killed half a billion people last century and no longer is with us? Or polio? How many of you remember the iron lung? We don't see scenes like this anymore because of vaccines.
Так что я здесь, чтобы возвестить о вакцинах. Но сначала я должен объяснить, почему они важны. Потому что вакцины, их сила подобна шёпоту. Когда они работают, они могут изменить историю, но спустя некоторое время вы едва можете услышать о них. Среди нас есть люди достаточно старые для того, чтобы иметь небольшой круглый шрам на плече от прививки, полученной в детстве. Но когда в последний раз вы опасались оспы, болезни, которая убила полмиллиарда людей в прошлом веке, но которой больше нет? Или полиомиелит – многие ли помнят аппарат искусственного дыхания? Мы с таким больше не сталкиваемся – благодаря вакцинам.
Now, it's interesting because there are 30-odd diseases that can be treated with vaccines now, but we're still threatened by things like HIV and flu. Why is that? Well, here's the dirty little secret. Until recently, we haven't had to know exactly how a vaccine worked. We knew they worked through old-fashioned trial and error. You took a pathogen, you modified it, you injected it into a person or an animal and you saw what happened. This worked well for most pathogens, somewhat well for crafty bugs like flu, but not at all for HIV, for which humans have no natural immunity.
Вы знаете, это интересно, ведь есть 30 с лишним болезней, которые можно лечить с помощью вакцин, но нам по-прежнему угрожают такие вещи, как ВИЧ и грипп. Почему это происходит? Вот вам маленький грязный секрет. До недавнего времени нам не нужно было знать, как именно работает вакцина. Мы проверяли их работу старомодным методом проб и ошибок. Берём патогенный микроорганизм, изменяем его, инъецируем человеку или животному и смотрим, что получится. Это работает для большинства патогенов, иногда для коварных зверей вроде гриппа, но никогда для ВИЧ, против которого у людей нет природного иммунитета.
So let's explore how vaccines work. They basically create a cache of weapons for your immune system which you can deploy when needed. Now, when you get a viral infection, what normally happens is it takes days or weeks for your body to fight back at full strength, and that might be too late. When you're pre-immunized, what happens is you have forces in your body pre-trained to recognize and defeat specific foes. So that's really how vaccines work. Now, let's take a look at a video that we're debuting at TED, for the first time, on how an effective HIV vaccine might work.
Давайте посмотрим, как работают вакцины. Они создают запас вооружения для вашей иммунной системы, который можно задействовать при необходимости. Когда вы получаете вирусную инфекцию, обычно вашему телу нужно несколько дней или недель, чтобы начать сопротивляться в полную силу, а это может быть слишком поздно. Если вы заранее иммунизированы, в вашем теле есть заранее тренированные силы, обученные распознавать и поражать конкретных врагов. Вот как работают вакцины на самом деле. Теперь давайте посмотрим видео, которое мы представляем впервые здесь на TED, о том, какой может быть эффективная вакцина против ВИЧ.
(Music)
(Музыка)
Narrator: A vaccine trains the body in advance how to recognize and neutralize a specific invader. After HIV penetrates the body's mucosal barriers, it infects immune cells to replicate. The invader draws the attention of the immune system's front-line troops. Dendritic cells, or macrophages, capture the virus and display pieces of it. Memory cells generated by the HIV vaccine are activated when they learn HIV is present from the front-line troops. These memory cells immediately deploy the exact weapons needed. Memory B cells turn into plasma cells, which produce wave after wave of the specific antibodies that latch onto HIV to prevent it from infecting cells, while squadrons of killer T cells seek out and destroy cells that are already HIV infected. The virus is defeated. Without a vaccine, these responses would have taken more than a week. By that time, the battle against HIV would already have been lost.
За кадром: вакцина обучает ваше тело заранее, как распознать и обезвредить конкретных захватчиков. После того как ВИЧ проникает через слизистые оболочки, он заражает клетки иммунной системы для репликации. Захватчик привлекает внимание передней линии обороны иммунной системы. Дендритные клетки, или макрофаги, захватывают вирус и отображают его части. Клетки памяти, порождённые вакциной против ВИЧ, активируются, когда они узнают от первой линии обороны, что присутствует ВИЧ. Эти клетки памяти немедленно мобилизуют конкретное необходимое оружие. Клетки памяти Б превращаются в плазматические клетки, которые производят волна за волной специфические антитела, которые захватывают ВИЧ, чтобы он не заражал клетки, а эскадроны Т-клеток-убийц ищут и уничтожают клетки, уже зараженные ВИЧ. Вирус побеждён. Без вакцины такая реакция организма занимает более недели. К тому моменту битва против ВИЧ бывает уже проиграна.
Seth Berkley: Really cool video, isn't it? The antibodies you just saw in this video, in action, are the ones that make most vaccines work. So the real question then is: How do we ensure that your body makes the exact ones that we need to protect against flu and HIV? The principal challenge for both of these viruses is that they're always changing. So let's take a look at the flu virus. In this rendering of the flu virus, these different colored spikes are what it uses to infect you. And also, what the antibodies use is a handle to essentially grab and neutralize the virus. When these mutate, they change their shape, and the antibodies don't know what they're looking at anymore. So that's why every year you can catch a slightly different strain of flu. It's also why in the spring, we have to make a best guess at which three strains are going to prevail the next year, put those into a single vaccine and rush those into production for the fall.
Сет Беркли: Классное видео, правда? Антитела, которые вы видели в этом видео в действии, – те самые, благодаря которым работают вакцины. Настоящий вопрос состоит в следующем: Как мы можем убедиться, что наше тело производит именно те антитела, которые нужны, чтобы защитить от гриппа и ВИЧ? Главной проблемой в обоих этих случаях является то, что они постоянно меняются. Итак, давайте взглянем на вирус гриппа. Вот модель вируса гриппа. Он заражает вас именно с помощью этих разноцветных шипов. Также, именно их используют антитела, чтобы захватить и нейтрализовать вирус. Когда вирус мутирует, они меняют свою форму, и антитела больше не могут узнать того, что они видят. Вот почему каждый год Вы можете подхватить несколько иной штамм гриппа. И именно поэтому весной нам приходится угадывать, какие три штамма будут преобладать в следующем году, затем помещать их в одну вакцину и срочно запускать в производство к осени.
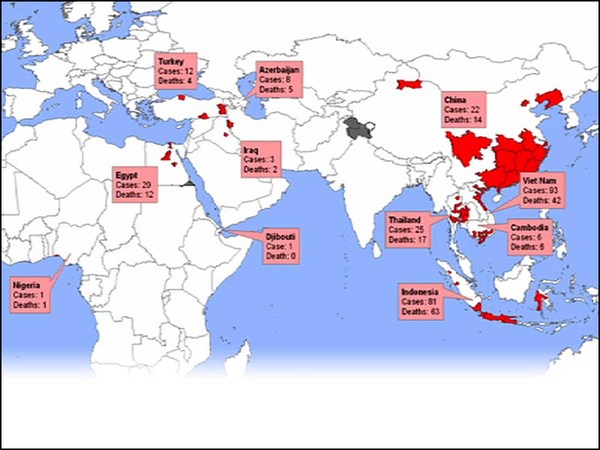
Even worse, the most common influenza -- influenza A -- also infects animals that live in close proximity to humans, and they can recombine in those particular animals. In addition, wild aquatic birds carry all known strains of influenza. So, you've got this situation: In 2003, we had an H5N1 virus that jumped from birds into humans in a few isolated cases with an apparent mortality rate of 70 percent. Now luckily, that particular virus, although very scary at the time, did not transmit from person to person very easily. This year's H1N1 threat was actually a human, avian, swine mixture that arose in Mexico. It was easily transmitted, but, luckily, was pretty mild. And so, in a sense, our luck is holding out, but you know, another wild bird could fly over at anytime.
Что еще хуже, наиболее распространенный грипп типа А также поражает животных, которые живут в непосредственной близости от людей, и они могут рекомбинировать в этих животных. Кроме того, дикие водоплавающие птицы переносят все известные штаммы гриппа. Итак, перед нами проблема. В 2003 году у нас был вирус H5N1, распространявшийся от птиц к людям, в нескольких отдельных случаях с явной смертностью 70 процентов. К счастью, конкретно этот вирус, хотя он и напугал всех в то время, не передавался от человека к человеку так уж легко. В этом году угроза H1N1 – этой смеси от человека, птицы и свиньи, которая появилась в Мексике, легко передавалась. Но, к счастью, он был довольно мягким. Итак, в этом смысле, удача от нас не отвернулась, но знаете, мимо может пролететь другая дикая птица.
Now let's take a look at HIV. As variable as flu is, HIV makes flu look like the Rock of Gibraltar. The virus that causes AIDS is the trickiest pathogen scientists have ever confronted. It mutates furiously, it has decoys to evade the immune system, it attacks the very cells that are trying to fight it and it quickly hides itself in your genome. Here's a slide looking at the genetic variation of flu and comparing that to HIV, a much wilder target. In the video a moment ago, you saw fleets of new viruses launching from infected cells. Now realize that in a recently infected person, there are millions of these ships; each one is just slightly different. Finding a weapon that recognizes and sinks all of them makes the job that much harder.
Теперь давайте посмотрим на ВИЧ. Он такой же изменчивый, как и грипп. Да грипп даже и в подмётки не годится изменчивому ВИЧ. Вирус, который вызывает СПИД, – это наиболее сложный патоген, с которым когда-либо сталкивались учёные. Он яростно мутирует. Он использует приманки, чтобы обойти иммунную систему. Он нападает именно на клетки, которые пытаются бороться с ним. И он быстро скрывается в вашем геноме. Вот слайд, который показывает генетическую изменчивость гриппа в сравнении с ВИЧ, у которого более необузданный характер. В том видео минуту назад вы видели флот новых вирусов, плывущих от инфицированных клеток. Представьте, что в недавно инфицированном человеке есть миллионы таких "судов", каждое из которых чуть-чуть иное. Поиск оружия, которое распознает и потопит их все, делает работу гораздо сложнее.
Now, in the 27 years since HIV was identified as the cause of AIDS, we've developed more drugs to treat HIV than all other viruses put together. These drugs aren't cures, but they represent a huge triumph of science because they take away the automatic death sentence from a diagnosis of HIV, at least for those who can access them. The vaccine effort though is really quite different. Large companies moved away from it because they thought the science was so difficult and vaccines were seen as poor business. Many thought that it was just impossible to make an AIDS vaccine, but today, evidence tells us otherwise.
На данный момент прошло 27 лет с тех пор, как с ВИЧ был признан причиной СПИДа, и мы разработали больше препаратов для лечения ВИЧ, чем для всех других вирусов вместе взятых. Эти препараты не излечивают, но они представляют огромный триумф науки, потому что диагноз ВИЧ-инфекции – это уже не автоматический смертный приговор, по крайней мере, для тех, кто может получить к ним доступ. Попытка вакцинации – это на самом деле совсем другое. Крупные компании отошли от этого, потому что они решили, что там слишком сложная наука, а вакцины не дадут хорошего дохода. Многие думали, что сделать вакцину против СПИДа просто невозможно, но сегодня факты свидетельствуют о противном.
In September, we had surprising but exciting findings from a clinical trial that took place in Thailand. For the first time, we saw an AIDS vaccine work in humans -- albeit, quite modestly -- and that particular vaccine was made almost a decade ago. Newer concepts and early testing now show even greater promise in the best of our animal models. But in the past few months, researchers have also isolated several new broadly neutralizing antibodies from the blood of an HIV infected individual. Now, what does this mean? We saw earlier that HIV is highly variable, that a broad neutralizing antibody latches on and disables multiple variations of the virus. If you take these and you put them in the best of our monkey models, they provide full protection from infection. In addition, these researchers found a new site on HIV where the antibodies can grab onto, and what's so special about this spot is that it changes very little as the virus mutates. It's like, as many times as the virus changes its clothes, it's still wearing the same socks, and now our job is to make sure we get the body to really hate those socks.
В сентябре мы получили удивительные, но захватывающие результаты клинических испытаний, проведённых в Таиланде. Впервые мы увидели работающую вакцину против СПИДа у людей, хотя и слабо работающую. И эта вакцина была сделана почти 10 лет назад. Новые концепты проходят первичные проверки и дают многообещающие результаты на тестовых животных. Но также за последние месяцы исследователи выделили несколько новых антител широкого спектра из крови ВИЧ-инфицированного человека. Итак, что это значит? Мы видели ранее, что ВИЧ очень изменчив, а антитела широкого спектра захватывают и нейтрализуют несколько вариаций вируса. Если вы возьмёте их и поместите в наших тестовых обезьян, вы получите полную защиту от инфекции. Кроме того, эти исследователи обнаружили у ВИЧ новое место, где антитела могут ухватиться. А что особенного в этом месте? А то, что оно почти не меняется, когда вирус мутирует. Вроде того, как если бы вирус постоянно менял свою одежду, но по-прежнему носил те же носки. И теперь наша задача убедиться, что наше тело по-настоящему ненавидит эти носки.
So what we've got is a situation. The Thai results tell us we can make an AIDS vaccine, and the antibody findings tell us how we might do that. This strategy, working backwards from an antibody to create a vaccine candidate, has never been done before in vaccine research. It's called retro-vaccinology, and its implications extend way beyond that of just HIV. So think of it this way. We've got these new antibodies we've identified, and we know that they latch onto many, many variations of the virus. We know that they have to latch onto a specific part, so if we can figure out the precise structure of that part, present that through a vaccine, what we hope is we can prompt your immune system to make these matching antibodies. And that would create a universal HIV vaccine. Now, it sounds easier than it is because the structure actually looks more like this blue antibody diagram attached to its yellow binding site, and as you can imagine, these three-dimensional structures are much harder to work on. And if you guys have ideas to help us solve this, we'd love to hear about it.
Итак, у нас есть задача. Результаты из Таиланда говорят нам, что мы можем сделать вакцину против СПИДа. И исследования антител говорят, что мы можем это сделать. Стратегия разработки в обратном направлении – от антител к созданию вакцины-кандидата – никогда не использовалась раньше в разработке вакцин. Это называется ретро-вакцинология, и её результаты распространяются далеко за пределы ВИЧ-инфекции. Посмотрим на это так. Мы распознали эти новые антитела, и мы знаем, что они захватывают много разных вариаций вируса. Мы знаем, что они должны захватывать конкретную часть, так что, если мы можем определить чёткую структуру этой части, представить её через вакцину, то мы надеемся, что мы сможем подсказать иммунной системе, какие антитела нужно делать. И это создало бы универсальную вакцину против ВИЧ. Это звучит проще, чем оно есть, потому что структура больше похожа на то, как эта синяя диаграмма антитела соединяется с жёлтой точкой захвата. И, как вы можете себе представить, с трёхмерными структурами гораздо труднее работать. И если у вас, ребята, есть идеи, как помочь с этой проблемой, мы хотели бы их услышать.
But, you know, the research that has occurred from HIV now has really helped with innovation with other diseases. So for instance, a biotechnology company has now found broadly neutralizing antibodies to influenza, as well as a new antibody target on the flu virus. They're currently making a cocktail -- an antibody cocktail -- that can be used to treat severe, overwhelming cases of flu. In the longer term, what they can do is use these tools of retro-vaccinology to make a preventive flu vaccine. Now, retro-vaccinology is just one technique within the ambit of so-called rational vaccine design.
Но, вы знаете, исследования, которые производились с ВИЧ, действительно помогли с инновациями и для других заболеваний. Так, например, биотехнологическая компания обнаружила нейтрализующие антитела широкого спектра против гриппа, а также новую точку захвата для антител на вирусе гриппа. Они сейчас готовят коктейль из антител, который можно использовать для лечения тяжелых, неодолимых случаев гриппа. В долгосрочной перспективе они могут использовать эти инструменты ретро-вакцинологии для разработки профилактической вакцины гриппа. Ретро-вакцинология – лишь одна из технологий в пределах так называемой рациональной разработки вакцины.
Let me give you another example. We talked about before the H and N spikes on the surface of the flu virus. Notice these other, smaller protuberances. These are largely hidden from the immune system. Now it turns out that these spots also don't change much when the virus mutates. If you can cripple these with specific antibodies, you could cripple all versions of the flu. So far, animal tests indicate that such a vaccine could prevent severe disease, although you might get a mild case. So if this works in humans, what we're talking about is a universal flu vaccine, one that doesn't need to change every year and would remove the threat of death. We really could think of flu, then, as just a bad cold.
Позвольте дать вам еще один пример. Мы говорили о шипах Н и М на поверхности вируса гриппа. Обратите внимание на другие, более мелкие выступы. Они в основном скрыты от иммунной системы. Теперь оказывается, что эти места также не меняются, когда вирус мутирует. Если вы можете нейтрализовать их специфическими антителами, вы сможете нейтрализовать все версии гриппа. Пока испытания на животных показывают, что такая вакцина может предотвратить тяжелое заболевание либо может свести его к лёгкой форме. Так что, если это работает для людей, то мы сейчас говорим об универсальной вакцине против гриппа, которую не нужно менять каждый год, и которая устранила бы угрозу смерти. Мы действительно сможем думать о гриппе как просто о простуде.
Of course, the best vaccine imaginable is only valuable to the extent we get it to everyone who needs it. So to do that, we have to combine smart vaccine design with smart production methods and, of course, smart delivery methods. So I want you to think back a few months ago. In June, the World Health Organization declared the first global flu pandemic in 41 years. The U.S. government promised 150 million doses of vaccine by October 15th for the flu peak. Vaccines were promised to developing countries. Hundreds of millions of dollars were spent and flowed to accelerating vaccine manufacturing. So what happened?
Конечно, даже самая лучшая вакцина бесполезна, если мы не можем дать её всем нуждающимся. Чтобы сделать это, мы должны объединить умную разработку вакцины с умными методами производства и, конечно, умными методами доставки. Прошу вас вспомнить, что было несколько месяцев назад. В июне Всемирная Организация Здравоохранения объявила о первой глобальной пандемии гриппа за последний 41 год. Правительство США обещало 150 миллионов доз вакцины к 15 октября, к пику гриппа. Вакцины были обещаны для развивающихся стран. Сотни миллионов долларов были потрачены на ускоренное производство вакцины. И что же случилось?
Well, we first figured out how to make flu vaccines, how to produce them, in the early 1940s. It was a slow, cumbersome process that depended on chicken eggs, millions of living chicken eggs. Viruses only grow in living things, and so it turned out that, for flu, chicken eggs worked really well. For most strains, you could get one to two doses of vaccine per egg. Luckily for us, we live in an era of breathtaking biomedical advances. So today, we get our flu vaccines from ... chicken eggs, (Laughter) hundreds of millions of chicken eggs. Almost nothing has changed. The system is reliable but the problem is you never know how well a strain is going to grow. This year's swine flu strain grew very poorly in early production: basically .6 doses per egg. So, here's an alarming thought. What if that wild bird flies by again? You could see an avian strain that would infect the poultry flocks, and then we would have no eggs for our vaccines. So, Dan [Barber], if you want billions of chicken pellets for your fish farm, I know where to get them. So right now, the world can produce about 350 million doses of flu vaccine for the three strains, and we can up that to about 1.2 billion doses if we want to target a single variant like swine flu. But this assumes that our factories are humming because, in 2004, the U.S. supply was cut in half by contamination at one single plant. And the process still takes more than half a year.
Впервые мы узнали, как делать вакцины против гриппа, как производить их, в начале 1940-х. Это был медленный, трудоемкий процесс, зависящий от куриных яиц, миллионов живых куриных яиц. Вирусы растут только в живых существах, и так оказалось, что для гриппа куриные яйца хорошо подходили. Для большинства штаммов можно получить одну-две дозы вакцины на яйцо. К счастью для нас, мы живем в эпоху захватывающих биомедицинских достижений. Так что сегодня мы получаем вакцину против гриппа... ...из куриных яиц. (Смех в зале) Сотни миллионов куриных яиц. Вы знаете, почти ничего не изменилось. Вы знаете, что система надежна. Но проблема в том, что вы никогда не знаете, насколько хорошо будет расти штамм. Штамм свиного гриппа в этом году рос очень плохо в начале производства, около 0,6 дозы на яйцо. Вот она, тревожная мысль. Что делать, если дикие птицы пролетят снова? Вы могли видеть, что птичий штамм мог бы заразить домашних птиц, и тогда у нас не было бы яиц для наших вакцин. Так, Дэн Барбер [известный владелец ресторанов], если вам нужны миллиарды куриных гранул для рыбного хозяйства, я знаю, где их достать. Прямо сейчас мир может произвести около 350 миллионов доз вакцины от гриппа для трех штаммов. И мы можем поднять производство до 1,2 миллиарда доз, если используем лишь один целевой вариант, вроде свиного гриппа. Но это возможно, если заводы будут работать в полную силу, потому что в 2004 году поставка из США была сокращена вдвое из-за загрязнения на одном из заводов. И процесс по-прежнему занимает более полугода.
So are we better prepared than we were in 1918? Well, with the new technologies emerging now, I hope we can say definitively, "Yes." Imagine we could produce enough flu vaccine for everyone in the entire world for less than half of what we're currently spending now in the United States. With a range of new technologies, we could. Here's an example: A company I'm engaged with has found a specific piece of the H spike of flu that sparks the immune system. If you lop this off and attach it to the tail of a different bacterium, which creates a vigorous immune response, they've created a very powerful flu fighter. This vaccine is so small it can be grown in a common bacteria, E. coli. Now, as you know, bacteria reproduce quickly -- it's like making yogurt -- and so we could produce enough swine origin flu for the entire world in a few factories, in a few weeks, with no eggs, for a fraction of the cost of current methods.
Неужели мы лучше подготовлены, чем были в 1918 году? Ну, с последними новыми технологиями, я надеюсь, мы окончательно можем сказать "да". Представьте, если бы мы могли произвести достаточно вакцины против гриппа для всех в мире менее чем за половину денег, которые мы расходуем сейчас в Соединенных Штатах. Это возможно с рядом новых технологий. Вот вам пример. Компания, где я работаю, обнаружила специфическую часть шипа H гриппа, запускающую иммунную систему. Если вы отрежете его и приделаете к хвосту различных бактерий, которые дают мощный отклик иммунной системы, они создадут очень мощного борца против гриппа. Такая вакцина настолько мала, что её можно вырастить в обычной бактерии вроде кишечной палочки. Как вы знаете, бактерии размножаются быстро. Это как приготовить йогурт. Так мы могли бы производить достаточно гриппа свиного происхождения для всего мира на нескольких заводах за несколько недель без яиц лишь за часть стоимости существующих методов.
(Applause)
(Аплодисменты)
So here's a comparison of several of these new vaccine technologies. And, aside from the radically increased production and huge cost savings -- for example, the E. coli method I just talked about -- look at the time saved: this would be lives saved. The developing world, mostly left out of the current response, sees the potential of these alternate technologies and they're leapfrogging the West. India, Mexico and others are already making experimental flu vaccines, and they may be the first place we see these vaccines in use. Because these technologies are so efficient and relatively cheap, billions of people can have access to lifesaving vaccines if we can figure out how to deliver them.
Вот сравнение некоторых из этих новых технологий вакцинации. И, помимо радикального увеличения производства и огромной экономии средств, например, метод с кишечной палочкой, который я упоминал, посмотрите, сколько сэкономлено времени – это будут спасённые жизни. Развивающиеся страны в основном не следуют текущей моде и видят потенциал этих альтернативных технологий, и они опережают Запад. Индия, Мексика и другие уже создают экспериментальные вакцины против гриппа, и они могут выйти на первое место среди стран, где используют такие вакцины. Эти технологии настолько эффективны и относительно недороги, что спасительными вакцинами можно обеспечить миллиарды людей, если мы сможем придумать, как доставить их.
Now think of where this leads us. New infectious diseases appear or reappear every few years. Some day, perhaps soon, we'll have a virus that is going to threaten all of us. Will we be quick enough to react before millions die? Luckily, this year's flu was relatively mild. I say, "luckily" in part because virtually no one in the developing world was vaccinated. So if we have the political and financial foresight to sustain our investments, we will master these and new tools of vaccinology, and with these tools we can produce enough vaccine for everyone at low cost and ensure healthy productive lives. No longer must flu have to kill half a million people a year. No longer does AIDS need to kill two million a year. No longer do the poor and vulnerable need to be threatened by infectious diseases, or indeed, anybody. Instead of having Vaclav Smil's "massively fatal discontinuity" of life, we can ensure the continuity of life. What the world needs now are these new vaccines, and we can make it happen.
Подумайте, куда это нас приведёт. Каждые несколько лет появляются новые инфекционные болезни или заново проявляются старые. Когда-нибудь, возможно, очень скоро мы столкнёмся с вирусом, который будет угрожать всем нам. Сможем ли мы достаточно быстро отреагировать до того, как умрут миллионы? К счастью, грипп в этом году был относительно мягким. Я говорю "к счастью" лишь частично, потому что в развивающихся странах практически никто не был вакцинирован. Так что если у нас есть политическая и финансовая дальновидность для сохранения наших инвестиций, мы овладеем этими и другими инструментами вакцинологии. И с помощью этих инструментов мы можем произвести достаточно вакцины для всех при низкой себестоимости и обеспечить здоровую продуктивную жизнь людей. Хватит позволять гриппу убивать полмиллиона человек в год. Хватит позволять СПИДу убивать два миллиона в год. Хватить подвергать неимущих и восприимчивых угрозе инфекционных заболеваний, да, собственно, не только их, а всех. Вместо "массово фатального разрыва" жизни Вацлава Смила мы можем обеспечить непрерывность жизни. Сейчас мир нуждается именно в этих новых вакцинах, и мы можем дать их ему.
Thank you very much.
Большое спасибо.
(Applause)
(Аплодисменты)
Chris Anderson: Thank you. (Applause) Thank you. So, the science is changing. In your mind, Seth -- I mean, you must dream about this -- what is the kind of time scale on, let's start with HIV, for a game-changing vaccine that's actually out there and usable?
Крис Андерсон: Спасибо. (Аплодисменты) Спасибо. Итак, наука меняется. Как ты думаешь, Сет... – в смысле, ты, наверно мечтаешь об этом... в какие приблизительно сроки – давайте начнем с ВИЧ, – можно разработать и использовать вакцину, которая изменит ход игры?
SB: The game change can come at any time, because the problem we have now is we've shown we can get a vaccine to work in humans; we just need a better one. And with these types of antibodies, we know humans can make them. So, if we can figure out how to do that, then we have the vaccine, and what's interesting is there already is some evidence that we're beginning to crack that problem. So, the challenge is full speed ahead.
СБ: Игра может измениться в любой момент, потому что сейчас проблема как раз в том, что мы уже показали, что вакцина может работать для людей, нам просто нужна вакцина получше. Мы уже знаем, что люди могут вырабатывать эти типы антител. Поэтому, если мы можем понять, как это сделать, то мы получим вакцину. И что интересно, уже есть некоторые признаки того, что мы близки к решению проблемы. То есть сейчас главное – не останавливаться.
CA: In your gut, do you think it's probably going to be at least another five years?
КА: Как ты чувствуешь, вероятно, придётся ждать ещё минимум лет пять?
SB: You know, everybody says it's 10 years, but it's been 10 years every 10 years. So I hate to put a timeline on scientific innovation, but the investments that have occurred are now paying dividends.
СБ: Знаешь, все говорят, что лет десять, но каждые 10 лет все говорят, что ещё лет 10. Так что я очень не хочу указывать сроки для научных разработок, но сделанные инвестиции уже сейчас дают дивиденды.
CA: And that's the same with universal flu vaccine, the same kind of thing?
КА: А что насчёт универсальной вакцины против гриппа – то же самое?
SB: I think flu is different. I think what happened with flu is we've got a bunch -- I just showed some of this -- a bunch of really cool and useful technologies that are ready to go now. They look good. The problem has been that, what we did is we invested in traditional technologies because that's what we were comfortable with. You also can use adjuvants, which are chemicals you mix. That's what Europe is doing, so we could have diluted out our supply of flu and made more available, but, going back to what Michael Specter said, the anti-vaccine crowd didn't really want that to happen.
СБ: Я думаю, с гриппом по-другому. Я думаю, как раз с гриппом у нас есть куча – я уже показал некоторые из них – куча действительно хороших и полезных технологий, которые готовы работать. Они выглядят неплохо. Проблема в том, что мы инвестировали именно в традиционные технологии, потому что это привычнее. Также можно использовать вспомогательные химикаты, которые вы подмешиваете. Именно это делают в Европе, так что мы могли бы разбавить наши запасы против гриппа и сделать их более доступными, Но, возвращаясь к тому, что заявил Майкл Спектер, толпа антивакцинистов действительно не хотела этого.
CA: And malaria's even further behind?
КА: А с малярией отставание ещё больше?
SB: No, malaria, there is a candidate that actually showed efficacy in an earlier trial and is currently in phase three trials now. It probably isn't the perfect vaccine, but it's moving along.
СБ.: Нет, для малярии есть кандидат, уже показавший эффективность в процессе испытаний, и в настоящее время проходящий третий этап испытаний. Вероятно, это не идеальная вакцина, но прогресс есть.
CA: Seth, most of us do work where every month, we produce something; we get that kind of gratification. You've been slaving away at this for more than a decade, and I salute you and your colleagues for what you do. The world needs people like you. Thank you.
КА: Сет, большинство из нас работают над чем-то таким, знаешь, мы производим что-то каждый месяц и получаем от этого удовольствие. А ты, как раб, работаешь над проблемой более 10 лет, и я преклоняюсь перед тобой и твоими коллегами за то, что вы делаете. Миру нужны такие люди, как вы. Спасибо.
SB: Thank you.
СБ: Спасибо.
(Applause)
(Аплодисменты)