Do you worry about what is going to kill you? Heart disease, cancer, a car accident? Most of us worry about things we can't control, like war, terrorism, the tragic earthquake that just occurred in Haiti. But what really threatens humanity? A few years ago, Professor Vaclav Smil tried to calculate the probability of sudden disasters large enough to change history. He called these, "massively fatal discontinuities," meaning that they could kill up to 100 million people in the next 50 years. He looked at the odds of another world war, of a massive volcanic eruption, even of an asteroid hitting the Earth. But he placed the likelihood of one such event above all others at close to 100 percent, and that is a severe flu pandemic. Now, you might think of flu as just a really bad cold, but it can be a death sentence. Every year, 36,000 people in the United States die of seasonal flu. In the developing world, the data is much sketchier but the death toll is almost certainly higher. You know, the problem is if this virus occasionally mutates so dramatically, it essentially is a new virus and then we get a pandemic.
Vă faceți griji de ce v-ar putea ucide? Boli cardiace, cancer, accident de mașină? Mulți ne îngrijorăm de lucruri ce nu le putem controla: război, terorism, tragicul cutremur ce tocmai a avut loc in Haiti. Însă ce anume amenință cu adevărat umanitatea? Acum câțiva ani, profesorul Vaclav Smil a încercat să calculeze probabilitatea unor dezastre neprevăzute suficient de mari să schimbe istoria. Le-a numit 'discontinuități fatale masive' însemnând că ar putea ucide până la 100 milioane de persoane în următorii 50 de ani. A calculat probabilitatea unui alt război mondial, unei erupții vulcanice masive, chiar impactul unui asteroid cu Pământul. Dar a plasat probabilitatea unui anume eveniment, desupra tuturor celorlalte, la aproape 100% : o epidemie de gripă severă. Poate considerați gripa doar o răceală neplăcută. Dar poate fi o sentiță la moarte. În fiecare an, 36.000 de oameni din SUA mor de gripă sezonieră. Țările în curs de dezvoltare au date sumare, însă numărul deceselor e aproape sigur mai mare. Problema e că dacă virusul suferă ocazional mutații radicale, devine practic un nou virus. Așa se declanșează o pandemie.
In 1918, a new virus appeared that killed some 50 to 100 million people. It spread like wildfire and some died within hours of developing symptoms. Are we safer today? Well, we seem to have dodged the deadly pandemic this year that most of us feared, but this threat could reappear at any time. The good news is that we're at a moment in time when science, technology, globalization is converging to create an unprecedented possibility: the possibility to make history by preventing infectious diseases that still account for one-fifth of all deaths and countless misery on Earth. We can do this. We're already preventing millions of deaths with existing vaccines, and if we get these to more people, we can certainly save more lives. But with new or better vaccines for malaria, TB, HIV, pneumonia, diarrhea, flu, we could end suffering that has been on the Earth since the beginning of time.
În 1918 a apărut un nou virus care a ucis între 50-100 millioane de oameni. S-a răspândit ca fulgerul. Unii au murit la câteva ore de la manifestarea simptomelor. Suntem mai în siguranță în prezent? Ei bine, se pare că am scăpat, de pandemia mortală anul acesta, de care mulți ne-am temut, dar amenințarea ar putea să reapară oricând. Veste bună este că trăim vremuri în care știința, tehnologia, globalizarea converg spre crearea unei situații fără precedent, posibilitatea de a rămâne în istorie prin prevenirea bolilor infecțioase care încă revendică o cincime din decese și imensă suferință pe Pământ. Posibil să reușim. Deja prevenim milioane de decese cu vaccinurile existente, Și dacă le distribuim mai multor oameni, cu siguranță putem salva mai multe vieți. Dar cu vaccinuri noi sau mai bune pentru malarie, tuberculoză, HIV, pneumonie, diaree, gripă am putea pune capăt unor suferințe care au existat pe Pământ de la începutul timpurilor.
So, I'm here to trumpet vaccines for you. But first, I have to explain why they're important because vaccines, the power of them, is really like a whisper. When they work, they can make history, but after a while you can barely hear them. Now, some of us are old enough to have a small, circular scar on our arms from an inoculation we received as children. But when was the last time you worried about smallpox, a disease that killed half a billion people last century and no longer is with us? Or polio? How many of you remember the iron lung? We don't see scenes like this anymore because of vaccines.
Așadar, sunt aici să pledez în favoarea vaccinurilor. Dar întâi, trebuie să explic de ce sunt importante. Deoarece vaccinurile, puterea lor e ca o șoaptă. Când își fac efectul pot intra în istorie, dar după un timp, de abia le mai auzi. Unii din noi suntem suficient de în vârstă să avem o cicatrice mică circulară pe braț, de la un vaccin primit în copilărie. Când v-ați făcut ultima oară griji de variolă -- boală care a ucis ½ miliard de oameni secolul trecut, care acum nu mai există? Sau poliomielita – câți vă amintiți de 'plămânul de fier'? Nu mai vedem asemenea scenarii mulțumită vaccinurilor.
Now, it's interesting because there are 30-odd diseases that can be treated with vaccines now, but we're still threatened by things like HIV and flu. Why is that? Well, here's the dirty little secret. Until recently, we haven't had to know exactly how a vaccine worked. We knew they worked through old-fashioned trial and error. You took a pathogen, you modified it, you injected it into a person or an animal and you saw what happened. This worked well for most pathogens, somewhat well for crafty bugs like flu, but not at all for HIV, for which humans have no natural immunity.
Totuși e interesant pentru că sunt 30 de boli ciudate care pot fi prevenite prin vaccinare acum, dar încă suntem amenințați de afecțiuni ca HIV și gripă. De ce oare? Iată micul secret. Până nu demult, nu trebuia să știm exact cum fucționează un vaccin. Știam că se aplica tradiționala eliminare succesivă. Se alegea un agent patogen, se modifica, se injecta într-o persoană sau un animal, și vedeai ce se întâmplă. A fucționat bine pentru majoritatea patogenilor, binișor pentru gripa amăgitoare, dar deloc pentru HIV, pentru care oamenii nu au imunitate naturală.
So let's explore how vaccines work. They basically create a cache of weapons for your immune system which you can deploy when needed. Now, when you get a viral infection, what normally happens is it takes days or weeks for your body to fight back at full strength, and that might be too late. When you're pre-immunized, what happens is you have forces in your body pre-trained to recognize and defeat specific foes. So that's really how vaccines work. Now, let's take a look at a video that we're debuting at TED, for the first time, on how an effective HIV vaccine might work.
Deci să analizăm cum funcționează vaccinurile. Practic, ele creeză un depozit de arme pentru sistemul imunitar care pot fi lansate la nevoie. Când contactați o infecție virală, normal îi trebuie zile sau săptămâni organismului pentru a contraataca cu toată puterea, și asta ar putea fi prea târziu. Dacă sunteți pre-imunizați organismul dispune de forțe pre-instruite pentru a recunoaște și învinge anumiți agenți patogeni. Cam așa funcționează vaccinurile. Acum, să ne uităm la un video, prezentat la TED în premieră, despre cum funcționează un vaccin HIV eficient.
(Music)
(Muzică)
Narrator: A vaccine trains the body in advance how to recognize and neutralize a specific invader. After HIV penetrates the body's mucosal barriers, it infects immune cells to replicate. The invader draws the attention of the immune system's front-line troops. Dendritic cells, or macrophages, capture the virus and display pieces of it. Memory cells generated by the HIV vaccine are activated when they learn HIV is present from the front-line troops. These memory cells immediately deploy the exact weapons needed. Memory B cells turn into plasma cells, which produce wave after wave of the specific antibodies that latch onto HIV to prevent it from infecting cells, while squadrons of killer T cells seek out and destroy cells that are already HIV infected. The virus is defeated. Without a vaccine, these responses would have taken more than a week. By that time, the battle against HIV would already have been lost.
Narator: Un vaccin instruiește corpul anticipat să recunoască și să neutralizeze un anume invadator. După ce virusul HIV penetrează membrana mucoasă, infectează celulele imune pentru a se înmulți. Invadatorul atrage atenția agenților din prima linie de apărare a sistemului imunitar. Celulele dendritice, sau macrofage, capturează virusul și expun bucăți din el. Celulele de memorie generate de vaccinul HIV sunt activate când află că HIV e prezent de la agenții din prima linie . Aceste celule de memorie lansează imediat armele necesare. Celulele de memorie B se transformă in celule plasmatice, care produc val după val anticorpi specifici care anihilează virusul HIV, împiedicându-l să infecteze alte celule, în timp ce batalioane de celule T ucigașe vânează și distrug celulele care sunt deja infectate cu HIV. Virusul este învins. Fără vaccin, aceste reacții ar fi luat mai mult de o săptămână. Până atunci, lupta împotriva virusului ar fi fost deja pierdută.
Seth Berkley: Really cool video, isn't it? The antibodies you just saw in this video, in action, are the ones that make most vaccines work. So the real question then is: How do we ensure that your body makes the exact ones that we need to protect against flu and HIV? The principal challenge for both of these viruses is that they're always changing. So let's take a look at the flu virus. In this rendering of the flu virus, these different colored spikes are what it uses to infect you. And also, what the antibodies use is a handle to essentially grab and neutralize the virus. When these mutate, they change their shape, and the antibodies don't know what they're looking at anymore. So that's why every year you can catch a slightly different strain of flu. It's also why in the spring, we have to make a best guess at which three strains are going to prevail the next year, put those into a single vaccine and rush those into production for the fall.
Seth Berkley: Grozav video-clip, nu-i așa? Anticorpii pe care i-ați văzut în acest video în acțiune sunt cei care fac majoritatea vaccinurilor să funcționeze. Așadar, adevărata întrebarea este: Cum ne asigurăm că organismul nostru produce exact acei anticorpi de care avem nevoie pentru protecția împotriva gripei și a virusului HIV? Principala provocare e că ambele virusuri sunt mereu în schimbare. Să ne uitam la virusul gripal. În această reprezentare a virusului gripal, vârfurile colorate diferit sunt folosite pentru a vă infecta. Anticorpii folosesc o agăţătoare, pentru a prinde și neutraliza virusul. Când aceștia suferă mutații, își schimbă forma, iar anticorpii nu-i mai recunosc. De aceea, în fiecare an, puteți contracta alt tip de gripă. Acesta e motivul pentru care primăvara trebuie să estimăm care trei tipuri vor predomina anul următor, să le combatem cu un singur vaccin și să le grăbim producția pentru toamnă.
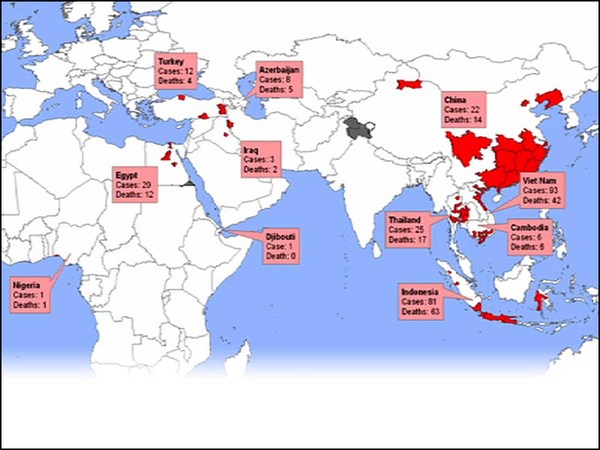
Even worse, the most common influenza -- influenza A -- also infects animals that live in close proximity to humans, and they can recombine in those particular animals. In addition, wild aquatic birds carry all known strains of influenza. So, you've got this situation: In 2003, we had an H5N1 virus that jumped from birds into humans in a few isolated cases with an apparent mortality rate of 70 percent. Now luckily, that particular virus, although very scary at the time, did not transmit from person to person very easily. This year's H1N1 threat was actually a human, avian, swine mixture that arose in Mexico. It was easily transmitted, but, luckily, was pretty mild. And so, in a sense, our luck is holding out, but you know, another wild bird could fly over at anytime.
Mai rău, cea mai obișnuită gripă, gripa A, afectează și animalele, care trăiesc în imediată proximitate cu oamenii, și se pot recombina în aceste animale. În plus, păsările acvatice sălbatice poartă toate tipurile cunoscute de gripă. Deci am avut următoarea situație. În 2003, virusul H5N1 s-a transferat de la păsări la oameni în câteva cazuri izolate, cu o rată aparentă a mortalității de 70%. Din fericire, acest virus, deși foarte îngrijorător la acel moment, nu se transmitea de la persoana la persoană foarte ușor. Anul acesta, virusul H1N1 a fost un mix uman, aviar și porcin care a apărut în Mexic. Se transmitea ușor, dar, din fericire, era destul de blând. Şi într-un fel, am avut iar noroc, însă o altă pasăre sălbatică ar putea apărea, în orice moment.
Now let's take a look at HIV. As variable as flu is, HIV makes flu look like the Rock of Gibraltar. The virus that causes AIDS is the trickiest pathogen scientists have ever confronted. It mutates furiously, it has decoys to evade the immune system, it attacks the very cells that are trying to fight it and it quickly hides itself in your genome. Here's a slide looking at the genetic variation of flu and comparing that to HIV, a much wilder target. In the video a moment ago, you saw fleets of new viruses launching from infected cells. Now realize that in a recently infected person, there are millions of these ships; each one is just slightly different. Finding a weapon that recognizes and sinks all of them makes the job that much harder.
Hadeți să ne uităm acum la virusul HIV. Deși gripa e variabilă, HIV face gripa să pară invariabilă ca Roca Gibraltarului. Virusul care cauzează SIDA e cel mai viclean patogen cu care biologii s-au confruntat vreodată. Suferă mutații profuze. Are subterfugii de a evita sistemul imunitar. Atacă exact celulele care încearcă să lupte împotriva lui. Apoi se ascunde rapid în genom. Această reprezentare compară variația genetică a virusului gripal cu cea a virusului HIV, o țintă mai sălbatică. În video-clipul precedent, aţi văzut flote de viruși noi ieșind din celule infectate. Acum imaginaţi-vă că într-o persoană recent infectată sunt milioanele de astfel de 'nave', fiecare ușor diferită de celelalte. Găsirea unei arme care să recunoască și să le scufunde pe toate devine o sarcină destul de dificilă.
Now, in the 27 years since HIV was identified as the cause of AIDS, we've developed more drugs to treat HIV than all other viruses put together. These drugs aren't cures, but they represent a huge triumph of science because they take away the automatic death sentence from a diagnosis of HIV, at least for those who can access them. The vaccine effort though is really quite different. Large companies moved away from it because they thought the science was so difficult and vaccines were seen as poor business. Many thought that it was just impossible to make an AIDS vaccine, but today, evidence tells us otherwise.
Acum, la 27 de ani de când HIV a fost identificat drept cauza SIDA, dispunem de mai multe medicamente care pot trata HIV decât pentru toate celelalte virusuri laolaltă. Aceste medicamente nu vindecă însă reprezintă un triumf al științei deoarece elimină sentința automată de moarte a diagnosticului HIV, cel puțin pentru cei care au acces la medicamente. Eforturile pentru găsirea unui vaccin sunt destul de diferite. Companiile mari s-au retras, deoarece au considerat cercetarea dificilă, iar vaccinurile erau percepute ca o afacere slabă. Mulți au crezut imposibilă crearea unui vaccin anti-SIDA, însă astăzi experiența ne spune altceva.
In September, we had surprising but exciting findings from a clinical trial that took place in Thailand. For the first time, we saw an AIDS vaccine work in humans -- albeit, quite modestly -- and that particular vaccine was made almost a decade ago. Newer concepts and early testing now show even greater promise in the best of our animal models. But in the past few months, researchers have also isolated several new broadly neutralizing antibodies from the blood of an HIV infected individual. Now, what does this mean? We saw earlier that HIV is highly variable, that a broad neutralizing antibody latches on and disables multiple variations of the virus. If you take these and you put them in the best of our monkey models, they provide full protection from infection. In addition, these researchers found a new site on HIV where the antibodies can grab onto, and what's so special about this spot is that it changes very little as the virus mutates. It's like, as many times as the virus changes its clothes, it's still wearing the same socks, and now our job is to make sure we get the body to really hate those socks.
În septembrie s-au făcut descoperiri suprinzătoare și promițătoare în cadrul unui test clinic realizat în Tailanda. Pentru prima dată, am văzut un vaccin anti-Sida eficace, deși, destul de modest. Acel vaccin specific a fost creat cu aproape un deceniu în urmă. Concepte mai noi și testări timpurii indică o speranță mai mare pe modele animale. Dar, în ultimele luni, cercetătorii au izolat mai mulți anticorpi noi cu spectru larg de neutralizare, din sîngele unei persoane infectate cu HIV. Ce înseamnă asta? Am văzut mai devreme că HIV este extrem de schimbător și că un anticorp cu spectru larg de neutralizare capturează și dezactivează mutanți multipli ai virusului. Daca extragem acești anticorpi și-i introducem in organismul celei mai bune maimuțe model, vor asigura protecție totală împotriva infecției. În plus, cercetătorii au găsit un nou site în HIV unde anticorpii se pot agăța. Zona aceasta e specială deoarece se modifică foarte puțin când virusul suferă mutații. E ca și cum, de căte ori virusul își schimbă hainele continuă să poarte aceleași șosete iar acum sarcina noastră e să determinăm organismul să urască aceste șosete.
So what we've got is a situation. The Thai results tell us we can make an AIDS vaccine, and the antibody findings tell us how we might do that. This strategy, working backwards from an antibody to create a vaccine candidate, has never been done before in vaccine research. It's called retro-vaccinology, and its implications extend way beyond that of just HIV. So think of it this way. We've got these new antibodies we've identified, and we know that they latch onto many, many variations of the virus. We know that they have to latch onto a specific part, so if we can figure out the precise structure of that part, present that through a vaccine, what we hope is we can prompt your immune system to make these matching antibodies. And that would create a universal HIV vaccine. Now, it sounds easier than it is because the structure actually looks more like this blue antibody diagram attached to its yellow binding site, and as you can imagine, these three-dimensional structures are much harder to work on. And if you guys have ideas to help us solve this, we'd love to hear about it.
Avem următoarea situație: Rezultatele tailandeze spun că putem crea un vaccin anti-SIDA; Iar descoperirile legate de anticorpi indică cum am putea pune în practică. Această strategie, mergând invers, de la anticorp la vaccinul candidat, nu s-a mai adoptat niciodată în cercetarea vaccinurilor. Se numește retro-vaccinologie, implicațiile ei se extind dincolo de HIV. Gândiți în felul următor. Avem acești anticorpi noi pe care i-am identificat și știm că anihilează mulți mutanți ai virusului. Știm că trebuie să se fixeze pe o anumită parte a virusului, și configurând precis structura acelei părți o putem include în vaccin și sperăm că vom stimula sistemul imunitar să fabrice acești anticorpi. Astfel am crea vaccinul HIV universal. Sună mai ușor decât este, deoarece structura arată mai degrabă ca acest anticorp din schemă atașat în zona galbenă de fixare. Și cum vă puteți imagina, pe aceste structuri tri-dimensionale e mai dificil de lucrat. Dacă aveți idei pentru rezolvarea acestei probleme, ne-ar plăcea să le auzim.
But, you know, the research that has occurred from HIV now has really helped with innovation with other diseases. So for instance, a biotechnology company has now found broadly neutralizing antibodies to influenza, as well as a new antibody target on the flu virus. They're currently making a cocktail -- an antibody cocktail -- that can be used to treat severe, overwhelming cases of flu. In the longer term, what they can do is use these tools of retro-vaccinology to make a preventive flu vaccine. Now, retro-vaccinology is just one technique within the ambit of so-called rational vaccine design.
Cercetările întreprinse pentru HIV au stimulat inovații pentru alte boli. De exemplu, o companie de biotehnologie a descoperit anticorpi cu spectru larg de neutralizare pentru gripă, precum și un anticorp țintă pentru virusul gripei. În prezent se fabrică un cocktail, un cocktail de anticorpi, care poate fi utilizat în tratarea unor cazuri severe și dificile de gripă. Acum, pe termen lung se pot folosi metodele retro-vaccinologiei pentru a crea un vaccin preventiv pentru gripă. Retro-vaccinologia e doar o tehnică, în așa numita proiectare rațională a vaccinului.
Let me give you another example. We talked about before the H and N spikes on the surface of the flu virus. Notice these other, smaller protuberances. These are largely hidden from the immune system. Now it turns out that these spots also don't change much when the virus mutates. If you can cripple these with specific antibodies, you could cripple all versions of the flu. So far, animal tests indicate that such a vaccine could prevent severe disease, although you might get a mild case. So if this works in humans, what we're talking about is a universal flu vaccine, one that doesn't need to change every year and would remove the threat of death. We really could think of flu, then, as just a bad cold.
Să vă dau un alt exemplu. Am vorbit mai devreme de vârfurile H și M de pe suprafața virusului gripei. Observați și aceste protuberanțe mai mici. Astea sunt în mare parte ascuse de sistemul imunitar. Se pare că nici aceste zone nu se modifică prea mult când virusul suferă mutații. Dacă le putem inhiba cu antibiotice specifice, am putea inhiba toate versiunile de gripă. Până acum, testele pe animale prezic că un asemenea vaccin ar putea preveni boli grave, fiind în schimb înlocuit cu o variantă blândă. Dacă funcționează la oameni, atunci discutăm despre un vaccin universal împotriva gripei, ce nu trebuie modificat în fiecare an și care ar înlătura amenințarea cu moartea. Ne-am putea gândi atunci la gripă într-adevăr doar ca la o răceală mai rea.
Of course, the best vaccine imaginable is only valuable to the extent we get it to everyone who needs it. So to do that, we have to combine smart vaccine design with smart production methods and, of course, smart delivery methods. So I want you to think back a few months ago. In June, the World Health Organization declared the first global flu pandemic in 41 years. The U.S. government promised 150 million doses of vaccine by October 15th for the flu peak. Vaccines were promised to developing countries. Hundreds of millions of dollars were spent and flowed to accelerating vaccine manufacturing. So what happened?
Bineînțeles, cel mai bun vaccin imaginabil e valoros doar în măsura în care îl putem distribui tuturor celor care au nevoie. Așadar trebuie să combinăm inteligent proiectarea vaccinului cu metodele de producție și bineînțeles cu metodele de livrare. Acum gândiți-vă cu câteva luni în urmă. În iunie, Organizația Mondială a Sănătății a declarat prima gripă pandemică globală din ultimii 41 de ani. Guvernul S.U.A. a promis 150 milioane de doze de vaccin până la 15 Octombrie pentru sezonul de gripă. Vaccinurile au fost promise țărilor în curs de dezvoltare. Sute de milioane de dolari au fost cheltuiți pentru accelerarea fabricării vaccinurilor. Și ce s-a întâmplat?
Well, we first figured out how to make flu vaccines, how to produce them, in the early 1940s. It was a slow, cumbersome process that depended on chicken eggs, millions of living chicken eggs. Viruses only grow in living things, and so it turned out that, for flu, chicken eggs worked really well. For most strains, you could get one to two doses of vaccine per egg. Luckily for us, we live in an era of breathtaking biomedical advances. So today, we get our flu vaccines from ... chicken eggs, (Laughter) hundreds of millions of chicken eggs. Almost nothing has changed. The system is reliable but the problem is you never know how well a strain is going to grow. This year's swine flu strain grew very poorly in early production: basically .6 doses per egg. So, here's an alarming thought. What if that wild bird flies by again? You could see an avian strain that would infect the poultry flocks, and then we would have no eggs for our vaccines. So, Dan [Barber], if you want billions of chicken pellets for your fish farm, I know where to get them. So right now, the world can produce about 350 million doses of flu vaccine for the three strains, and we can up that to about 1.2 billion doses if we want to target a single variant like swine flu. But this assumes that our factories are humming because, in 2004, the U.S. supply was cut in half by contamination at one single plant. And the process still takes more than half a year.
Ei bine, la început ne-am dat seama cum să facem vaccinurile, cum să le producem, pe la începutul anilor 1940. A fost un proces lent, greoi, care depindea de ouăle de găină, milioane de ouă vii de găină. Virușii se dezvoltă doar în ființe vii și s-a descoperit că, pentru gripă, ouăle de găină funcționează foarte bine. Pentru majoritatea tulpinilor, se puteau obține 1sau 2 doze de vaccin la un ou. Din fericire pentru noi, trăim într-o eră uimitoare de descoperiri biomedicale. Așadar astăzi, obținem vaccinurile pentru gripă din ... ... ouă de găină. (Râsete) sute de milioane de ouă de găină. Aproape nimic nu s-a schimbat. Sistemul este sigur. Dar problema e că niciodată nu știm cât de bine se va dezvolta o tulpină. Tulpina gripei porcine de anul acesta s-a dezvoltat foarte puțin la începutul producției obținându-se practic 0,6 doze la un ou. Și așa apare un gând alarmant. Ce ne facem dacă pasărea sălbatică zboară iar pe aici? Am vedea o tulpină aviară care ar putea infecta păsările de curte și atunci n-am mai avea ouă pentru vaccinurile noastre. Așadar, Dan [Barber], dacă dorești miliarde de pelete de găină pentru pescăria ta știu unde să le procuri. În prezent, lumea poate produce cam 350 milioane de doze de vaccin antigripal pentru aceste tulpini. Și putem mări până la 1,2 miliarde de doze, dacă dorim sa țintim o singură variantă precum gripa porcină. Dar asta ar presupune ca fabricile noastre să meargă în foc continuu deoarece, în 2004 aprovizionările din S.U.A au fost reduse la jumătate prin contaminare la o singură fabrică. Și procesul durează mai mult de jumătate de an.
So are we better prepared than we were in 1918? Well, with the new technologies emerging now, I hope we can say definitively, "Yes." Imagine we could produce enough flu vaccine for everyone in the entire world for less than half of what we're currently spending now in the United States. With a range of new technologies, we could. Here's an example: A company I'm engaged with has found a specific piece of the H spike of flu that sparks the immune system. If you lop this off and attach it to the tail of a different bacterium, which creates a vigorous immune response, they've created a very powerful flu fighter. This vaccine is so small it can be grown in a common bacteria, E. coli. Now, as you know, bacteria reproduce quickly -- it's like making yogurt -- and so we could produce enough swine origin flu for the entire world in a few factories, in a few weeks, with no eggs, for a fraction of the cost of current methods.
Deci suntem mai bine pregătiți decât eram în 1918 ? Ei bine, cu noile tehnologii care apar acum, sper să putem spune categoric ”Da.” Imaginați-vă că am putea produce suficient vaccin antigripal pentru toți în lumea întreaga pentru mai puțin de jumătate din cât cheltuim acum în Statele Unite. Cu o gamă de tehnologii noi, am putea. Iată un exemplu. O companie, cu care colaborez, a descoperit o parte specifică din vârful H al virusului gripal care stimulează sistemul imunitar. Dacă o izolăm și o atașăm pe coada unor bacterii diferite care inițiază un răspuns imun viguros, creăm o armă foarte puternică. Acest vaccin e atât de mic, încât poate fi crescut pe o bacterie obișnuită, E. coli. Așa cum știți bacteriile se reproduc foarte rapid. Seamănă cu prepararea iaurtului. Și așa am putea produce suficiente vaccinuri porcine pentru întreaga lume, în câteva fabrici, în câteva săptămîni fără ouă cu o fracție din costul metodelor curente.
(Applause)
(Aplauze)
So here's a comparison of several of these new vaccine technologies. And, aside from the radically increased production and huge cost savings -- for example, the E. coli method I just talked about -- look at the time saved: this would be lives saved. The developing world, mostly left out of the current response, sees the potential of these alternate technologies and they're leapfrogging the West. India, Mexico and others are already making experimental flu vaccines, and they may be the first place we see these vaccines in use. Because these technologies are so efficient and relatively cheap, billions of people can have access to lifesaving vaccines if we can figure out how to deliver them.
Priviți aici o comparație a diferitelor tehnologii noi pentru vaccinuri. Pe lângă mărirea radicală a producției și reducerea masivă a costurilor, de exemplu, metoda E. coli despre care spuneam, priviți timpul economisit -- asta înseamnă vieți salvate. Țările în dezvoltare, private până acum de șanse reale, identifică potențialul acestor tehnologii alternative și depășesc occidentul. India, Mexic și altele produc deja vaccinuri antigripale experimentale și s-ar putea să fie primele locuri unde vom vedea aplicate aceste vaccinuri. Deoarece aceste tehnologii sunt așa eficiente și relativ ieftine, miliarde de oameni pot avea acces la vaccinuri salvatoare, dacă găsim o cale de-a le livra.
Now think of where this leads us. New infectious diseases appear or reappear every few years. Some day, perhaps soon, we'll have a virus that is going to threaten all of us. Will we be quick enough to react before millions die? Luckily, this year's flu was relatively mild. I say, "luckily" in part because virtually no one in the developing world was vaccinated. So if we have the political and financial foresight to sustain our investments, we will master these and new tools of vaccinology, and with these tools we can produce enough vaccine for everyone at low cost and ensure healthy productive lives. No longer must flu have to kill half a million people a year. No longer does AIDS need to kill two million a year. No longer do the poor and vulnerable need to be threatened by infectious diseases, or indeed, anybody. Instead of having Vaclav Smil's "massively fatal discontinuity" of life, we can ensure the continuity of life. What the world needs now are these new vaccines, and we can make it happen.
Acum gândiți-vă unde ar putea duce asta. Noi boli infecțioase apar și reapar la fiecare câțiva ani. Într-o zi, posibil curând, vom avea un virus care ne va amenința pe toți. Vom fi suficient de rapizi înainte să moară milioane? Din fericire, gripa din acest an a fost relativ blândă. Spun, parțial ”din fericire” deoarece practic nimeni din țările în curs de dezvoltare nu a fost vaccinată. Deci dacă avem viziunea politică și financiară de-a susține investiția noastră, vom stăpâni mijloacele vechi și noi ale vaccinologiei. Și cu aceste metode putem produce suficient vaccin pentru toți la costuri mici și să asigurăm vieți sănătoase și productive. Gripa n-ar mai omorî anual jumătate de milion de oameni. SIDA n-ar mai omorî două milioane anual. Cei săraci și vulnerabili n-ar mai trebui să fie amenințați de boli infecțioase, de fapt, nimeni. În loc să ne confruntăm cu 'discontinuitate fatală masivă' a vieții, putem asigura continuitatea vieții. Lumea are nevoie acum de aceste noi vaccinuri și putem avea succes.
Thank you very much.
Mulțumesc foarte mult.
(Applause)
(Aplauze)
Chris Anderson: Thank you. (Applause) Thank you. So, the science is changing. In your mind, Seth -- I mean, you must dream about this -- what is the kind of time scale on, let's start with HIV, for a game-changing vaccine that's actually out there and usable?
Chris Anderson: Mulțumesc. (Aplauze) Mulțumesc. Așadar, știința se schimbă. În mintea ta, Seth -- trebuie că visezi la asta -- care e durata în timp să zicem pentru HIV, pentru ca un vaccin radical să fie disponibil?
SB: The game change can come at any time, because the problem we have now is we've shown we can get a vaccine to work in humans; we just need a better one. And with these types of antibodies, we know humans can make them. So, if we can figure out how to do that, then we have the vaccine, and what's interesting is there already is some evidence that we're beginning to crack that problem. So, the challenge is full speed ahead.
SB: Minunea poate surveni oricând deoarece problema în prezent e că avem un vaccin care funcționează la oameni, dar ne trebuie unul mai bun. Aceste noi tipuri de anticorpi pot fi produse de organismul uman. Deci, dacă reușim să facem asta, atunci avem un vaccin. E interesant că deja există dovezi că ne apropiem de rezolvarea problemei. Așadar problema e să accelerăm.
CA: In your gut, do you think it's probably going to be at least another five years?
CA: După tine, crezi că va mai dura cinci ani?
SB: You know, everybody says it's 10 years, but it's been 10 years every 10 years. So I hate to put a timeline on scientific innovation, but the investments that have occurred are now paying dividends.
SB: Toți spun ca mai durează 10 ani, dar au tot fost 10 ani la fiecare 10 ani. Nu îmi place să prezic pentru o inovație științifică dar investițiile recente aduc acum dividente.
CA: And that's the same with universal flu vaccine, the same kind of thing?
CA: E la fel cu vaccinul antigripal universal?
SB: I think flu is different. I think what happened with flu is we've got a bunch -- I just showed some of this -- a bunch of really cool and useful technologies that are ready to go now. They look good. The problem has been that, what we did is we invested in traditional technologies because that's what we were comfortable with. You also can use adjuvants, which are chemicals you mix. That's what Europe is doing, so we could have diluted out our supply of flu and made more available, but, going back to what Michael Specter said, the anti-vaccine crowd didn't really want that to happen.
SB: Cred că gripa e diferită. În ce privește gripa avem o gamă largă -- am arătat o parte -- o gamă de tehnologii utile și eficiente puse la punct. Arată bine. Problema fusese că se investea în tehnologii tradiționale cu care eram obișnuiți. Pot fi folosiți și adjuvanți, substanțe care se amestecă. Asta face Europa; am fi putut dilua stocurile de vaccinuri ca să facem disponibile mai multe dar, întorcându-ne la ce a spus Michael Specter, grupul antivaccin n-a favorizat alternativa asta.
CA: And malaria's even further behind?
CA: Iar malaria e și mai în urmă ?
SB: No, malaria, there is a candidate that actually showed efficacy in an earlier trial and is currently in phase three trials now. It probably isn't the perfect vaccine, but it's moving along.
SB: Nu, malaria e un candidat care și-a demonstrat eficiența într-un test anterior și acum se află în etapa a treia de testare. Probabil nu e un vaccin perfect, dar progresează.
CA: Seth, most of us do work where every month, we produce something; we get that kind of gratification. You've been slaving away at this for more than a decade, and I salute you and your colleagues for what you do. The world needs people like you. Thank you.
CA: Seth, majoritatea lucrăm undeva unde în fiecare lună producem ceva și avem o satisfacție. Tu ești privat de așa ceva de mai bine de o decadă și salut ceea ce faci tu și colegii tăi. Lumea are nevoie de oameni ca tine. Mulțumesc.
SB: Thank you.
SB: Mulțumesc.
(Applause)
(Aplauze)