Do you worry about what is going to kill you? Heart disease, cancer, a car accident? Most of us worry about things we can't control, like war, terrorism, the tragic earthquake that just occurred in Haiti. But what really threatens humanity? A few years ago, Professor Vaclav Smil tried to calculate the probability of sudden disasters large enough to change history. He called these, "massively fatal discontinuities," meaning that they could kill up to 100 million people in the next 50 years. He looked at the odds of another world war, of a massive volcanic eruption, even of an asteroid hitting the Earth. But he placed the likelihood of one such event above all others at close to 100 percent, and that is a severe flu pandemic. Now, you might think of flu as just a really bad cold, but it can be a death sentence. Every year, 36,000 people in the United States die of seasonal flu. In the developing world, the data is much sketchier but the death toll is almost certainly higher. You know, the problem is if this virus occasionally mutates so dramatically, it essentially is a new virus and then we get a pandemic.
Preocupam-se com o que vos vai matar? Um ataque cardíaco, um cancro, um acidente de automóvel? Muitos de nós preocupam-se com coisas que não controlamos, como a guerra, o terrorismo, um trágico terramoto como o que ocorreu no Haiti. Mas quais são as reais ameaças para a humanidade? Há uns anos, o Professor Vaclav Smil tentou calcular a probabilidade de catástrofes repentinas suficientemente grandes para alterar a História. Chamou-lhes "descontinuidades maciçamente fatais", ou seja, que podiam matar mais de 100 milhões de pessoas num prazo de 50 anos. Olhou para a possibilidade de outra guerra mundial, duma erupção vulcânica enorme, até de um asteroide que colidisse com a Terra. Mas colocou a probabilidade de um acontecimento desses acima de todos os outros, perto dos 100%. Seria uma grave pandemia de gripe. Vocês podem pensar na gripe apenas como uma forte constipação mas pode ser uma sentença de morte. Todos os anos, morrem 36 000 pessoas nos EUA com a gripe sazonal. No mundo em desenvolvimento, os dados são muito incompletos, mas o total de mortes é certamente mais elevado. O problema é que, se esse vírus sofrer uma mutação ocasional, de modo significativo, é essencialmente um vírus novo e depois temos uma pandemia.
In 1918, a new virus appeared that killed some 50 to 100 million people. It spread like wildfire and some died within hours of developing symptoms. Are we safer today? Well, we seem to have dodged the deadly pandemic this year that most of us feared, but this threat could reappear at any time. The good news is that we're at a moment in time when science, technology, globalization is converging to create an unprecedented possibility: the possibility to make history by preventing infectious diseases that still account for one-fifth of all deaths and countless misery on Earth. We can do this. We're already preventing millions of deaths with existing vaccines, and if we get these to more people, we can certainly save more lives. But with new or better vaccines for malaria, TB, HIV, pneumonia, diarrhea, flu, we could end suffering that has been on the Earth since the beginning of time.
Em 1918, apareceu um novo vírus que matou entre 50 a 100 milhões de pessoas. Espalhou-se como um rastilho e houve quem morresse horas depois de apresentar sintomas. Estaremos hoje mais seguros? Bom, parece que nos esquivámos a uma pandemia mortal deste ano que muita gente temia, mas esta ameaça pode repetir-se em qualquer altura. Felizmente, vivemos numa época em que a ciência, a tecnologia e a globalização convergem para criar uma possibilidade sem precedentes, a possibilidade de fazer história evitando doenças infecciosas que ainda são responsáveis por um quinto de todas as mortes e uma grande fatalidade no planeta. Podemos fazê-lo. Já estamos a evitar milhões de mortes com as vacinas existentes. Se abrangermos mais pessoas certamente salvaremos mais vidas. Mas com as novas vacinas ou vacinas melhores para a malária, a tuberculose, o VIH, a pneumonia, a diarreia, a gripe, podemos acabar com o sofrimento que existe na Terra desde o início dos tempos.
So, I'm here to trumpet vaccines for you. But first, I have to explain why they're important because vaccines, the power of them, is really like a whisper. When they work, they can make history, but after a while you can barely hear them. Now, some of us are old enough to have a small, circular scar on our arms from an inoculation we received as children. But when was the last time you worried about smallpox, a disease that killed half a billion people last century and no longer is with us? Or polio? How many of you remember the iron lung? We don't see scenes like this anymore because of vaccines.
Venho aqui anunciar-vos vacinas. Mas, primeiro, tenho de explicar porque é que são importantes porque as vacinas, o poder das vacinas, são como um boato. Quando funcionam, podem fazer história, mas, ao fim de uns tempos, mal ouvimos falar delas. Alguns de nós têm idade suficiente para terem uma pequena cicatriz circular num braço devido à inoculação que receberam em criança. Mas quanto foi a última vez que nos preocupámos com a varíola, uma doença que matou meio milhão de pessoas no século passado e já não existe entre nós? Ou a poliomielite? Quantos se lembram do pulmão de aço? Já não vemos cenas destas graças às vacinas.
Now, it's interesting because there are 30-odd diseases that can be treated with vaccines now, but we're still threatened by things like HIV and flu. Why is that? Well, here's the dirty little secret. Until recently, we haven't had to know exactly how a vaccine worked. We knew they worked through old-fashioned trial and error. You took a pathogen, you modified it, you injected it into a person or an animal and you saw what happened. This worked well for most pathogens, somewhat well for crafty bugs like flu, but not at all for HIV, for which humans have no natural immunity.
É interessante porque há umas 30 doenças que podem ser tratadas com vacinas mas ainda somos ameaçados por coisas como o VIH e a gripe. Porquê? Bom, o segredo é este. Até há pouco, não sabíamos ao certo como funcionavam as vacinas. Funcionavam, à moda antiga, através de tentativas e erros. Agarrávamos num agente patogénico, modificávamo-lo, injetávamo-lo numa pessoa ou animal e víamos o que acontecia. Isso funcionava bem para a maioria dos agentes patogénicos, mais ou menos bem para micróbios astutos, como o da gripe, mas não para o VIH, um vírus para o qual não temos imunidade natural.
So let's explore how vaccines work. They basically create a cache of weapons for your immune system which you can deploy when needed. Now, when you get a viral infection, what normally happens is it takes days or weeks for your body to fight back at full strength, and that might be too late. When you're pre-immunized, what happens is you have forces in your body pre-trained to recognize and defeat specific foes. So that's really how vaccines work. Now, let's take a look at a video that we're debuting at TED, for the first time, on how an effective HIV vaccine might work.
Vamos ver como funcionam as vacinas. Basicamente, criam uma reserva de armas para o sistema imunitário que pode ser usado quando for necessário. Quando apanhamos uma infeção viral, habitualmente, o nosso corpo demora dias ou semanas até reagir com toda a força e, nessa altura, pode ser tarde demais. Quando estamos pré-imunizados, possuímos forças no nosso corpo pré-treinadas para reconhecer e derrotar inimigos específicos. É assim que funcionam as vacinas. Agora vamos ver um vídeo que é apresentado na TED pela primeira vez, sobre como poderá funcionar uma vacina eficaz contra o VIH.
(Music)
(Vídeo) [Como poderá funcionar uma vacina contra o VIH]
Narrator: A vaccine trains the body in advance how to recognize and neutralize a specific invader. After HIV penetrates the body's mucosal barriers, it infects immune cells to replicate. The invader draws the attention of the immune system's front-line troops. Dendritic cells, or macrophages, capture the virus and display pieces of it. Memory cells generated by the HIV vaccine are activated when they learn HIV is present from the front-line troops. These memory cells immediately deploy the exact weapons needed. Memory B cells turn into plasma cells, which produce wave after wave of the specific antibodies that latch onto HIV to prevent it from infecting cells, while squadrons of killer T cells seek out and destroy cells that are already HIV infected. The virus is defeated. Without a vaccine, these responses would have taken more than a week. By that time, the battle against HIV would already have been lost.
Narradora: Uma vacina treina o corpo de antemão a reconhecer e neutralizar um invasor específico. Depois de o VIH penetrar as defesas mucosas do corpo, infeta as células imunitárias para elas se reproduzirem. O invasor chama a atenção das tropas da linha da frente do sistema imunitário. As células dendríticas ou macrófagos captam o vírus e expõem certos elementos. As células de memória geradas pela vacina do VIH são ativadas quando reconhecem a presença do VIH pelas tropas da linha da frente. Essas células de memória deslocam imediatamente as armas necessárias. As células B de memória transformam-se em células de plasma que produzem, onda após onda, os anticorpos específicos que aprisionam o VIH para o impedir de infetar células, enquanto esquadrões de células T assassinas procuram e destroem células já infetadas pelo VIH. O vírus é derrotado. Sem uma vacina, estas respostas levariam mais de uma semana. Nessa altura, a batalha contra o VIH já estaria perdida.
Seth Berkley: Really cool video, isn't it? The antibodies you just saw in this video, in action, are the ones that make most vaccines work. So the real question then is: How do we ensure that your body makes the exact ones that we need to protect against flu and HIV? The principal challenge for both of these viruses is that they're always changing. So let's take a look at the flu virus. In this rendering of the flu virus, these different colored spikes are what it uses to infect you. And also, what the antibodies use is a handle to essentially grab and neutralize the virus. When these mutate, they change their shape, and the antibodies don't know what they're looking at anymore. So that's why every year you can catch a slightly different strain of flu. It's also why in the spring, we have to make a best guess at which three strains are going to prevail the next year, put those into a single vaccine and rush those into production for the fall.
Seth Berkley: Um vídeo muito giro, não é? Os anticorpos que viram em ação no vídeo são os que fazem com que a maioria das vacinas funcionem. Portanto, a pergunta é: Como garantimos que o corpo produza os anticorpos que precisamos para nos protegerem contra a gripe e o VIH? O principal problema para estes dois vírus é que estão sempre a mudar. Por isso, observemos o vírus da gripe. Nesta versão do vírus da gripe estas pontas de cor diferente são usadas para nos infetarem. Os anticorpos também as usam como uma pega onde se agarram, para neutralizar o vírus. Quando estes sofrem uma mutação, mudam de forma e os anticorpos deixam de reconhecer o que estão a procurar. É por isso que, todos os anos, podemos apanhar uma estirpe diferente de gripe. É também por isso que, na primavera, temos de tentar adivinhar quais as três estirpes que vão predominar no ano seguinte, metê-las numa só vacina e produzi-la rapidamente para a aplicar no outono.
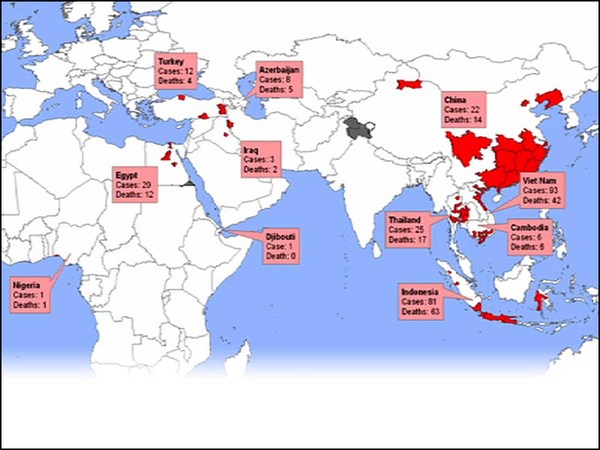
Even worse, the most common influenza -- influenza A -- also infects animals that live in close proximity to humans, and they can recombine in those particular animals. In addition, wild aquatic birds carry all known strains of influenza. So, you've got this situation: In 2003, we had an H5N1 virus that jumped from birds into humans in a few isolated cases with an apparent mortality rate of 70 percent. Now luckily, that particular virus, although very scary at the time, did not transmit from person to person very easily. This year's H1N1 threat was actually a human, avian, swine mixture that arose in Mexico. It was easily transmitted, but, luckily, was pretty mild. And so, in a sense, our luck is holding out, but you know, another wild bird could fly over at anytime.
Pior ainda, a gripe mais vulgar — a gripe A — também infeta os animais que vivem próximo dos seres humanos e o vírus pode-se recombinar nesses animais. Para além disso, as aves aquáticas selvagens também são portadoras de todas as estirpes de gripe. Assim, já tivemos esta situação: Em 2003, tivemos um vírus H5N1 que passou das aves para as pessoas nalguns casos isolados com uma taxa de mortalidade aparente de 70%. Felizmente, esse vírus especial, embora assustador na altura, não se transmitia de pessoa para pessoa, com muita facilidade. A ameaça do H1N1 deste ano foi uma mistura de pessoas, aves e porcos que surgiu no México. Transmitia-se com facilidade mas, felizmente, era pouco virulento. Em certo sentido, temos tido sorte, mas pode aparecer outra ave, a qualquer momento.
Now let's take a look at HIV. As variable as flu is, HIV makes flu look like the Rock of Gibraltar. The virus that causes AIDS is the trickiest pathogen scientists have ever confronted. It mutates furiously, it has decoys to evade the immune system, it attacks the very cells that are trying to fight it and it quickly hides itself in your genome. Here's a slide looking at the genetic variation of flu and comparing that to HIV, a much wilder target. In the video a moment ago, you saw fleets of new viruses launching from infected cells. Now realize that in a recently infected person, there are millions of these ships; each one is just slightly different. Finding a weapon that recognizes and sinks all of them makes the job that much harder.
Observemos agora o VIH. Por mais variável que o vírus da gripe seja, o VIH faz com que a gripe pareça o Rochedo de Gibraltar. Este é o vírus que provoca a SIDA é o agente patogénico mais traiçoeiro que os cientistas já encontraram. Está sempre em mutação, tem manhas para se esquivar ao sistema imunitário, ataca as células que estão a tentar combatê-lo e esconde-se rapidamente no nosso genoma. Este é um diapositivo que ilustra a variação genética da gripe e a compara com a do VIH, um alvo muito maior. No vídeo de há pouco vimos esquadrões de novos vírus lançados pelas células infetadas. Agora percebemos que, numa pessoa recém-infetada, há milhões destes veículos, cada um deles ligeiramente diferente. Encontrar uma arma que os reconheça e os neutralize a todos é uma tarefa muito mais difícil.
Now, in the 27 years since HIV was identified as the cause of AIDS, we've developed more drugs to treat HIV than all other viruses put together. These drugs aren't cures, but they represent a huge triumph of science because they take away the automatic death sentence from a diagnosis of HIV, at least for those who can access them. The vaccine effort though is really quite different. Large companies moved away from it because they thought the science was so difficult and vaccines were seen as poor business. Many thought that it was just impossible to make an AIDS vaccine, but today, evidence tells us otherwise.
Durante os 27 anos, desde que o VIH foi identificado como o causador da SIDA, desenvolvemos mais medicamentos para tratar o VIH do que todos os outros vírus em conjunto. Estes medicamentos não curam mas representam um enorme triunfo da ciência porque afastam a automática sentença de morte num diagnóstico de VIH, pelo menos, para os que lhes têm acesso. Os esforços para uma vacina são uma coisa muito diferente. As grandes empresas desistiram dela, porque acharam que a ciência era muito difícil e consideraram que as vacinas eram um mau negócio. Muitas pensaram que era impossível fazer uma vacina para a SIDA mas hoje, os indícios mostram-nos o contrário.
In September, we had surprising but exciting findings from a clinical trial that took place in Thailand. For the first time, we saw an AIDS vaccine work in humans -- albeit, quite modestly -- and that particular vaccine was made almost a decade ago. Newer concepts and early testing now show even greater promise in the best of our animal models. But in the past few months, researchers have also isolated several new broadly neutralizing antibodies from the blood of an HIV infected individual. Now, what does this mean? We saw earlier that HIV is highly variable, that a broad neutralizing antibody latches on and disables multiple variations of the virus. If you take these and you put them in the best of our monkey models, they provide full protection from infection. In addition, these researchers found a new site on HIV where the antibodies can grab onto, and what's so special about this spot is that it changes very little as the virus mutates. It's like, as many times as the virus changes its clothes, it's still wearing the same socks, and now our job is to make sure we get the body to really hate those socks.
Em setembro, fizemos descobertas surpreendentes mas animadoras a partir dum teste clínico que ocorreu na Tailândia. Pela primeira vez, vimos uma vacina da SIDA a funcionar em seres humanos, — embora de forma muito modesta. Essa vacina especial foi feita há quase 10 anos. Conceitos mais recentes e testes recentes são mesmo mais promissores nos nossos melhores modelos animais. Mas nos últimos meses, os investigadores também isolaram vários anticorpos amplamente neutralizadores no sangue de indivíduos infetados com VIH. O que é que isso significa? Já vimos há bocado que o VIH é muito variável, e que um grande número de anticorpos neutralizadores se ligam e invalidam múltiplas variantes do vírus. Se agarrarmos neles e os pusermos nos melhores modelos de macacos, eles proporcionam uma proteção total para a infeção. Além disso, os investigadores descobriram um novo sítio no VIH onde os anticorpos se podem ligar. O que é especial nesse local é que muda muto pouco mesmo quando o vírus sofre uma mutação. É como se o vírus, sempre que muda de roupa, continue a usar as mesmas meias. Agora, a nossa tarefa é garantir que o nosso corpo odeie essas meias´.
So what we've got is a situation. The Thai results tell us we can make an AIDS vaccine, and the antibody findings tell us how we might do that. This strategy, working backwards from an antibody to create a vaccine candidate, has never been done before in vaccine research. It's called retro-vaccinology, and its implications extend way beyond that of just HIV. So think of it this way. We've got these new antibodies we've identified, and we know that they latch onto many, many variations of the virus. We know that they have to latch onto a specific part, so if we can figure out the precise structure of that part, present that through a vaccine, what we hope is we can prompt your immune system to make these matching antibodies. And that would create a universal HIV vaccine. Now, it sounds easier than it is because the structure actually looks more like this blue antibody diagram attached to its yellow binding site, and as you can imagine, these three-dimensional structures are much harder to work on. And if you guys have ideas to help us solve this, we'd love to hear about it.
Temos assim a seguinte situação. Os resultados da Tailândia mostram que podemos fazer uma vacina para a SIDA e as descobertas dos anticorpos dizem-nos como podemos fazê-la. Esta estratégia, que funciona ao contrário a partir de um anticorpo para criar uma possível vacina, nunca foi efetuada na investigação sobre vacinas. Chama-se retro-vacinologia e as suas implicações estendem-se muito para além do VIH. Pensem assim. Temos estes novos anticorpos que identificámos e sabemos que eles se ligam a muitas variantes do vírus. Sabemos que têm de se fixar numa parte específica. Se pudermos encontrar a estrutura rigorosa dessa parte, e apresentá-la na vacina, esperamos poder incitar o sistema imunitário a fazer esses anticorpos correspondentes. Isso irá criar uma vacina universal para o VIH. Parece mais fácil do que é porque a estrutura é mais parecida com este diagrama de um anticorpo azul ligado aos locais de fixação a amarelo. Como podemos imaginar, estas estruturas a 3D são muito mais difíceis de trabalhar. Se tiverem ideias para ajudar a resolver isto, gostávamos de as ouvir.
But, you know, the research that has occurred from HIV now has really helped with innovation with other diseases. So for instance, a biotechnology company has now found broadly neutralizing antibodies to influenza, as well as a new antibody target on the flu virus. They're currently making a cocktail -- an antibody cocktail -- that can be used to treat severe, overwhelming cases of flu. In the longer term, what they can do is use these tools of retro-vaccinology to make a preventive flu vaccine. Now, retro-vaccinology is just one technique within the ambit of so-called rational vaccine design.
Mas a investigação que existe hoje sobre o VIH ajudou na investigação de outras doenças. Por exemplo, uma empresa de biotecnologia encontrou numerosos anticorpos que neutralizam a gripe assim como um novo alvo dos anticorpos no vírus da gripe. Atualmente, estão a fazer um "cocktail" — um "cocktail" de anticorpos — que pode ser usado para tratar casos de gripe muito graves. A longo prazo, podemos usar estes instrumentos de retro-vacinologia para criar uma vacina preventiva da gripe. Mas a retro-vacinologia é apenas uma técnica no âmbito da conceção das vacinas chamadas "racionais".
Let me give you another example. We talked about before the H and N spikes on the surface of the flu virus. Notice these other, smaller protuberances. These are largely hidden from the immune system. Now it turns out that these spots also don't change much when the virus mutates. If you can cripple these with specific antibodies, you could cripple all versions of the flu. So far, animal tests indicate that such a vaccine could prevent severe disease, although you might get a mild case. So if this works in humans, what we're talking about is a universal flu vaccine, one that doesn't need to change every year and would remove the threat of death. We really could think of flu, then, as just a bad cold.
Vou dar-vos um exemplo. Já falámos das pontas H e N na superfície do vírus da gripe. Reparem nestas protuberâncias mais pequenas. Estão muito bem escondidas do sistema imunitário. Acontece que estes locais também não mudam muito quando o vírus sofre uma mutação. Se pudermos inutilizar estes anticorpos específicos, também inutilizamos todas as versões da gripe. Até aqui, os testes em animais indicam que essa vacina poderá impedir doenças graves, embora possamos tê-la numa forma amena. Se isto funcionar nas pessoas, estamos a falar duma vacina para a gripe universal, uma vacina que não precise de mudar todos os anos e que afastará a ameaça de morte. Nessa altura, podemos pensar na gripe simplesmente como uma forte constipação.
Of course, the best vaccine imaginable is only valuable to the extent we get it to everyone who needs it. So to do that, we have to combine smart vaccine design with smart production methods and, of course, smart delivery methods. So I want you to think back a few months ago. In June, the World Health Organization declared the first global flu pandemic in 41 years. The U.S. government promised 150 million doses of vaccine by October 15th for the flu peak. Vaccines were promised to developing countries. Hundreds of millions of dollars were spent and flowed to accelerating vaccine manufacturing. So what happened?
Claro que a melhor vacina que podemos imaginar só tem valor na medida em que seja aplicada em todos os que precisam dela. Para isso, temos de aliar a conceção duma vacina inteligente com métodos de produção inteligentes e, claro, métodos inteligentes de distribuição. Gostava que pensassem nos meses passados. Em junho, a Organização Mundial de Saúde declarou a primeira pandemia mundial de gripe, em 41 anos. O governo dos EUA prometeu 150 milhões de doses de vacinas até 15 de outubro, para o pico da gripe. Prometeram-se vacinas aos países em desenvolvimento. Gastaram-se centenas de milhões de dólares destinados a acelerar a produção das vacinas. O que é que aconteceu?
Well, we first figured out how to make flu vaccines, how to produce them, in the early 1940s. It was a slow, cumbersome process that depended on chicken eggs, millions of living chicken eggs. Viruses only grow in living things, and so it turned out that, for flu, chicken eggs worked really well. For most strains, you could get one to two doses of vaccine per egg. Luckily for us, we live in an era of breathtaking biomedical advances. So today, we get our flu vaccines from ... chicken eggs, (Laughter) hundreds of millions of chicken eggs. Almost nothing has changed. The system is reliable but the problem is you never know how well a strain is going to grow. This year's swine flu strain grew very poorly in early production: basically .6 doses per egg. So, here's an alarming thought. What if that wild bird flies by again? You could see an avian strain that would infect the poultry flocks, and then we would have no eggs for our vaccines. So, Dan [Barber], if you want billions of chicken pellets for your fish farm, I know where to get them. So right now, the world can produce about 350 million doses of flu vaccine for the three strains, and we can up that to about 1.2 billion doses if we want to target a single variant like swine flu. But this assumes that our factories are humming because, in 2004, the U.S. supply was cut in half by contamination at one single plant. And the process still takes more than half a year.
Primeiro, imaginámos como fazer as vacinas para a gripe, como produzi-las. No início dos anos 40, era um processo moroso, complicado que dependia dos ovos de galinha, milhões de ovos de galinhas vivas. Os vírus só crescem em coisas vivas por isso, aconteceu que, para a gripe, os ovos de galinha funcionavam muito bem. Para a maioria das estirpes, podíamos obter uma a duas doses de vacina, por ovo. Felizmente para nós vivemos numa época de progressos biomédicos espantosos. Assim, hoje obtemos as vacinas da gripe, a partir... ... de ovos de galinha, (Risos) de centenas de milhões de ovos de galinha. Quase nada se alterou. O sistema é fiável mas o problema é que nunca sabemos como a estirpe vai vingar. A estirpe de gripe suína deste ano evoluiu fracamente na primeira produção, basicamente 0,6 doses por ovo. Este é um pensamento alarmante. Que acontecerá se uma ave selvagem passe por aqui de novo? Podíamos ver uma estirpe de aves que infetaria os bandos dos aviários e ficaríamos sem ovos para as vacinas. Portanto, Dan, se quiseres milhares de milhões de granulados de galinhas para as tuas pisciculturas, eu sei onde os ir buscar. Neste momento, o mundo pode produzir cerca de 350 milhões de doses da vacina para a gripe para as três estirpes. Podemos chegar a cerca de 1200 milhões de doses, se quisermos visar uma única variante, como a gripe suína. Mas isso pressupõe que as fábricas trabalhem em pleno porque, em 2004, o abastecimento dos EUA foi reduzido a metade pela contaminação numa única instalação. O processo ainda demora mais de meio ano.
So are we better prepared than we were in 1918? Well, with the new technologies emerging now, I hope we can say definitively, "Yes." Imagine we could produce enough flu vaccine for everyone in the entire world for less than half of what we're currently spending now in the United States. With a range of new technologies, we could. Here's an example: A company I'm engaged with has found a specific piece of the H spike of flu that sparks the immune system. If you lop this off and attach it to the tail of a different bacterium, which creates a vigorous immune response, they've created a very powerful flu fighter. This vaccine is so small it can be grown in a common bacteria, E. coli. Now, as you know, bacteria reproduce quickly -- it's like making yogurt -- and so we could produce enough swine origin flu for the entire world in a few factories, in a few weeks, with no eggs, for a fraction of the cost of current methods.
Então, estaremos mais bem preparados do que estávamos em 1918? Com as novas tecnologias que surgem agora espero poder responder definitivamente "Sim". Imaginem que podemos produzir vacinas suficientes da gripe para toda a gente no mundo inteiro por menos de metade do custo atual, hoje nos EUA. Com uma série de novas tecnologias, será possível. Este é um exemplo: Uma empresa onde trabalho descobriu uma parte específica da ponta H do vírus da gripe que ativa o sistema imunitário. Se o isolarmos e o ligarmos à cauda duma bactéria diferente, que crie uma resposta imunitária vigorosa, eles criarão um combatente muito poderoso contra a gripe. Esta vacina é tão pequena que pode ser criada em bactérias E.coli vulgares. Como sabem, as bactérias reproduzem-se rapidamente — é como fazer iogurte — e podemos produzir muitas contra a gripe suína para o mundo inteiro, em poucas fábricas, em poucas semanas, sem ovos, por uma fração do custo dos métodos atuais.
(Applause)
(Aplausos)
So here's a comparison of several of these new vaccine technologies. And, aside from the radically increased production and huge cost savings -- for example, the E. coli method I just talked about -- look at the time saved: this would be lives saved. The developing world, mostly left out of the current response, sees the potential of these alternate technologies and they're leapfrogging the West. India, Mexico and others are already making experimental flu vaccines, and they may be the first place we see these vaccines in use. Because these technologies are so efficient and relatively cheap, billions of people can have access to lifesaving vaccines if we can figure out how to deliver them.
Esta é uma comparação de várias destas novas tecnologias de vacinas. Para além da produção radicalmente aumentada e da enorme poupança de custos — por exemplo, o método E.coli a que me referi — pensem no tempo que se poupa: serão muitas vidas poupadas. O mundo em desenvolvimento, que na sua maior parte está fora da resposta atual, vê o potencial destas tecnologias alternativas e está a ultrapassar o Ocidente. A Índia, o México e outros já estão a experimentar vacinas para a gripe e poderão ser o primeiro local onde veremos estas vacinas em ação. Como estas tecnologias são muito eficazes e relativamente baratas, milhares de milhões de pessoas podem aceder a vacinas que salvam vidas se arranjarmos forma de as distribuir.
Now think of where this leads us. New infectious diseases appear or reappear every few years. Some day, perhaps soon, we'll have a virus that is going to threaten all of us. Will we be quick enough to react before millions die? Luckily, this year's flu was relatively mild. I say, "luckily" in part because virtually no one in the developing world was vaccinated. So if we have the political and financial foresight to sustain our investments, we will master these and new tools of vaccinology, and with these tools we can produce enough vaccine for everyone at low cost and ensure healthy productive lives. No longer must flu have to kill half a million people a year. No longer does AIDS need to kill two million a year. No longer do the poor and vulnerable need to be threatened by infectious diseases, or indeed, anybody. Instead of having Vaclav Smil's "massively fatal discontinuity" of life, we can ensure the continuity of life. What the world needs now are these new vaccines, and we can make it happen.
Pensem onde isto nos pode levar. Novas doenças infecciosas aparecem ou reaparecem de anos em anos. Um dia, talvez em breve, teremos um vírus que nos vai ameaçar a todos nós. Será possível reagir rapidamente antes de morrerem milhões? Felizmente, a gripe deste ano foi relativamente benigna. Eu digo "felizmente" em parte porque, na prática, ninguém no mundo em desenvolvimento estava vacinado. Se tivermos a visão política e financeira de sustentar os nossos investimentos, dominaremos os instrumentos. atuais e novos, da vacinologia e com esses instrumentos podemos produzir vacinas suficientes para todos, a baixo custo e garantir vidas saudáveis produtivas. A maioria das gripes já não precisa de matar meio milhão de pessoas por ano. Nem a SIDA precisa de matar dois milhões por ano. Os pobres e vulneráveis já não precisam de ser ameaçados por doenças infecciosas, nem ninguém mais, claro. Em vez de termos a "descontinuidade fatal em massa" da vida de Vaclav Smil, podemos assegurar a continuidade da vida. O mundo precisa destas vacinas novas e podemos fazer com que isso aconteça.
Thank you very much.
Muito obrigado.
(Applause)
(Aplausos)
Chris Anderson: Thank you. (Applause) Thank you. So, the science is changing. In your mind, Seth -- I mean, you must dream about this -- what is the kind of time scale on, let's start with HIV, for a game-changing vaccine that's actually out there and usable?
Chris Anderson: Obrigado. (Aplausos) Obrigado. A ciência está a mudar. Seth, na tua opinião — deves sonhar com isso — qual é mais ou menos o tempo — por exemplo, para o VIH — para uma vacina revolucionária disponível e utilizável?
SB: The game change can come at any time, because the problem we have now is we've shown we can get a vaccine to work in humans; we just need a better one. And with these types of antibodies, we know humans can make them. So, if we can figure out how to do that, then we have the vaccine, and what's interesting is there already is some evidence that we're beginning to crack that problem. So, the challenge is full speed ahead.
SB: Pode acontecer em qualquer altura, porque o problema que temos agora é que mostrámos que podemos ter uma vacina que funcione. Só precisamos de a melhorar. Com este tipo de anticorpos, podemos fazê-las. Se percebermos como fazer isso, teremos a vacina. O interessante é que já há indícios de que estamos a penetrar no problema. O problema avança a todo o gás.
CA: In your gut, do you think it's probably going to be at least another five years?
CA: Achas que pode aparecer dentro de cinco anos?
SB: You know, everybody says it's 10 years, but it's been 10 years every 10 years. So I hate to put a timeline on scientific innovation, but the investments that have occurred are now paying dividends.
SB: Toda a gente fala em 10 anos, mas há 10 anos que são sempre 10 anos. Não gosto de avançar com uma data para as inovações científicas, mas os investimentos que fizemos já estão a pagar dividendos.
CA: And that's the same with universal flu vaccine, the same kind of thing?
CA: E passa-se o mesmo com a vacina universal da gripe?
SB: I think flu is different. I think what happened with flu is we've got a bunch -- I just showed some of this -- a bunch of really cool and useful technologies that are ready to go now. They look good. The problem has been that, what we did is we invested in traditional technologies because that's what we were comfortable with. You also can use adjuvants, which are chemicals you mix. That's what Europe is doing, so we could have diluted out our supply of flu and made more available, but, going back to what Michael Specter said, the anti-vaccine crowd didn't really want that to happen.
SB: Com a gripe é diferente. O que acontece com a gripe é que temos uma série de tecnologias novas e úteis que já estão disponíveis. Parecem ser boas. O problema é que temos investido em tecnologias tradicionais porque é com elas que nos sentimos à vontade. Também podemos usar adjuvantes, que são químicos que adicionamos. É o que a Europa está a fazer. Podemos diluir as reservas da gripe e torná-las mais acessível. Como disse Michael Specter: as pessoas anti-vacinas não querem que isso aconteça.
CA: And malaria's even further behind?
CA: E a malária virá logo a seguir?
SB: No, malaria, there is a candidate that actually showed efficacy in an earlier trial and is currently in phase three trials now. It probably isn't the perfect vaccine, but it's moving along.
SB: Não. Há uma candidata para a malária que mostrou eficácia num teste antigo e está agora numa fase de testes. Provavelmente não será a vacina perfeita, mas está a melhorar.
CA: Seth, most of us do work where every month, we produce something; we get that kind of gratification. You've been slaving away at this for more than a decade, and I salute you and your colleagues for what you do. The world needs people like you. Thank you.
CA: Seth, muitos de nós trabalham e todos os meses produzimos qualquer coisa e obtemos uma certa gratificação. Tu tens trabalhado nisto como um escravo há mais de 10 anos e cumprimento-te e aos teus colegas pelo que fazem. O mundo precisa de pessoas como tu. Obrigado.
SB: Thank you.
SB: Obrigado.
(Applause)
(Aplausos)