Do you worry about what is going to kill you? Heart disease, cancer, a car accident? Most of us worry about things we can't control, like war, terrorism, the tragic earthquake that just occurred in Haiti. But what really threatens humanity? A few years ago, Professor Vaclav Smil tried to calculate the probability of sudden disasters large enough to change history. He called these, "massively fatal discontinuities," meaning that they could kill up to 100 million people in the next 50 years. He looked at the odds of another world war, of a massive volcanic eruption, even of an asteroid hitting the Earth. But he placed the likelihood of one such event above all others at close to 100 percent, and that is a severe flu pandemic. Now, you might think of flu as just a really bad cold, but it can be a death sentence. Every year, 36,000 people in the United States die of seasonal flu. In the developing world, the data is much sketchier but the death toll is almost certainly higher. You know, the problem is if this virus occasionally mutates so dramatically, it essentially is a new virus and then we get a pandemic.
Czy zastanawiacie się nad tym, co może was zabić? Zawał, rak czy wypadek samochodowy? Większość z nas zamartwia się rzeczami nad którymi nie mają kontroli jak wojna, terroryzm, tragiczne trzęsienie ziemi, jak to, które niedawno nawiedziło Haiti. Ale co na prawdę zagraża ludzkości? Parę lat temu, profesor Vaclaw Smil próbował obliczyć prawdopodobieństwo nagłych katastrof, które są na tyle duże, by zmienić bieg historii. Nazwał je "wielkimi śmiertelnymi przerwami," co oznacza, że mogłyby one zabić powyżej 100 milionów ludzi w przeciągu najbliższych 50 lat. Skupiał się na wydarzeniach jak następna wojna światowa, potężny wybuch wulkanu, nawet uderzenie w Ziemię asteroidy. Ale uznał, że największe prawdopodobieństwo, spośród podobnych wydarzeń -- bo blisko 100 procentowe -- ma dotkliwa pandemia grypy. Teraz myślicie może o grypie, że jest to po prostu trochę cięższe przeziębienie. Jednak może ona być śmiertelna. Każdego roku 36 000 ludzi w Stanach Zjednoczonych umiera na grypę sezonową. Mamy trochę mniej informacji na temat krajów rozwijających się, ale tam śmiertelność, jest znacznie wyższa. Z pewnością wiecie, że problem pojawia się, gdy wirus niespodziewanie zmutuje w pechowy sposób, tak, że właściwie powstanie nowy wirus. Właśnie wtedy wybuchają pandemie.
In 1918, a new virus appeared that killed some 50 to 100 million people. It spread like wildfire and some died within hours of developing symptoms. Are we safer today? Well, we seem to have dodged the deadly pandemic this year that most of us feared, but this threat could reappear at any time. The good news is that we're at a moment in time when science, technology, globalization is converging to create an unprecedented possibility: the possibility to make history by preventing infectious diseases that still account for one-fifth of all deaths and countless misery on Earth. We can do this. We're already preventing millions of deaths with existing vaccines, and if we get these to more people, we can certainly save more lives. But with new or better vaccines for malaria, TB, HIV, pneumonia, diarrhea, flu, we could end suffering that has been on the Earth since the beginning of time.
W 1918 roku pojawiła się nowa odmiana wirusa, która zabiła od 50 do 100 milionów ludzi. Rozprzestrzeniała się błyskawicznie. Ludzie umierali w kilka godzin po pierwszych objawach. Czy dziś jest bezpieczniej? Wygląda na to, że uniknęliśmy śmiertelnej pandemii tego roku która nabawiła strachem większość z nas, ale to zagrożenie, może pojawić się ponownie. Dobre wieści są takie, że żyjemy w takich czasach, gdzie nauka, technologia i globalizacja łączą się, aby stworzyć bezprecedensową możliwość, tworzenia historii poprzez, zapobieganie chorobom zakaźnym które nadal powodują 1/5 wszystkich śmierci, oraz niezliczonemu cierpieniu na Ziemi. Możemy tego dokonać Na dzień dzisiejszy zapobiegamy milionom śmiertelnych przypadków poprzez szczepienia. I jeśli podamy je większej ilości ludzi. to ocalimy więcej istnień. Ale jeśli zdobędziemy nowe, lub lepsze szczepionki na malarię, gruźlicę, HIV, zapalenie płuc, biegunkę czy grypę, będziemy mogli zakończyć istnienie chorób, które towarzyszą nam od początku świata.
So, I'm here to trumpet vaccines for you. But first, I have to explain why they're important because vaccines, the power of them, is really like a whisper. When they work, they can make history, but after a while you can barely hear them. Now, some of us are old enough to have a small, circular scar on our arms from an inoculation we received as children. But when was the last time you worried about smallpox, a disease that killed half a billion people last century and no longer is with us? Or polio? How many of you remember the iron lung? We don't see scenes like this anymore because of vaccines.
Jestem tutaj, aby rozgłaszać o tych szczepionkach. Ale na początku muszę wam wyjaśnić, dlaczego są one tak ważne. Szczepionki, ich wielka siła jest podobna do szeptu. Kiedy zaczynają działać, mogą zmienić historię, ale po chwili, ledwo o nich słychać. Część z nas ma na tyle lat, aby mieć jeszcze małą bliznę na ramieniu po szczepieniu, które dostaliśmy jako dzieci. Ale czy kiedykolwiek zastanawiałeś się nad ospą, która zabiła pół miliarda ludzi w minionym stuleciu ale teraz nam już nie zagraża? Albo nad polio -- czy pamiętasz w ogóle żelazne płuca? Nigdy więcej nie będziemy patrzyć na taki widok dzięki szczepionkom.
Now, it's interesting because there are 30-odd diseases that can be treated with vaccines now, but we're still threatened by things like HIV and flu. Why is that? Well, here's the dirty little secret. Until recently, we haven't had to know exactly how a vaccine worked. We knew they worked through old-fashioned trial and error. You took a pathogen, you modified it, you injected it into a person or an animal and you saw what happened. This worked well for most pathogens, somewhat well for crafty bugs like flu, but not at all for HIV, for which humans have no natural immunity.
Bardzo interesujące jest, że dzięki szczepionkom jesteśmy w stanie pokonać ponad 30 chorób, ale w dalszym ciągu nic nie możemy poradzić na grypę czy HIV. Dlaczego? Jest pewna niechciana prawda: do niedawna jeszcze nie wiedzieliśmy jak właściwie działają szczepionki. Tworzyliśmy je staromodną metodą prób i błędów. Bierzesz patogen, modyfikujesz go, wstrzykujesz człowiekowi lub zwierzęciu i patrzysz co się dzieje. Ta metoda działała bardzo dobrze dla większości chorób, w pewnym stopniu również na tak przebiegłe choroby jak grypa, ale nie działa na wirus HIV, na który ludzie nie mają wrodzonej odporności.
So let's explore how vaccines work. They basically create a cache of weapons for your immune system which you can deploy when needed. Now, when you get a viral infection, what normally happens is it takes days or weeks for your body to fight back at full strength, and that might be too late. When you're pre-immunized, what happens is you have forces in your body pre-trained to recognize and defeat specific foes. So that's really how vaccines work. Now, let's take a look at a video that we're debuting at TED, for the first time, on how an effective HIV vaccine might work.
Odpowiedzmy sobie na pytanie: Jak działają szczepionki? Otóż tworzą one zapas "broni" który jest używany przez system odpornościowy, kiedy zajdzie taka potrzeba. Zwykle upływa kilka dni bądź nawet tygodni, od momentu zarażenia się wirusem, zanim twoje ciało zacznie bronić się wszystkimi możliwymi środkami, ale czasem jest już na to za późno. Ale jeśli w jakiś sposób nabierzesz wcześniej odporności, twoje ciało natychmiastowo rozpoznaje intruza i atakuje go. Oto właśnie metoda, na jakiej opierają się szczepionki. Teraz obejrzyjmy wideo, które debiutuje na TED, i pierwszy raz w historii tłumaczy jak mogłyby działać szczepionki na HIV.
(Music)
(Muzyka)
Narrator: A vaccine trains the body in advance how to recognize and neutralize a specific invader. After HIV penetrates the body's mucosal barriers, it infects immune cells to replicate. The invader draws the attention of the immune system's front-line troops. Dendritic cells, or macrophages, capture the virus and display pieces of it. Memory cells generated by the HIV vaccine are activated when they learn HIV is present from the front-line troops. These memory cells immediately deploy the exact weapons needed. Memory B cells turn into plasma cells, which produce wave after wave of the specific antibodies that latch onto HIV to prevent it from infecting cells, while squadrons of killer T cells seek out and destroy cells that are already HIV infected. The virus is defeated. Without a vaccine, these responses would have taken more than a week. By that time, the battle against HIV would already have been lost.
Lektor: Szczepionka przygotowuje z wyprzedzeniem nasze ciało jak rozpoznać i zneutralizować określonego intruza. Kiedy HIV przeniknie do ciała przez błony śluzowe, atakuje białe krwinki, aby się w nich namnożyć. Wirus przyciąga uwagę "zwiadowców" systemu immunologicznego. Są nimi komórki dendrytyczne lub makrofagi, które łapią wirusa i prezentują jego fragmenty. Komórki pamięci, wytworzone dzięki szczepionce są aktywowane kiedy dowiedzą się, że wirus HIV jest obecny w ustroju właśnie dzięki "zwiadowcom". Komórki pamięci stosują dokładnie tę broń która jest potrzebna. Komórki pamięci typu B przemieniają się w plazmocyty produkujące seria za serią konkretne przeciwciała, które przyczepiają się do wirusa HIV i zapobiegają dalszemu zakażaniu, podczas gdy oddziały zabójczych limfocytów T odszukują i niszczą komórki, które już zostały zarażone HIV. Wirus jest pokonany. Bez szczepionki, ta odpowiedź organizmu mogła by zająć ponad tydzień. Po tym czasie bitwa przeciwko HIV byłaby już przegrana.
Seth Berkley: Really cool video, isn't it? The antibodies you just saw in this video, in action, are the ones that make most vaccines work. So the real question then is: How do we ensure that your body makes the exact ones that we need to protect against flu and HIV? The principal challenge for both of these viruses is that they're always changing. So let's take a look at the flu virus. In this rendering of the flu virus, these different colored spikes are what it uses to infect you. And also, what the antibodies use is a handle to essentially grab and neutralize the virus. When these mutate, they change their shape, and the antibodies don't know what they're looking at anymore. So that's why every year you can catch a slightly different strain of flu. It's also why in the spring, we have to make a best guess at which three strains are going to prevail the next year, put those into a single vaccine and rush those into production for the fall.
Seth Berkley: Naprawdę fajna jest ta animacja, co nie? Przeciwciała, które właśnie widzieliście na filmie w akcji są tymi, które odgrywają najważniejszą rolę w szczepionkach. Teraz tak naprawdę powstaje pytanie: Czy jesteśmy w stanie sprawić, aby twoje ciało produkowało te specyficzne przeciwciała, które są niezbędne do obrony przed grypą czy HIV? Głównym wyzwaniem jest to, że oba te wirusy cały czas się zmieniają. Przyjrzyjmy się bliżej wirusowi grypy. Na modelu tego wirusa te kolorowe wypustki są odpowiedzialne za zarażanie. Przeciwciała wykorzystują je również, aby "przyczepić się" do wirusa i w pewnym sensie złapać go i zneutralizować. Mutacje wirusów polegają na zmianie ich kształtu, przez co przeciwciała nie wiedzą co robić. Dlatego też, każdego roku mamy nieco inne odmiany grypy. Również dlatego, na wiosnę, specjaliści muszą zgadywać, jakie trzy odmiany przetrwają w następnym roku, by stworzyć na nie szczepionkę i wdrożyć w produkcję na jesień.
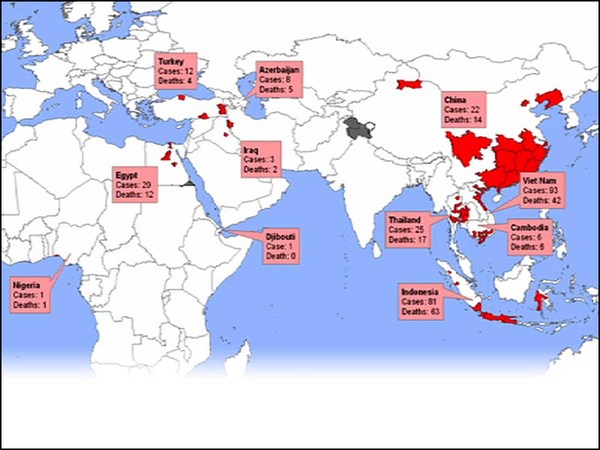
Even worse, the most common influenza -- influenza A -- also infects animals that live in close proximity to humans, and they can recombine in those particular animals. In addition, wild aquatic birds carry all known strains of influenza. So, you've got this situation: In 2003, we had an H5N1 virus that jumped from birds into humans in a few isolated cases with an apparent mortality rate of 70 percent. Now luckily, that particular virus, although very scary at the time, did not transmit from person to person very easily. This year's H1N1 threat was actually a human, avian, swine mixture that arose in Mexico. It was easily transmitted, but, luckily, was pretty mild. And so, in a sense, our luck is holding out, but you know, another wild bird could fly over at anytime.
Co gorsze, najbardziej powszechna odmiana grypy - grypa typu A, atakuje również zwierzęta, które żyją w bliskiej obecności człowieka, przez co mogą mutować także w nich. Na dodatek, dzikie ptaki wodne roznoszą wszystkie możliwe odmiany grypy. W taki też sposób mieliśmy nie dawno kłopot. W 2003 panował wirus H5N1 który przeszedł w kilku przypadkach z ptaków na ludzi, ze śmiertelnością około 70 procent. Mieliśmy to szczęście, że odmiana ta, która wtedy bardzo nas przerażała, nie przenosiła się łatwo z człowieka na człowieka. Tego roku cierpieliśmy na H1N1, która powstała w Meksyku i dotykała ludzi, ptaków, świń. Była bardzo łatwo przenoszona ale na szczęście był to łagodny szczep. Tym razem wystarczyło nam szczęścia, ale w każdym momencie może do nas wrócić jak bumerang.
Now let's take a look at HIV. As variable as flu is, HIV makes flu look like the Rock of Gibraltar. The virus that causes AIDS is the trickiest pathogen scientists have ever confronted. It mutates furiously, it has decoys to evade the immune system, it attacks the very cells that are trying to fight it and it quickly hides itself in your genome. Here's a slide looking at the genetic variation of flu and comparing that to HIV, a much wilder target. In the video a moment ago, you saw fleets of new viruses launching from infected cells. Now realize that in a recently infected person, there are millions of these ships; each one is just slightly different. Finding a weapon that recognizes and sinks all of them makes the job that much harder.
Przypatrzmy się teraz HIV. Zdolność do mutacji wirusa grypy w porównaniu do HIV jest śmiesznie mała. Wirus powodujący AIDS jest najsprytniejszym patogenem spośród wszystkich znanych obecnie naukowcom. Mutuje szalenie szybko. Stosuje rozmaite sztuczki, by uchronić się przed układem odpornościowym. Atakuje tylko te komórki, które zaczną z nim walczyć. Na dodatek bardzo szybko ukrywa się w ludzkim genomie. Na tym slajdzie pokazana jest różnorodność genetyczna wirusa grypy i porównana do różnorodności HIV, która jest o wiele bardziej rozwinięta. Przed chwilą na animacji widzieliście całą flotę nowych wirusów wydostających się z zainfekowanych komórek. Teraz wyobraźcie sobie, że w organizmie zainfekowanej osoby jest miliony takich statków i każdy z nich jest nieco inny Dlatego też znalezienie broni, która rozpoznawałaby i zatapiałaby je wszystkie jest o wiele trudniejsze.
Now, in the 27 years since HIV was identified as the cause of AIDS, we've developed more drugs to treat HIV than all other viruses put together. These drugs aren't cures, but they represent a huge triumph of science because they take away the automatic death sentence from a diagnosis of HIV, at least for those who can access them. The vaccine effort though is really quite different. Large companies moved away from it because they thought the science was so difficult and vaccines were seen as poor business. Many thought that it was just impossible to make an AIDS vaccine, but today, evidence tells us otherwise.
Dziś, 27 lat po odkryciu, że HIV jest przyczyną AIDS, stworzyliśmy więcej leków na HIV niż na wszystkie inne wirusy razem. Leki te nie mogą całkowicie wyleczyć z choroby ale są wielkim triumfem nauki, ponieważ dzięki nim diagnoza HIV nie jest równoznaczna z wyrokiem śmierci -- przynajmniej dla tych, którzy się leczą. Chociaż wysiłki włożone w szczepionkę przeciw HIV są nieco inne. Wielkie spółki odwracają się od tego pomysłu, bo myślą, że badania będą tak trudne i kosztowne, że szczepionki będą nieudanym biznesem. Wielu ludzi myśli, że wynalezienie szczepionki na AIDS jest niemożliwe, ale dzisiejsze doniesienia mówią inaczej.
In September, we had surprising but exciting findings from a clinical trial that took place in Thailand. For the first time, we saw an AIDS vaccine work in humans -- albeit, quite modestly -- and that particular vaccine was made almost a decade ago. Newer concepts and early testing now show even greater promise in the best of our animal models. But in the past few months, researchers have also isolated several new broadly neutralizing antibodies from the blood of an HIV infected individual. Now, what does this mean? We saw earlier that HIV is highly variable, that a broad neutralizing antibody latches on and disables multiple variations of the virus. If you take these and you put them in the best of our monkey models, they provide full protection from infection. In addition, these researchers found a new site on HIV where the antibodies can grab onto, and what's so special about this spot is that it changes very little as the virus mutates. It's like, as many times as the virus changes its clothes, it's still wearing the same socks, and now our job is to make sure we get the body to really hate those socks.
We wrześniu mieliśmy niezwykle ekscytujące i zaskakujące odkrycie podczas eksperymentu klinicznego przeprowadzonego w Tajlandii. Po raz pierwszy w historii ujrzeliśmy skuteczną szczepionkę na AIDS, ale w mało huczny sposób. Idea tej szczepionki narodziła się prawie 10 lat temu. Najnowsze pomysły i aktualne badania bardzo obiecująco działają na naszych najlepszych zwierzęcych modelach. Jednak podczas ostatnich kilku miesięcy, badacze wyodrębnili kilka nowych przeciwciał o szerokim działaniu z krwi osobnika zarażonej HIV. Ale co to tak właściwie znaczy? Przed chwilą widzieliśmy, że wirus HIV ekstremalnie szybko się zmienia, tak, że żadne z przeciwciał nie potrafi przytwierdzić się i zneutralizować każdej wersji wirusa. Ale jeśli zarażony zostanie nasz najlepszy małpi model, to jego organizm wytworzy pełną odporność na wirusa. Co więcej, badacze odkryli słaby punkt wirusa HIV, w który mogą uderzyć przeciwciała. Na dodatek miejsce to prawie w ogóle nie ulega zmianie podczas mutacji. Innymi słowy, nawet jeśli wirus bardzo często zmienia swój ubiór, to nadal nosi te same skarpetki i nasza praca polega na tym, aby wytworzyć przeciwciała, które naprawdę nie znoszą tych skarpetek.
So what we've got is a situation. The Thai results tell us we can make an AIDS vaccine, and the antibody findings tell us how we might do that. This strategy, working backwards from an antibody to create a vaccine candidate, has never been done before in vaccine research. It's called retro-vaccinology, and its implications extend way beyond that of just HIV. So think of it this way. We've got these new antibodies we've identified, and we know that they latch onto many, many variations of the virus. We know that they have to latch onto a specific part, so if we can figure out the precise structure of that part, present that through a vaccine, what we hope is we can prompt your immune system to make these matching antibodies. And that would create a universal HIV vaccine. Now, it sounds easier than it is because the structure actually looks more like this blue antibody diagram attached to its yellow binding site, and as you can imagine, these three-dimensional structures are much harder to work on. And if you guys have ideas to help us solve this, we'd love to hear about it.
I co osiągnęliśmy? Tajskie wyniki mówią jasno, że da się wyprodukować szczepionkę na AIDS. Poszukiwania przeciwciał również idą w dobrym kierunku. Próbuje się również pracować na odwrót: na podstawie przeciwciała stworzyć szczepionkę, czego nigdy wcześniej nie osiągnięto. Jest to tzw. odwrotna wakcynologia z którego wnioski wykraczają daleko poza pokonanie samego HIV. Wyobraźcie to sobie w ten sposób. Wiemy, że przeciwciała, które wyizolowaliśmy, są zdolne neutralizować wiele wariacji wirusa. Wiemy też, że muszą się one przytwierdzać do tego specyficznego punktu. Jeśli go opiszemy, dokładnie zbadamy i zaprezentujemy poprzez szczepionkę, to mamy nadzieję, że nasz układ immunologiczny zacznie produkować pasujące przeciwciała. Ten sposób pozwoli stworzyć uniwersalną szczepionkę na HIV. Brzmi to o wiele prościej niż jest w rzeczywistości, ponieważ kształt przeciwciała wygląda jak ten niebieski model na grafice, i musi przytwierdzić się do punktu wiązania zaznaczonego na żółto. Jak widzicie, te trójwymiarowe struktury sprawiają, że praca nad nimi jest bardzo trudna. I jeśli ktoś z was ma pomysł jak rozwiązać ten problem, z przyjemnością go wysłuchamy.
But, you know, the research that has occurred from HIV now has really helped with innovation with other diseases. So for instance, a biotechnology company has now found broadly neutralizing antibodies to influenza, as well as a new antibody target on the flu virus. They're currently making a cocktail -- an antibody cocktail -- that can be used to treat severe, overwhelming cases of flu. In the longer term, what they can do is use these tools of retro-vaccinology to make a preventive flu vaccine. Now, retro-vaccinology is just one technique within the ambit of so-called rational vaccine design.
Ale te badania, które były prowadzone nad wirusem HIV, bardzo pomogły wprowadzić innowacje do leczenia innych chorób. Na przykład pewna spółka biotechnologiczna wynalazła nie dawno szeroko działające przeciwciała na wirus grypy, jak również przeciwciało skierowane na konkretnego wirusa. Tworzą oni koktajl, koktajl przeciwciał, który może być użyty do leczenia kilku bardzo poważnych odmian grypy. W najbliższej przyszłości będą starali się użyć odwrotnej wakcynologii by wyprodukować zapobiegawczą szczepionkę na grypę. W obecnej chwili odwrotna wakcynologia jest tylko jedną z całej grupy technik tzw. racjonalnego projektowania szczepionek.
Let me give you another example. We talked about before the H and N spikes on the surface of the flu virus. Notice these other, smaller protuberances. These are largely hidden from the immune system. Now it turns out that these spots also don't change much when the virus mutates. If you can cripple these with specific antibodies, you could cripple all versions of the flu. So far, animal tests indicate that such a vaccine could prevent severe disease, although you might get a mild case. So if this works in humans, what we're talking about is a universal flu vaccine, one that doesn't need to change every year and would remove the threat of death. We really could think of flu, then, as just a bad cold.
Podam wam inny przykład. Mówiłem przed chwilą o wypustkach H i M tworzące otoczkę białkową na powierzchni wirusa grypy. Spójrzcie na te małe wypukłości. Są one prawie niewidoczne dla systemu odpornościowego. Okazuje się, że te punkty również nie zmieniają się podczas mutacji wirusa. Jeśli można by zaatakować je specjalnymi przeciwciałami, można by atakować wszystkie odmiany wirusa grypy. Jak dotąd, testy na zwierzętach wykazały, że taka szczepionka mogłaby zapobiec wielu chorobom, lub przynajmniej zapewnić łagodniejszy przebieg. Tak więc, jeśli szczepionka ta działałyby na ludziach byłaby uniwersalną szczepionką na grypę, która nie wymaga zmian każdego roku, i pomogłaby wyeliminować wszystkie śmiertelne przypadki. Wtedy dopiero moglibyśmy myśleć o grypie, że jest jedynie cięższym przeziębieniem.
Of course, the best vaccine imaginable is only valuable to the extent we get it to everyone who needs it. So to do that, we have to combine smart vaccine design with smart production methods and, of course, smart delivery methods. So I want you to think back a few months ago. In June, the World Health Organization declared the first global flu pandemic in 41 years. The U.S. government promised 150 million doses of vaccine by October 15th for the flu peak. Vaccines were promised to developing countries. Hundreds of millions of dollars were spent and flowed to accelerating vaccine manufacturing. So what happened?
Oczywiście nawet najlepsza szczepionka działa tylko wtedy, gdy poda się ją ludziom, którzy jej potrzebują. Aby tego dokonać, musimy połączyć przemyślane projektowanie szczepionek, z mądrymi sposobami produkcji i oczywiście skutecznymi metodami podawania. Przypomnijcie sobie co działo się kilka miesięcy temu. W czerwcu, Światowa Organizacja Zdrowia ogłosiła pierwszą od 41 lat światową pandemię grypy. Rząd Stanów Zjednoczonych zgromadził 150 milionów dawek szczepionki do 15 października, kiedy to miał być szczyt zachorowalności. Obiecano szczepionki dla krajów rozwijających się. Setki milionów dolarów wydano aby rozwinąć produkcję szczepionek. I co się stało?
Well, we first figured out how to make flu vaccines, how to produce them, in the early 1940s. It was a slow, cumbersome process that depended on chicken eggs, millions of living chicken eggs. Viruses only grow in living things, and so it turned out that, for flu, chicken eggs worked really well. For most strains, you could get one to two doses of vaccine per egg. Luckily for us, we live in an era of breathtaking biomedical advances. So today, we get our flu vaccines from ... chicken eggs, (Laughter) hundreds of millions of chicken eggs. Almost nothing has changed. The system is reliable but the problem is you never know how well a strain is going to grow. This year's swine flu strain grew very poorly in early production: basically .6 doses per egg. So, here's an alarming thought. What if that wild bird flies by again? You could see an avian strain that would infect the poultry flocks, and then we would have no eggs for our vaccines. So, Dan [Barber], if you want billions of chicken pellets for your fish farm, I know where to get them. So right now, the world can produce about 350 million doses of flu vaccine for the three strains, and we can up that to about 1.2 billion doses if we want to target a single variant like swine flu. But this assumes that our factories are humming because, in 2004, the U.S. supply was cut in half by contamination at one single plant. And the process still takes more than half a year.
Na początku, w latach 40. odkryliśmy jak produkować szczepionki. Była to powolna, nieporęczna metoda, która opierała się na kurzych jajach -- milionach żywych kurzych jaj. Wirusy rozwijają się tylko w żywych organizmach i okazało się, że dla wirusa grypy, kurze jaja bardzo dobrze się sprawdzają. Dla większości szczepów można uzyskać jedną, do dwóch dawek z jednego jajka. Na szczęście żyjemy w czasach zapierających dech w piersiach odkryć biomedycznych. Dlatego dzisiaj szczepionki na grypę pozyskujemy z ... ... kurzych jaj, (Śmiech) setek milionów kurzych jaj. Prawie nic nie zmieniło się od tamtych czasów. Ten sposób się sprawdza. Ale problem jest w tym, że nigdy nie wiesz, jak dobrze rozwija się dany szczep. Tego roku odmiana świńskiej grypy rozwijała się bardzo słabo, około 0.6 dawki na jajko. Jest to bardzo niepokojące. Co jeśli jeszcze raz nawiedzi nas grypa roznoszona przez dzikie ptaki? Ona atakuje również fermy drobiu, a wtedy nie mielibyśmy odpowiednich jaj do produkcji szczepionek. Dan [Barber], jeśli chcesz olbrzymich ilości kurzej karmy aby nakarmić twoją hodowlę ryb, wiem, gdzie ją dostaniesz. Na dzień dzisiejszy placówki na całym świecie mogą wytworzyć 350 milionów dawek szczepionki na grypę zabezpieczającą przed trzema szczepami. Możemy zwiększyć tę liczbę do 1.2 miliarda dawek, jeśli chcielibyśmy utworzyć szczepionkę na tylko jedną odmianę wirusa, jak świńska grypa. Ale tylko przy założeniu, że fabryki będą pracować bez przeszkód. W 2004 amerykańskie zapasy były zmniejszone o połowę, przez skażenie w jednej z fabryk. Metoda ta, w dalszym ciągu pochłania ponad pół roku.
So are we better prepared than we were in 1918? Well, with the new technologies emerging now, I hope we can say definitively, "Yes." Imagine we could produce enough flu vaccine for everyone in the entire world for less than half of what we're currently spending now in the United States. With a range of new technologies, we could. Here's an example: A company I'm engaged with has found a specific piece of the H spike of flu that sparks the immune system. If you lop this off and attach it to the tail of a different bacterium, which creates a vigorous immune response, they've created a very powerful flu fighter. This vaccine is so small it can be grown in a common bacteria, E. coli. Now, as you know, bacteria reproduce quickly -- it's like making yogurt -- and so we could produce enough swine origin flu for the entire world in a few factories, in a few weeks, with no eggs, for a fraction of the cost of current methods.
Tak więc, czy jesteśmy przygotowani na pandemię lepiej, niż byliśmy w 1918? Biorąc pod uwagę najnowsze technologie, z którymi się stykamy sądzę, że możemy śmiało powiedzieć "Tak." Jak myślicie? Czy jesteśmy w stanie wyprodukować szczepionkę dla każdego na całym świecie za mniej niż połowę tego co aktualnie wydają Stany Zjednoczone? Dzięki najnowszym technologiom, możemy. Już podaje przykład. Spółka z którą jestem związany odkryła niedawno, że za pobudzenie do działania układu odpornościowego odpowiada jedna z wypustek typu H tworzących otoczkę białkową. Jeśliby tak odciąć to ostrze, i przytwierdzić do innej bakterii, która powodowałaby żywiołową odpowiedź organizmu, stworzylibyśmy bardzo silnego wroga grypy. Szczepionka ta jest tak mała, że można ją wyhodować w powszechnej bakterii E.coli. Jak dobrze wiecie, bakterie mnożą się bardzo szybko. Odbywałoby się to jak produkcja jogurtu. Potrafilibyśmy wyprodukować wystarczającą ilość na grypę pochodzenia świńskiego dla każdego na świecie, w zaledwie kilku fabrykach, przez kilka tygodni, bez żadnych jajek, za niewielką część kwoty, która jest przeznaczana na obecne metody.
(Applause)
(Brawa)
So here's a comparison of several of these new vaccine technologies. And, aside from the radically increased production and huge cost savings -- for example, the E. coli method I just talked about -- look at the time saved: this would be lives saved. The developing world, mostly left out of the current response, sees the potential of these alternate technologies and they're leapfrogging the West. India, Mexico and others are already making experimental flu vaccines, and they may be the first place we see these vaccines in use. Because these technologies are so efficient and relatively cheap, billions of people can have access to lifesaving vaccines if we can figure out how to deliver them.
Tutaj mamy porównanie kilku najnowszych technologii produkcji szczepionek. Poza tym, że produkcja zostałaby radykalnie zwiększona, a potężne kwoty pieniędzy zaoszczędzone, to na przykład metoda oparta na E. coli, o której mówiłem, zabiera o wiele mniej czasu -- ratuje o wiele więcej żyć. Kraje rozwijające się, porzuciły aktualne rozwiązania widząc potencjał alternatywnych metod, i w tej dziedzinie wyprzedzają Zachód. Indie, Meksyk oraz inne kraje produkują eksperymentalne szczepionki na grypę, i mogą być pierwszymi krajami, w których zobaczymy takie szczepionki w użyciu. Technologie te są niesamowicie wydajne i stosunkowo tanie, dlatego też miliardy ludzi mogłoby mieć dostęp do ratujących życie szczepionek, jeśli znajdziemy sposób, jak je dostarczyć.
Now think of where this leads us. New infectious diseases appear or reappear every few years. Some day, perhaps soon, we'll have a virus that is going to threaten all of us. Will we be quick enough to react before millions die? Luckily, this year's flu was relatively mild. I say, "luckily" in part because virtually no one in the developing world was vaccinated. So if we have the political and financial foresight to sustain our investments, we will master these and new tools of vaccinology, and with these tools we can produce enough vaccine for everyone at low cost and ensure healthy productive lives. No longer must flu have to kill half a million people a year. No longer does AIDS need to kill two million a year. No longer do the poor and vulnerable need to be threatened by infectious diseases, or indeed, anybody. Instead of having Vaclav Smil's "massively fatal discontinuity" of life, we can ensure the continuity of life. What the world needs now are these new vaccines, and we can make it happen.
Gdzie więc zmierzamy? Nowe choroby zakaźne powstają, lub pojawiają się na nowo co kilka lat. Pewnego dnia, być może w niedalekiej przyszłości będziemy mieli do czynienia z wirusem, który zagrozi nam wszystkim. Czy będziemy w stanie zadziałać na tyle szybko, zanim zginą miliony? Całe szczęście, tego roku grypa była stosunkowo łagodna. Powiedziałem "szczęście", ponieważ praktycznie nikt nie był szczepiony w krajach rozwijających się. Jeśli potrafimy spojrzeć w przyszłość polityczną i finansową by podtrzymać nasze obecne inwestycje musimy skupić się na nowych metodach w produkcji szczepionek. Dzięki tym metodom, możemy produkować wystarczającą ilość szczepionek niskim kosztem i zapewnić zdrowe i produktywne życie. Nigdy więcej grypa nie będzie zabijała co roku pół miliona ludzi. Nigdy więcej AIDS nie będzie co roku zabijało dwóch milionów ludzi. Nigdy więcej biedni oraz inni narażeni, nie będą cierpieli na choroby zakaźne. Choroby zakaźne przestaną być groźne. Zamiast "wielkich śmiertelnych przerw" Vaclav'a Smil'a możemy zapewnić ciągłość życia. Dziś świat potrzebuje nowych szczepionek, a my możemy tego dokonać.
Thank you very much.
Dziękuję za uwagę.
(Applause)
(Brawa)
Chris Anderson: Thank you. (Applause) Thank you. So, the science is changing. In your mind, Seth -- I mean, you must dream about this -- what is the kind of time scale on, let's start with HIV, for a game-changing vaccine that's actually out there and usable?
Chris Anderson: Dziękuje. (Brawa) Dziękuję. Nauka się rozwija: jak sądzisz, Seth -- myślę, że o tym na pewno marzysz -- jak dużo czasu upłynie zanim -- w przypadku HIV -- do użycia zostanie wprowadzona ta rewolucyjna szczepionka?
SB: The game change can come at any time, because the problem we have now is we've shown we can get a vaccine to work in humans; we just need a better one. And with these types of antibodies, we know humans can make them. So, if we can figure out how to do that, then we have the vaccine, and what's interesting is there already is some evidence that we're beginning to crack that problem. So, the challenge is full speed ahead.
SB: Rewolucja może nadejść w każdej chwili, ponieważ problem jest w tym, że właściwie mamy szczepionkę działającą na ludziach, po prostu potrzebujemy lepszej. A z tego typu przeciwciałami, wiemy, że ludzie mogą je wytwarzać. Jeśli odkryjemy jak to osiągnąć, wtedy powstanie szczepionka. Interesujące jest to, że mamy pewne znaki mówiące, że zaczynamy rozwiązywać ten problem. Prace nad tym idą pełną parą.
CA: In your gut, do you think it's probably going to be at least another five years?
CA: Uważasz, że może się to stać w ciągu najbliższych 5 lat?
SB: You know, everybody says it's 10 years, but it's been 10 years every 10 years. So I hate to put a timeline on scientific innovation, but the investments that have occurred are now paying dividends.
SB: Widzisz, każdy mówi że w ciągu 10, ale powtarzają to co 10 lat. Nie znoszę wprowadzania osi czasu do odkryć naukowych, ale inwestycje, jakie zostały w to włożone zaczynają się zwracać.
CA: And that's the same with universal flu vaccine, the same kind of thing?
CA: Czy podobnie sprawa wygląda ze szczepionką na grypę?
SB: I think flu is different. I think what happened with flu is we've got a bunch -- I just showed some of this -- a bunch of really cool and useful technologies that are ready to go now. They look good. The problem has been that, what we did is we invested in traditional technologies because that's what we were comfortable with. You also can use adjuvants, which are chemicals you mix. That's what Europe is doing, so we could have diluted out our supply of flu and made more available, but, going back to what Michael Specter said, the anti-vaccine crowd didn't really want that to happen.
SB: Z grypą jest trochę inaczej. Uważam, że w sprawie grypy powstała masa -- części z nich dziś przedstawiłem -- masa naprawdę genialnych i przydatnych technologii, które są gotowe do wprowadzenia. Wyglądają naprawdę dobrze, ale problem jest w tym, że nadal za dużo inwestujemy w tradycyjne rozwiązania, ponieważ jest nam z nimi wygodnie. Można też używać adiuwantów, które są mieszaniną związków chemicznych. Nad tym właśnie pracuje się w Europie, można więc rozcieńczyć nasze zapasy szczepionek na grypę i uczynić je łatwiej dostępnymi. Ale nawiązując do tego, co mówił Michael Specter, przeciwnicy szczepień nie chcą do tego dopuścić.
CA: And malaria's even further behind?
CA: Czy malaria jest jeszcze dalej?
SB: No, malaria, there is a candidate that actually showed efficacy in an earlier trial and is currently in phase three trials now. It probably isn't the perfect vaccine, but it's moving along.
SB: Nie, w przypadku malarii jest kandydat który wykazał się skutecznością we wczesnych badaniach i jest obecnie w trzeciej fazie badań. Prawdopodobnie nie jest to doskonała szczepionka, ale wszystko zmierza do przodu.
CA: Seth, most of us do work where every month, we produce something; we get that kind of gratification. You've been slaving away at this for more than a decade, and I salute you and your colleagues for what you do. The world needs people like you. Thank you.
CA: Seth, większość z nas pracuje, i co miesiąc ma coś w rodzaju, osiągnięcia jakiegoś celu, i mamy z tego jakiś rodzaj satysfakcji. Ty harujesz nad tym tematem ponad 10 lat, dlatego składam pokłon tobie, i twoim kolegom z pracy, za to co robicie. Świat potrzebuje ludzi takich jak ty. Dziękuję.
SB: Thank you.
SB: Dziękuję.
(Applause)
(Brawa)