Do you worry about what is going to kill you? Heart disease, cancer, a car accident? Most of us worry about things we can't control, like war, terrorism, the tragic earthquake that just occurred in Haiti. But what really threatens humanity? A few years ago, Professor Vaclav Smil tried to calculate the probability of sudden disasters large enough to change history. He called these, "massively fatal discontinuities," meaning that they could kill up to 100 million people in the next 50 years. He looked at the odds of another world war, of a massive volcanic eruption, even of an asteroid hitting the Earth. But he placed the likelihood of one such event above all others at close to 100 percent, and that is a severe flu pandemic. Now, you might think of flu as just a really bad cold, but it can be a death sentence. Every year, 36,000 people in the United States die of seasonal flu. In the developing world, the data is much sketchier but the death toll is almost certainly higher. You know, the problem is if this virus occasionally mutates so dramatically, it essentially is a new virus and then we get a pandemic.
Avete paura di quale sarà la causa della vostra morte? Malattie cardiache, cancro un incidente stradale? Ci preoccupiamo delle cose che non possiamo controllare come la guerra, il terrorismo il tragico terremoto che ha colpito Haiti. Ma che cosa veramente minaccia l'umanità? Qualche anno fa il professor Vaclav Smil cercò di calcolare la probabilità di un disastro improvviso e abbastanza grande da cambiare la storia. Chiamò questi eventi "discontinuità mortali di massa" per indicare che avrebbero potuto uccidere fino a 100 milioni di persone nei prossimi 50 anni. Guardò alle probabilità di un'altra guerra mondiale di un'enorme eruzione vulcanica anche di un asteroide colpire la Terra. Ma per un evento in particolare assegnò una probabilità più alta rispetto agli altri vicino al 100%. Si trattava di un'epidemia di influenza. Ora: potreste pensare a un'influenza come a un brutto raffreddore. Ma potrebbe anche trattarsi di una condanna a morte. Ogni anno, negli Stati Uniti muoiono 36.000 persone di influenza stagionale. Nei Paesi in via di sviluppo i dati sono meno certi ma la mortalità è quasi certamente più alta. Il vero problema è se il virus muta occasionalmente in modo così profondo da diventare praticamente un virus nuovo. A quel punto scoppia un'epidemia.
In 1918, a new virus appeared that killed some 50 to 100 million people. It spread like wildfire and some died within hours of developing symptoms. Are we safer today? Well, we seem to have dodged the deadly pandemic this year that most of us feared, but this threat could reappear at any time. The good news is that we're at a moment in time when science, technology, globalization is converging to create an unprecedented possibility: the possibility to make history by preventing infectious diseases that still account for one-fifth of all deaths and countless misery on Earth. We can do this. We're already preventing millions of deaths with existing vaccines, and if we get these to more people, we can certainly save more lives. But with new or better vaccines for malaria, TB, HIV, pneumonia, diarrhea, flu, we could end suffering that has been on the Earth since the beginning of time.
Nel 1918 apparve un nuovo virus che uccise fra i 50 e i 100 milioni di persone. Si diffuse senza controllo come un incendio. Alcuni morirono a poche ore dai primi sintomi. Oggi siamo più al sicuro? Sembra che quest' anno abbiamo evitato l'epidemia potenzialmente fatale che molti di noi temevano. Ma questo pericolo potrebbe presentarsi in ogni momento. La buona notizia è che viviamo in un epoca in cui la scienza, la tecnologia e la globalizzazione convergono per offrire una possibilità senza precedenti: la possibilità di fare la storia prevenendo malattie infettive che causano ancora oggi un quinto delle morti sul pianeta e sofferenze senza fine. Oggi possiamo farcela. Grazie ai vaccini di oggi possiamo prevenire già milioni di morti. Se riusciamo a estendere l'accesso ad ancora più persone possiamo salvare sicuramente molte altre vite. Ma con vaccini nuovi o migliori per malaria, tubercolosi, Hiv polmonite, diarrea, influenza potremmo eliminare le malattie che affliggono il pianeta dall' inizio dei tempi.
So, I'm here to trumpet vaccines for you. But first, I have to explain why they're important because vaccines, the power of them, is really like a whisper. When they work, they can make history, but after a while you can barely hear them. Now, some of us are old enough to have a small, circular scar on our arms from an inoculation we received as children. But when was the last time you worried about smallpox, a disease that killed half a billion people last century and no longer is with us? Or polio? How many of you remember the iron lung? We don't see scenes like this anymore because of vaccines.
Sono qui per promuovere i vaccini. Ma prima, devo spiegare perché sono importanti. L'efficacia dei vaccini è come quella di un bisbiglio. Quando funzionano, passano alla storia ma dopo un po' di tempo non ci fai più caso. Alcuni di noi sono abbastanza anziani da avere sul braccio la piccola cicatrice di una iniezione fatta da piccoli. Ma da quando non vi preoccupa più il vaiolo una malattia che ha fatto mezzo milione di vittime il secolo passato e oggi non esiste più? O la poliomelite: quanti di voi ricordano il polmone d'acciaio? Non vediamo più immagini come queste grazie ai vaccini.
Now, it's interesting because there are 30-odd diseases that can be treated with vaccines now, but we're still threatened by things like HIV and flu. Why is that? Well, here's the dirty little secret. Until recently, we haven't had to know exactly how a vaccine worked. We knew they worked through old-fashioned trial and error. You took a pathogen, you modified it, you injected it into a person or an animal and you saw what happened. This worked well for most pathogens, somewhat well for crafty bugs like flu, but not at all for HIV, for which humans have no natural immunity.
La cosa è interessante perché oggi possiamo curare 30 malattie attraverso i vaccini, anche se siamo ancora minacciati da cose come Hiv e influenza. Perché? Ecco il segreto. Fino a tempi recenti, non abbiamo dovuto sapere esattamente come funzionani i vaccini. Sapevamo che funzionavano col vecchio metodo per prove ed errori. Prendi un agente patogeno, lo modifichi lo inetti in una persona o in un animale e stai a vedere che cosa succede. Ha funzionato bene per la maggior parte degli agenti patogeni abbastanza bene per germi smaliziati come quelli dell'influenza ma per niente con i virus dell'Hiv verso cui gli esseri umani non hanno un' immunità naturale.
So let's explore how vaccines work. They basically create a cache of weapons for your immune system which you can deploy when needed. Now, when you get a viral infection, what normally happens is it takes days or weeks for your body to fight back at full strength, and that might be too late. When you're pre-immunized, what happens is you have forces in your body pre-trained to recognize and defeat specific foes. So that's really how vaccines work. Now, let's take a look at a video that we're debuting at TED, for the first time, on how an effective HIV vaccine might work.
Vediamo adesso come funzionano i vaccini. In pratica creano una riserva di armi che il nostro sistema immunitario usa quando servono. quando vi prendete un'infezione di origine virale quel che succede normalmente è che ci vogliono giorni o settimane prima che il corpo possa rispondere all'attacco con tutte le proprie forze e certe volte potrebbe essere troppo tardi. Se invece vi immunizzate preventivamente nel vostro corpo avete forze di difesa già addestrate per riconoscere e debellare nemici specifici. Ecco come funzionano i vaccini. Vediamo adesso un video che mostriamo per la prima volta qui a TED su come funzionerebbe un vaccino efficace contro l'Hiv.
(Music)
(musica)
Narrator: A vaccine trains the body in advance how to recognize and neutralize a specific invader. After HIV penetrates the body's mucosal barriers, it infects immune cells to replicate. The invader draws the attention of the immune system's front-line troops. Dendritic cells, or macrophages, capture the virus and display pieces of it. Memory cells generated by the HIV vaccine are activated when they learn HIV is present from the front-line troops. These memory cells immediately deploy the exact weapons needed. Memory B cells turn into plasma cells, which produce wave after wave of the specific antibodies that latch onto HIV to prevent it from infecting cells, while squadrons of killer T cells seek out and destroy cells that are already HIV infected. The virus is defeated. Without a vaccine, these responses would have taken more than a week. By that time, the battle against HIV would already have been lost.
Un vaccino addestra il corpo preventivamente a riconoscere e neutralizzare un invasore specifico. Dopo aver penetrato le barriere delle mucose il virus Hiv infetta le cellule immunitarie per riprodursi. L' invasore attira l'attenzione delle sentinelle di prima linea del sistema immunitario. Le cellule dendritiche, o macrofagi catturano il virus e ne mostrano alcuni componenti. Le cellule di memoria generate dal vaccino dell'Hiv si attivano quando apprendono della presenza del virus dalle sentinelle di prima linea. Queste cellule rilasciano immediatamente le armi necessarie per combattere. Le cellule di memoria B diventano cellule del plasma che producono onda dopo onda anticorpi specifici che si attaccano al virus per impedirgli di infettare altre cellule mentre squadroni di cellule T cercano e neutralizzano quelle cellule che sono già state infettate. Il virus è sconfitto. Senza un vaccino queste risposte immunitarie avrebbero richiesto più di una settimana. a quel punto, la battaglia contro l'Hiv sarebbe già stata persa.
Seth Berkley: Really cool video, isn't it? The antibodies you just saw in this video, in action, are the ones that make most vaccines work. So the real question then is: How do we ensure that your body makes the exact ones that we need to protect against flu and HIV? The principal challenge for both of these viruses is that they're always changing. So let's take a look at the flu virus. In this rendering of the flu virus, these different colored spikes are what it uses to infect you. And also, what the antibodies use is a handle to essentially grab and neutralize the virus. When these mutate, they change their shape, and the antibodies don't know what they're looking at anymore. So that's why every year you can catch a slightly different strain of flu. It's also why in the spring, we have to make a best guess at which three strains are going to prevail the next year, put those into a single vaccine and rush those into production for the fall.
Un bel video, non è vero? Gli anticorpi che avete visto in azione nel video sono quelli che fanno funzionare la maggior parte dei vaccini. Quindi la vera domanda è questa: come facciamo ad essere sicuri che il nostro corpo produca gli anticorpi necessari per proteggerci dall'influenza e dall'Hiv? La sfida principale per vincere entrambi i virus è che mutano continuamente. Guardiamo adesso il virus dell'influenza. In questo modello di virus vedete le punte colorate che usa per infettare. Gli anticorpi usano essenzialmente dei manici per agguantare il virus e neutralizzarlo. Quando i virus mutano, cambiano la loro forma e gli anticorpi non sanno più che cosa cercare. Per questo ogni anno potete prendere una forma di influenza sempre diversa. Ed è anche per questo che in primavera dobbiamo indovinare quale dei tre ceppi di influenza prevarrà l'anno dopo metterli in un unico vaccino e mandarli rapidamente in produzione per l'autunno.
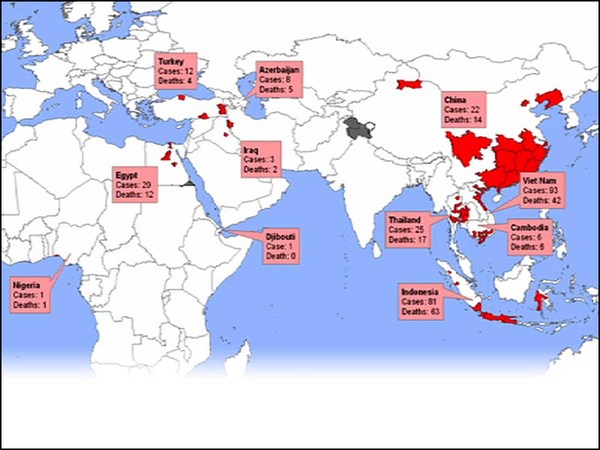
Even worse, the most common influenza -- influenza A -- also infects animals that live in close proximity to humans, and they can recombine in those particular animals. In addition, wild aquatic birds carry all known strains of influenza. So, you've got this situation: In 2003, we had an H5N1 virus that jumped from birds into humans in a few isolated cases with an apparent mortality rate of 70 percent. Now luckily, that particular virus, although very scary at the time, did not transmit from person to person very easily. This year's H1N1 threat was actually a human, avian, swine mixture that arose in Mexico. It was easily transmitted, but, luckily, was pretty mild. And so, in a sense, our luck is holding out, but you know, another wild bird could fly over at anytime.
Ancora peggio: l'influenza più comune, la A infetta anche gli animali che vivono in prossimità degli uomini e possono ricombinarsi negli stessi animali. Inoltre, gli uccelli acquatici selvatici sono portatori di tutti i ceppi dell'influenza. Questo è quanto. Nel 2003 abbiamo avuto il virus H5N1 che è passato dagli uccelli agli uomini in alcuni casi isolati con una mortalità apparente del 70%. Fortunatamente, quel virus specifico nonostante sembrasse molto pericoloso non si trasmise da persona a persona molto facilmente. Quest'anno il pericolo dell'H1N1 è stato un misto fra umano, aviario e suino comparso in Messico. Si trasmetteva facilmente ma fortunatamente era abbastanza lieve. Dunque, in un certo senso siamo fortunati ma un uccello selvatico potrebbe volare da noi in ogni momento.
Now let's take a look at HIV. As variable as flu is, HIV makes flu look like the Rock of Gibraltar. The virus that causes AIDS is the trickiest pathogen scientists have ever confronted. It mutates furiously, it has decoys to evade the immune system, it attacks the very cells that are trying to fight it and it quickly hides itself in your genome. Here's a slide looking at the genetic variation of flu and comparing that to HIV, a much wilder target. In the video a moment ago, you saw fleets of new viruses launching from infected cells. Now realize that in a recently infected person, there are millions of these ships; each one is just slightly different. Finding a weapon that recognizes and sinks all of them makes the job that much harder.
Guardiamo adesso l'Hiv. Per quanto variabile possa essere l'influenza questo virus la fa sembrare come la Rocca di Gibilterra. Il virus che provoca l'Aids è il più difficile che gli scienziati abbiano mai affrontato. Muta incredibilmente. Mette in atto dei trucchi per ingannare il sistema immunitario. Attacca proprio le cellule che sono fatte per distruggerlo e rapidamente si nasconde nel genoma. Ecco un grafico che mostra la variazione genetica dell'influenza a confronto con quella dell'Hiv: un obbiettivo molto più difficile. Nel video di un attimo fa avete visto nuovi virus che emergevano da cellule infette. Dovete sapere che in un individuo infettato di recente ci sono milioni di queste navi ciascuna un po' diversa dalle altre. Trovare un arma che le riconosca e le affondi tutte rende il compito molto difficile.
Now, in the 27 years since HIV was identified as the cause of AIDS, we've developed more drugs to treat HIV than all other viruses put together. These drugs aren't cures, but they represent a huge triumph of science because they take away the automatic death sentence from a diagnosis of HIV, at least for those who can access them. The vaccine effort though is really quite different. Large companies moved away from it because they thought the science was so difficult and vaccines were seen as poor business. Many thought that it was just impossible to make an AIDS vaccine, but today, evidence tells us otherwise.
Nei 27 anni successivi a quando l'Hiv è stato identificato come la causa dell'Aids abbiamo sviluppato più farmaci per trattare questo virus rispetto a quelli per trattare tutti gli altri virus messi insieme. Questi farmaci non guariscono dall'infezione ma rappresentano un grande successo scientifico perché hanno escluso una sentenza di morte sicura una volta diagnosticata l'infezione da Hiv almeno a quelle persone che hanno accesso alle cure. Lo sforzo per trovare un vaccino è davvero un'altra cosa. Grandi industrie farmaceutiche hanno rinunciato perché pensavano che la ricerca fosse troppo difficile e i vaccini erano visti come un cattivo affare. Molti pensavano che un vaccino per l'Aids fosse impossibile ma oggi l'evidenza ci dice l'opposto.
In September, we had surprising but exciting findings from a clinical trial that took place in Thailand. For the first time, we saw an AIDS vaccine work in humans -- albeit, quite modestly -- and that particular vaccine was made almost a decade ago. Newer concepts and early testing now show even greater promise in the best of our animal models. But in the past few months, researchers have also isolated several new broadly neutralizing antibodies from the blood of an HIV infected individual. Now, what does this mean? We saw earlier that HIV is highly variable, that a broad neutralizing antibody latches on and disables multiple variations of the virus. If you take these and you put them in the best of our monkey models, they provide full protection from infection. In addition, these researchers found a new site on HIV where the antibodies can grab onto, and what's so special about this spot is that it changes very little as the virus mutates. It's like, as many times as the virus changes its clothes, it's still wearing the same socks, and now our job is to make sure we get the body to really hate those socks.
A settembre abbiamo fatto scoperte inaspettate ma eccitanti da un esperimento clinico in Tailandia. Per la prima volta abbiamo visto un vaccino per l'Aids funzionare sull'uomo anche se a livelli modesti. Quel vaccino specifico fu realizzato quasi dieci anni fa. Nuove idee e test preliminari mostrano un potenziale ancora maggiore in modelli animali. Pochi mesi fa dei ricercatori hanno anche isolato alcuni nuovi anticorpi con potere ampiamente neutralizzante dal sangue di un individuo sieropositivo. Che cosa vuol dire? Abbiamo visto prima che l'Hiv cambia molto e che un anticorpo a largo raggio di neutralizzazione si accoppia e distrugge diversi ceppi del virus. Se li prendete e li mettete nei migliori nostri modelli di scimmie garantiscono una protezione totale dal virus. Per di più questi scienziati hanno trovato un nuovo punto nel virus a cui gli anticorpi si possono attaccare. L'importanza di questo punto è che cambia molto poco al mutare del virus. È come se per quanto il virus si cambi di vestito porti sempre le stesse calze e il nostro compito è quello di convincere il nostro corpo a odiare quelle calze.
So what we've got is a situation. The Thai results tell us we can make an AIDS vaccine, and the antibody findings tell us how we might do that. This strategy, working backwards from an antibody to create a vaccine candidate, has never been done before in vaccine research. It's called retro-vaccinology, and its implications extend way beyond that of just HIV. So think of it this way. We've got these new antibodies we've identified, and we know that they latch onto many, many variations of the virus. We know that they have to latch onto a specific part, so if we can figure out the precise structure of that part, present that through a vaccine, what we hope is we can prompt your immune system to make these matching antibodies. And that would create a universal HIV vaccine. Now, it sounds easier than it is because the structure actually looks more like this blue antibody diagram attached to its yellow binding site, and as you can imagine, these three-dimensional structures are much harder to work on. And if you guys have ideas to help us solve this, we'd love to hear about it.
Siamo arrivati a un punto importante. I risultati delle ricerche tailandesi ci dicono che possiamo fare un vaccino e le ricerche sugli anticorpi ci dicono come farlo. Questa strategia di lavorare a ritroso a partire da un anticorpo per creare un vaccino non è mai stata tentata prima nella ricerca sui vaccini. Si chiama retro-vaccinologia e le sue implicazioni si estendono ben oltre il virus Hiv. Pensateci in questi termini: abbiamo identificato questi nuovi anticorpi e sappiamo che si combinano con molte variazioni del virus. Sappiamo che si devono agganciare a un punto specifico così, se scopriamo la struttura precisa di quel punto e la evidenziamo con un vaccino possiamo sperare che il sistema immunitario produca gli anticorpi corrispondenti. Questo creerebbe un vaccino universale per l'Hiv. Sembra più facile di quanto lo sia davvero perché la struttura assomiglia molto a questo diagramma blu di anticorpo attaccato al suo punto di collegamento giallo. Come potete immaginare, queste strutture tridimensionali sono molto più difficili da trattare. Se voi avete delle idee utili per risolvere il problema saremmo felici di sentirle.
But, you know, the research that has occurred from HIV now has really helped with innovation with other diseases. So for instance, a biotechnology company has now found broadly neutralizing antibodies to influenza, as well as a new antibody target on the flu virus. They're currently making a cocktail -- an antibody cocktail -- that can be used to treat severe, overwhelming cases of flu. In the longer term, what they can do is use these tools of retro-vaccinology to make a preventive flu vaccine. Now, retro-vaccinology is just one technique within the ambit of so-called rational vaccine design.
Dovete sapere che la ricerca che è stata fatta fino a oggi sull'Hiv ha portato a molte innovazioni nella cura di altre malattie. Per esempio, una società di biotecnologie ha trovato degli anticorpi per l'influenza con un'ampia azione neutralizzante così come un nuovo bersaglio per anticorpi sul virus dell'influenza. In questo momento si stanno preparando un cocktail di anticorpi per curare casi di influenza gravi. Nel lungo periodo, quello che si può fare è usare questi strumenti di retrovaccinologia per fare un vaccino preventivo dell'influenza. Oggi la retrovaccinologia è solo una delle tecniche nell'ambito della sperimentazione dei vaccini cosiddetti "razionali".
Let me give you another example. We talked about before the H and N spikes on the surface of the flu virus. Notice these other, smaller protuberances. These are largely hidden from the immune system. Now it turns out that these spots also don't change much when the virus mutates. If you can cripple these with specific antibodies, you could cripple all versions of the flu. So far, animal tests indicate that such a vaccine could prevent severe disease, although you might get a mild case. So if this works in humans, what we're talking about is a universal flu vaccine, one that doesn't need to change every year and would remove the threat of death. We really could think of flu, then, as just a bad cold.
Lasciate che vi faccia un altro esempio. Abbiamo già parlato delle punte H e M sulla superficie del virus dell'influenza. Guardate queste altre piccole protuberanze. Risultano in gran parte nascoste al sistema immunitario. Abbiamo scoperto che anche questi punti non cambiano molto al mutare del virus. Se riusciamo ad attaccarli con anticorpi specifici riusciamo a colpire tutte le varianti di influenza. Fino ad oggi i test sugli animali indicano che un vaccino così potrebbe prevenire malattie gravi anche se ci si potrebbe ammalare in forma lieve. Se fosse così anche negli umani avremmo trovato un vaccino universale un vaccino che non dovrebbe cambiare ogni anno e che eliminerebbe i casi mortali. Potremmo allora pensare all'influenza come a un brutto raffreddore.
Of course, the best vaccine imaginable is only valuable to the extent we get it to everyone who needs it. So to do that, we have to combine smart vaccine design with smart production methods and, of course, smart delivery methods. So I want you to think back a few months ago. In June, the World Health Organization declared the first global flu pandemic in 41 years. The U.S. government promised 150 million doses of vaccine by October 15th for the flu peak. Vaccines were promised to developing countries. Hundreds of millions of dollars were spent and flowed to accelerating vaccine manufacturing. So what happened?
Naturalmente, il miglior vaccino immaginabile ha valore solo se possono averlo tutti quelli che ne hanno bisogno. Per raggiungere l'obiettivo dobbiamo combinare un vaccino intelligente con una produzione efficiente e, naturalmente, efficienti canali di distribuzione. Tornate indietro nel tempo, a qualche mese fa. A giugno l'Organizzazione Mondiale della Sanità ha dichiarato la prima epidemia globale di influenza in 41 anni. Il governo degli Stati Uniti ha promesso 150 milioni di dosi di vaccino entro il 15 ottobre per il picco dei contagi. Sono stati promessi vaccini ai Paesi in via di sviluppo. Centinaia di milioni di dollari sono stati spesi per accelerare la produzione del vaccino. Che cos'è successo?
Well, we first figured out how to make flu vaccines, how to produce them, in the early 1940s. It was a slow, cumbersome process that depended on chicken eggs, millions of living chicken eggs. Viruses only grow in living things, and so it turned out that, for flu, chicken eggs worked really well. For most strains, you could get one to two doses of vaccine per egg. Luckily for us, we live in an era of breathtaking biomedical advances. So today, we get our flu vaccines from ... chicken eggs, (Laughter) hundreds of millions of chicken eggs. Almost nothing has changed. The system is reliable but the problem is you never know how well a strain is going to grow. This year's swine flu strain grew very poorly in early production: basically .6 doses per egg. So, here's an alarming thought. What if that wild bird flies by again? You could see an avian strain that would infect the poultry flocks, and then we would have no eggs for our vaccines. So, Dan [Barber], if you want billions of chicken pellets for your fish farm, I know where to get them. So right now, the world can produce about 350 million doses of flu vaccine for the three strains, and we can up that to about 1.2 billion doses if we want to target a single variant like swine flu. But this assumes that our factories are humming because, in 2004, the U.S. supply was cut in half by contamination at one single plant. And the process still takes more than half a year.
Abbiamo imparato come fare i vaccini come produrli nei primi anni Quaranta. Era un processo lento e difficile che dipendeva dalle uova di gallina milioni di uova vive. I virus crescono solo negli esseri viventi e si scoprì che per l'influenza le uova di gallina funzionavano molto bene. Per la maggior parte dei ceppi si ottengono una o due dosi per uovo. Per fortuna viviamo in un epoca di straordinari avanzamenti nel campo della biomedicina. Quindi oggi otteniamo i vaccini dell'influenza da... ... dalle uova di gallina. (risata) centinaia di milioni di uova di gallina. Quasi niente è cambiato. Il metodo è affidabile. Il problema è che non possiamo mai sapere come un ceppo crescerà. Il ceppo dell'influenza suina di quest' anno è cresciuto molto male nella produzione preliminare: circa 0,6 dosi per uovo. Ecco un pensiero allarmante: che cosa succede se quell'uccello selvatico ci vola ancora vicino? Potremmo ritrovarci con un ceppo aviario che infetterebbe la maggior parte dei polli lasciandoci senza uova per i vaccini. Quindi, Dan (Barber), se vuoi miliardi di palline di pollo per la tua itticultura io so dove trovarle. Ora il mondo può produrre circa 350 milioni di dosi di vaccino per l'influenza per i tre ceppi. E possiamo arrivare a 1,2 miliardi se vogliamo preoccuparci di una sola varietà come la suina. Questo partendo dal presupposto che i laboratori funzionino al massimo perché nel 2004 la produzione negli USA fu dimezzata dalla contaminazione di una sola fabbrica. Il processo richiede più di 6 mesi.
So are we better prepared than we were in 1918? Well, with the new technologies emerging now, I hope we can say definitively, "Yes." Imagine we could produce enough flu vaccine for everyone in the entire world for less than half of what we're currently spending now in the United States. With a range of new technologies, we could. Here's an example: A company I'm engaged with has found a specific piece of the H spike of flu that sparks the immune system. If you lop this off and attach it to the tail of a different bacterium, which creates a vigorous immune response, they've created a very powerful flu fighter. This vaccine is so small it can be grown in a common bacteria, E. coli. Now, as you know, bacteria reproduce quickly -- it's like making yogurt -- and so we could produce enough swine origin flu for the entire world in a few factories, in a few weeks, with no eggs, for a fraction of the cost of current methods.
Siamo preparati meglio di quanto non lo fossimo nel 1918? Con le nuove tecnologie che stanno emergendo spero di poter dire definitivamente di sì. Immaginate se potessimo produrre abbastanza vaccino influenzale per tutti, in tutto il mondo a un costo inferiore alla metà di quel che spendiamo ora negli Stati Uniti. Con una gamma di tecnologie innovative, potremmo riuscirci. Ecco un esempio. Un'azienda con la quale collaboro ha trovato una parte specifica della punta H del virus dell'influenza che attiva il sistema immunitario. Se riuscissimo a staccarlo e poi a ri-attaccarlo alla coda di un batterio diverso capace di generare una vigorosa risposta immunitaria avremmo inventato un potente combattente dell'influenza. Questo vaccino è così piccolo che possiamo farlo crescere in un batterio molto comune, l'Eschericchia Coli. Come sapete, i batteri si riproducono in fretta. È un po' come fare lo yogurt. In questo modo potremmo produrre abbastanza influenza di origine suina per tutto il mondo, in pochi laboratori, in poche settimane senza uova e a una frazione del costo che richiedono i metodi attuali.
(Applause)
(applauso)
So here's a comparison of several of these new vaccine technologies. And, aside from the radically increased production and huge cost savings -- for example, the E. coli method I just talked about -- look at the time saved: this would be lives saved. The developing world, mostly left out of the current response, sees the potential of these alternate technologies and they're leapfrogging the West. India, Mexico and others are already making experimental flu vaccines, and they may be the first place we see these vaccines in use. Because these technologies are so efficient and relatively cheap, billions of people can have access to lifesaving vaccines if we can figure out how to deliver them.
Ecco un confronto tra alcune delle tecnologie per i vaccini. A parte l'aumento radicale della produzione e il grande risparmio il metodo dell'E. Coli di cui ho appena parlato, per esempio, guardate il risparmio di tempo: questo vuol dire vite salvate. I Paesi in via di sviluppo per la maggior parte attualmente esclusi dalle cure vedono il potenziale di queste tecnologie alternative e stanno sorpassando l'Occidente. L'India, il Messico e altri stanno già facendo vaccini sperimentali per l'influenza e potrebbero diventare i primi luoghi dove vedremo questi vaccini in azione. Queste tecnologie sono così efficienti e così economiche che potranno salvare la vita a miliardi di persone se troviamo il modo di distribuirle.
Now think of where this leads us. New infectious diseases appear or reappear every few years. Some day, perhaps soon, we'll have a virus that is going to threaten all of us. Will we be quick enough to react before millions die? Luckily, this year's flu was relatively mild. I say, "luckily" in part because virtually no one in the developing world was vaccinated. So if we have the political and financial foresight to sustain our investments, we will master these and new tools of vaccinology, and with these tools we can produce enough vaccine for everyone at low cost and ensure healthy productive lives. No longer must flu have to kill half a million people a year. No longer does AIDS need to kill two million a year. No longer do the poor and vulnerable need to be threatened by infectious diseases, or indeed, anybody. Instead of having Vaclav Smil's "massively fatal discontinuity" of life, we can ensure the continuity of life. What the world needs now are these new vaccines, and we can make it happen.
Pensate ora alle conseguenze. Nuove malattie infettive compaiono o riappaiono nel giro di qualche anno. Un giorno, forse presto, comparirà un virus che minaccerà tutti noi. Sapremo reagire abbastanza in fretta prima che muoiano milioni di persone? Fortunatamente, l'influenza quest'anno è stata relativamente leggera. Ho detto fortunatamente perché nel mondo sviluppato quest'anno non era vaccinato praticamente nessuno. Quindi se abbiamo la lungimiranza politica e finanziaria di sostenere i nostri investimenti potremo impadronirci di questi e di nuovi strumenti di vaccinologia. E con questi produrre abbastanza vaccini per tutti a basso costo assicurandoci vite produttive e sane. L'influenza non deve più uccidere ogni anno mezzo milione di vite. E neppure l'Aids deve ucciderne 2 milioni all'anno. I poveri e i più deboli non devono più essere minacciati da malattie infettive anzi: nessuno deve più esserlo. Invece della "discontinuità di morti di massa" di Vaclav Smil potremo assicurare la continuità della vita. Quello di cui il mondo ora ha bisogno sono questi nuovi vaccini e noi possiamo fare in modo che li abbia.
Thank you very much.
Grazie mille.
(Applause)
(applauso)
Chris Anderson: Thank you. (Applause) Thank you. So, the science is changing. In your mind, Seth -- I mean, you must dream about this -- what is the kind of time scale on, let's start with HIV, for a game-changing vaccine that's actually out there and usable?
Chris Anderson: Grazie. (applauso) Grazie. Dunque, la scienza sta cambiando. Seth, secondo te, immagino che tu sogni tutto questo, qual è la scala temporale cominciamo con l'Hiv per un vaccino rivoluzionario, di fatto in produzione e sul mercato?
SB: The game change can come at any time, because the problem we have now is we've shown we can get a vaccine to work in humans; we just need a better one. And with these types of antibodies, we know humans can make them. So, if we can figure out how to do that, then we have the vaccine, and what's interesting is there already is some evidence that we're beginning to crack that problem. So, the challenge is full speed ahead.
SB: La rivoluzione può arrivare da un momento all'altro perché il nostro problema, ora, è che abbiamo mostrato che possiamo fare un vaccino che funziona nell'uomo ne abbiamo soltanto bisogno di uno migliore. Sappiamo che l'uomo può produrre questo tipo di anticorpi. Dunque, se riusciamo a capire come farlo, abbiamo un vaccino. La cosa interessante è che c'è già l'evidenza che stiamo riuscendo a risolvere il problema. La sfida, ora, è andare avanti velocemente.
CA: In your gut, do you think it's probably going to be at least another five years?
CA: Te la sentiresti di ipotizzare che ci vogliano altri cinque anni?
SB: You know, everybody says it's 10 years, but it's been 10 years every 10 years. So I hate to put a timeline on scientific innovation, but the investments that have occurred are now paying dividends.
SB: Tutti dicono 10 anni ma ogni 10 anni diciamo che ce ne vogliono ancora 10. Non voglio mettere una data precisa sull'innovazione scientifica ma gli investimenti che sono stati fatti, ora pagano dei dividendi.
CA: And that's the same with universal flu vaccine, the same kind of thing?
CA: E per quanto riguarda il vaccino influenzale universale, è la stessa cosa?
SB: I think flu is different. I think what happened with flu is we've got a bunch -- I just showed some of this -- a bunch of really cool and useful technologies that are ready to go now. They look good. The problem has been that, what we did is we invested in traditional technologies because that's what we were comfortable with. You also can use adjuvants, which are chemicals you mix. That's what Europe is doing, so we could have diluted out our supply of flu and made more available, but, going back to what Michael Specter said, the anti-vaccine crowd didn't really want that to happen.
SB: Penso che per l'influenza sia diverso. Quel che è successo è che abbiamo un gruppo di tecnologie attraenti - ne ho appena mostrate alcune e alcune nuove tecnologie pronte per essere usate da subito. Mi sembra che possano funzionare. Il problema è che abbiamo investito in tecnologie tradizionali con le quali ci sentiamo a nostro agio. Si possono anche usare degli adiuvanti, prodotti chimici aggiuntivi. Lo sta facendo l'Europa, in questo modo possiamo aver diluito la scorta di influenza e averne resa disponibile di più Ritornando a quanto detto da Michael Specter i ricercatori dell'antivaccino non volevano che accadesse.
CA: And malaria's even further behind?
CA: E il vaccino per la malaria è ancora più lontano?
SB: No, malaria, there is a candidate that actually showed efficacy in an earlier trial and is currently in phase three trials now. It probably isn't the perfect vaccine, but it's moving along.
SB: No. Per la malaria c'è un candidato che ha mostrato la sua efficacia in un test e si trova attualmente nella fase tre. Non è probabilmente il vaccino ideale ma sta migliorando.
CA: Seth, most of us do work where every month, we produce something; we get that kind of gratification. You've been slaving away at this for more than a decade, and I salute you and your colleagues for what you do. The world needs people like you. Thank you.
CA: Seth, la maggior parte di noi lavora ogni mese dove può produrre di più cerchiamo questo tipo di gratificazione. Tu hai lavorato in questo campo per più di dieci anni e ti ringrazio, con i tuoi colleghi, per quel che fai. Il mondo ha bisogno di gente come te. Grazie.
SB: Thank you.
SB: Grazie a te.
(Applause)
(applauso)