Do you worry about what is going to kill you? Heart disease, cancer, a car accident? Most of us worry about things we can't control, like war, terrorism, the tragic earthquake that just occurred in Haiti. But what really threatens humanity? A few years ago, Professor Vaclav Smil tried to calculate the probability of sudden disasters large enough to change history. He called these, "massively fatal discontinuities," meaning that they could kill up to 100 million people in the next 50 years. He looked at the odds of another world war, of a massive volcanic eruption, even of an asteroid hitting the Earth. But he placed the likelihood of one such event above all others at close to 100 percent, and that is a severe flu pandemic. Now, you might think of flu as just a really bad cold, but it can be a death sentence. Every year, 36,000 people in the United States die of seasonal flu. In the developing world, the data is much sketchier but the death toll is almost certainly higher. You know, the problem is if this virus occasionally mutates so dramatically, it essentially is a new virus and then we get a pandemic.
האם אתם מודאגים לגבי מה עלול להרוג אתכם? מחלת-לב, סרטן, תאונה? רובנו דואגים בקשר לדברים שאין לנו שליטה עליהם כמו מלחמות, טרור, רעידת האדמה הטרגית שהתרחשה זה עתה בהאיטי. אבל מה באמת מאיים על האנושות? לפני מספר שנים, פרופ' ואקלאוו סמיל ניסה לחשב את הסבירות לאסונות פתאומיים הגדולים מספיק כדי לשנות את ההיסטוריה. הוא קרא להם "אי-רציפויות מסיביות קטלניות" זה אומר שהם מסוגלים לחסל עד 100 מיליון אנשים ב-50 השנים הבאות. הוא בחן את הסיכויים למלחמת עולם נוספת, להתפרצות געשית גדולה, ואפילו לפגיעת אסטרואיד בכדור-הארץ. אבל הוא מיקם את הסבירות לאירוע אחד מעל כולם, קרוב ל-100 אחוז, והוא מגיפת שפעת חמורה. אתם עשויים לחשוב על שפעת בתור איזו הצטננות חמורה. אבל היא עלולה להיות גזר-דין מוות. כל שנה, 36,000 תושבים בארה"ב מתים משפעת עונתית. בעולם המתפתח, הנתונים הרבה פחות מדוייקים, אבל כמעט בטוח שהמספר יותר גבוה. הבעיה נוצרת כאשר לפעמים נגיף זה עובר מוטאציה כל-כך דרמטית, שהוא בעצם הופך לנגיף חדש. ואז יש לנו מגיפה.
In 1918, a new virus appeared that killed some 50 to 100 million people. It spread like wildfire and some died within hours of developing symptoms. Are we safer today? Well, we seem to have dodged the deadly pandemic this year that most of us feared, but this threat could reappear at any time. The good news is that we're at a moment in time when science, technology, globalization is converging to create an unprecedented possibility: the possibility to make history by preventing infectious diseases that still account for one-fifth of all deaths and countless misery on Earth. We can do this. We're already preventing millions of deaths with existing vaccines, and if we get these to more people, we can certainly save more lives. But with new or better vaccines for malaria, TB, HIV, pneumonia, diarrhea, flu, we could end suffering that has been on the Earth since the beginning of time.
בשנת 1918 הופיע נגיף חדש אשר חיסל משהו כמו 50 עד 100 מיליון אנשים. הוא התפשט כמו שריפה בשדה קוצים. חלק מתו תוך שעות לאחר הופעת התסמינים. האם היום אנו יותר בטוחים? ובכן, נראה שהשנה התחמקנו מהמגיפה הקטלנית שממנה רובנו חששנו. אבל איום זה עלול להופיע שנית בכל רגע. החדשות הטובות הן שאנו נמצאים בנקודת זמן כאשר מדע, טכנולוגיה וגלובליזציה משתלבים יחד כדי ליצור אפשרות חסרת תקדים, האפשרות לעשות היסטוריה על-ידי מניעת מחלות מידבקות אשר עדיין אחראיות לחמישית מכלל מקרי המוות ולסבל אין-קץ על-פני כדור-הארץ. אנחנו יכולים לעשות זאת. כבר עכשיו אנחנו מונעים מיליוני מיתות בעזרת חיסונים קיימים. ואם נגיע איתם ליותר אנשים, בטוח שנוכל להציל יותר חיים. אבל עם חיסונים חדשים או יותר טובים למלריה, שחפת, איידס, דלקת ריאות, שלשולים, שפעת נוכל להביא לסוף הסבל השורר על כדור-הארץ מראשית ההיסטוריה.
So, I'm here to trumpet vaccines for you. But first, I have to explain why they're important because vaccines, the power of them, is really like a whisper. When they work, they can make history, but after a while you can barely hear them. Now, some of us are old enough to have a small, circular scar on our arms from an inoculation we received as children. But when was the last time you worried about smallpox, a disease that killed half a billion people last century and no longer is with us? Or polio? How many of you remember the iron lung? We don't see scenes like this anymore because of vaccines.
אני כאן כדי להשמיע את קולם של החיסונים. אבל תחילה, עליי להסביר מדוע הם כה חשובים. מכיוון שחיסונים, העוצמה שלהם, היא ממש כמו לחש. כאשר הם פועלים, הם יכולים לעשות היסטוריה, אבל לאחר זמן מה, ניתן בקושי לשמוע אותם. חלקנו מספיק מבוגרים כדי שתהיה לנו צלקת קטנה ועגולה על זרועותינו מחיסון שקיבלנו כילדים. אבל מתי היתה הפעם האחרונה שדאגתם בגלל אבעבועות שחורות, מחלה שחיסלה חצי מיליארד בני-אדם במאה שעברה ואשר כבר איננה איתנו? או פוליו -- כמה מכם זוכרים את ריאת הברזל? איננו רואים כבר מראות כאלה בגלל החיסונים.
Now, it's interesting because there are 30-odd diseases that can be treated with vaccines now, but we're still threatened by things like HIV and flu. Why is that? Well, here's the dirty little secret. Until recently, we haven't had to know exactly how a vaccine worked. We knew they worked through old-fashioned trial and error. You took a pathogen, you modified it, you injected it into a person or an animal and you saw what happened. This worked well for most pathogens, somewhat well for crafty bugs like flu, but not at all for HIV, for which humans have no natural immunity.
עכשיו, זה מעניין כי ישנן 30 ומשהו מחלות שניתן לטפל בהן בעזרת חיסונים, אבל אנחנו עדיין מאויימים על-ידי דברים כמו איידס ושפעת. מדוע זה כך? אז הנה סוד אחד קטן. עד לא מזמן, לא היינו צריכים לדעת בדיוק איך החיסון עובד. ידענו שזה עובד בעזרת ניסוי וטעיה. לקחנו את הגורם למחלה, שינינו אותו, הזרקנו אותו לאדם או בהמה, ובדקנו מה קורה. זה פעל היטב נגד רוב גורמי המחלות, די טוב נגד גורמי מחלות ערמומיים כמו של שפעת, אבל כלל לא נגד איידס, שעבורו אין לאנשים חיסון טבעי.
So let's explore how vaccines work. They basically create a cache of weapons for your immune system which you can deploy when needed. Now, when you get a viral infection, what normally happens is it takes days or weeks for your body to fight back at full strength, and that might be too late. When you're pre-immunized, what happens is you have forces in your body pre-trained to recognize and defeat specific foes. So that's really how vaccines work. Now, let's take a look at a video that we're debuting at TED, for the first time, on how an effective HIV vaccine might work.
אז בואו נבחן כיצד חיסון פועל. באופן בסיסי החיסון יוצר מאגר תחמושת בשביל מערכת החיסון אשר ניתן לשימוש בעת הצורך. כעת, אם נדבקים בנגיף, מה שקורה בדרך-כלל זה שלוקח לגופנו ימים או שבועות להתחיל להילחם במלוא העוצמה, וזה עלול להיות מאוחר מדיי. כאשר מתחסנים מראש, נוצרים בגופנו כוחות המאומנים מראש לזיהוי והתגברות על פולשים. וכך באמת החיסון עובד. עכשיו בואו נעיף מבט על וידאו בהקרנת בכורה, שמראה כיצד חיסון יעיל לאיידס עשוי לפעול.
(Music)
(מוזיקה)
Narrator: A vaccine trains the body in advance how to recognize and neutralize a specific invader. After HIV penetrates the body's mucosal barriers, it infects immune cells to replicate. The invader draws the attention of the immune system's front-line troops. Dendritic cells, or macrophages, capture the virus and display pieces of it. Memory cells generated by the HIV vaccine are activated when they learn HIV is present from the front-line troops. These memory cells immediately deploy the exact weapons needed. Memory B cells turn into plasma cells, which produce wave after wave of the specific antibodies that latch onto HIV to prevent it from infecting cells, while squadrons of killer T cells seek out and destroy cells that are already HIV infected. The virus is defeated. Without a vaccine, these responses would have taken more than a week. By that time, the battle against HIV would already have been lost.
קריינית: חיסון מכשיר את הגוף מראש לזיהוי וניטרול של פולש מסויים. לאחר שנגיף האיידס פורץ את מחסומי הריריות, הוא חודר לתאים חיסוניים על מנת להשתכפל. הפולש מושך תשומת לב של כוחות קו-החזית של מערכת החיסונית. תאים דנדריטים או מאקרופאגים תופסים את הנגיף ומציגים חלקים ממנו לראווה. תאי זיכרון הנוצרים על-ידי חיסון האיידס מופעלים כאשר הם מגלים באמצעות כוחות קו-החזית את נוכחות נגיף האיידס. תאי זיכרון אלה מפעילים מייד ובמדוייק את כלי-הנשק הדרושים. תאי זיכרון B הופכים לתאי פלזמה, המייצרים גלים גלים של נוגדנים ספציפיים הנצמדים לנגיף האיידס כדי למנוע ממנו להדביק תאים בעוד שלהקות של תאי חיסול T מחפשות ומשמידות תאים שכבר נגועים בנגיף האיידס. הנגיף מובס. ללא חיסון, תגובות אלו היו לוקחות יותר משבוע. עד אז, המלחמה נגד האיידס היתה מסתיימת בהפסד.
Seth Berkley: Really cool video, isn't it? The antibodies you just saw in this video, in action, are the ones that make most vaccines work. So the real question then is: How do we ensure that your body makes the exact ones that we need to protect against flu and HIV? The principal challenge for both of these viruses is that they're always changing. So let's take a look at the flu virus. In this rendering of the flu virus, these different colored spikes are what it uses to infect you. And also, what the antibodies use is a handle to essentially grab and neutralize the virus. When these mutate, they change their shape, and the antibodies don't know what they're looking at anymore. So that's why every year you can catch a slightly different strain of flu. It's also why in the spring, we have to make a best guess at which three strains are going to prevail the next year, put those into a single vaccine and rush those into production for the fall.
סת ברקלי: וידאו מגניב, נכון? הנוגדנים שראיתם כרגע בוידאו, בפעולה, הם אלה שמאפשרים לרוב החיסונים לפעול. לכן השאלה האמיתית היא: כיצד נבטיח שגופנו ייצר בדיוק את אותם אלה הדרושים להגנה מפני שפעת ואיידס? האתגר העיקרי בשני הנגיפים הללו הוא ששניהם משתנים ללא הרף. אז בואו נתבונן בנגיף השפעת. בתיאור הזה של נגיף השפעת, הדרבנים הצבועים הם אלה המשמשים להדבקה. וגם, מה שהנוגדנים משתמשים זה ידית כדי לאחוז בוירוס ולנטרל אותו. כאשר אלה עוברים מוטאציה, הם משנים את צורתם, ואז הנוגדנים כבר לא יודעים על מה הם מסתכלים. וזו הסיבה שכל שנה תופסים שפעת מזן קצת שונה. וזו גם הסיבה שבאביב עלינו לנחש אלו שלושה זנים הולכים לשלוט בשנה הבאה, להכניס אותם לחיסון אחד ולמהר לייצרו לקראת הסתיו.
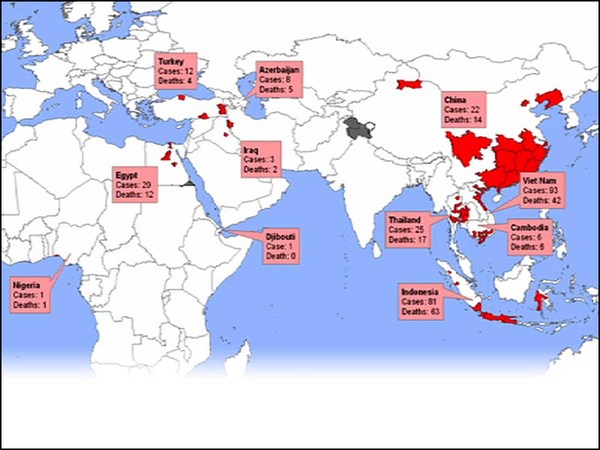
Even worse, the most common influenza -- influenza A -- also infects animals that live in close proximity to humans, and they can recombine in those particular animals. In addition, wild aquatic birds carry all known strains of influenza. So, you've got this situation: In 2003, we had an H5N1 virus that jumped from birds into humans in a few isolated cases with an apparent mortality rate of 70 percent. Now luckily, that particular virus, although very scary at the time, did not transmit from person to person very easily. This year's H1N1 threat was actually a human, avian, swine mixture that arose in Mexico. It was easily transmitted, but, luckily, was pretty mild. And so, in a sense, our luck is holding out, but you know, another wild bird could fly over at anytime.
ואפילו יותר גרוע, השפעת השכיחה ביותר, שפעת A, מדביקה גם בעלי-חיים החיים בסמיכות לבני-אדם, והם יכולים ליצור צירופים שונים בבעלי-החיים המסויימים הללו. בנוסף, ציפורי מים בפרא נושאות עימם את כל הזנים הידועים של שפעת. אז יש לנו את המצב הזה. ב-2003, היה לנו הנגיף H5N1 שקפץ מציפורים לבני-אדם במספר מקרים בודדים עם שיעור תמותה של 70 אחוזים. למרבה המזל, אותו נגיף מסויים, למרות שעורר פחד בזמנו, לא עבר מאדם לאדם בקלות. האיום מ-H1N1 של השנה הנוכחית היה למעשה תערובת של אדם, עופות וחזירים שמקורה במכסיקו. הוא הועבר בקלות, אבל למזלנו, היה די חלש. וכך, במובן מסויים, המזל הטוב שלנו עדיין מחזיק מעמד, אבל כידוע, ציפור בר אחרת יכולה לעוף מעלינו בכל רגע.
Now let's take a look at HIV. As variable as flu is, HIV makes flu look like the Rock of Gibraltar. The virus that causes AIDS is the trickiest pathogen scientists have ever confronted. It mutates furiously, it has decoys to evade the immune system, it attacks the very cells that are trying to fight it and it quickly hides itself in your genome. Here's a slide looking at the genetic variation of flu and comparing that to HIV, a much wilder target. In the video a moment ago, you saw fleets of new viruses launching from infected cells. Now realize that in a recently infected person, there are millions of these ships; each one is just slightly different. Finding a weapon that recognizes and sinks all of them makes the job that much harder.
כעת בואו נעיף מבט על איידס. עד כמה שנגיף השפעת משנה את צורותיו, נגיף האיידס גורם לנגיף השפעת להיראות כצוק גיברלטר. הנגיף אשר גורם לאיידס הוא גורם מחלה הערמומי ביותר שמדענים נתקלו בו אי-פעם. הוא משתנה במרץ. יש לו פתיונות כדי להתחמק ממערכת החיסון. הוא תוקף את התאים עצמם אשר נלחמים נגדו. והוא מתחבא במהירות בתאי הגנים שלנו. הנה שקופית המראה את השינוי הגנטי של שפעת ומשווה אותו לנגיף של איידס, מטרה הרבה יותר פראית. בוידאו לפני רגע, ראיתם להקות של נגיפים חדשים המשוגרים מתאים נגועים. כעת תחשבו שבאדם שנדבק לאחרונה, ישנן מיליוני ספינות כאלה, כאשר כל אחת שונה במעט. מציאת כלי-נשק המזהה ומטביע את כולן היא משימה קשה בהרבה.
Now, in the 27 years since HIV was identified as the cause of AIDS, we've developed more drugs to treat HIV than all other viruses put together. These drugs aren't cures, but they represent a huge triumph of science because they take away the automatic death sentence from a diagnosis of HIV, at least for those who can access them. The vaccine effort though is really quite different. Large companies moved away from it because they thought the science was so difficult and vaccines were seen as poor business. Many thought that it was just impossible to make an AIDS vaccine, but today, evidence tells us otherwise.
27 שנים מאז ש-HIV זוהה כגורם לאיידס, פיתחנו יותר תרופות לטיפול בנגיף האיידס מאשר לכל הנגיפים ביחד. תרופות הללו אינן המרפא, אבל הן מייצגות ניצחון גדול של המדע מאחר והן מרחיקות את גזר-דין המוות האוטומטי מרגע גילוי הנגיף, לפחות עבור אלה שיש להם גישה אליהן. בכל אופן, המאמצים לפיתוח חיסון הם די שונים. חברות גדולות הרחיקו עצמן מנושא זה מכיוון שהן סברו שמבחינה מדעית זה מסובך וחיסונים נחשבו להשקעה גרועה. רבים חשבו שזה פשוט יהיה בלתי אפשרי לייצר חיסון נגד איידס, אבל כיום, הראיות מצביעות אחרת.
In September, we had surprising but exciting findings from a clinical trial that took place in Thailand. For the first time, we saw an AIDS vaccine work in humans -- albeit, quite modestly -- and that particular vaccine was made almost a decade ago. Newer concepts and early testing now show even greater promise in the best of our animal models. But in the past few months, researchers have also isolated several new broadly neutralizing antibodies from the blood of an HIV infected individual. Now, what does this mean? We saw earlier that HIV is highly variable, that a broad neutralizing antibody latches on and disables multiple variations of the virus. If you take these and you put them in the best of our monkey models, they provide full protection from infection. In addition, these researchers found a new site on HIV where the antibodies can grab onto, and what's so special about this spot is that it changes very little as the virus mutates. It's like, as many times as the virus changes its clothes, it's still wearing the same socks, and now our job is to make sure we get the body to really hate those socks.
בספטמבר, הגענו לממצאים מפתיעים, אך מרגשים, מניסוי רפואי שנערך בתאילנד. לראשונה, ראינו חיסון איידס משפיע על בני-אדם, אף על-פי שההשפעה היתה די מוגבלת. ואותו חיסון מסויים יוצר כמעט לפני עשור. חשיבה חדשה ובדיקות ראשוניות נראות אפילו יותר מבטיחות במודלים המתקדמים ביותר שלנו על חיות. אבל בחודשים האחרונים, חוקרים אף בודדו מספר נוגדנים חדשים המסוגלים לנטרל מגוון רחב (של נגיפים) מתוך דם של אדם הנגוע בנגיף איידס. מה כל זה אומר? ראינו מקודם שנגיף איידס נתון לשינויים רבים, שנוגדן בעל יכולת נטרול רחבה נצמד ומנטרל וריאציות רבות של הנגיף. אם לוקחים את כל זה ושמים במודל על קופים, זה נותן הגנה מלאה מהדבקה. בנוסף, חוקרים הללו מצאו אזור חדש על-פני הנגיף שאליו הנוגדנים יכולים להיצמד. ומה שכה מיוחד בנקודה זו שהיא משתנה במעט מאוד כאשר הנגיף עובר שינוי. זה כאילו שלא משנה כמה פעמים הנגיף מחליף את בגדיו, הוא עדיין נשאר עם אותן הגרביים, וכעת העבודה שלנו היא לוודא שאנו גורמים לגוף ממש לשנוא את הגרביים הללו.
So what we've got is a situation. The Thai results tell us we can make an AIDS vaccine, and the antibody findings tell us how we might do that. This strategy, working backwards from an antibody to create a vaccine candidate, has never been done before in vaccine research. It's called retro-vaccinology, and its implications extend way beyond that of just HIV. So think of it this way. We've got these new antibodies we've identified, and we know that they latch onto many, many variations of the virus. We know that they have to latch onto a specific part, so if we can figure out the precise structure of that part, present that through a vaccine, what we hope is we can prompt your immune system to make these matching antibodies. And that would create a universal HIV vaccine. Now, it sounds easier than it is because the structure actually looks more like this blue antibody diagram attached to its yellow binding site, and as you can imagine, these three-dimensional structures are much harder to work on. And if you guys have ideas to help us solve this, we'd love to hear about it.
אז זה המצב שבו אנו נמצאים. התוצאות מתאילנד מספרות לנו שנוכל ליצור חיסון לאיידס. וממצאי הנוגדנים מספרים לנו כיצד נוכל לעשות זאת. שיטת פעולה זו, לפעול אחורנית, הפיכת הנוגדן למועמד ליצירת חיסון, מעולם לא נוסתה בעבר בחקר החיסונים. זה נקרא חקר חיסונים במבט לאחור, והשלכותיו מגיעים הרחק מעבר לנגיף האיידס בלבד. חישבו על זה כך. יש לנו את הנוגדנים החדשים הללו שזיהינו, ואנו יודעים שהם נצמדים להמון וריאציות של הנגיף. אנו יודעים שעליהם להיצמד לחלק מסויים, ולכן אם נוכל לגלות את המבנה המדוייק של אותו חלק, להציגו באמצעות חיסון, אנו מקווים שנוכל להניע את המערכת החיסונית שלנו ליצור את הנוגדנים המתאימים למבנה. וזה ייצור חיסון אוניברסלי לאיידס. זה נשמע קל ממה שזה באמת מכיוון שהמבנה נראה למעשה יותר כמו תרשים כחול זה של נוגדן המוצמד לאזור ההיצמדות הצהוב. וכפי שאתם מדמיינים, הרבה יותר קשה לעבוד עם המבנים התלת-מימדיים הללו. הם הרבה יותר קשים לעבוד איתם. ואם יש לכם רעיונות איך לפתור את זה, נשמח לשמוע על כך.
But, you know, the research that has occurred from HIV now has really helped with innovation with other diseases. So for instance, a biotechnology company has now found broadly neutralizing antibodies to influenza, as well as a new antibody target on the flu virus. They're currently making a cocktail -- an antibody cocktail -- that can be used to treat severe, overwhelming cases of flu. In the longer term, what they can do is use these tools of retro-vaccinology to make a preventive flu vaccine. Now, retro-vaccinology is just one technique within the ambit of so-called rational vaccine design.
אבל, המחקר שצמח מנגיף האיידס, ממש סייע ליצירת חידושים עבור מחלות אחרות. כך לדוגמא, חברה ביו-טכנולוגית גילתה עכשיו נוגדנים יעילים כנגד מגוון רחב של שפעות כמו גם מטרה לתקיפה של נוגדן על נגיף השפעת. כיום הם מייצרים קוקטייל, קוקטייל של נוגדנים, שישמש לטיפול במקרים קשים של שפעת. בטווח הארוך, מה שהם יכולים לעשות זה להשתמש בכלים אלה של מחקר במבט לאחור כדי ליצור חיסון מונע לשפעת. מחקר על חיסונים במבט לאחור היא רק טכניקה אחת בתחום הנקרא תכנון חיסונים רציונלי.
Let me give you another example. We talked about before the H and N spikes on the surface of the flu virus. Notice these other, smaller protuberances. These are largely hidden from the immune system. Now it turns out that these spots also don't change much when the virus mutates. If you can cripple these with specific antibodies, you could cripple all versions of the flu. So far, animal tests indicate that such a vaccine could prevent severe disease, although you might get a mild case. So if this works in humans, what we're talking about is a universal flu vaccine, one that doesn't need to change every year and would remove the threat of death. We really could think of flu, then, as just a bad cold.
ברשותכם אתן דוגמא נוספת. דיברנו קודם על דרבני ה-H ו-M על פני-השטח של נגיף השפעת. שימו לב לגבשושיות האחרות, הקטנות יותר. אלו ברובן חבויות ממערכת החיסונית. כעת מתברר שנקודות הללו גם כן, לא משתנות בהרבה כאשר הנגיף עובר שינוי. אם ניתן לשבש אותן עם נוגדנים מסויימים, ניתן לפגוע בכל צורות השפעת. נכון להיום, בדיקות על חיות מראות שחיסון כזה יכול למנוע חולי חמור, אף על-פי שאולי נחלה בחולי קל. אז אם זה פועל בהצלחה על בני-אדם, מה שאנו מדברים עליו זה חיסון אוניברסלי לשפעת, אחד שאין צורך לשנותו כל שנה ואשר יסיר את סכנת המוות. אז נוכל להתייחס לשפעת רק כאל הצטננות קשה.
Of course, the best vaccine imaginable is only valuable to the extent we get it to everyone who needs it. So to do that, we have to combine smart vaccine design with smart production methods and, of course, smart delivery methods. So I want you to think back a few months ago. In June, the World Health Organization declared the first global flu pandemic in 41 years. The U.S. government promised 150 million doses of vaccine by October 15th for the flu peak. Vaccines were promised to developing countries. Hundreds of millions of dollars were spent and flowed to accelerating vaccine manufacturing. So what happened?
כמובן שהחיסון הטוב ביותר שניתן לחשוב עליו הוא בעל-ערך רק באותו שיעור שמצליחים לספקו לכל מי שזקוק לו. לכן כדי לעשות זאת, עלינו לשלב תכנון חיסון חכם עם שיטות ייצור חכמות וכמובן, שיטות הובלה וחלוקה חכמות. אני מבקש שתחזרו מספר חודשים אחורה. ביוני, אירגון הבריאות העולמי הכריז לראשונה מזה 41 שנה על מגיפת שפעת עולמית. ממשלת ארה"ב הבטיחה 150 מיליון מנות של חיסון עד 15 לאוקטובר לתקופת שיא השפעת. חיסונים הובטחו למדינות מתפתחות. הוצאו מאות מיליוני דולרים אשר הוזרמו לייצור מזורז של חיסונים. אז מה בדיוק קרה כאן?
Well, we first figured out how to make flu vaccines, how to produce them, in the early 1940s. It was a slow, cumbersome process that depended on chicken eggs, millions of living chicken eggs. Viruses only grow in living things, and so it turned out that, for flu, chicken eggs worked really well. For most strains, you could get one to two doses of vaccine per egg. Luckily for us, we live in an era of breathtaking biomedical advances. So today, we get our flu vaccines from ... chicken eggs, (Laughter) hundreds of millions of chicken eggs. Almost nothing has changed. The system is reliable but the problem is you never know how well a strain is going to grow. This year's swine flu strain grew very poorly in early production: basically .6 doses per egg. So, here's an alarming thought. What if that wild bird flies by again? You could see an avian strain that would infect the poultry flocks, and then we would have no eggs for our vaccines. So, Dan [Barber], if you want billions of chicken pellets for your fish farm, I know where to get them. So right now, the world can produce about 350 million doses of flu vaccine for the three strains, and we can up that to about 1.2 billion doses if we want to target a single variant like swine flu. But this assumes that our factories are humming because, in 2004, the U.S. supply was cut in half by contamination at one single plant. And the process still takes more than half a year.
תחילה גילינו כיצד ליצור חיסוני שפעת, כיצד לייצרם, בשנות ה-40 המוקדמות. זה היה תהליך איטי ומסורבל שנעשה בעזרת ביצי תרנגולות, מיליוני ביצים של תרנגולות חיות. נגיפים גדלים רק בדברים חיים, ואז התברר שלחיסוני שפעת, ביצי תרנגולות היו דבר טוב. בשביל רוב הזנים, יכולנו להפיק מנה אחת עד שתיים של חיסון מכל ביצה. למרבה המזל, אנו חיים בעידן של התקדמות ביו-רפואית מדהימה. כך שהיום, אנו מפיקים את החיסונים שלנו מ.... ...ביצי תרנגולות. (צחוק) מאות מיליוני ביצי תרנגולות. כמעט כלום השתנה. השיטה אמינה. אבל הבעיה היא שאף פעם לא יודעים עד כמה טוב הזן יתפתח. הזן של שפעת החזירים השנה התפתח גרוע בייצור מוקדם. 0.6 מנות לביצה. אז הנה מחשבה מעוררת דאגה. מה יקרה אם ציפור נגועה תעוף בסביבה? נראה זן השייך לעופות שידביק להקות של תרנגולות, ואז לא יהיו לנו ביצים בשביל החיסונים. אז, דן [בארבר], אם אתה רוצה, מיליארדי טבליות של תרנגולות בשביל חוות הדגים שלך, אני יודע מהיכן להשיגן. באופן מיידי, העולם יכול לייצר כ-350 מיליון מנות של חיסון שפעת לשלושת הזנים. ונוכל להעלות את זה עד כ-1.2 מיליארד מנות, אם ברצוננו לכוון לזן יחיד כמו שפעת חזירים. אבל ההנחה כאן היא שהמפעלים שלנו עובדים במלוא התפוקה מפני שב-2004, התפוקה בארה"ב ירדה בחצי בגלל זיהום במתקן אחד ויחיד. והתהליך עדיין דורש יותר מחצי שנה.
So are we better prepared than we were in 1918? Well, with the new technologies emerging now, I hope we can say definitively, "Yes." Imagine we could produce enough flu vaccine for everyone in the entire world for less than half of what we're currently spending now in the United States. With a range of new technologies, we could. Here's an example: A company I'm engaged with has found a specific piece of the H spike of flu that sparks the immune system. If you lop this off and attach it to the tail of a different bacterium, which creates a vigorous immune response, they've created a very powerful flu fighter. This vaccine is so small it can be grown in a common bacteria, E. coli. Now, as you know, bacteria reproduce quickly -- it's like making yogurt -- and so we could produce enough swine origin flu for the entire world in a few factories, in a few weeks, with no eggs, for a fraction of the cost of current methods.
אז האם אנחנו מוכנים יותר ממה שהיינו ב-1918? ובכן, עם הטכנולוגיות החדשות הצצות היום, אני מקווה שניתן לומר בהחלטיות, "כן". תחשבו שהיינו יכולים לייצר מספיק חיסונים לשפעת בשביל כל אחד בכל העולם בעבור פחות מחצי ממה שאנו מבזבזים היום בארה"ב. בעזרת מגוון טכנולוגיות חדשות, אנחנו מסוגלים. הנה דוגמא. חברה שאני עובד איתה מצאה חלק מסויים מדרבן H של נגיף שפעת אשר מעורר את המערכת החיסונית. אם כורתים אותו ומצמידים אותו לזנב של חיידק אחר שמעורר תגובה חיסונית עוצמתית, יוצרים לוחם חזק ביותר נגד שפעת. חיסון זה הוא כה קטן, שניתן לגדלו בחיידק רגיל, E. coli. וכפי שכולנו יודעים, חיידקים מתרבים במהירות. זה כמו ליצור יוגורט. וכך נהיה מסוגלים לייצר מספיק חיסוני שפעת החזירים בשביל כל העולם במספר מפעלים, תוך מספר שבועות ללא ביצים ותמורת רק חלק מהעלות של השיטות הקיימות היום.
(Applause)
(מחיאות כפיים)
So here's a comparison of several of these new vaccine technologies. And, aside from the radically increased production and huge cost savings -- for example, the E. coli method I just talked about -- look at the time saved: this would be lives saved. The developing world, mostly left out of the current response, sees the potential of these alternate technologies and they're leapfrogging the West. India, Mexico and others are already making experimental flu vaccines, and they may be the first place we see these vaccines in use. Because these technologies are so efficient and relatively cheap, billions of people can have access to lifesaving vaccines if we can figure out how to deliver them.
אז הנה השוואה בין מספר טכנולוגיות חיסון חדשות הללו. ומלבד קצב הייצור הגבוה במידה ניכרת וחיסכון ענק בעלויות, לדוגמא, שיטת ה-E. coli שרק הזכרתי, תראו כמה זמן נחסך -- זה יציל חיים. העולם המתפתח, שברובו נשאר מחוץ למענה הנוכחי, רואה את הפוטנציאל בטכנולוגיות אלטרנטיביות הללו, והם עוקפים את המערב. הודו, מכסיקו ואחרות כבר יוצרות חיסוני שפעת ניסיוניים, והן עשויות להיות המקום הראשון שנראה שם את החיסונים בפעולה. מכיוון שטכנולוגיות הללו הן כה יעילות וזולות יחסית, למיליארדי אנשים יכולה להיות נגישות לחיסונים מצילי חיים, אם נוכל למצוא כיצד להוביל ולהפיץ אותם.
Now think of where this leads us. New infectious diseases appear or reappear every few years. Some day, perhaps soon, we'll have a virus that is going to threaten all of us. Will we be quick enough to react before millions die? Luckily, this year's flu was relatively mild. I say, "luckily" in part because virtually no one in the developing world was vaccinated. So if we have the political and financial foresight to sustain our investments, we will master these and new tools of vaccinology, and with these tools we can produce enough vaccine for everyone at low cost and ensure healthy productive lives. No longer must flu have to kill half a million people a year. No longer does AIDS need to kill two million a year. No longer do the poor and vulnerable need to be threatened by infectious diseases, or indeed, anybody. Instead of having Vaclav Smil's "massively fatal discontinuity" of life, we can ensure the continuity of life. What the world needs now are these new vaccines, and we can make it happen.
כעת תחשבו לאן כל זה מוביל אותנו. מחלות מידבקות חדשות מופיעות או מופיעות מחדש כל כמה שנים. באחד הימים, אולי בקרוב, יגיע נגיף שיאיים על כולנו. האם נהיה מספיק זריזים כדי להגיב לפני שימותו מיליונים? למרבה המזל, השפעת השנה היתה יחסית חלשה. אני אומר "למרבה המזל" בזהירות מכיוון שבעצם אף אחד בעולם המתפתח לא קיבל חיסון. לכן אם יש לנו חזון פוליטי וכלכלי לשאת את השקעותינו, אנחנו נלמד להיות מיומנים בכלים אלה ואחרים של חיסונים. ובעזרת הכלים הללו, נוכל לייצר מספיק חיסונים בשביל כל אחד בעלות נמוכה ולהבטיח חיים בריאים ופוריים. אין יותר סיבה ששפעת תהרוג חצי מיליון בני-אדם בשנה. גם אין צורך שאיידס יהרוג שני מיליון בשנה. אין יותר סיבה שהעניים והפגיעים יחיו תחת איום של מחלות מדבקות או, בעצם, כל אחד. במקום שתהיה לנו "אי-רציפות מסיבית קטלנית" של חיים על-פי ואקלאוו סמיל, נוכל להבטיח את המשכיות החיים. מה שהעולם זקוק לו כעת הם החיסונים החדשים הללו, ונוכל לגרום לזה לקרות.
Thank you very much.
תודה רבה לכם.
(Applause)
(מחיאות כפיים)
Chris Anderson: Thank you. (Applause) Thank you. So, the science is changing. In your mind, Seth -- I mean, you must dream about this -- what is the kind of time scale on, let's start with HIV, for a game-changing vaccine that's actually out there and usable?
כריס אנדרסון: תודה לך. (מחיאות כפיים) תודה. אז המדע משתנה. לפי דעתך, סת -- אני מתכוון, אתה בטח חולם על זה -- מהו טווח הזמן נגיד, נתחיל עם איידס, בשביל כזה חיסון שישנה את כללי המשחק שיהיה זמין ושימושי?
SB: The game change can come at any time, because the problem we have now is we've shown we can get a vaccine to work in humans; we just need a better one. And with these types of antibodies, we know humans can make them. So, if we can figure out how to do that, then we have the vaccine, and what's interesting is there already is some evidence that we're beginning to crack that problem. So, the challenge is full speed ahead.
ס.ב.: שינוי כללי המשחק יכול להתרחש בכל רגע מכיוון שהבעיה שיש לנו כרגע היא שהראינו שאנו יכולים ליצור חיסון שעובד על בני-אדם, רק צריך לשפר אותו. ובמקרה של נוגדנים כאלה, אנו יודעים שאפשר לייצרם. כך שאם נגלה כיצד לעשות זאת, אז יש לנו את החיסון. ומה שמעניין הוא שכבר יש כמה ראיות שאנו מתחילים לפצח את הבעיה. אנו חותרים לכך במלוא המרץ.
CA: In your gut, do you think it's probably going to be at least another five years?
כ.א.: לפי הרגשתך, האם אתה סבור שזה יקח לפחות עוד חמש שנים?
SB: You know, everybody says it's 10 years, but it's been 10 years every 10 years. So I hate to put a timeline on scientific innovation, but the investments that have occurred are now paying dividends.
ס.ב.: אתה יודע, כולם אומרים שזה 10 שנים, אבל זה כבר 10 שנים כל 10 שנים נוספות. לכן איני אוהב לקבוע לוחות זמנים למחקר מדעי, אבל ההשקעות שנעשו מחזירות עכשיו רווחים.
CA: And that's the same with universal flu vaccine, the same kind of thing?
כ.א.: והאם זה כך גם עם חיסון שפעת אוניברסלי?
SB: I think flu is different. I think what happened with flu is we've got a bunch -- I just showed some of this -- a bunch of really cool and useful technologies that are ready to go now. They look good. The problem has been that, what we did is we invested in traditional technologies because that's what we were comfortable with. You also can use adjuvants, which are chemicals you mix. That's what Europe is doing, so we could have diluted out our supply of flu and made more available, but, going back to what Michael Specter said, the anti-vaccine crowd didn't really want that to happen.
ס.ב.: אני סבור ששפעת זה משהו אחר. אני חושב שמה שקרה עם שפעת זה יש לנו קבוצה -- הראיתי את חלקן -- קבוצה של טכנולוגיות באמת נפלאות ומועילות אשר מוכנות לפעולה כיום. הן נראות מבטיחות. הבעיה היא שהשקענו בטכנולוגיות מסורתיות בגלל שהיה לנו נוח עם זה. ניתן להשתמש בתרופות עזר, שהן תערובות של כימיקלים. וזה מה שאירופה עושה, כך שיכלנו לדלל את אספקת חיסוני השפעת ולהפכם ליותר זמינים. אבל, אם נחזור למה שאמר מייקל ספקטר, מתנגדי החיסונים אינם מעוניינים שזה יקרה.
CA: And malaria's even further behind?
כ.א.: והאם מלריה אפילו יותר מאחור?
SB: No, malaria, there is a candidate that actually showed efficacy in an earlier trial and is currently in phase three trials now. It probably isn't the perfect vaccine, but it's moving along.
ס.ב.: לא, מלריה, יש מועמד שלמעשה הפגין יעילות במחקר ראשוני וכרגע נמצא במצב של ניסיונות שלב שלישי. ככל הנראה אין זה החיסון המושלם, אבל הוא מתקרב אליו.
CA: Seth, most of us do work where every month, we produce something; we get that kind of gratification. You've been slaving away at this for more than a decade, and I salute you and your colleagues for what you do. The world needs people like you. Thank you.
כ.א.: סת, רובנו עובדים במקום בו כל חודש אנחנו כזה, אתה יודע, מייצרים משהו, וזה הסיפוק שלנו. אתם כבר עובדים על זה בפרך במשך יותר מעשור, ואני מצדיע לך ולעמיתיך על מה שאתם עושים. העולם זקוק לאנשים כמוכם. תודה לך.
SB: Thank you.
ס.ב.: תודה.
(Applause)
(מחיאות כפיים)