Do you worry about what is going to kill you? Heart disease, cancer, a car accident? Most of us worry about things we can't control, like war, terrorism, the tragic earthquake that just occurred in Haiti. But what really threatens humanity? A few years ago, Professor Vaclav Smil tried to calculate the probability of sudden disasters large enough to change history. He called these, "massively fatal discontinuities," meaning that they could kill up to 100 million people in the next 50 years. He looked at the odds of another world war, of a massive volcanic eruption, even of an asteroid hitting the Earth. But he placed the likelihood of one such event above all others at close to 100 percent, and that is a severe flu pandemic. Now, you might think of flu as just a really bad cold, but it can be a death sentence. Every year, 36,000 people in the United States die of seasonal flu. In the developing world, the data is much sketchier but the death toll is almost certainly higher. You know, the problem is if this virus occasionally mutates so dramatically, it essentially is a new virus and then we get a pandemic.
نگران هستید که چه چیزی شما را خواهد کشت؟ بیماریهای قلبی، سرطان، تصادف با ماشین؟ بیشتر ما نگران چیزهایی هستیم که نمیتوانیم کنترل کنیم، مثل جنگ، تروریسم، زلزله غمانگیزی که در هائیتی رخ داد. اما چه چیزی واقعا انسانیت را تهدید میکند؟ چند سال قبل پروفسور واکلاو اسمیل تلاش کرد تا احتمال وقوع بلایای ناگهانی را محاسبه کند که برای تغییر تاریخ بحد کافی بزرگ هستنند. اسمش را گذاشت، «گسستهای بسیار مهلک»، به این معنی که آنها میتوانند در ۵۰ سال آینده حداقل ۱۰۰ میلیون نفر را بکشند. او احتمال جنگ جهانی دیگری را در نظر گرفت، یک فوران عظیم آتشفشانی، حتی برخورد یک سیارک را به زمین. اما او احتمال وقوع یک رویداد خاص را بالاتر از همه چیز قرار داد احتمالی نزدیک به ۱۰۰ درصد، و آن همهگیری جهانی آنفلوانزای حاد است. ممکن است فکر کنید که آنفلوانزا فقط سرماخوردگی شدید است، اما این مرض میتواند حکم اعدام باشد. هر ساله ۳۶ هزار نفر در ایالات متحده به دلیل آنفلوانزای فصلی میمیرند. در جهان در حال توسعه، دادهها سطحیتر هستند اما تعداد تلفات مرگ قطعا بالاتر است. میدانید، مشکل این است که اگر این ویروس گهگاه جهش ناگهانی شدید پیدا کند، در واقع به یک ویروس جدید بدل میشود و بعد مرض همهگیر میشود.
In 1918, a new virus appeared that killed some 50 to 100 million people. It spread like wildfire and some died within hours of developing symptoms. Are we safer today? Well, we seem to have dodged the deadly pandemic this year that most of us feared, but this threat could reappear at any time. The good news is that we're at a moment in time when science, technology, globalization is converging to create an unprecedented possibility: the possibility to make history by preventing infectious diseases that still account for one-fifth of all deaths and countless misery on Earth. We can do this. We're already preventing millions of deaths with existing vaccines, and if we get these to more people, we can certainly save more lives. But with new or better vaccines for malaria, TB, HIV, pneumonia, diarrhea, flu, we could end suffering that has been on the Earth since the beginning of time.
در ۱۹۱۸ ویروس جدیدی پیدا شد که بین ۵۰ تا ۱۰۰ میلیون نفر را کشت. بیماری مانند آتشی بزرگ پخش شد و برخی درعرض چند ساعت از بروز علائم جان دادند. آیا امروزه ایمنتر هستیم؟ خب، به نظر میرسد که ما امسال از همهگیری مرگباری قِسِر دررفتهایم که بیشتر ما نگرانش بودیم. اما این تهدید میتواند هر زمان باز ظاهر شود. خبر خوب این است که ما در مقطعی از زمان هستیم که علم، فناوری، و جهانی شدن هم راستا میشوند تا امکانی بیسابقه پدید آید: امکان ساختن تاریخ از طریق جلوگیری از بیماریهای مسری که هنوز هم موجب یک پنجم از همه مرگ ومیر و مصیبتهای بیشمار روی زمین میشود. ما میتوانیم این را انجام دهیم. امروزه جلوی میلیونها مرگ را با واکسنهای موجود میگیریم. و اگر این را برای افراد بیشتری میسر کنیم، قطعا میتوانیم جانهای بیشتری را نجات دهیم. اما با واکسنهای جدید یا بهتر برای مالاریا، سل، اچآیوی، ذاتالریه، اسهال، آنفلوانزا، توانستیم به رنجی پایان دهیم که از روز ازل روی زمین بوده است.
So, I'm here to trumpet vaccines for you. But first, I have to explain why they're important because vaccines, the power of them, is really like a whisper. When they work, they can make history, but after a while you can barely hear them. Now, some of us are old enough to have a small, circular scar on our arms from an inoculation we received as children. But when was the last time you worried about smallpox, a disease that killed half a billion people last century and no longer is with us? Or polio? How many of you remember the iron lung? We don't see scenes like this anymore because of vaccines.
پس برای شما از خوبی واکسنها میگویم. اما در ابتدا، باید اهمیت آن را توضیح دهم. چون واکسن، قدرت واکسنها، حقیقتا به زمزمه شبیه است. وقتی اثر میکنند تاریخساز میشوند، اما بعد از مدتی چیزی از آنها نمیشنوید. برخی از ما به اندازه کافی مسن هستیم که یک جای زخم گرد کوچک از تلقیحی که در کودکی دریافت کردیم روی بازویمان باشد. اما آخرین باری که نگران آبله بودید کی بود؟ بیماریای که نیم میلیارد نفر را در قرن گذشته از پا درآورد و دیگر وجود ندارد. یا فلج اطفال؟ چند نفر از شما ریه آهنی را یادتان است؟ ما دیگر صحنههایی از این قبیل را به دلیل وجود واکسنها نمیبینیم.
Now, it's interesting because there are 30-odd diseases that can be treated with vaccines now, but we're still threatened by things like HIV and flu. Why is that? Well, here's the dirty little secret. Until recently, we haven't had to know exactly how a vaccine worked. We knew they worked through old-fashioned trial and error. You took a pathogen, you modified it, you injected it into a person or an animal and you saw what happened. This worked well for most pathogens, somewhat well for crafty bugs like flu, but not at all for HIV, for which humans have no natural immunity.
خوب، این جالب است زیرا بیش از ۳۰ بیماری وجود دارد که اکنون با واکسن قابل درمان است، اما هنوز با چیزهایی مانند اچآیوی و آنفلوانزا تهدید میشویم دلیلش چیست؟ خب، یک راز کوچک مخفی در میان است. تا همین اواخر، ما مجبور نبودیم بدانیم که یک واکسن دقیقا چگونه کار میکند. جوابش را از طریق آزمون و خطاهای قدیمی میدانستیم. پاتوژن را گرفته و تغییرش دادید، آن را به فردی یا حیوانی تزریق کردید و دیدید که چه اتفاقی افتاد. این برای اکثر پاتوژنها به خوبی جواب داد، به ویروسهای موذی مثل آنفلوآنزا تا حدی جواب داد، اما روی اچآیوی که انسانها در مقابلش، هیچ مصونیت طبیعی ندارند مطلقا بیاثر بود.
So let's explore how vaccines work. They basically create a cache of weapons for your immune system which you can deploy when needed. Now, when you get a viral infection, what normally happens is it takes days or weeks for your body to fight back at full strength, and that might be too late. When you're pre-immunized, what happens is you have forces in your body pre-trained to recognize and defeat specific foes. So that's really how vaccines work. Now, let's take a look at a video that we're debuting at TED, for the first time, on how an effective HIV vaccine might work.
پس بیایید ببینیم که واکسنها چطور کار میکنند. آنها اساسا یک مخزن ایجاد میکنند متشکل از تسلیحاتی برای سیستم ایمنی شما که میتوانید هنگام ضرورت اعزامشان کنید. حال، هنگامی که یک عفونت ویروسی میگیرید، معمولا چند روز یا چند هفته طول میکشد تا بدن شما با تمام قوا در مقابلش بجنگد، و این ممکن است زیادی دیر باشد. هنگامی که شما مصونیت قبلی دارید، یعنی نیروهایی را در بدن دارید که قبلا آموزش دیدهاند تا دشمنان خاص را تشخیص و شکست دهند. این نحوه عملکرد واکسن است. حال بیایید به ویدئویی نگاه کنیم که برای اولین بار اینجا در TED نمایش میدهیم درباره این که یک واکسن موثراچآیوی ممکن است چطور عمل کند.
(Music)
(موسیقی)
Narrator: A vaccine trains the body in advance how to recognize and neutralize a specific invader. After HIV penetrates the body's mucosal barriers, it infects immune cells to replicate. The invader draws the attention of the immune system's front-line troops. Dendritic cells, or macrophages, capture the virus and display pieces of it. Memory cells generated by the HIV vaccine are activated when they learn HIV is present from the front-line troops. These memory cells immediately deploy the exact weapons needed. Memory B cells turn into plasma cells, which produce wave after wave of the specific antibodies that latch onto HIV to prevent it from infecting cells, while squadrons of killer T cells seek out and destroy cells that are already HIV infected. The virus is defeated. Without a vaccine, these responses would have taken more than a week. By that time, the battle against HIV would already have been lost.
گوینده: واکسن از قبل به بدن یاد میدهد که چطور یک مهاجم خاص را شناسایی و خنثی کند. بعد از نفوذ اچآیوی به موانع مخاطی بدن، سلولهای ایمنی بدن را آلوده میکند تا همانندسازی کند. مهاجم توجه نیروهای خط مقدم سیستم ایمنی را جلب میکند. سلولهای دندانهای یا ماکروفاژها ویروس را احاطه کرده و قطعات آن را نمایش میدهند. سلولهای خاطرهی تولید شده توسط واکسن اچآیوی موقعی که توسط سربازان خط مقدم از حضور اچآیوی مطلع میشوند فعال میشوند. این سلولهای خاطره بلافاصله سلاحی را که دقیقا مورد نیاز است اعزام میکنند. سلولهای خاطره «ب» به سلولهای پلاسما تبدیل میشوند، که باعث تولید گروه انبوه آنتیبادیهای خاص میشود که به اچآیوی میچسبند تا از آلودگی سلولها جلوگیری کنند، و همزمان لشکر سلولهای کشنده «ت» سلولهایی را جستجو کرده و میکشند که به اچآیوی آلوده شدهاند. ویروس شکست خورده است، بدون واکسن، این پاسخها بیش از یک هفته طول میکشیدند. تا این زمان، نبرد علیه اچآیوی محکوم به شکست بود.
Seth Berkley: Really cool video, isn't it? The antibodies you just saw in this video, in action, are the ones that make most vaccines work. So the real question then is: How do we ensure that your body makes the exact ones that we need to protect against flu and HIV? The principal challenge for both of these viruses is that they're always changing. So let's take a look at the flu virus. In this rendering of the flu virus, these different colored spikes are what it uses to infect you. And also, what the antibodies use is a handle to essentially grab and neutralize the virus. When these mutate, they change their shape, and the antibodies don't know what they're looking at anymore. So that's why every year you can catch a slightly different strain of flu. It's also why in the spring, we have to make a best guess at which three strains are going to prevail the next year, put those into a single vaccine and rush those into production for the fall.
سث برکلی: ویدیوی جالبی بود، اینطور نیست؟ آنتیبادیهایی که در این ویدئو دیدید، در عمل همانهایی هستند که باعث موثر بودن اکثر واکسنها میشوند. بنابراین پرسش واقعی این است: چگونه اطمینان حاصل کنیم که بدن شما دقیقا آنتیبادیهایی را تولید میکند که علیه آنفلوانزا و اچآیوی نیاز داریم؟ چالش اصلی هر دو این ویروسها این است که آنها همیشه در حال تغییرند. پس بیایید نگاهی به ویروس آنفلوانزا بکنیم. در این نمایش ویروس آنفلوانزا این میخهای چند رنگ همان چیزی است که برای آلوده کردن شما به کار میگیرد. و همچنین، آنچه آنتیبادیها استفاده میکنند، دستهای است که اساسا ویروس را جذب و خنثی میکند. وقتی اینها جهش میکنند شکلشان عوض میشود، و آنتیبادیها دیگر نمیدانند دنبال چه میگردند. به همین دلیل است که هر سال ممکن است نوع اندکی متفاوت از آنفلوآنزا را بگیرید. همچنین به همین دلیل است که در بهار، باید بهترین حدس را بزنیم که در سال آینده کدام یک از سه نوع آنفلوآنزا شایع میشود، تا آن را در یک واکسن جمع کنیم و سریع برای فصل پاییز تولیدش کنیم.
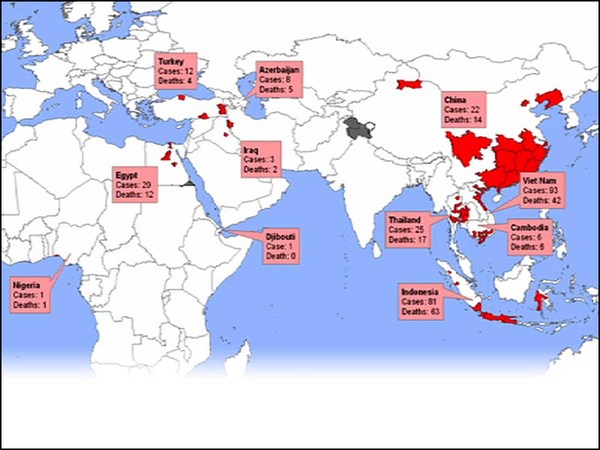
Even worse, the most common influenza -- influenza A -- also infects animals that live in close proximity to humans, and they can recombine in those particular animals. In addition, wild aquatic birds carry all known strains of influenza. So, you've got this situation: In 2003, we had an H5N1 virus that jumped from birds into humans in a few isolated cases with an apparent mortality rate of 70 percent. Now luckily, that particular virus, although very scary at the time, did not transmit from person to person very easily. This year's H1N1 threat was actually a human, avian, swine mixture that arose in Mexico. It was easily transmitted, but, luckily, was pretty mild. And so, in a sense, our luck is holding out, but you know, another wild bird could fly over at anytime.
حتی بدتر از آن، رایج ترین آنفوآانزا -- آنفلوآنزای نوع «آ» -- حیواناتی را هم آلوده میکند که در فاصله نزدیک به انسانها زندگی میکنند، و این ویروسها میتوانند در این حیوانات بازترکیب شوند. علاوه بر این، پرندگان آبزی وحشی ناقل تمام گونههای شناخته شده از آنفلوآنزا هستند. بنابراین، وضعیت از این قرار است: در سال ۲۰۰۳، ما یک ویروس H5N1 داشتیم که از چندین مورد جداگانه از پرندگان به انسان منتقل شد با میزان مرگ و میر۷۰ درصد. حالا، خوشبختانه، این ویروس خاص هرچند در آن زمان بسیار ترسناک بود، از شخص به شخص دیگر خیلی راحت منتقل نشد. تهدید H1N1 امسال یک ترکیب انسانی طیوری و خوکی بود که در مکزیک بوجود آمد. این یکی به راحتی منتقل شد، اما، خوشبختانه، بسیار خفیف بود. و خب، به قول معروف شانس با ما یار هستش اما میدانید، یک پرنده وحشی دیگر میتوانست در هر زمان پرواز کند.
Now let's take a look at HIV. As variable as flu is, HIV makes flu look like the Rock of Gibraltar. The virus that causes AIDS is the trickiest pathogen scientists have ever confronted. It mutates furiously, it has decoys to evade the immune system, it attacks the very cells that are trying to fight it and it quickly hides itself in your genome. Here's a slide looking at the genetic variation of flu and comparing that to HIV, a much wilder target. In the video a moment ago, you saw fleets of new viruses launching from infected cells. Now realize that in a recently infected person, there are millions of these ships; each one is just slightly different. Finding a weapon that recognizes and sinks all of them makes the job that much harder.
حالا بیاید به اچآیوی نگاه کنیم. به اندازه آنفلوانزا متغیر است، اچآیوی باعث میشود آنفلوانزا مانند صخره جبلالطارق شود. ویروسی که ایدز را ایجاد میکند تکان دهندهترین پاتوژنی است که دانشمندان تا به حال با آن برخورد داشتند. ویرویس آن وحشیانه جهش میکند، دامهایی برای فرار از سیستم ایمنی دارد، به بسیاری از سلولهایی که سعی دارند با آن مبارزه کنند حمله میکند و به سرعت خودش را در ژنوم شما مخفی میکند. در اینجا اسلایدی هست ناظر بر تغییرات ژنتیکی آنفلوآنزا و مقایسۀ آن با ویروس اچآیوی، که هدفی بسیار وحشیتر هست. در ویدیو چند لحظه قبل، خیزش ناوگان جدیدی از ویروسها از سلولهای آلوده را دیدید. اکنون متوجه شدید که در یک فرد تازه آلوده شده، میلیونها از این کشتیها وجود دارد: هر یک فقط کمی متفاوت است. پیدا کردن یک سلاح که همه آنها را شناخته و همه آنها را غرق کند کار را بسیار سختتر میکند.
Now, in the 27 years since HIV was identified as the cause of AIDS, we've developed more drugs to treat HIV than all other viruses put together. These drugs aren't cures, but they represent a huge triumph of science because they take away the automatic death sentence from a diagnosis of HIV, at least for those who can access them. The vaccine effort though is really quite different. Large companies moved away from it because they thought the science was so difficult and vaccines were seen as poor business. Many thought that it was just impossible to make an AIDS vaccine, but today, evidence tells us otherwise.
حالا، ۲۷ سال پس از زمانی که اچآیوی به عنوان علت ایدز شناخته شد، ما داروهای بیشتری را برای درمان ایدز نسبت به سایر ویروسهای دیگر به ارمغان آوردهایم. این داروها درمان نیستند، اما یک پیروزی عظیم علمی هستند زیرا تلقی برابری تشخیص اچآیوی با حکم مرگ را باطل کردند، حداقل برای کسانی که میتوانند به این داروها دسترسی پیدا کنند. اما تلاش برای تولید واکسن کاملا متفاوت است. شرکتهای بزرگ از این موضوع دور شدند زیرا فکر میکردند علم آن بسیار دشوار بود و واکسنها از لحاظ کسبوکار ضعیف دیده میشدند. بسیاری فکر میکردند که ساخت واکسن ایدز غیر ممکن است، اما امروز شواهد به ما چیزی دیگر میگوید.
In September, we had surprising but exciting findings from a clinical trial that took place in Thailand. For the first time, we saw an AIDS vaccine work in humans -- albeit, quite modestly -- and that particular vaccine was made almost a decade ago. Newer concepts and early testing now show even greater promise in the best of our animal models. But in the past few months, researchers have also isolated several new broadly neutralizing antibodies from the blood of an HIV infected individual. Now, what does this mean? We saw earlier that HIV is highly variable, that a broad neutralizing antibody latches on and disables multiple variations of the virus. If you take these and you put them in the best of our monkey models, they provide full protection from infection. In addition, these researchers found a new site on HIV where the antibodies can grab onto, and what's so special about this spot is that it changes very little as the virus mutates. It's like, as many times as the virus changes its clothes, it's still wearing the same socks, and now our job is to make sure we get the body to really hate those socks.
در سپتامبر، یافتههای غافلگیرانه اما هیجانانگیزی داشتیم از آزمایشهای بالینی که در تایلند اتفاق افتاد. برای اولین بار، ما یک واکسن ایدز دیدیم که در انسان کار میکرد -- با این حال، خیلی ملایم -- و این واکسن خاص تقریبا ده سال پیش ساخته شد. حالا مفاهیم جدید و تست زودهنگام نوید نتایج بهتری را در بهترین مدلهای حیوانی به ما میدهد. اما در چند ماه گذشته، محققان همچنین چندین آنتیبادی خنثیکننده گسترده جدید را از خون فرد آلوده به ویروس جدا کردهاند. حالا این چه معنی میدهد؟ ما پیشتر دیدیم که اچآیوی بسیار متغیر است، و اگر یک آنتیبادی خنثیکننده گسترده به آن بچسبد انواع مختلفی از ویروس را غیر فعال میکند. اگر این آنتیبادیها را بگیرید و آنها را در بهترین مدلهای میمونیمان قراردهید آنها باعث محافظت کامل در برابر بیماری میشوند. بعلاوه، این محققان محلهای جدیدی را در ویروس اچآیوی یافتند که آنتیبادیها میتوانند به آنجا بچسبند، و آنچه در مورد این نقطه بسیار ویژه است این است که این نقطه در طی جهش ویروس بسیار کم تغییر میکند. مثل این است که در هر دوره که ویروس لباسهایش را عوض میکند، باز هم جورابهای قبلیاش را میپوشد و اکنون کار ما این است که مطمئن شویم بدن واقعا از این جورابها متنفر میشود.
So what we've got is a situation. The Thai results tell us we can make an AIDS vaccine, and the antibody findings tell us how we might do that. This strategy, working backwards from an antibody to create a vaccine candidate, has never been done before in vaccine research. It's called retro-vaccinology, and its implications extend way beyond that of just HIV. So think of it this way. We've got these new antibodies we've identified, and we know that they latch onto many, many variations of the virus. We know that they have to latch onto a specific part, so if we can figure out the precise structure of that part, present that through a vaccine, what we hope is we can prompt your immune system to make these matching antibodies. And that would create a universal HIV vaccine. Now, it sounds easier than it is because the structure actually looks more like this blue antibody diagram attached to its yellow binding site, and as you can imagine, these three-dimensional structures are much harder to work on. And if you guys have ideas to help us solve this, we'd love to hear about it.
بنابراین آنچه که داریم یک موقعیت است. نتایج تایلندیها به ما میگوید ما میتوانیم یک واکسن ایدز ایجاد کنیم، و یافتههای آنتیبادی به ما میگوید که چگونه میتوانیم این کار را انجام دهیم این استراتژی، با انجام فرایندی معکوس از یک آنتیبادی یک واکسن کاندید میسازد، که پیش از این در تحقیقات واکسنسازی انجام نشده است. نام این راهبرد واکسنشناسی معکوس است و مفاهیم آن بسیار فراتر از صرفا ویروس اچآیوی است. خب به این شکل به آن فکر کنید. ما این آنتیبادیهای جدید را که شناختهایم در دست داریم، و میدانیم که آنها به بسیاری از انواع تغییرات ویروس میچسبند. میدانیم که آنها باید بر روی بخش خاصی چسبانده شوند، بنابراین اگر بتوانیم ساختار دقیق آن بخش را مشخص کنیم، و آن را وارد واکسن کنیم، امیدواریم که بتوانیم به سیستم ایمنی بدنتان بفهمانیم که این آنتیبادیهای مناسب را تولید کند. و این یک واکسن جهانی اچآیوی ایجاد خواهد کرد. حالا، این کار سادهتر از آنچه هست به نظر میرسد به این دلیل که ساختار در واقع بیشتر شبیه این نمودار آبی آنتیبادی است که به آن محل انقیاد زرد متصل شده، وهمان طور که در تصویر میبینید، این ساختارهای سه بعدی برای کار کردن بسیار سختتر است. اگر شما دوستان ایدههایی برای کمک به ما در حل این دارید، دوست داریم در مورد آن بشنویم.
But, you know, the research that has occurred from HIV now has really helped with innovation with other diseases. So for instance, a biotechnology company has now found broadly neutralizing antibodies to influenza, as well as a new antibody target on the flu virus. They're currently making a cocktail -- an antibody cocktail -- that can be used to treat severe, overwhelming cases of flu. In the longer term, what they can do is use these tools of retro-vaccinology to make a preventive flu vaccine. Now, retro-vaccinology is just one technique within the ambit of so-called rational vaccine design.
اما، میدانید، تحقیقاتی که روی اچآیوی رخ داده است اکنون به نگرشی نوآورانه در بیماریهای دیگر کمک کرده است. خب، به عنوان مثال، یک شرکت زیستفناوری اکنون آنتیبادی خنثیکننده گسترده ضد آنفلوآنزا را به همراه هدف جدید آنتیبادی در این ویروس یافته است. آنها در حال حاضر یک مخلوط ایجاد میکنند -- مخلوط آنتیبادی -- که میتواند برای درمان موارد شدید و قدرتمند آنفلوانزا مورد استفاده قرار گیرد. آنها میتوانند در بلند مدت، از واکسنشناسی معکوس برای ساخت واکسن پیشگیری آنفلوانزا استفاده کنند. خب، واکسنشناسی معکوس فقط یک تکنیک هست در محدودهی آنچه طراحیواکسن منطقی نامیده میشود.
Let me give you another example. We talked about before the H and N spikes on the surface of the flu virus. Notice these other, smaller protuberances. These are largely hidden from the immune system. Now it turns out that these spots also don't change much when the virus mutates. If you can cripple these with specific antibodies, you could cripple all versions of the flu. So far, animal tests indicate that such a vaccine could prevent severe disease, although you might get a mild case. So if this works in humans, what we're talking about is a universal flu vaccine, one that doesn't need to change every year and would remove the threat of death. We really could think of flu, then, as just a bad cold.
بگذارید مثال دیگری را به شما نشان دهم. ما قبلا در مورد گیرنده H و N در سطح ویروس آنفلوانزا صحبت کردیم. به این برآمدگیهای کوچک متفاوت توجه کنید. اینها عمدتا از دید سیستم ایمنی پنهان هستند. حالا معلوم شده است که این نقاط نیز زمانی که ویروس جهش میکند خیلی تغییر نمیکنند. اگر شما بتوانید این نقاط را با آنتیبادیهای خاص فلج کنید، می توانید تمام نسخههای آنفلوآنزا را فلج کنید. تا کنون آزمایشهای حیوانی نشان میدهد که چنین واکسنی میتواند از بیماری شدید جلوگیری کند. اگرچه ممکن است به یک مورد خفیف مبتلا شوید. پس اگر این روش در انسان کار کند، داریم راجع به یک واکسن آنفلوانزای جهانی حرف میزنیم، که نیازی به تغییر سالیانه ندارد و خطر مرگ را برطرف میکند. پس واقعا میشود به آنفلوانزا، به عنوان سرماخوردگی بد فکر کنیم.
Of course, the best vaccine imaginable is only valuable to the extent we get it to everyone who needs it. So to do that, we have to combine smart vaccine design with smart production methods and, of course, smart delivery methods. So I want you to think back a few months ago. In June, the World Health Organization declared the first global flu pandemic in 41 years. The U.S. government promised 150 million doses of vaccine by October 15th for the flu peak. Vaccines were promised to developing countries. Hundreds of millions of dollars were spent and flowed to accelerating vaccine manufacturing. So what happened?
البته، بهترین واکسن قابل تصور فقط زمانی ارزشمند است که ما آن را به همه کسانی که به آن نیاز دارند گسترش دهیم. بنابراین برای انجام این کار، ما باید طراحی واکسن هوشمند را با روشهای تولید هوشمند و البته روشهای تحویل هوشمند، ترکیب کنیم. خب میخواهم که به چند ماه پیش فکر کنید. در ماه ژوئن، سازمان جهانی بهداشت اولین همهگیری جهانی آنفلوآنزا را در ۴۱ سال گذشته اعلام کرد. دولت ایالات متحده متعهد شد تا ۱۵ اکتبر ۱۵۰ میلیون دوز واکسن را برای فصل ابتلا به آنفلوانزا تولید کند. واکسنها به کشورهای در حال توسعه وعده داده شدند. صدها میلیون دلار صرف شده و برای تسهیل تولید واکسن روانه شد. خب چه اتفاقی افتاد؟
Well, we first figured out how to make flu vaccines, how to produce them, in the early 1940s. It was a slow, cumbersome process that depended on chicken eggs, millions of living chicken eggs. Viruses only grow in living things, and so it turned out that, for flu, chicken eggs worked really well. For most strains, you could get one to two doses of vaccine per egg. Luckily for us, we live in an era of breathtaking biomedical advances. So today, we get our flu vaccines from ... chicken eggs, (Laughter) hundreds of millions of chicken eggs. Almost nothing has changed. The system is reliable but the problem is you never know how well a strain is going to grow. This year's swine flu strain grew very poorly in early production: basically .6 doses per egg. So, here's an alarming thought. What if that wild bird flies by again? You could see an avian strain that would infect the poultry flocks, and then we would have no eggs for our vaccines. So, Dan [Barber], if you want billions of chicken pellets for your fish farm, I know where to get them. So right now, the world can produce about 350 million doses of flu vaccine for the three strains, and we can up that to about 1.2 billion doses if we want to target a single variant like swine flu. But this assumes that our factories are humming because, in 2004, the U.S. supply was cut in half by contamination at one single plant. And the process still takes more than half a year.
خب، ما نخستین بار در ابتدای دهه ۱۹۴۰ نحوه ساخت واکسن آنفلوآنزا، و چگونگی تولید آن را متوجه شدیم. این روند آهسته و زمانبر بود که بستگی به تخممرغ داشت، میلیونها تخممرغ نطفهدار. ویروسها فقط در موجود زنده رشد میکنند، و به همین دلیل معلوم شد که برای آنفلوآنزا تخم مرغ کاملا خوب جواب میداد. برای اکثر سویهها، میتوانستید یک یا دو دوز واکسن در هر تخم داشته باشید. خوشبختانه، ما در عصر پیشرفتهای زیستپزشکی بسیار پر جنب و جوش زندگی میکنیم. بنابراین امروز، ما واکسن آنفلوآنزای خود را -- از تخممرغ میگیریم، (خنده) صدها میلیون تخممرغ. تقریبا هیچ چیز تغییر نکرده است. سیستم قابل اعتماد است اما مشکل این است که شما هرگز نمیدانید که سویه چگونه رشد میکند امسال سویه آنفلوانزای خوکی به صورت ضعیف در محصولات ابتدایی رشد کرد: اساسا ۰٫۶ دوز در هر تخم مرغ. خب در اینجا یک سوال نگران کننده وجود دارد. اگر این پرنده وحشی دوباره پرواز کند چه؟ شاید یک سویه طیوری را ببینید که جمعیت مرغهای پرورشی را آلوده میکند، آنوقت برای واکسنهایمان تخممرغی نداریم. پس، دن[باربر] (آشپز معروف)، اگر میلیاردها کپسول گوشت مرغ برای پرورش ماهیت میخواهی، من میدانم از کجا آن را تأمین کنی. بنابراین امروز، جهان میتواند ۳۵۰ میلیون دوز واکسن آنفلوانزا را برای سه سویه تولید کند، و میتوانیم آن را به حدود ۱٫۲ میلیارد دوز افزایش دهیم اگر بخواهیم تنها یک سویه را مثلا آنفلوانزای خوکی را هدف قرار دهیم. اما این فرض میشود که کارخانههای ما دایم مشغول کارند، زیرا در سال ۲۰۰۴، تولید ایالات متحده به نصف کاهش یافت فقط بخاطر آلوده شدن یک کارخانه. و این فرایند هنوز بیش از نصف سال زمان میبرد.
So are we better prepared than we were in 1918? Well, with the new technologies emerging now, I hope we can say definitively, "Yes." Imagine we could produce enough flu vaccine for everyone in the entire world for less than half of what we're currently spending now in the United States. With a range of new technologies, we could. Here's an example: A company I'm engaged with has found a specific piece of the H spike of flu that sparks the immune system. If you lop this off and attach it to the tail of a different bacterium, which creates a vigorous immune response, they've created a very powerful flu fighter. This vaccine is so small it can be grown in a common bacteria, E. coli. Now, as you know, bacteria reproduce quickly -- it's like making yogurt -- and so we could produce enough swine origin flu for the entire world in a few factories, in a few weeks, with no eggs, for a fraction of the cost of current methods.
خب آیا ما نسبت به سال ۱۹۱۸ آمادهتر هستیم؟ خب، با فناوریهای جدید در حال ظهور امروزه، امیدوارم بتوانیم بطور قطعی بگوییم، «بله». تصور کنید میتوانستیم واکسن آنفلوانزای کافی را برای هر کسی در سراسر جهان با نصف هزینه امروزی در ایالات متحده تولید کنیم. با طیف وسیعی از فناوریهای جدید، این کار شدنی است. در اینجا یک مثال میزنم: شرکتی که در آن مشغول هستم قطعه خاص از گیرنده اچ آنفلوانزا پیدا کرده که سیستم ایمنی بدن را تحریک میکند. اگر شما این را بریده و آن را به دم یک باکتری متفاوت متصل کنید، که پاسخ ایمنی شدیدی ایجاد میکند، آنها یک جنگنده قدرتمند ضد آنفلوانزا ایجاد کردهاند این واکسن بسیار کوچک است و میتواند در یک باکتری رایج مثل E. coli رشد کند. حالا، همانطور که میدانید، باکتریها به سرعت تولید مثل میکنند -- مثل درست کردن ماست است -- و بنابراین میتوانیم در چند کارخانه، ظرف مدت چند هفته، بدون هیچ تخم مرغی و با کسری از هزینه روشهای فعلی واکسن آنفلوانزای خوکی را به اندازه کافی تولید کنیم.
(Applause)
(تشویق)
So here's a comparison of several of these new vaccine technologies. And, aside from the radically increased production and huge cost savings -- for example, the E. coli method I just talked about -- look at the time saved: this would be lives saved. The developing world, mostly left out of the current response, sees the potential of these alternate technologies and they're leapfrogging the West. India, Mexico and others are already making experimental flu vaccines, and they may be the first place we see these vaccines in use. Because these technologies are so efficient and relatively cheap, billions of people can have access to lifesaving vaccines if we can figure out how to deliver them.
خب اینجا مقایسهای هست بین چند مورد از این فناوریهای جدید واکسن. و جدا از افزایش قابل توجه تولید و صرفهجویی عظیم در هزینهها -- مثلا روش ایکولای که صحبت کردم -- به زمان ذخیره شده نگاه کنید: همان مقدار زندگی میتواند نجات یابد. جهان در حال توسعه، که اغلب از جریان فعلی جا مانده، توانایی این فناوریهای جایگزین را میبیند و غرب را پشت سر میگذارد. هند، مکزیک و دیگران در حال حاضر واکسنهای آزمایشی آنفلوانزا را تولید میکنند. و ممکن است اولین مکانی باشند که کاربرد واکسن را در آن ببینیم. چون که این فناوریها بسیار کارآمد و نسبتا ارزان هستند، اگر بتوانیم چگونگی تأمین آنها را پیدا کنیم میلیاردها نفر میتوانند به واکسنهای نجاتبخش دسترسی پیدا کنند
Now think of where this leads us. New infectious diseases appear or reappear every few years. Some day, perhaps soon, we'll have a virus that is going to threaten all of us. Will we be quick enough to react before millions die? Luckily, this year's flu was relatively mild. I say, "luckily" in part because virtually no one in the developing world was vaccinated. So if we have the political and financial foresight to sustain our investments, we will master these and new tools of vaccinology, and with these tools we can produce enough vaccine for everyone at low cost and ensure healthy productive lives. No longer must flu have to kill half a million people a year. No longer does AIDS need to kill two million a year. No longer do the poor and vulnerable need to be threatened by infectious diseases, or indeed, anybody. Instead of having Vaclav Smil's "massively fatal discontinuity" of life, we can ensure the continuity of life. What the world needs now are these new vaccines, and we can make it happen.
حالا فکر کنید که این ما را به کجا میبرد. بیماریهای جدید مسری هر چند سال یک بار ظاهر میشوند یکروز، شاید به زودی ما ویروسی خواهیم داشت که همه ما را تهدید میکند. آیا به اندازه کافی سریع واکنش نشان خواهیم داد قبل از اینکه میلیونها نفر بمیرند؟ خوشبختانه، آنفلوآنزای امسال نسبتا خفیف بود. من میگویم، «خوشبختانه» به این دلیل که تقریبا هیچکس در جهان در حال توسعه واکسینه نشده بود. بنابراین اگر پیشبینیهای سیاسی و مالی را برای سرمایهگذاریهایمان حفظ کنیم. ما این ابزارها و روشهای جدید واکسنشناسی را به کار خواهیم گرفت و با استفاده از این ابزار میتوانیم واکسن کافی برای هرکسی را با هزینه کم تولید کنیم و از زندگی پربار سالم اطمینان حاصل کنیم. دیگر آنفلوانزا نباید نیم میلیوننفر را در سال نابود کند ایدز دیگر نیازی به کشتن دو میلیون نفر در سال ندارد. دیگر فقر و آسیبپذیری نباید توسط بیماریهای عفونی تهدید شود. یا در واقع هیچکسی. عوض داشتن فجایع تهدید کننده زندگی از نظر واکلاو اسمیل موسوم به «گسستگی بسیار مهلک»، میتوانیم تداوم زندگی را تضمین کنیم. الان جهان به واکسنهای جدید نیاز دارد و ما میتوانیم آن را عملی کنیم.
Thank you very much.
بسیار ممنونم.
(Applause)
(تشویق)
Chris Anderson: Thank you. (Applause) Thank you. So, the science is changing. In your mind, Seth -- I mean, you must dream about this -- what is the kind of time scale on, let's start with HIV, for a game-changing vaccine that's actually out there and usable?
کریس اندرسون: ممنونم (تشویق) ممنونم. خب، علم رو به تغییر است. از دیدگاه تو، سث -- تو حتما در این باره رویایی داری -- چه مدت طول خواهد کشید بگذار با اچآیوی شروع کنیم، تا واکسنی برتر و کاملا در دسترس تولید شود؟
SB: The game change can come at any time, because the problem we have now is we've shown we can get a vaccine to work in humans; we just need a better one. And with these types of antibodies, we know humans can make them. So, if we can figure out how to do that, then we have the vaccine, and what's interesting is there already is some evidence that we're beginning to crack that problem. So, the challenge is full speed ahead.
س.ب: واکسن برتر هر لحظه ممکن است تولید شود، چرا که مشکلی که ما اکنون داریم این است که نشان دادهایم میتوانیم واکسنی بسازیم که در انسان کار کند؛ فقط باید بهترش کنیم. و با این آنتیبادیها انسان میتواند آنها را بسازد. بنابراین، اگر چگونگی انجام آن را بفهمیم، آنگاه واکسن را داریم، و نکته جالب این است که در حال حاضر شواهدی هست که شروع به حل این مشکل کردیم. بنابراین، چالش با سرعت حل میشود.
CA: In your gut, do you think it's probably going to be at least another five years?
ک ا: به نظرت، حداقل پنج سال دیگر بشود؟
SB: You know, everybody says it's 10 years, but it's been 10 years every 10 years. So I hate to put a timeline on scientific innovation, but the investments that have occurred are now paying dividends.
میدونید، هرکسی میگوید ۱۰ سال است. اما هر۱۰ سال ۱۰ سال است. بنابراین من متنفرم که یک جدول زمانی در نوآوری علمی قرار دهم. اما سرمایهگذاریهایی که رخ دادهاست اکنون سود را پرداخت میکنند
CA: And that's the same with universal flu vaccine, the same kind of thing?
ک.ا: و درباره واکسن جهانی آنفلوانزا هم همینطور هست؟
SB: I think flu is different. I think what happened with flu is we've got a bunch -- I just showed some of this -- a bunch of really cool and useful technologies that are ready to go now. They look good. The problem has been that, what we did is we invested in traditional technologies because that's what we were comfortable with. You also can use adjuvants, which are chemicals you mix. That's what Europe is doing, so we could have diluted out our supply of flu and made more available, but, going back to what Michael Specter said, the anti-vaccine crowd didn't really want that to happen.
س ب: فکر میکنم آنفلوانزا فرق دارد. برای آن کلی چیز داریم --که چند تا را نشان دادم -- که امروزه آماده استفاده هستند. آنها خوب به نظر میرسند. مشکل این بوده که سرمایهگذاری ما روی فناوریهای سنتی انجام شده زیرا با این فناوری راحتتر بودیم. میتوانید از مکملهای واکسن استفاده کنید که ترکیبی شیمیایی است. این کار را الان اروپا انجام میدهد، تا بتوانیم ذخیره واکسنها را رقیقتر کرده و در دسترس بیشتر قرار دهیم، اما، همانطور که مایکل اسپکتر قبلا گفت، جمعیت ضد واکسن واقعا نمیخواهد که این اتفاق بیافتد.
CA: And malaria's even further behind?
ک ا: و مالاریا حتی از این هم عقبتر است؟
SB: No, malaria, there is a candidate that actually showed efficacy in an earlier trial and is currently in phase three trials now. It probably isn't the perfect vaccine, but it's moving along.
س.ب: خیر، مالاریا، واکسن کاندیدایی دارد که در آزمایش پیشین اثربخشی نشان داده است و اکنون در مرحله سوم آزمایش قرار دارد. احتمالا این واکسن کامل نیست. اما در حال پیشرفت است.
CA: Seth, most of us do work where every month, we produce something; we get that kind of gratification. You've been slaving away at this for more than a decade, and I salute you and your colleagues for what you do. The world needs people like you. Thank you.
ک ا: سث، اکثر ما ماهانه جایی کار میکنیم که چیزی را تولید میکنیم؛ و از آن نوعی احساس رضایت میکنیم. شما برای بیش از یک دهه از این کار خودداری کردهاید، و من برای آنچه انجام میدهید به شما و همکارانتان درود میفرستم، دنیا به مردمانی مثل شما نیاز دارد.
SB: Thank you.
س.ب: ممنونم.
(Applause)
(تشویق)