Do you worry about what is going to kill you? Heart disease, cancer, a car accident? Most of us worry about things we can't control, like war, terrorism, the tragic earthquake that just occurred in Haiti. But what really threatens humanity? A few years ago, Professor Vaclav Smil tried to calculate the probability of sudden disasters large enough to change history. He called these, "massively fatal discontinuities," meaning that they could kill up to 100 million people in the next 50 years. He looked at the odds of another world war, of a massive volcanic eruption, even of an asteroid hitting the Earth. But he placed the likelihood of one such event above all others at close to 100 percent, and that is a severe flu pandemic. Now, you might think of flu as just a really bad cold, but it can be a death sentence. Every year, 36,000 people in the United States die of seasonal flu. In the developing world, the data is much sketchier but the death toll is almost certainly higher. You know, the problem is if this virus occasionally mutates so dramatically, it essentially is a new virus and then we get a pandemic.
¿Les preocupa lo que les va a matar? ¿Una enfermedad cardíaca, cáncer un accidente de tránsito? La mayoría de nosotros se preocupa por cosas que no podemos controlar como la guerra, el terrorismo, el terremoto trágico que acaba de ocurrir en Haití. ¿Pero qué es lo que realmente amenaza a la humanidad? Hace unos años el profesor Vaclav Smil intentó calcular la probabilidad de desastres repentinos lo suficientemente grandes como para cambiar la historia. Los llamó "discontinuidades fatales masivas", lo que significa que podrían causar la muerte de hasta 100 millones de personas en los próximos 50 años. Estudió la probabilidad de una nueva guerra mundial, de una erupción volcánica masiva incluso del impacto de un asteroide contra la Tierra. Pero situó la probabilidad de uno de tales eventos sobre todas los demás y cercana a un 100%: la posibilidad de una epidemia grave de gripe. Ahora bien, se podría pensar que la gripe es sólo un resfriado muy fuerte. Pero puede ser una sentencia de muerte. Cada año mueren 36.000 personas en EE.UU. de gripe estacional. En el mundo en desarrollo la información es más incompleta pero el número de víctimas es casi seguro, mayor. Ya saben, el problema es que si este virus muta en ocasiones de manera espectacular esencialmente, es un virus nuevo. Y entonces tenemos una pandemia.
In 1918, a new virus appeared that killed some 50 to 100 million people. It spread like wildfire and some died within hours of developing symptoms. Are we safer today? Well, we seem to have dodged the deadly pandemic this year that most of us feared, but this threat could reappear at any time. The good news is that we're at a moment in time when science, technology, globalization is converging to create an unprecedented possibility: the possibility to make history by preventing infectious diseases that still account for one-fifth of all deaths and countless misery on Earth. We can do this. We're already preventing millions of deaths with existing vaccines, and if we get these to more people, we can certainly save more lives. But with new or better vaccines for malaria, TB, HIV, pneumonia, diarrhea, flu, we could end suffering that has been on the Earth since the beginning of time.
En 1918 apareció un nuevo virus que mató a entre 50 y 100 millones de personas. Se extendió como reguero de pólvora. Y algunos murieron pocas horas después de desarrollar los síntomas. ¿Estamos más seguros hoy? Bueno, parece que hemos evitado la pandemia mortal de este año que la mayoría temíamos, pero esta amenaza podría reaparecer en cualquier momento. La buena noticia es que estamos en un momento en el que la convergencia de ciencia, tecnología y globalización está creando una posibilidad sin precedentes, la posibilidad de hacer historia mediante la prevención de enfermedades infecciosas que siguen representando una quinta parte de todas las muertes e incontable desdicha en la Tierra. Podemos hacerlo. Ya estamos evitando millones de muertes con las vacunas existentes. Y si llevamos éstas a más personas seguramente podemos salvar más vidas. Pero con nuevas o mejores vacunas contra la malaria, la tuberculosis, el VIH, la neumonía, la diarrea o la gripe podríamos terminar con el sufrimiento que ha estado presente en la Tierra desde el principio de los tiempos.
So, I'm here to trumpet vaccines for you. But first, I have to explain why they're important because vaccines, the power of them, is really like a whisper. When they work, they can make history, but after a while you can barely hear them. Now, some of us are old enough to have a small, circular scar on our arms from an inoculation we received as children. But when was the last time you worried about smallpox, a disease that killed half a billion people last century and no longer is with us? Or polio? How many of you remember the iron lung? We don't see scenes like this anymore because of vaccines.
Así que estoy aquí para anunciarles con bombo y platillo las vacunas. Pero primero tengo que explicar por qué son importantes. Porque las vacunas, el poder que tienen, es realmente como un susurro. Si funcionan, pueden hacer historia, pero después de un rato apenas se las oye. Ahora bien, algunos somos lo suficientemente mayores como para tener una pequeña cicatriz circular en nuestros brazos de una inoculación que recibimos de niños. ¿Pero cuándo fue la última vez que se preocuparon ustedes por la viruela?, una enfermedad que mató a 500 millones de personas el siglo pasado y ya no está con nosotros. O la polio, ¿cuántos recuerdan el pulmón de acero o pulmotor? Ya no vemos escenas como esta gracias a las vacunas.
Now, it's interesting because there are 30-odd diseases that can be treated with vaccines now, but we're still threatened by things like HIV and flu. Why is that? Well, here's the dirty little secret. Until recently, we haven't had to know exactly how a vaccine worked. We knew they worked through old-fashioned trial and error. You took a pathogen, you modified it, you injected it into a person or an animal and you saw what happened. This worked well for most pathogens, somewhat well for crafty bugs like flu, but not at all for HIV, for which humans have no natural immunity.
Ahora, ya saben, es interesante porque hay unas 30 enfermedades que hoy pueden tratarse con vacunas pero todavía estamos amenazados por cosas como el VIH y la gripe. ¿Por qué? Bueno, esta es la cruel realidad. Hasta hace poco no hemos necesitado saber exactamente cómo funcionaban las vacunas. Sabíamos que funcionaban mediante el método tradicional de prueba y error. Uno tomaba un patógeno, lo modificaba, se lo inyectaba a una persona o animal y se veía lo que pasaba. Esto funcionaba bien para la mayoría de los patógenos, bastante bien para bichos astutos como la gripe pero no funciona en absoluto para el VIH para el que los humanos carecemos de inmunidad natural.
So let's explore how vaccines work. They basically create a cache of weapons for your immune system which you can deploy when needed. Now, when you get a viral infection, what normally happens is it takes days or weeks for your body to fight back at full strength, and that might be too late. When you're pre-immunized, what happens is you have forces in your body pre-trained to recognize and defeat specific foes. So that's really how vaccines work. Now, let's take a look at a video that we're debuting at TED, for the first time, on how an effective HIV vaccine might work.
Así que vamos a estudiar cómo funcionan las vacunas. Básicamente crean una batería de armas para el sistema inmunológico que uno puede desplegar cuando sea necesario. Cuando uno tiene una infección viral, lo que sucede normalmente es que al cuerpo le lleva días o semanas defenderse a pleno rendimiento, y eso podría ser demasiado tarde. Cuando uno está preinmunizado lo que sucede es que uno tiene fuerzas en el cuerpo preentrenadas para reconocer y derrotar a enemigos específicos. Así es como funcionan realmente las vacunas. Ahora, echemos un vistazo a un video que estamos estrenando en TED por primera vez de cómo podría funcionar una vacuna eficaz contra el VIH.
(Music)
(Música)
Narrator: A vaccine trains the body in advance how to recognize and neutralize a specific invader. After HIV penetrates the body's mucosal barriers, it infects immune cells to replicate. The invader draws the attention of the immune system's front-line troops. Dendritic cells, or macrophages, capture the virus and display pieces of it. Memory cells generated by the HIV vaccine are activated when they learn HIV is present from the front-line troops. These memory cells immediately deploy the exact weapons needed. Memory B cells turn into plasma cells, which produce wave after wave of the specific antibodies that latch onto HIV to prevent it from infecting cells, while squadrons of killer T cells seek out and destroy cells that are already HIV infected. The virus is defeated. Without a vaccine, these responses would have taken more than a week. By that time, the battle against HIV would already have been lost.
Narradora: una vacuna entrena al cuerpo por anticipado sobre cómo reconocer y neutralizar a un invasor específico. Una vez que el VIH atraviesa las barreras mucosas del cuerpo infecta a células inmunes para replicarse. El invasor llama la atención de las tropas de vanguardia del sistema inmune. Las células dendríticas o los macrófagos capturan el virus y muestran partes de él. Las células de memoria generadas por la vacuna del VIH se activan cuando se enteran por las tropas de vanguardia de que el VIH está presente. Estas células de memoria despliegan inmediatamente las armas exactas necesarias. Las células de memoria B se convierten en células plasmáticas, que producen oleadas sucesivas de anticuerpos específicos que se adhieren al VIH para evitar que infecte las células mientras que escuadrones de células asesinas T buscan y destruyen células ya infectadas por el VIH. El virus es derrotado. Sin una vacuna, estas respuestas habrían llevado más de una semana. Para ese entonces, la batalla contra el VIH ya se habría perdido.
Seth Berkley: Really cool video, isn't it? The antibodies you just saw in this video, in action, are the ones that make most vaccines work. So the real question then is: How do we ensure that your body makes the exact ones that we need to protect against flu and HIV? The principal challenge for both of these viruses is that they're always changing. So let's take a look at the flu virus. In this rendering of the flu virus, these different colored spikes are what it uses to infect you. And also, what the antibodies use is a handle to essentially grab and neutralize the virus. When these mutate, they change their shape, and the antibodies don't know what they're looking at anymore. So that's why every year you can catch a slightly different strain of flu. It's also why in the spring, we have to make a best guess at which three strains are going to prevail the next year, put those into a single vaccine and rush those into production for the fall.
Seth Berkley: un video estupendo, ¿no? Los anticuerpos que acaban de ver en acción en el vídeo son los que hacen funcionar la mayoría de las vacunas. Así que la pregunta real es entonces: ¿Cómo podemos asegurarnos de que el cuerpo produzca exactamente los anticuerpos que necesitamos para protegernos de la gripe y el VIH? El desafío principal respecto a ambos virus es que siempre están cambiando. Así que echemos un vistazo a los virus de la gripe. En esta visualización del virus de la gripe estos picos de diferentes colores son lo que éste utiliza para infectarnos. Y, además, son lo que los anticuerpos utilizan como un asidero esencialmente para agarrar y neutralizar el virus. Cuando estos mutan, cambian de forma y los anticuerpos ya no saben lo que están viendo. Por esta razón, cada año, uno puede pescar una cepa ligeramente diferente de la gripe. Es por eso que en la primavera tenemos que hacer conjeturas sobre qué tres cepas van a prevalecer al año siguiente, las ponemos en una sola vacuna y, deprisa y corriendo, hacemos que se produzcan para que estén listas para el otoño.
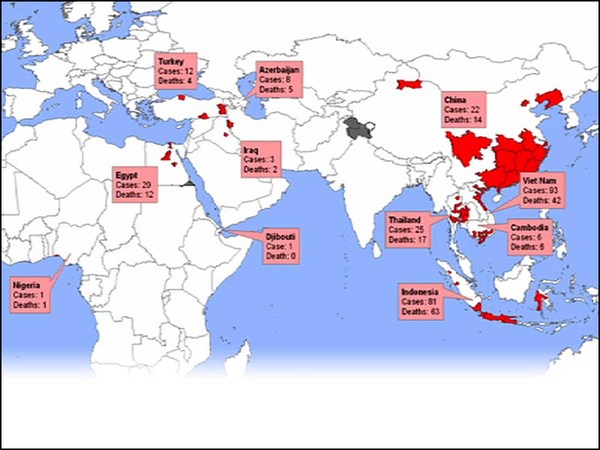
Even worse, the most common influenza -- influenza A -- also infects animals that live in close proximity to humans, and they can recombine in those particular animals. In addition, wild aquatic birds carry all known strains of influenza. So, you've got this situation: In 2003, we had an H5N1 virus that jumped from birds into humans in a few isolated cases with an apparent mortality rate of 70 percent. Now luckily, that particular virus, although very scary at the time, did not transmit from person to person very easily. This year's H1N1 threat was actually a human, avian, swine mixture that arose in Mexico. It was easily transmitted, but, luckily, was pretty mild. And so, in a sense, our luck is holding out, but you know, another wild bird could fly over at anytime.
Y lo que es peor, la gripe más común, la gripe A, también infecta a los animales que viven cerca de las personas, y puede recombinarse en esos animales en particular. Además, las aves acuáticas silvestres son portadoras de todas las cepas conocidas de la influenza. Por lo tanto nos encontramos en esta situación. En 2003 tuvimos un virus H5N1 que pasó de las aves a las personas en algunos casos aislados con una tasa de mortalidad aparente del 70%. Por suerte, ese virus en particular, aunque fue muy aterrador en su momento, no se transmitió con facilidad de unas personas a otras. La amenaza de este año del H1N1 era en realidad una mezcla humano-aviar-porcina que surgió en México. Se transmitió fácilmente pero, por suerte, fue bastante leve. Por eso, en cierto sentido, nuestra suerte está durando pero, ya saben, las aves silvestres podrían sobrevolar en cualquier momento.
Now let's take a look at HIV. As variable as flu is, HIV makes flu look like the Rock of Gibraltar. The virus that causes AIDS is the trickiest pathogen scientists have ever confronted. It mutates furiously, it has decoys to evade the immune system, it attacks the very cells that are trying to fight it and it quickly hides itself in your genome. Here's a slide looking at the genetic variation of flu and comparing that to HIV, a much wilder target. In the video a moment ago, you saw fleets of new viruses launching from infected cells. Now realize that in a recently infected person, there are millions of these ships; each one is just slightly different. Finding a weapon that recognizes and sinks all of them makes the job that much harder.
Ahora echemos un vistazo al VIH. Por muy variable que sea la gripe, el VIH hace que la gripe parezca el Peñón de Gibraltar. El virus que causa el SIDA es el patógeno más taimado con el que los científicos se han enfrentado jamás. Muta con furia. Cuenta con trampas para evadir el sistema inmune. Ataca a las mismas células que están tratando de luchar contra él. Y rápidamente se esconde en el genoma. En esta diapositiva se ve la variación genética de la gripe en comparación con la del VIH, un objetivo mucho más salvaje. En el video de hace un momento veíamos flotas de nuevos virus que se lanzaban desde células infectadas. Ahora piensen que en una persona recién infectada hay millones de estos barcos y cada uno es ligeramente diferente. Encontrar un arma que reconozca a todos y los hunda hace que el trabajo sea mucho más difícil.
Now, in the 27 years since HIV was identified as the cause of AIDS, we've developed more drugs to treat HIV than all other viruses put together. These drugs aren't cures, but they represent a huge triumph of science because they take away the automatic death sentence from a diagnosis of HIV, at least for those who can access them. The vaccine effort though is really quite different. Large companies moved away from it because they thought the science was so difficult and vaccines were seen as poor business. Many thought that it was just impossible to make an AIDS vaccine, but today, evidence tells us otherwise.
Ahora bien, en los 27 años pasados desde que se identificó el VIH como la causa del SIDA, hemos desarrollado más fármacos para tratar el VIH que todos los demás virus juntos. Estos medicamentos no son la cura, pero representan un gran triunfo de la ciencia, porque eliminan la pena de muerte automática a partir de un diagnóstico de VIH, al menos para los que pueden acceder a ellos. El esfuerzo de la vacuna, sin embargo, es muy diferente. Las grandes empresas se retiraban de él porque pensaban que la ciencia era muy difícil y las vacunas se veían como un mal negocio. Muchos pensaron que era imposible hacer una vacuna contra el SIDA, pero hoy, las pruebas muestran que no es así.
In September, we had surprising but exciting findings from a clinical trial that took place in Thailand. For the first time, we saw an AIDS vaccine work in humans -- albeit, quite modestly -- and that particular vaccine was made almost a decade ago. Newer concepts and early testing now show even greater promise in the best of our animal models. But in the past few months, researchers have also isolated several new broadly neutralizing antibodies from the blood of an HIV infected individual. Now, what does this mean? We saw earlier that HIV is highly variable, that a broad neutralizing antibody latches on and disables multiple variations of the virus. If you take these and you put them in the best of our monkey models, they provide full protection from infection. In addition, these researchers found a new site on HIV where the antibodies can grab onto, and what's so special about this spot is that it changes very little as the virus mutates. It's like, as many times as the virus changes its clothes, it's still wearing the same socks, and now our job is to make sure we get the body to really hate those socks.
En septiembre se obtuvieron resultados sorprendentes y emocionantes en un ensayo clínico realizado en Tailandia. Por primera vez, vimos una vacuna contra el SIDA que, si bien modestamente, funcionaba en las personas. Y esa vacuna, en particular, se hizo hace casi una década. Nuevos conceptos y pruebas tempranas ofrecen resultados incluso más prometedores en el mejor de nuestros modelos animales. Pero en hace pocos meses los investigadores han aislado también varios nuevos anticuerpos ampliamente neutralizantes ("broadly neutralizing antibodies" o bnAbs) a partir de la sangre de una persona infectada con VIH. Ahora, ¿qué significa esto? Ya hemos visto que el VIH es muy variable, que un anticuerpo ampliamente neutralizante se adhiere y desactiva variaciones múltiples del virus. Y que si se toman estos bnAb y se ponen en el mejor de nuestros modelos en monos proporcionan una protección completa contra la infección. Además, estos investigadores encontraron un nuevo sitio de fijación en el VIH al que pueden agarrarse los anticuerpos. Y la característica que convierte este punto en algo muy especial es que cambia muy poco a medida que el virus muta. Es como si por muchas veces que el virus se cambiara de ropa siguiera dejándose siempre los mismos calcetines, y ahora nuestro trabajo consiste en asegurarnos de conseguir que el cuerpo odie realmente esos calcetines.
So what we've got is a situation. The Thai results tell us we can make an AIDS vaccine, and the antibody findings tell us how we might do that. This strategy, working backwards from an antibody to create a vaccine candidate, has never been done before in vaccine research. It's called retro-vaccinology, and its implications extend way beyond that of just HIV. So think of it this way. We've got these new antibodies we've identified, and we know that they latch onto many, many variations of the virus. We know that they have to latch onto a specific part, so if we can figure out the precise structure of that part, present that through a vaccine, what we hope is we can prompt your immune system to make these matching antibodies. And that would create a universal HIV vaccine. Now, it sounds easier than it is because the structure actually looks more like this blue antibody diagram attached to its yellow binding site, and as you can imagine, these three-dimensional structures are much harder to work on. And if you guys have ideas to help us solve this, we'd love to hear about it.
Así que lo que tenemos es una situación. Los resultados tailandeses nos dicen que podemos hacer una vacuna contra el SIDA. Y los resultados con anticuerpos nos dicen cómo podría hacerse. Esta estrategia, trabajar hacia atrás, a partir de un anticuerpo para crear un candidato a vacuna nunca se había hecho antes en la investigación de vacunas. Se llama retrovacunología y sus consecuencias se extienden mucho más allá del VIH. Piénsenlo de esta manera. Hemos identificado estos nuevos anticuerpos y sabemos que se adhieren a muchas, muchas variaciones de este virus. Sabemos que tienen que adherirse a una parte específica así que si podemos imaginarnos la estructura precisa de esa parte y presentarla en forma de vacuna, lo que esperamos es poder empujar al sistema inmunológico a que produzca los anticuerpos correspondientes. Y eso crearía una vacuna universal para el VIH. Ahora bien, suena más fácil de lo que es porque la estructura en realidad se parece más a este diagrama de anticuerpos azul amarrado a su sitio de fijación amarillo. Y como pueden imaginar, es mucho más difícil trabajar con estas estructuras tridimensionales. Y si Uds., amigos, tienen ideas para ayudarnos a resolver esto, sepan que nos encantaría oírlas.
But, you know, the research that has occurred from HIV now has really helped with innovation with other diseases. So for instance, a biotechnology company has now found broadly neutralizing antibodies to influenza, as well as a new antibody target on the flu virus. They're currently making a cocktail -- an antibody cocktail -- that can be used to treat severe, overwhelming cases of flu. In the longer term, what they can do is use these tools of retro-vaccinology to make a preventive flu vaccine. Now, retro-vaccinology is just one technique within the ambit of so-called rational vaccine design.
Pero, ya saben, la investigación relacionada con el VIH ha ayudado realmente a la innovación para otras enfermedades. Así, por ejemplo, una empresa de biotecnología ha encontrado anticuerpos ampliamente neutralizantes para la influenza, así como una nueva diana para los anticuerpos en el virus de la influenza. Actualmente están haciendo un cóctel, un cóctel de anticuerpos que puede usarse para tratar casos graves, abrumadores, de la gripe. Ahora, a largo plazo, lo que pueden hacer es usar estas herramientas en retrovacunología para hacer una vacuna antigripal preventiva. Ahora bien, la retrovacunología es sólo una técnica en el ámbito del denominado diseño de vacunas racional.
Let me give you another example. We talked about before the H and N spikes on the surface of the flu virus. Notice these other, smaller protuberances. These are largely hidden from the immune system. Now it turns out that these spots also don't change much when the virus mutates. If you can cripple these with specific antibodies, you could cripple all versions of the flu. So far, animal tests indicate that such a vaccine could prevent severe disease, although you might get a mild case. So if this works in humans, what we're talking about is a universal flu vaccine, one that doesn't need to change every year and would remove the threat of death. We really could think of flu, then, as just a bad cold.
Permítanme mostrarles otro ejemplo. Hablamos antes de los picos H y M en la superficie del virus de la influenza. Observen estas otras protuberancias de menor tamaño. En su mayoría permanecen ocultas para el sistema inmune. Pero resulta que estos puntos no cambian mucho cuando el virus muta. Si se pudieran inutilizar con anticuerpos específicos, se podrían inutilizar todas las versiones de la gripe. Hasta el momento, las pruebas en animales indican que tal vacuna podría prevenir la enfermedad grave, aunque se podría contraer un caso leve. Así que si esto funciona con humanos, estamos hablando de una vacuna antigripal universal, una que no haya que cambiar cada año y que elimine la amenaza de muerte. En ese caso sí que podríamos ver la gripe sólo como un resfriado fuerte.
Of course, the best vaccine imaginable is only valuable to the extent we get it to everyone who needs it. So to do that, we have to combine smart vaccine design with smart production methods and, of course, smart delivery methods. So I want you to think back a few months ago. In June, the World Health Organization declared the first global flu pandemic in 41 years. The U.S. government promised 150 million doses of vaccine by October 15th for the flu peak. Vaccines were promised to developing countries. Hundreds of millions of dollars were spent and flowed to accelerating vaccine manufacturing. So what happened?
Claro, la mejor vacuna imaginable sólo es valiosa en la medida en que podamos hacer que llegue a todo el mundo que la necesite. Así que para hacer eso, tenemos que combinar diseño de vacunas inteligente con métodos de producción inteligentes y, por supuesto, con métodos de administración inteligentes. Así que quiero que se retrotraigan a unos meses atrás. En junio, la Organización Mundial de la Salud declaró la primer pandemia mundial de gripe en 41 años. El gobierno de EE.UU. prometió 150 millones de dosis de vacunas para antes del 15 de octubre para el pico de gripe. Se prometieron vacunas para los países en desarrollo. Se gastaron cientos de millones de dólares en acelerar la fabricación de vacunas. ¿Y qué pasó?
Well, we first figured out how to make flu vaccines, how to produce them, in the early 1940s. It was a slow, cumbersome process that depended on chicken eggs, millions of living chicken eggs. Viruses only grow in living things, and so it turned out that, for flu, chicken eggs worked really well. For most strains, you could get one to two doses of vaccine per egg. Luckily for us, we live in an era of breathtaking biomedical advances. So today, we get our flu vaccines from ... chicken eggs, (Laughter) hundreds of millions of chicken eggs. Almost nothing has changed. The system is reliable but the problem is you never know how well a strain is going to grow. This year's swine flu strain grew very poorly in early production: basically .6 doses per egg. So, here's an alarming thought. What if that wild bird flies by again? You could see an avian strain that would infect the poultry flocks, and then we would have no eggs for our vaccines. So, Dan [Barber], if you want billions of chicken pellets for your fish farm, I know where to get them. So right now, the world can produce about 350 million doses of flu vaccine for the three strains, and we can up that to about 1.2 billion doses if we want to target a single variant like swine flu. But this assumes that our factories are humming because, in 2004, the U.S. supply was cut in half by contamination at one single plant. And the process still takes more than half a year.
Bueno, primero descubrimos cómo hacer vacunas antigripales, cómo producirlas, a principios de los años 40. Era un proceso lento y complejo que dependía de los huevos de gallina, millones de huevos de gallina vivos. Los virus sólo crecen en cosas vivas y resultó que, para la gripe, los huevos de gallina funcionaban muy bien. Para la mayoría de las cepas se podía conseguir una o dos dosis de vacuna por huevo. Por suerte para nosotros vivimos en una era de espectaculares avances biomédicos. Así que hoy día, obtenemos nuestras vacunas de... ...huevos de gallina. (Risas) cientos de millones de huevos de gallina. Ya saben, casi nada ha cambiado. Bueno, el sistema es fiable. Pero el problema es que uno nunca sabe lo bien que va a crecer una cepa. La cepa de la gripe porcina de este año creció muy poco en la producción temprana básicamente 0,6 dosis por huevo. Y he aquí un pensamiento alarmante. ¿Qué pasaría si pasase otra vez ese pájaro silvestre? Podríamos ver una cepa aviar que infectaría a las aves de corral y entonces no tendríamos huevos para nuestras vacunas. Por lo tanto, Dan [Barber], si quieres miles de millones de pellets de pollo para tu granja de peces, sé donde conseguirlos. Así que, actualmente, el mundo puede producir unos 350 millones de dosis de vacuna antigripal para las tres cepas. Y podemos incrementar eso a 1.200 millones de dosis si queremos centrarnos en una sola variante como la gripe porcina. Pero eso suponiendo que nuestras fábricas trabajen a pleno rendimiento porque, en 2004, el suministro de EE.UU. se redujo a la mitad por la contaminación en una sola planta. Y el proceso aún lleva más de medio año.
So are we better prepared than we were in 1918? Well, with the new technologies emerging now, I hope we can say definitively, "Yes." Imagine we could produce enough flu vaccine for everyone in the entire world for less than half of what we're currently spending now in the United States. With a range of new technologies, we could. Here's an example: A company I'm engaged with has found a specific piece of the H spike of flu that sparks the immune system. If you lop this off and attach it to the tail of a different bacterium, which creates a vigorous immune response, they've created a very powerful flu fighter. This vaccine is so small it can be grown in a common bacteria, E. coli. Now, as you know, bacteria reproduce quickly -- it's like making yogurt -- and so we could produce enough swine origin flu for the entire world in a few factories, in a few weeks, with no eggs, for a fraction of the cost of current methods.
Así que, ¿estamos mejor preparados de lo que estábamos en 1918? Bueno, con las nuevas tecnologías emergentes ahora espero que podamos decir definitivamente "Sí". Imaginen si pudiéramos producir suficientes vacunas para todos en el mundo entero por menos de la mitad de lo que estamos gastando actualmente en Estados Unidos. Con una gama de nuevas tecnologías, podríamos. Aquí va un ejemplo: una empresa con la que estoy trabajando ha descubierto una parte específica de la gripe H [poco claro] capaz de despertar el sistema inmune. Si se corta y se anexa a la cola de una bacteria diferente que crea una respuesta inmunológica rotunda, se habrá creado un antigripal muy potente. Esta vacuna es tan pequeña que se puede cultivar en una bacteria común, la E. coli. Como saben, las bacterias se reproducen rápidamente. Es como hacer yogurt. Y así podríamos producir suficientes vacunas contra la gripe de origen porcino para el mundo entero en unas cuantas fábricas, en pocas semanas, sin huevos y por una pequeña parte del costo de los métodos actuales.
(Applause)
(Aplausos)
So here's a comparison of several of these new vaccine technologies. And, aside from the radically increased production and huge cost savings -- for example, the E. coli method I just talked about -- look at the time saved: this would be lives saved. The developing world, mostly left out of the current response, sees the potential of these alternate technologies and they're leapfrogging the West. India, Mexico and others are already making experimental flu vaccines, and they may be the first place we see these vaccines in use. Because these technologies are so efficient and relatively cheap, billions of people can have access to lifesaving vaccines if we can figure out how to deliver them.
Aquí tienen una comparación de varias de estas tecnologías de nuevas vacunas. Y, al margen del incremento radical en la producción y del gran ahorro de costos, por ejemplo, el método con E. coli que acabo de mencionar, miren el tiempo ahorrado... esto serían vidas salvadas. En el mundo en desarrollo, en su mayoría al margen de la respuesta actual, ven el potencial de estas tecnologías alternativas y están dejando atrás a Occidente. India, México y otros ya están produciendo vacunas experimentales contra la gripe y podrían ser el primer lugar donde veamos utilizar estas vacunas. Dado que estas tecnologías son tan eficientes y relativamente baratas miles de millones de personas pueden tener acceso a vacunas que salvan vidas si podemos encontrar la manera de administrarlas.
Now think of where this leads us. New infectious diseases appear or reappear every few years. Some day, perhaps soon, we'll have a virus that is going to threaten all of us. Will we be quick enough to react before millions die? Luckily, this year's flu was relatively mild. I say, "luckily" in part because virtually no one in the developing world was vaccinated. So if we have the political and financial foresight to sustain our investments, we will master these and new tools of vaccinology, and with these tools we can produce enough vaccine for everyone at low cost and ensure healthy productive lives. No longer must flu have to kill half a million people a year. No longer does AIDS need to kill two million a year. No longer do the poor and vulnerable need to be threatened by infectious diseases, or indeed, anybody. Instead of having Vaclav Smil's "massively fatal discontinuity" of life, we can ensure the continuity of life. What the world needs now are these new vaccines, and we can make it happen.
Ahora piensen adónde nos lleva eso. Nuevas enfermedades infecciosas aparecen o reaparecen cada pocos años. Un día, quizá pronto, tendremos un virus que nos va a amenazar a todos. ¿Seremos lo suficientemente rápidos en reaccionar antes de que mueran millones de personas? Por suerte, la gripe de este año fue relativamente leve. Digo "por suerte", en parte porque prácticamente no se vacunó a nadie en el mundo en desarrollo. Así que si tenemos la visión política y financiera para mantener nuestras inversiones, vamos a dominar estas herramientas de vacunología y otras nuevas. Y con estas herramientas podemos producir suficientes vacunas para todo el mundo a bajo costo y asegurar vidas sanas y productivas. La gripe ya no debe matar a medio millón de personas al año. El SIDA ya no tiene que matar a 2 millones al año. Los pobres y los vulnerables ya no tienen que verse amenazados por enfermedades infecciosas o, de hecho, nadie. En vez de tener la "discontinuidad masiva fatal" de la vida, de Vaclav Smil, podemos asegurar la continuidad de la vida. Lo que el mundo necesita actualmente son estas nuevas vacunas, y podemos hacer que esto se logre.
Thank you very much.
Muchas gracias.
(Applause)
(aplausos)
Chris Anderson: Thank you. (Applause) Thank you. So, the science is changing. In your mind, Seth -- I mean, you must dream about this -- what is the kind of time scale on, let's start with HIV, for a game-changing vaccine that's actually out there and usable?
Chris Anderson: gracias. (Aplausos) Gracias. Entonces, la ciencia está cambiando. En tu opinión, Seth --quiero decir, debes soñar con esto-- ¿cuál es el tipo de escala temporal en..., vamos a empezar con el VIH, para obtener una vacuna revolucionaria y que ésta esté disponible para su uso?
SB: The game change can come at any time, because the problem we have now is we've shown we can get a vaccine to work in humans; we just need a better one. And with these types of antibodies, we know humans can make them. So, if we can figure out how to do that, then we have the vaccine, and what's interesting is there already is some evidence that we're beginning to crack that problem. So, the challenge is full speed ahead.
SB: Este cambio revolucionario puede darse en cualquier momento porque el problema que hoy tenemos, como hemos demostrado, es que ya podemos obtener una vacuna que funcione en humanos, sencillamente necesitamos una mejor. Y con estos tipos de anticuerpos, sabemos que los seres humanos pueden producirlos. Por lo tanto, si podemos encontrar la manera de hacerlo, entonces tenemos la vacuna. Y lo interesante es que ya hay algunos indicios de que estamos comenzando a resolver ese problema. Así que el reto va a toda velocidad.
CA: In your gut, do you think it's probably going to be at least another five years?
CA: Instintivamente, ¿crees que probablemente va a tardar por lo menos otros cinco años?
SB: You know, everybody says it's 10 years, but it's been 10 years every 10 years. So I hate to put a timeline on scientific innovation, but the investments that have occurred are now paying dividends.
SB: Sabes, todo el mundo dice que será en diez años, pero han dicho diez años cada diez años. Así que detesto poner una línea de tiempo a la innovación científica, pero las inversiones realizadas están ya reportando beneficios.
CA: And that's the same with universal flu vaccine, the same kind of thing?
CA: Y ¿sucede lo mismo con la vacuna antigripal universal? ¿Pasa algo por el estilo?
SB: I think flu is different. I think what happened with flu is we've got a bunch -- I just showed some of this -- a bunch of really cool and useful technologies that are ready to go now. They look good. The problem has been that, what we did is we invested in traditional technologies because that's what we were comfortable with. You also can use adjuvants, which are chemicals you mix. That's what Europe is doing, so we could have diluted out our supply of flu and made more available, but, going back to what Michael Specter said, the anti-vaccine crowd didn't really want that to happen.
SB: Creo que la gripe es diferente. Creo que lo que ocurrió con la gripe es que tenemos un montón, sólo he mostrado algunas de ellas, un montón de tecnologías geniales y útiles que ya están listas. Parecen estupendas. El problema es que hemos invertido en tecnologías tradicionales porque era con lo que estábamos cómodos. También pueden usarse adyuvantes, que son sustancias químicas que se mezclan. Y eso es lo que se está haciendo Europa, y así podríamos diluir nuestro suministro de [vacunas contra la] gripe y aumentar su disponibilidad pero, volviendo a lo que dijo Michael Specter, la gente antivacunación no quiere que eso suceda.
CA: And malaria's even further behind?
CA: ¿Y la malaria está aún más atrás?
SB: No, malaria, there is a candidate that actually showed efficacy in an earlier trial and is currently in phase three trials now. It probably isn't the perfect vaccine, but it's moving along.
SB: No, para la malaria, hay un candidato que en realidad demostró eficacia en un ensayo anterior y actualmente se encuentra en la fase tres de los ensayos. Probablemente no se trata de la vacuna perfecta, pero se está avanzando.
CA: Seth, most of us do work where every month, we produce something; we get that kind of gratification. You've been slaving away at this for more than a decade, and I salute you and your colleagues for what you do. The world needs people like you. Thank you.
CA: Seth, la mayoría de nosotros trabaja cada mes en cosas que, ya sabes, producen algo, tenemos ese tipo de gratificación. Tu has estado trabajando como un burro en esto durante más de una década, y quiero rendiros homenaje a ti y a tus colegas por lo que hacéis. El mundo necesita gente como vosotros. Gracias.
SB: Thank you.
SB: Gracias.
(Applause)
(Aplausos)