Fragen Sie sich, was Sie umbringen wird? Eine Herzerkrankung, Krebs, ein Autounfall? Die meisten von uns sorgen sich über Dinge, die wir nicht kontrollieren können wie Krieg, Terrorismus, das tragische Erdbeben, das gerade in Haiti stattgefunden hat. Aber was bedroht die Menschheit wirklich? Vor ein paar Jahren versuchte Professor Vaclav Smil, die Wahrscheinlichkeit von plötzlichen Katastrophen zu berechnen, die groß genug sind, um Geschichte zu schreiben. Er nannte sie: "massiv fatale Diskontinuitäten", was bedeutet, dass sie bis zu 100 Millionen Leute in den nächsten 50 Jahren töten könnten. Er schaute sich die Wahrscheinlichkeit für einen weiteren Weltkrieg an, für einen gewaltigen Vulkanausbruch, sogar dafür, dass ein Asteroid die Erde treffen wird. Aber er stufte die Wahrscheinlichkeit für eines dieser Ereignisse höher als die für alle anderen ein, mit beinahe 100 Prozent, und zwar für eine schwere Grippe-Pandemie. Nun mögen Sie die Grippe bloß für eine wirklich schlimme Erkältung halten. Aber sie kann ein Todesurteil sein. Jedes Jahr sterben 36.000 Menschen in den USA pro Saison an der Grippe. In den Entwicklungsländern sind die Daten viel lückenhafter, aber die Zahl der Todesopfer ist beinahe garantiert höher. Wissen Sie, das Problem ist: Wenn dieses Virus gelegentlich so drastisch mutiert ist es im Grunde ein neues Virus. Und dann bekommen wir eine Pandemie.
Do you worry about what is going to kill you? Heart disease, cancer, a car accident? Most of us worry about things we can't control, like war, terrorism, the tragic earthquake that just occurred in Haiti. But what really threatens humanity? A few years ago, Professor Vaclav Smil tried to calculate the probability of sudden disasters large enough to change history. He called these, "massively fatal discontinuities," meaning that they could kill up to 100 million people in the next 50 years. He looked at the odds of another world war, of a massive volcanic eruption, even of an asteroid hitting the Earth. But he placed the likelihood of one such event above all others at close to 100 percent, and that is a severe flu pandemic. Now, you might think of flu as just a really bad cold, but it can be a death sentence. Every year, 36,000 people in the United States die of seasonal flu. In the developing world, the data is much sketchier but the death toll is almost certainly higher. You know, the problem is if this virus occasionally mutates so dramatically, it essentially is a new virus and then we get a pandemic.
1918 erschien ein neues Virus, das ungefähr 50 bis 100 Millionen Menschen tötete. Es breitete sich aus wie ein Lauffeuer. Und manche starben schon Stunden nachdem sie Symptome entwickelten. Sind wir heute sicherer? Na, wir scheinen dieses Jahr die tödliche Pandemie, die die meisten von uns befürchteten vermieden zu haben, aber diese Bedrohung könnte jederzeit wieder auftauchen. Die gute Nachricht ist, dass wir an einem Zeitpunkt angelangt sind, an dem Wissenschaft, Technologie und Globalisierung zusammen kommen und eine nie dagewesene Möglichkeit schaffen, die Möglichkeit, Geschichte zu schreiben, indem Infektionskrankheiten verhindert werden, die immer noch ein Fünftel aller Todesfälle und zahlloses Leid auf der Erde ausmachen. Wir können das schaffen. Wir verhindern bereits Millionen von Todesfällen durch vorhandene Impfstoffe. Und wenn wir die an mehr Leute bringen können, können wir sicherlich mehr Leben retten. Aber mit neuen oder besseren Impfstoffen für Malaria, TB, HIV, Lungenentzündung, Durchfall, Grippe, könnten wir Leid beenden, das es auf der Erde seit Anfang aller Zeiten gibt.
In 1918, a new virus appeared that killed some 50 to 100 million people. It spread like wildfire and some died within hours of developing symptoms. Are we safer today? Well, we seem to have dodged the deadly pandemic this year that most of us feared, but this threat could reappear at any time. The good news is that we're at a moment in time when science, technology, globalization is converging to create an unprecedented possibility: the possibility to make history by preventing infectious diseases that still account for one-fifth of all deaths and countless misery on Earth. We can do this. We're already preventing millions of deaths with existing vaccines, and if we get these to more people, we can certainly save more lives. But with new or better vaccines for malaria, TB, HIV, pneumonia, diarrhea, flu, we could end suffering that has been on the Earth since the beginning of time.
Ich bin also hier, um Ihnen das Lob auf die Impfstoffe zu singen. Aber zuerst muss ich erklären, warum sie wichtig sind. Denn Impfstoffe, ihre Macht, ist eher wie ein Säuseln. Wenn sie funktionieren können sie Geschichte schreiben, aber nach einer Weile kann man sie kaum noch hören. Nun sind manche von uns alt genug um eine kleine kreisförmige Narbe auf unseren Armen zu haben - von einer Impfung, die wir als Kinder bekommen haben. Aber wann haben Sie sich zum letzten Mal wegen Pocken Sorgen gemacht, einer Krankheit, die im letzten Jahrhundert eine halbe Milliarde Menschen das Leben gekostet hat, und die es nicht mehr gibt? Oder Kinderlähmung - wie viele von Ihnen erinnern sich an die eiserne Lunge? Wir sehen Bilder wie dieses nicht mehr, wegen der Impfstoffe.
So, I'm here to trumpet vaccines for you. But first, I have to explain why they're important because vaccines, the power of them, is really like a whisper. When they work, they can make history, but after a while you can barely hear them. Now, some of us are old enough to have a small, circular scar on our arms from an inoculation we received as children. But when was the last time you worried about smallpox, a disease that killed half a billion people last century and no longer is with us? Or polio? How many of you remember the iron lung? We don't see scenes like this anymore because of vaccines.
Na wissen Sie, das ist interessant, weil es um die 30 Krankheiten gibt, die jetzt mit Impfstoffen behandelt werden können, aber Dinge wie HIV und die Grippe gefährden uns immer noch. Warum? Nun, hier ist unser kleines schmutziges Geheimnis. Bis vor Kurzem brauchten wir nicht zu wissen, wie ein Impfstoff genau wirkte. Wir wussten durch guten alten Versuch und Irrtum, dass sie wirkten. Man nahm einen Krankheitserreger, modifizierte ihn, injizierte ihn einem Menschen oder einem Tier und beobachtete, was passierte. Für die meisten Krankheitserreger hat das gut funktioniert, halbwegs gut für schlaue Bazillen wie die Grippe, aber überhaupt nicht für HIV, für das Menschen keine natürliche Immunität haben.
Now, it's interesting because there are 30-odd diseases that can be treated with vaccines now, but we're still threatened by things like HIV and flu. Why is that? Well, here's the dirty little secret. Until recently, we haven't had to know exactly how a vaccine worked. We knew they worked through old-fashioned trial and error. You took a pathogen, you modified it, you injected it into a person or an animal and you saw what happened. This worked well for most pathogens, somewhat well for crafty bugs like flu, but not at all for HIV, for which humans have no natural immunity.
Lassen Sie uns also untersuchen, wie Impfstoffe wirken. Sie schaffen im Grunde ein Waffenlager für Ihr Immunsystem, das Sie einsetzen können, wenn Sie es brauchen. Wenn Sie nun eine Virusinfektion bekommen dauert es normalerweise Tage oder Wochen bis Ihr Körper sich mit voller Kraft zur Wehr setzt, und das könnte zu spät sein. Wenn Sie vor-immunisiert sind haben Sie Kräfte in Ihrem Körper, die vor-geschult sind, bestimmte Feinde zu erkennen und zu besiegen. So funktionieren Impfstoffe also eigentlich. Schauen wir nun in ein Video, das wir bei TED zum ersten Mal zeigen, darüber, wie ein wirksamer HIV-Impfstoff funktionieren könnte.
So let's explore how vaccines work. They basically create a cache of weapons for your immune system which you can deploy when needed. Now, when you get a viral infection, what normally happens is it takes days or weeks for your body to fight back at full strength, and that might be too late. When you're pre-immunized, what happens is you have forces in your body pre-trained to recognize and defeat specific foes. So that's really how vaccines work. Now, let's take a look at a video that we're debuting at TED, for the first time, on how an effective HIV vaccine might work.
(Musik)
(Music)
Erzähler: Ein Impfstoff trainiert den Körper im Voraus darauf, einen bestimmten Eindringling zu erkennen und auszuschalten. Nachdem HIV durch die Schleimhaut-Barrieren des Körpers eindringt, infiziert es Zellen des Immunsystems, um sich zu vervielfältigen. Der Eindringling zieht die Aufmerksamkeit der Front-Truppen des Immunsystems auf sich. Dendritische Zellen oder Makrophagen fassen das Virus und zeigen Stücke davon. Gedächtniszellen, die der HIV-Impfstoff schafft werden aktiviert, wenn sie von den Fronttruppen hören, dass HIV da ist. Diese Gedächtniszellen setzen sofort genau die Waffen ein, die nötig sind. B-Gedächtniszellen werden zu Plasmazellen, die Schub um Schub spezifische Antikörper produzieren, die an HIV andocken, um es daran zu hindern, Zellen zu infizieren, während Geschwader von T-Killerzellen hinausgehen und Zellen zerstören, die bereits HIV-infiziert sind. Das Virus ist besiegt. Ohne einen Impfstoff würden diese Reaktionen über eine Woche brauchen. Bis dahin wäre der Kampf gegen HIV schon verloren.
Narrator: A vaccine trains the body in advance how to recognize and neutralize a specific invader. After HIV penetrates the body's mucosal barriers, it infects immune cells to replicate. The invader draws the attention of the immune system's front-line troops. Dendritic cells, or macrophages, capture the virus and display pieces of it. Memory cells generated by the HIV vaccine are activated when they learn HIV is present from the front-line troops. These memory cells immediately deploy the exact weapons needed. Memory B cells turn into plasma cells, which produce wave after wave of the specific antibodies that latch onto HIV to prevent it from infecting cells, while squadrons of killer T cells seek out and destroy cells that are already HIV infected. The virus is defeated. Without a vaccine, these responses would have taken more than a week. By that time, the battle against HIV would already have been lost.
Seth Berkley: Echt cooles Video, oder? Die Antikörper, die Sie gerade in diesem Video in Aktion gesehen haben sind diejenigen, die in den meisten Impfstoffen wirken. Die eigentliche Frage ist dann also: Wir stellen wir sicher, dass der Körper genau die produziert, die wir brauchen, um uns vor Grippe und HIV zu schützen? Die hauptsächliche Herausforderung für diese beiden Viren ist, dass sie sich ständig verändern. Schauen wir uns also das Grippevirus an. In dieser Darstellung des Grippevirus sind diese verschiedenfarbigen Spikes das, womit es Sie infiziert. Und was die Antikörper nutzen ist ein Griff, um im Grunde das Virus zu greifen und auszuschalten. Wenn die mutieren ändern sie ihre Form und die Antikörper wissen nicht mehr, womit sie es zu tun haben. Das ist der Grund weshalb Sie jedes Jahr einen etwas anderen Grippestrang kriegen können. Es ist auch der Grund weshalb wir im Frühjahr abschätzen müssen, welche drei Stränge im nächsten Jahr vorherrschend sein werden, die in einen einzigen Impfstoff packen und für den Herbst schnell in Produktion geben müssen.
Seth Berkley: Really cool video, isn't it? The antibodies you just saw in this video, in action, are the ones that make most vaccines work. So the real question then is: How do we ensure that your body makes the exact ones that we need to protect against flu and HIV? The principal challenge for both of these viruses is that they're always changing. So let's take a look at the flu virus. In this rendering of the flu virus, these different colored spikes are what it uses to infect you. And also, what the antibodies use is a handle to essentially grab and neutralize the virus. When these mutate, they change their shape, and the antibodies don't know what they're looking at anymore. So that's why every year you can catch a slightly different strain of flu. It's also why in the spring, we have to make a best guess at which three strains are going to prevail the next year, put those into a single vaccine and rush those into production for the fall.
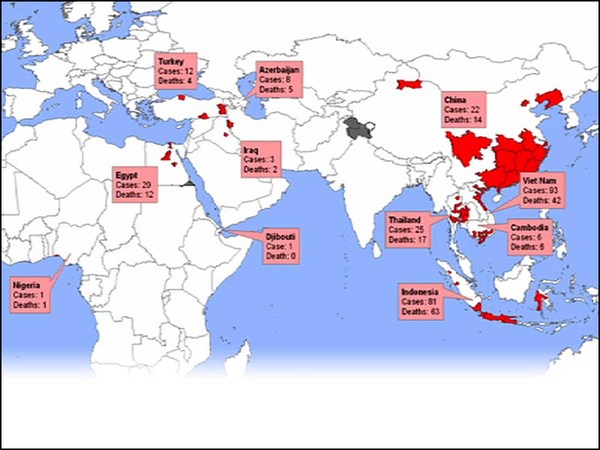
Schlimmer noch infiziert die häufigste Grippe, Influenza A auch Tiere, die in direkter Nähe zu Menschen leben, und kann sich in diesen bestimmten Tieren rekombinieren. Außerdem sind wild lebende Wasservögel Träger für alle uns bekannten Stränge von Influenza. Man hat also diese Situation. 2003 hatten wir ein H5N1-Virus, das in ein paar Einzelfällen von Vögeln auf Menschen übergesprungen ist, mit einer augenscheinlichen Sterblichkeitsrate von 70 Prozent. Glücklicherweise wurde genau dieses Virus, obwohl es damals sehr furchteinflößend war, nicht sehr leicht von Mensch zu Mensch übertragen. Die H1N1-Bedrohung diesen Jahres war tatsächlich eine Mensch-, Vogel-, Schweine-Mischung, die in Mexico aufkam. Sie wurde leicht übertragen, war aber glücklicherweise ziemlich harmlos. Und so hält gewissermaßen unser Glück an, aber wissen Sie, ein anderer wild lebender Vogel könnte jederzeit vorüber fliegen.
Even worse, the most common influenza -- influenza A -- also infects animals that live in close proximity to humans, and they can recombine in those particular animals. In addition, wild aquatic birds carry all known strains of influenza. So, you've got this situation: In 2003, we had an H5N1 virus that jumped from birds into humans in a few isolated cases with an apparent mortality rate of 70 percent. Now luckily, that particular virus, although very scary at the time, did not transmit from person to person very easily. This year's H1N1 threat was actually a human, avian, swine mixture that arose in Mexico. It was easily transmitted, but, luckily, was pretty mild. And so, in a sense, our luck is holding out, but you know, another wild bird could fly over at anytime.
Schauen wir uns nun HIV an. So variabel die Grippe auch ist, HIV lässt die Grippe wie den Fels von Gibraltar aussehen. Das Virus, das AIDS verursacht ist der kniffligste Krankheitserreger, mit dem Wissenschaftler je konfrontiert waren. Es mutiert rasend schnell. Es hat Fallen, um das Immunsystem zu umgehen. Es greift genau die Zellen an, die versuchen, es zu bekämpfen. Und es versteckt sich schnell in Ihrem Genom. Hier ist eine Folie, die die genetische Variation der Grippe zeigt und sie mit HIV vergleicht, einem viel ungezügelterem Ziel. In dem Video haben Sie vor einigen Augenblicken Flotten neuer Viren aus infizierten Zellen starten sehen. Sie müssen verstehen, dass es in einer kürzlich infizierten Person Millionen dieser Schiffe gibt, jedes ein kleines bisschen anders. Eine Waffe finden zu müssen, die sie alle erkennt und versenkt macht es viel schwieriger.
Now let's take a look at HIV. As variable as flu is, HIV makes flu look like the Rock of Gibraltar. The virus that causes AIDS is the trickiest pathogen scientists have ever confronted. It mutates furiously, it has decoys to evade the immune system, it attacks the very cells that are trying to fight it and it quickly hides itself in your genome. Here's a slide looking at the genetic variation of flu and comparing that to HIV, a much wilder target. In the video a moment ago, you saw fleets of new viruses launching from infected cells. Now realize that in a recently infected person, there are millions of these ships; each one is just slightly different. Finding a weapon that recognizes and sinks all of them makes the job that much harder.
In den 27 Jahren seit HIV als Ursache von AIDS identifiziert wurde haben wir mehr Medikamente entwickelt, um HIV zu behandeln als für alle anderen Viren zusammen. Diese Medikamente sind keine Heilmittel, aber sie stellen einen riesigen Triumph der Wissenschaft dar, weil sie das automatische Todesurteil von einer HIV-Diagnose wegnehmen, zumindest für diejenigen, die Zugang zu ihnen haben. Die Bemühungen um einen Impfstoff sind aber ganz anders. Große Firmen sind davon abgekommen, weil sie dachten, dass die Wissenschaft so schwierig sei und weil Impfstoffe als schlechtes Geschäft angesehen wurden. Viele dachten, dass es einfach unmöglich wäre, einen AIDS-Impfstoff zu machen, aber heute sprechen die Indizien eine andere Sprache.
Now, in the 27 years since HIV was identified as the cause of AIDS, we've developed more drugs to treat HIV than all other viruses put together. These drugs aren't cures, but they represent a huge triumph of science because they take away the automatic death sentence from a diagnosis of HIV, at least for those who can access them. The vaccine effort though is really quite different. Large companies moved away from it because they thought the science was so difficult and vaccines were seen as poor business. Many thought that it was just impossible to make an AIDS vaccine, but today, evidence tells us otherwise.
Im September gab es überraschende, aber aufregende Befunde aus einer klinischen Studie, die in Thailand stattgefunden hatte. Zum ersten Mal sahen wir, dass ein AIDS-Impfstoff in Menschen funktionierte, wenn auch nur mäßig. Und genau dieser Impfstoff war fast ein Jahrzehnt zuvor hergestellt worden. Neuere Konzepte und frühzeitige Tests sind noch vielversprechender in den besten unserer Modelle an Tieren. Aber in den letzten paar Monaten haben Forscher auch verschiedene neue, breit angreifende Antikörper aus dem Blut eines HIV-Infizierten isoliert. Nun, was bedeutet das? Wir haben vorhin gesehen, dass HIV sehr variabel ist, dass ein breit angreifender Antikörper andockt und mehrere Varianten des Virus ausschaltet. Wenn man die nimmt und in die besten unserer Affen-Modelle steckt bieten sie vollständigen Schutz vor Infektion. Zusätzlich haben diese Forscher eine neue Stelle auf dem HIV gefunden, an der die Antikörper angreifen können. Und das Besondere an dieser Stelle ist, dass sie sich sehr wenig verändert, während das Virus mutiert. Es ist als ob das Virus, egal wie oft es seine Kleider wechselt, immer noch die selben Socken trägt, und unsere Aufgabe ist es jetzt, sicher zu stellen, dass der Körper diese Socken wirklich hasst.
In September, we had surprising but exciting findings from a clinical trial that took place in Thailand. For the first time, we saw an AIDS vaccine work in humans -- albeit, quite modestly -- and that particular vaccine was made almost a decade ago. Newer concepts and early testing now show even greater promise in the best of our animal models. But in the past few months, researchers have also isolated several new broadly neutralizing antibodies from the blood of an HIV infected individual. Now, what does this mean? We saw earlier that HIV is highly variable, that a broad neutralizing antibody latches on and disables multiple variations of the virus. If you take these and you put them in the best of our monkey models, they provide full protection from infection. In addition, these researchers found a new site on HIV where the antibodies can grab onto, and what's so special about this spot is that it changes very little as the virus mutates. It's like, as many times as the virus changes its clothes, it's still wearing the same socks, and now our job is to make sure we get the body to really hate those socks.
So ist also die Lage. Die thailändischen Ergebnisse zeigen uns, dass wir einen AIDS-Impfstoff machen können. Und die Antikörper-Befunde zeigen uns, wie wir das anstellen könnten. Diese Strategie, von einem Antikörper rückwärts zu arbeiten, um einen Impfstoff-Kandidaten zu entwickeln ist in der Impfstoff-Forschung nie zuvor verfolgt worden. Man nennt das "Retro-Vaccinology" (Retro-Impfstofflehre) und die Implikationen davon erstrecken sich weit über HIV hinaus. Stellen Sie sich das also so vor. Wir haben diese neuen Antikörper, die wir identifiziert haben und wir wissen, dass sie an viele, viele Varianten des Virus andocken. Wir wissen, dass sie an ein spezielles Teil andocken müssen, wenn wir also die genaue Struktur dieses Teils herausfinden können, das durch einen Impfstoff darbieten, können wir hoffen, das Immunsystem anzuregen, die passenden Antikörper zu bilden. Und das würde einen universallen HIV-Impfstoff schaffen. Nun, das klingt leichter als es ist, denn die Struktur sieht eigentlich eher wie dieses blaue Antikörper-Diagramm aus, das an seine gelbe Bindungsstelle angeschlossen ist. Wie Sie sich vorstellen können ist es viel schwieriger, an diesen dreidimensionalen Strukturen zu arbeiten. Und wenn Sie hier irgendwelche Ideen haben, wie wir das lösen können, würden wir die gerne hören.
So what we've got is a situation. The Thai results tell us we can make an AIDS vaccine, and the antibody findings tell us how we might do that. This strategy, working backwards from an antibody to create a vaccine candidate, has never been done before in vaccine research. It's called retro-vaccinology, and its implications extend way beyond that of just HIV. So think of it this way. We've got these new antibodies we've identified, and we know that they latch onto many, many variations of the virus. We know that they have to latch onto a specific part, so if we can figure out the precise structure of that part, present that through a vaccine, what we hope is we can prompt your immune system to make these matching antibodies. And that would create a universal HIV vaccine. Now, it sounds easier than it is because the structure actually looks more like this blue antibody diagram attached to its yellow binding site, and as you can imagine, these three-dimensional structures are much harder to work on. And if you guys have ideas to help us solve this, we'd love to hear about it.
Aber wissen Sie, die Forschung, die an HIV stattgefunden hat hat uns sehr mit dem Fortschritt für andere Krankheiten geholfen. Eine Biotechnologie-Firma hat zum Beispiel breit angreifende Antikörper für Influenza gefunden und auch ein neues Antikörper-Ziel auf dem Grippevirus. Sie machen gerade einen Cocktail, einen Antikörper-Cocktail, der genutzt werden kann, um schwerwiegende, überwältigende Fälle von Grippe zu behandeln. Was sie auf längere Sicht tun können, ist diese Werkzeuge der Retro-Vaccinology zu nutzen, um einen vorbeugenden Grippeimpfstoff zu machen. Retro-Vaccinologie ist nun aber nur eine Technik im Bereich des sogenannten rationalen Impfstoff-Designs.
But, you know, the research that has occurred from HIV now has really helped with innovation with other diseases. So for instance, a biotechnology company has now found broadly neutralizing antibodies to influenza, as well as a new antibody target on the flu virus. They're currently making a cocktail -- an antibody cocktail -- that can be used to treat severe, overwhelming cases of flu. In the longer term, what they can do is use these tools of retro-vaccinology to make a preventive flu vaccine. Now, retro-vaccinology is just one technique within the ambit of so-called rational vaccine design.
Lassen Sie mich ein weiteres Beispiel anführen. Wir haben bereits über die H- und M-Spikes auf der Oberfläche des Grippevirus gesprochen. Schauen Sie auf diese andere, kleineren Protuberanzen. Die sind vor dem Immunsystem weitgehend versteckt. Es stellt sich nun heraus, dass diese Stellen sich auch nicht sehr verändern, wenn das Virus mutiert. Wenn man die mit bestimmten Antikörpern kaputt machen kann, könnte man alle Varianten der Grippe kaputt machen. Bisher zeigen Tierversuche, dass solch ein Impfstoff schwere Krankheiten verhindern kann, obwohl man mildere Fälle bekommen könnte. Wenn das beim Menschen funktioniert, sprechen wir hier über einen universellen Grippeimpfstoff, einen, der nicht jedes Jahr verändert werden muss, der die Gefahr des Todes abwenden würde. Wir könnten uns die Grippe dann wirklich als nur eine schlimme Erkältung vorstellen.
Let me give you another example. We talked about before the H and N spikes on the surface of the flu virus. Notice these other, smaller protuberances. These are largely hidden from the immune system. Now it turns out that these spots also don't change much when the virus mutates. If you can cripple these with specific antibodies, you could cripple all versions of the flu. So far, animal tests indicate that such a vaccine could prevent severe disease, although you might get a mild case. So if this works in humans, what we're talking about is a universal flu vaccine, one that doesn't need to change every year and would remove the threat of death. We really could think of flu, then, as just a bad cold.
Natürlich ist der beste vorstellbare Impfstoff nur wertvoll zu dem Grad, zu dem wir ihn zu jedem bringen können, der ihn braucht. Um das also zu tun, müssen wir intelligentes Impfstoff-Design mit cleveren Produktionsmethoden und natürlich cleveren Verbreitungsmethoden kombinieren. Ich möchte, dass sie sich ein paar Monate zurück erinnern. Im Juni erklärte die Weltgesundheitsorganisation die erste weltweite Grippe-Pandemie in 41 Jahren. Die amerikanische Regierung versprach 150 Millionen Dosen Impfstoff bis zum 15. Oktober für die Spitze der Grippewelle. Entwicklungsländern wurden Impfstoffe versprochen. Hunderte Millionen Dollar wurden ausgegeben und flossen in die beschleunigte Herstellung von Impfstoffen. Was passierte also?
Of course, the best vaccine imaginable is only valuable to the extent we get it to everyone who needs it. So to do that, we have to combine smart vaccine design with smart production methods and, of course, smart delivery methods. So I want you to think back a few months ago. In June, the World Health Organization declared the first global flu pandemic in 41 years. The U.S. government promised 150 million doses of vaccine by October 15th for the flu peak. Vaccines were promised to developing countries. Hundreds of millions of dollars were spent and flowed to accelerating vaccine manufacturing. So what happened?
Nun, wie man Grippe-Impfstoffe macht, wie man sie produziert, fanden wir zum ersten Mal in den frühen 1940ern heraus. Das war ein langsamer, mühevoller Prozess, der von Hühnereiern abhängig war, Millionen lebender Hühnereier. Viren wachsen nur in Lebewesen und so stellte es sich heraus, dass für Grippe Hühnereier sehr gut funktionierten. Für die meisten Stränge konnte man ein bis zwei Dosen Impfstoff pro Ei bekommen. Zum Glück leben wir in einer Zeit atemberaubenden biomedizinischen Fortschritts. Heute bekommen wir also unseren Grippe-Impfstoff von... ... Hühnereiern, (Gelächter) hunderte Millionen Hühnereier. Wissen Sie, fast nichts hat sich geändert. Wissen Sie, das System ist zuverlässig. Aber das Problem ist, dass Sie nie wissen, wie gut ein Strang wachsen wird. Der Schweinegrippestrang aus diesem Jahr wuchs in der anfänglichen Produktion sehr schlecht, im Grunde 0,6 Dosen pro Ei. Hier ist also ein beunruhigender Gedanke. Was, wenn dieser wilde Vogel wieder vorbei fliegt? Wir könnten einen Vogel-Strang erleben, der die Geflügelbestände infizieren würde und dann hätten wir keine Eier für unsere Impfstoffe. Wenn Du, Dan (Barber) also Milliarden von Hühner-Pellets für Deine Fischzucht willst, ich weiß, wo Du sie kriegen kannst. Zur Zeit kann die Welt ungefähr 350 Millionen Dosen Grippeimpfstoff für die drei Stränge produzieren. Und wir können das auf ungefähr 1,2 Milliarden Dosen hochschrauben, wenn wir eine einzelne Variante wie Schweinegrippe anzielen. Aber da gehen wir davon aus, dass unsere Fabriken brummen, denn 2004 war der amerikanische Nachschub durch Kontaminierung einer einzelnen Fabrik halbiert. Und der Prozess dauert immer noch über ein halbes Jahr.
Well, we first figured out how to make flu vaccines, how to produce them, in the early 1940s. It was a slow, cumbersome process that depended on chicken eggs, millions of living chicken eggs. Viruses only grow in living things, and so it turned out that, for flu, chicken eggs worked really well. For most strains, you could get one to two doses of vaccine per egg. Luckily for us, we live in an era of breathtaking biomedical advances. So today, we get our flu vaccines from ... chicken eggs, (Laughter) hundreds of millions of chicken eggs. Almost nothing has changed. The system is reliable but the problem is you never know how well a strain is going to grow. This year's swine flu strain grew very poorly in early production: basically .6 doses per egg. So, here's an alarming thought. What if that wild bird flies by again? You could see an avian strain that would infect the poultry flocks, and then we would have no eggs for our vaccines. So, Dan [Barber], if you want billions of chicken pellets for your fish farm, I know where to get them. So right now, the world can produce about 350 million doses of flu vaccine for the three strains, and we can up that to about 1.2 billion doses if we want to target a single variant like swine flu. But this assumes that our factories are humming because, in 2004, the U.S. supply was cut in half by contamination at one single plant. And the process still takes more than half a year.
Sind wir also besser vorbereitet als 1918? Nun, mit den gerade aufkommenden neuen Technologien hoffe ich, dass wir definitiv "Ja" sagen können. Stellen Sie sich vor, wenn wir genug Grippeimpfstoff für jeden auf der Welt für die Hälfte dessen, was wir im Moment in den USA ausgeben machen könnten. Mit einer Reihe neuer Technologien könnten wir das. Hier ein Beispiel. Eine Firma, mit der ich zu tun habe hat ein bestimmtes Stück der H (undeutlich) Grippe gefunden, die das Immunsystem entfacht. Wenn man das abschneidet und an den Schwanz eines anderen Bakteriums heftet, das eine starke Immunreaktion schafft, haben sie einen sehr mächtigen Grippe-Bekämpfer geschaffen. Dieser Impfstoff ist so klein, dass er in einem weit verbreiteten Bakterium, E. coli, gezüchtet werden kann. Wie Sie wissen vermehren sich Bakterien schnell. Das ist wie wenn man Joghurt macht. Und so könnten wir genug Grippe mit Schweine-Ursprung für die ganze Welt ein ein paar Fabriken in ein paar Wochen machen, ohne Eier, für einen Bruchteil der Kosten der aktuellen Methoden.
So are we better prepared than we were in 1918? Well, with the new technologies emerging now, I hope we can say definitively, "Yes." Imagine we could produce enough flu vaccine for everyone in the entire world for less than half of what we're currently spending now in the United States. With a range of new technologies, we could. Here's an example: A company I'm engaged with has found a specific piece of the H spike of flu that sparks the immune system. If you lop this off and attach it to the tail of a different bacterium, which creates a vigorous immune response, they've created a very powerful flu fighter. This vaccine is so small it can be grown in a common bacteria, E. coli. Now, as you know, bacteria reproduce quickly -- it's like making yogurt -- and so we could produce enough swine origin flu for the entire world in a few factories, in a few weeks, with no eggs, for a fraction of the cost of current methods.
(Beifall)
(Applause)
Hier ist also ein Vergleich einiger dieser neuen Impf-Technologien. Und abseits der radikal gestiegenen Produktion und der riesigen Kosteneinsparungen der E. coli Methode zum Beispiel, über die ich gerade gesprochen habe - schauen Sie sich die gewonnene Zeit an - das wären gerettete Leben. Die Entwicklungsländer, die aus der aktuellen Reaktion weitgehend ausgeschlossen sind sehen das Potenzial dieser alternativen Technologien, und überholen den Westen. Indien, Mexico und andere machen bereits experimentelle Grippe-Impfstoffe, und das könnten die ersten Orte sein, in denen diese Impfstoffe benutzt werden. Weil diese Technologien so effizient und relativ preiswert sind können Milliarden von Menschen Zugang zu lebensrettenden Impfstoffen haben, wenn wir herausfinden können, wir wir sie ausliefern können.
So here's a comparison of several of these new vaccine technologies. And, aside from the radically increased production and huge cost savings -- for example, the E. coli method I just talked about -- look at the time saved: this would be lives saved. The developing world, mostly left out of the current response, sees the potential of these alternate technologies and they're leapfrogging the West. India, Mexico and others are already making experimental flu vaccines, and they may be the first place we see these vaccines in use. Because these technologies are so efficient and relatively cheap, billions of people can have access to lifesaving vaccines if we can figure out how to deliver them.
Überlegen Sie, wohin uns das führt. Neue Infektionskrankheiten erscheinen alle paar Jahre neu oder wieder. Eines Tages, vielleicht schon bald, werden wir einen Virus haben, der uns alle bedroht. Werden wir schnell genug sein, um zu reagieren bevor Millionen sterben? Zum Glück war die diesjährige Grippe relativ mild. Ich sage "zum Glück" teilweise, weil praktisch niemand in den Entwicklungsländern geimpft wurde. Wenn wir die politische und finanzielle Voraussicht haben, unsere Investitionen zu erhalten, werden wir diese und andere neue Werkzeuge der Impfstoff-Lehre beherrschen. Und mit diesen Werkzeugen können wir genug Impfstoff für alle zu niedrigen Kosten herstellen und gesunde produktive Leben sicher stellen. Die Grippe muss nicht länger eine halbe Million Leute pro Jahr töten. AIDS muss nicht länger zwei Millionen pro Jahr töten. Die Armen und Verwundbaren müssen nicht länger durch Infektionskrankheiten bedroht werden, niemand muss das. Anstatt Vaclav Smils "massiv fatale Diskontinuität" des Lebens zu haben können wir die Kontinuität des Lebens sicher stellen. Was die Welt jetzt braucht sind diese neuen Impfstoffe, und wir können dafür sorgen.
Now think of where this leads us. New infectious diseases appear or reappear every few years. Some day, perhaps soon, we'll have a virus that is going to threaten all of us. Will we be quick enough to react before millions die? Luckily, this year's flu was relatively mild. I say, "luckily" in part because virtually no one in the developing world was vaccinated. So if we have the political and financial foresight to sustain our investments, we will master these and new tools of vaccinology, and with these tools we can produce enough vaccine for everyone at low cost and ensure healthy productive lives. No longer must flu have to kill half a million people a year. No longer does AIDS need to kill two million a year. No longer do the poor and vulnerable need to be threatened by infectious diseases, or indeed, anybody. Instead of having Vaclav Smil's "massively fatal discontinuity" of life, we can ensure the continuity of life. What the world needs now are these new vaccines, and we can make it happen.
Vielen Dank.
Thank you very much.
(Beifall)
(Applause)
Chris Anderson: Danke. (Beifall) Danke. Die Wissenschaft verändert sich also. Deiner Meinung nach, Seth - Ich meine, Du musst davon träumen - wie sieht der zeitliche Maßstab aus, fangen wir mit HIV an, für einen alles in den Schatten stellenden Impfstoff, der wirklich da und nutzbar ist?
Chris Anderson: Thank you. (Applause) Thank you. So, the science is changing. In your mind, Seth -- I mean, you must dream about this -- what is the kind of time scale on, let's start with HIV, for a game-changing vaccine that's actually out there and usable?
SB: Diese bahnbrechende Veränderung kann jederzeit kommen, denn im Moment haben wir das Problem, dass wir gezeigt haben, dass der Impfstoff in Menschen wirken kann, wir brauchen nur einen besseren. Und mit diesen Arten von Antikörpern - wir wissen, dass Menschen sie machen können. Wenn wir also herausfinden können, wie wir das tun können, haben wir den Impfstoff. Und es ist interessant, dass es schon einige Hinweise darauf gibt, dass wir anfangen, dieses Problem zu lösen. Die Herausforderung ist also volle Kraft voraus.
SB: The game change can come at any time, because the problem we have now is we've shown we can get a vaccine to work in humans; we just need a better one. And with these types of antibodies, we know humans can make them. So, if we can figure out how to do that, then we have the vaccine, and what's interesting is there already is some evidence that we're beginning to crack that problem. So, the challenge is full speed ahead.
CA: Aus dem Bauch heraus, glaubst Du, dass es wahrscheinlich noch mindestens fünf Jahre dauern wird?
CA: In your gut, do you think it's probably going to be at least another five years?
SB: Weißt Du, jeder sagt es sind 10 Jahre, aber es waren alle 10 Jahre 10 Jahre. Ich würde wirklich nicht gerne eine Zeitleiste an wissenschaftlichen Fortschritt anlegen, aber die Investitionen, die stattgefunden haben zahlen sich jetzt aus.
SB: You know, everybody says it's 10 years, but it's been 10 years every 10 years. So I hate to put a timeline on scientific innovation, but the investments that have occurred are now paying dividends.
CA: Und mit dem universellen Grippeimpfstoff ist es das Selbe?
CA: And that's the same with universal flu vaccine, the same kind of thing?
SB: Ich glaube die Grippe ist anders. Ich glaube, was mit der Grippe passiert ist, ist dass wir eine Menge - ich habe gerade einige davon gezeigt - eine Menge wirklich cooler und nützlicher Technologien haben, die jetzt fertig sind. Sie sehen gut aus. Das Problem war, dass wir in traditionelle Technologien investiert haben, weil wir damit zufrieden waren. Man kann auch Adjuvantien benutzen, das sind eingemischte Chemikalien. Und das macht Europa, wir hätten also unseren Vorrat an Grippe verdünnen und weiter verfügbar machen können, aber um darauf zurück zu kommen, was Michael Specter sagte, die Anti-Impfungs-Leute wollten das wirklich nicht.
SB: I think flu is different. I think what happened with flu is we've got a bunch -- I just showed some of this -- a bunch of really cool and useful technologies that are ready to go now. They look good. The problem has been that, what we did is we invested in traditional technologies because that's what we were comfortable with. You also can use adjuvants, which are chemicals you mix. That's what Europe is doing, so we could have diluted out our supply of flu and made more available, but, going back to what Michael Specter said, the anti-vaccine crowd didn't really want that to happen.
CA: Und Malaria hinkt noch weiter zurück?
CA: And malaria's even further behind?
SB: Nein, für Malaria gibt es einen Kandidaten, der tatsächlich Wirksamkeit in einer früheren Studie zeigte und im Moment in Phase III Studien ist. Das ist wahscheinlich nicht der perfekte Impfstoff, aber es geht voran.
SB: No, malaria, there is a candidate that actually showed efficacy in an earlier trial and is currently in phase three trials now. It probably isn't the perfect vaccine, but it's moving along.
CA: Seth, die meisten von uns erledigen Arbeit, wo wir jeden Monat irgendwas produzieren, wir bekommen diese Art von Belohnung. Du hast Dich hier dran über ein Jahrzehnt abgerackert und ich ziehe vor Dir und Deinen Kollegen den Hut für das, was ihr tut. Die Welt braucht Leute wie euch. Danke.
CA: Seth, most of us do work where every month, we produce something; we get that kind of gratification. You've been slaving away at this for more than a decade, and I salute you and your colleagues for what you do. The world needs people like you. Thank you.
SB: Danke.
SB: Thank you.
(Beifall)
(Applause)