Chris Anderson: Dr. Şahin and Dr. Türeci, welcome. Such a treat to speak with you.
คริส แอนเดอร์สัน: ดร.ชาฮีน ดร.ทูเรชี ยินดีต้อนรับครับ เป็นเกียรติมากที่ได้มาสนทนากับคุณทั้งสอง
Özlem Türeci: Thank you very much, Chris. It's a pleasure to be here.
เอิซแลม ทูเรชี: ขอบคุณมากค่ะคริส ยินดีเช่นกันค่ะที่ได้มาสนทนากัน
CA: So tell me, as you think back over the last 18 months, what words pop to mind for you?
คริส: บอกผมหน่อยสิครับ หากคิดย้อนกลับไปช่วง 18 เดือนที่แล้ว มีคำไหนที่ผุดขึ้นมาในใจคุณบ้าง
ÖT: Well, one word which comes to mind is breathless. It was indeed a breathless 16, 17 months for us. When we started in January last year, it was already at that time clear to us that we were already in a pandemic. What was not known was how fast this pandemic would evolve and whether we would have the time in the first place to have a vaccine ready soon enough in due time. And understanding this, it meant for us that there was not even one day to lose. And this was the mindset of the entire team here in Mainz and at BioNTech and later on also of our partners which were involved, Pfizer and others, to keep going and be fast.
ทูเรชี: คำหนึ่งที่ผุดขึ้นมาในใจฉันคือ หายใจไม่ทันค่ะ เป็นช่วงเวลา 16 ถึง 17 เดือน ที่เราหายใจกันไม่ทันทีเดียว ตอนที่เราเริ่มในเดือนมกราคมปีที่แล้ว เวลานั้นก็เป็นเวลาที่เกิดโรคระบาดขึ้นแล้ว สิ่งที่เราไม่รู้คือ การระบาด จะขยายวงกว้างรวดเร็วแค่ไหน และที่สำคัญ เราไม่รู้ว่า เราจะมีเวลาพอหรือเปล่า ในการมีวัคซีนที่พร้อมใช้ทันเวลา เมื่อเราเข้าใจในเรื่องนี้ นั่นก็ทำให้เราตระหนักว่า เราเสียเวลาไม่ได้แม้แต่วันเดียว และนี่เป็นหลักคิดของทั้งทีม ที่นี่ ที่ไมนซ์และไบออนเทค และรวมไปถึงพันธมิตรทางธุรกิจ ที่เข้ามามีส่วนร่วม ไฟเซอร์และพันธมิตรอื่น ๆ ที่จะต้องเดินหน้าต่อไปและต้องเร็วด้วย
CA: I mean, it's so extraordinary that the ideas and the work in your minds have now impacted hundreds of millions, perhaps billions of people. That must feel overwhelming. And yet, I know at the same time, you don't believe in this notion of a flash-in-the-pan ideas. Steven Johnson, the author, in his book "Where [Good] Ideas Come From," speaks of the slow hunch, that the best ideas happen over many years. And I know that you believe that is true in your case. I'd like us to go back a couple of decades to -- tell us how this began. How did you meet?
คริส: ผมคิดว่ามันน่าทึ่งมากเลยนะครับ ที่แนวคิดและงานของคุณ ได้มีผลต่อชีวิตผู้คนนับร้อยล้านคน หรือบางทีอาจจะพันล้านคน นั่นคงเป็นความรู้สึกที่ท่วมท้นน่าดู แต่ในขณะเดียวกัน ผมก็ทราบว่า คุณไม่เชื่อเรื่องความคิดบรรเจิด ที่อยู่ดี ๆ ก็บังเอิญแวบเข้ามา สตีเวน จอห์นสัน ผู้แต่งหนังสือเรื่อง “ความคิดบรรเจิดมาจากไหน” ได้พูดถึงความรู้สึกตะหงิด ๆ ที่ว่า ไอเดียบรรเจิดก่อตัว โดยใช้เวลาหลายปี และผมรู้ว่ามันเป็นเช่นนั้นในกรณีของคุณ ผมอยากจะพาเราย้อนกลับไปหลายทศวรรษที่แล้ว บอกเราหน่อยสิครับ เรื่องราวเป็นมาอย่างไร พวกคุณพบกันได้อย่างไร
ÖT: We met on an oncohematology ward, Uğur being a young physician, and I was still in medical school training on ward. Which means we met in one of the worlds which became important to us, the world of patient care, of treating oncohematology patients. And we soon found out that there was a second world which we liked, namely the world of science. We were haunted by the same dilemma, namely that whereas there was not much we could offer our cancer patients, there were so many potential technologies we encountered in the lab which could address this. So one of our shared visions was to bridge this dilemma by working on bringing science and technology fast. And that's an important word here. Fast to the patient's bedside to address high medical need.
ทูเรชี: เราพบกันที่หอผู้ป่วย มะเร็งเม็ดเลือด ตอนนั้นอูกัวยังเป็นแพทย์ใหม่ และตอนนั้นฉันยังเป็นนักศึกษาแพทย์มาฝึกงาน นั่นหมายถึงเราพบกันในโลกหนึ่ง ที่ได้กลายมาเป็นโลกที่สำคัญสำหรับเรา โลกของการดูแลผู้ป่วย ในการรักษาโรคมะเร็งเม็ดเลือด และทันใดเราก็ได้พบว่า ยังมีโลกอีกใบที่เราชอบ และนั่นก็คือโลกของวิทยาศาสตร์ เราถูกตามหลอกหลอนด้วยปัญหาเดียวกัน คือเราพบว่าเราไม่สามารถมอบการรักษา ให้กับผู้ป่วยมะเร็งของเราได้มากเท่าที่ควร แม้เราจะรู้จักเทคโนโลยีที่มีประสิทธิภาพ มากมายในห้องปฏิบัติการ ที่สามารถแก้ไขปัญหานี้ได้ หนึ่งในวิสัยทัศน์ที่เรามีร่วมกัน คือการเชื่อมปัญหากับทางออก โดยการนำวิทยาศาสตร์และเทคโนโลยี เข้ามาใช้อย่างรวดเร็ว นั่นเป็นคำที่สำคัญมากเลยนะคะ ต้องเร็วเพื่อที่จะช่วยรักษาผู้ป่วย ได้อย่างทันท่วงที
CA: So I think the first company you founded nearly 20 years ago was to use the power of the human immune system to tackle cancer.
คริส: ดูเหมือนว่าบริษัทแรก ที่คุณก่อตั้งมาเกือบ 20 ปีที่แล้ว จะใช้พลังจากระบบภูมิคุ้มกันของมนุษย์ ในการจัดการกับมะเร็ง
Uğur Şahin: We were always interested in using the patient's immune system to fight cancer and other type of diseases. As immunologists, we knew how powerful the human immune system is. But it was also clear that the human immune system, in the case of cancer, did not fight cancer cells. It could fight it, but it didn't. And for that, we wanted to develop immunotherapies. That means treatments that use the power of the immune system and redirect the power of the immune system to cancer cells. It was clear that in the university setting, we could not continue to develop monoclonal antibodies because the cost for development of monoclonal antibodies before you can start a clinical trial, was in the range of 20, 30 million euros, and therefore we decided to start a company to get the funding.
อูกัว ชาฮีน: เรามีความสนใจมาตลอด ในการใช้ระบบภูมิคุ้มกันของผู้ป่วย ในการต่อสู้กับมะเร็งและโรคประเภทอื่น ๆ ในฐานะนักภูมิคุ้มกันวิทยา เราทราบว่า ระบบภูมิคุ้มกันของมนุษย์ทรงพลังแค่ไหน แต่มันก็เป็นที่ชัดเจนว่า ระบบภูมิคุ้มกันของมนุษย์นั้น ในกรณีของมะเร็ง ไม่ต่อสู่กับเซลล์มะเร็ง มันต่อสู้มะเร็งได้ แต่มันไม่ทำ และเมื่อเป็นเช่นนั้น เราจึงอยากจะพัฒนา การรักษาด้วยภูมิคุ้มกันบำบัด ซึ่งหมายถึงการรักษา ที่ใช้พลังจากระบบภูมิคุ้มกัน และกำหนดทิศทางของความสามารถ ของระบบภูมิคุ้มกันนั้นในการจัดการมะเร็ง เรารู้ดีว่า ในบริบทของมหาวิทยาลัย เราไม่สามารถที่จะดำเนินการพัฒนา สารภูมิต้านทานแบบโมโนโคลนอลต่อได้ เนื่องด้วยต้นทุนการพัฒนา สารภูมิต้านทานแบบโมโนโคลนอลมีราคาสูง ก่อนที่จะเริ่มการทดลองทางคลินิก ซึ่งอยู่ระหว่าง 20 ถึง 30 ล้านยูโร เราจึงตัดสินใจก่อตั้งบริษัทเพื่อหาทุน
CA: Now, soon after you started this company, you decided to get married. Tell me about your wedding day.
คริส: ไม่นานหลังจากคุณก่อตั้งบริษัท คุณก็ตัดสินใจที่จะแต่งงานกัน เล่าให้ฟังหน่อยสิครับเกี่ยวกับวันแต่งงาน
ÖT: Day was well planned, a quick wedding. And thereafter we went back to the laboratory and our guests at our wedding, that was basically our team, our research team. So no time to lose, Chris.
ทูเรชี: วันนั้นเราวางแผนอย่างดี เป็นงานแต่งงานที่รวดเร็วค่ะ และหลังจากจบงานเราก็กลับไปที่ห้องทดลอง และแขกที่มาในงานก็คือทีมของเรา ทีมวิจัย เราจะเสียเวลาไม่ได้ค่ะคริส
CA: (Laughs) That was a pretty special honeymoon. I mean, it seems like your love for each other is very much bound up in your love for this work and your sense of the importance of this work. How would you characterize those intersecting relationships there?
คริส: (เสียงหัวเราะ) นั่นเป็นการฮันนีมูนที่พิเศษมากเลย ผมหมายถึง ความรักที่คุณมีให้กันและกันนั้น ผูกพันกันด้วยความรักที่พวกคุณมีต่องานนี้ และการตระหนักถึงความสำคัญของงานนี้ คุณจะอธิบายความสัมพันธ์ ของคุณทั้งสองที่เชื่อมกันอย่างไรครับ
UŞ: We are really two scientists. At the end of the day, we love what we do, and for us, we don't differentiate between work and life balance. It's for us really a privilege to be scientists, to be able to do what we love. And therefore, we combine our normal life with our professional life. And therefore, this is pretty normal for us.
ชาฮีน: เราเป็นนักวิทยาศาสตร์ทั้งคู่ ซึ่งท้ายที่สุด เราก็รักงานของเรา และสำหรับเราแล้ว เราไม่ได้แบ่งความสมดุลระหว่าง ชีวิตและการทำงาน นี่เป็นข้อได้เปรียบ ของการเป็นนักวิทยาศาสตร์ ที่สามารถทำสิ่งที่เรารักได้ และเราจึงผสานชีวิตปกติของเรา เข้ากับการทำงาน และนี่ก็เป็นเรื่องธรรมดาสำหรับเรา
CA: So talk to me about this extraordinary molecule RNA, and how you got interested in it and how it became, as I understand it, an increasing focus of your work. And indeed, it led to the founding of BioNTech. Talk about that.
คริส: ช่วยเล่าให้ผมฟังหน่อยสิครับ เกี่ยวกับโมเลกุลที่น่าทึ่งอย่างอาร์เอ็นเอ และคุณเริ่มมาสนใจมันได้อย่างไร และเท่าที่ผมเข้าใจ ทำไมมันถึงเริ่มกลายเป็น จุดเน้นในงานของคุณ และแน่นอน มันนำไปสู่ การก่อตั้งไบออนเทค เล่าให้ฟังหน่อยครับ
UŞ: Yeah, mRNA is a natural molecule, it's one of the first molecules of life. It is a carrier of genetic information. But in contrast to DNA, it's not stable. So it can be used to transfer information to human cells. And the human cells can use this information to build proteins, which can be used for therapeutic settings, for example, to make a protein which is a vaccine, or to make a protein which is an antibody, or to make a protein which is another type of drug. And we were fascinated by this molecule class, because it was very clear that mRNA can be produced pretty fast, within a few days. And we were, as MDs, we were particularly interested to develop personalized medicines. That means a treatment and immunotherapy specifically designed for a cancer patient, because one of the key challenges in cancer treatment, is that every patient has a different tumor. If you compare two tumors of two patients with the same type of tumor, the similarity of the tumors is less than three percent and 97 percent is really unique. And today, it's still not possible to address the uniqueness of the tumor of a patient. And therefore, we were seeking for a technology which could be used for immunotherapy and which could be used to develop a treatment within the shortest possible time. The idea to get the genetic sequence of the tumor and then make a vaccine which is personalized, within a few weeks.
ชาฮีน: ครับ เอ็มอาร์เอ็นเอ เป็นโมเลกุลตามธรรมชาติ เป็นหนึ่งในโมเลกุลแรก ๆ ของชีวิต มันบรรจุข้อมูลทางพันธุกรรม แต่เมื่อเทียบกับดีเอ็นเอ มันไม่ค่อยเสถียรครับ หน้าที่ของมันคือการถ่ายทอดข้อมูล ไปสู่เซลล์ของมนุษย์ และเซลล์ของมนุษย์ก็สามารถใช้ข้อมูลนี้ ในการสร้างโปรตีน ซึ่งสามารถนำมาใช้เพื่อการรักษาโรคได้ เช่น การสร้างโปรตีนที่เป็นวัคซีน หรือการสร้างโปรตีนที่เป็นสารภูมิต้านทาน หรือการสร้างโปรตีนที่เป็นยาประเภทอื่น เรารู้สึกหลงไหลในโมเลกุลประเภทนี้ เพราะมันชัดเจนว่า เอ็มอาร์เอ็นเอถูกผลิตได้อย่างรวดเร็ว ภายในไม่กี่วัน และในฐานะที่เราเป็นแพทย์ เรามีความสนใจเป็นพิเศษในเรื่อง การพัฒนายาเฉพาะบุคคล นั่นหมายถึง การรักษา และการใช้ภูมิคุ้มกันบำบัด ที่ออกแบบมาเฉพาะผู้ป่วยมะเร็งเป็นรายบุคคล เพราะหนึ่งในความท้าทายในการรักษามะเร็ง คือการที่ผู้ป่วยทุกราย มีเนื้องอกที่แตกต่างกัน หากคุณเปรียบเทียบเนื้องอกของผู้ป่วยสองราย ที่มีเนื้องอกประเภทเดียวกัน คุณจะพบความเหมือนของเนื้องอก น้อยกว่าร้อยละสาม และความแตกต่างเฉพาะตัวที่ร้อยละ 97 และทุกวันนี้ มันก็ยังเป็นไปไม่ได้ ในการจัดการกับความแตกต่างเฉพาะตัว ของเนื้องอกในผู้ป่วยแต่ละราย เพราะฉะนั้น เราเลยแสวงหาเทคโนโลยีที่จะสามารถ นำมาใช้กับการรักษาด้วยภูมิคุ้มกันบำบัด และสามารถใช้เพื่อการพัฒนาการรักษา ในเวลาที่สั้นที่สุดเท่าที่จะเป็นไปได้ ความคิดนี้คือ การนำลำดับพันธุกรรม ของเนื้องอก มาใช้ในการสร้างวัคซีนเฉพาะบุคคล ภายในไม่กี่สัปดาห์
CA: Is it fair to say that almost all of the significant things that happen to us biologically are actions done by proteins, and that it's mRNA that actually makes those proteins? If you can understand the language of mRNA, you can get involved in pretty much everything of significance to the well-being of a human being.
คริส: ผมเข้าใจถูกไหมครับ ว่าเกือบทุกสิ่งที่สำคัญที่เกิดขึ้นกับเรา ในทางชีววิทยา เป็นผลจากการกระทำของโปรตีน และเอ็มอาร์เอ็นเอคือสิ่งที่ สร้างโปรตีนเหล่านั้น หากคุณเข้าใจภาษาของเอ็มอาร์เอ็นเอ คุณก็จะสามารถเข้าไปมีส่วนร่วม ในเกือบทุกด้าน ของสวัสดิภาพของมนุษย์
ÖT: Exactly. So in principle, the information instructions are in the DNA. These have to be translated into protein because proteins are the actors which keep our cells alive and our organism functional. And the way how to translate what is instructed by DNA in a fashion that it is well-timed and happens at the right places, into protein, there is messenger RNA. Messenger RNA sort of instructs when and how much of which protein has to be built in order to ensure the activity of our body.
ทูเรชี: ถูกต้องค่ะ ในทางหลักการ ข้อมูลคำสั่งนั้นอยู่ในดีเอ็นเอ ซึ่งจะถูกแปลรหัสเพื่อสังเคราะห์โปรตีน เพราะโปรตีนมีบทบาทสำคัญ ในการทำให้เซลล์ของเรามีชีวิตอยู่ได้ และทำให้ระบบต่าง ๆ ทำงานเป็นปรกติ และการแปลรหัส สิ่งที่สั่งโดยดีเอ็นเอ ในเวลาที่เหมาะสม และเกิดขึ้นที่ตำแหน่งที่ถูกต้อง เป็นหน้าที่ของอาร์เอ็นเอนำรหัส อาร์เอ็นเอนำรหัสจะบอกว่าเมื่อไหร่ และจำนวนเท่าใดที่โปรตีนใดจะถูกสังเคราะห์ เพื่อที่จะแน่ใจว่าร่างกายทำงานเป็นปรกติ
CA: So you can almost think of DNA as the sort of The Oxford English Dictionary of Language. It sort of sits there as the reference point. But for the actual living work, the living work of language out there in the world instructing things, that is done by mRNA.
คริส: ฉะนั้นคุณสามารถมองดีเอ็นเอ เป็นเหมือนพจนานุกรมภาษาอังกฤษ ของอ็อกซ์ฟอร์ด ที่วางอยู่ตรงนั้นเพื่อใช้อ้างอิง แต่ส่วนที่ใช้งานจริง ๆ ก็เหมือนภาษาที่เราใช้เพื่อทำสิ่งต่าง ๆ ซึ่งนี่เป็นหน้าที่ของเอ็มอาร์เอ็นเอ
UŞ: Yeah, absolutely, it is possible. So the human cells, exactly, DNA is like a library. If you have the platform for the messenger RNA therapy, you can deliver any type of message and the body cells ensure that the message is translated into the right protein.
ชาฮีน: ครับ ใช่เลย ประมาณนั้น เมื่อพูดถึงเซลล์ของมนุษย์ ซึ่งอันที่จริง ดีเอ็นเอเป็นเหมือนห้องสมุด หากคุณมีเครื่องมือสำหรับการบำบัดรักษา ด้วยอาร์เอ็นเอนำรหัส คุณจะสามารถส่งข้อความใด ๆ ก็ได้ และแน่นอนที่เซลล์ของร่างกายจะแปลรหัสนั้น เป็นโปรตีนที่ถูกต้อง
ÖT: A high advantage of mRNA is that it is so versatile. You can deliver all sorts of messages, as Uğur has called them. On the one hand, you can deliver the blueprint for the protein which you want to be produced in this cell. But you can, with the same molecule, also design into the mRNA instructions how this protein should be built, instructions to the protein factories of the cell. So you can define whether you want this protein to be built in high amounts or for a long duration, how the pharmacokinetics of this protein should be in the cell.
ทูเรชี: ประโยชน์ที่สำคัญมาก ของเอ็มอาร์เอ็นเอ คือมันทำได้หลายอย่าง คุณสามารถที่จะถ่ายทอดข้อความใด ๆ อย่างที่อูกัวได้บอกไป ในทางหนึ่ง คุณสามารถที่จะส่งพิมพ์เขียว ในการสังเคราะห์โปรตีน ที่คุณต้องการ ให้เกิดขึ้นในเซลล์นั้น ๆ แต่ด้วยโมเลกุลเดียวกันนี้ คุณก็สามารถออกแบบให้เป็น คำสังของเอ็มอาร์เอ็นเอ ว่าควรสังเคราะห์โปรตีนแบบใด เป็นคำสั่งไปยังโรงงานสร้างโปรตีนในเซลล์ ฉะนั้นคุณจึงสามารถกำหนด ว่าคุณอยากให้โปรตีนนี้ผลิตในปริมาณที่มาก หรือในระยะยาว การกำหนดเภสัชจลนศาสตร์ ของโปรตีนในเซลล์ว่าควรเป็นอย่างไร
CA: So talk about January of last year when you first heard about this new virus that was spreading.
คริส: เดือนมกราคมปีที่แล้ว เป็นยังไงบ้างครับ เมื่อคุณได้ยินเกี่ยวกับไวรัสชนิดใหม่ ที่กำลังระบาด
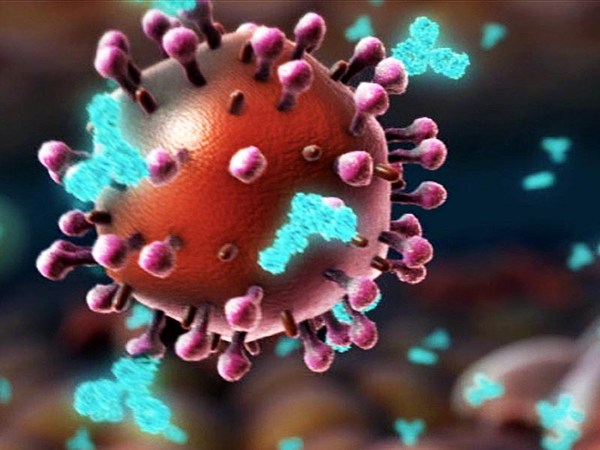
UŞ: So in the end of January, we read a paper published about this outbreak in Wuhan, and realized that this new outbreak has all features to become a global pandemic, and we were concerned that our life will change, that this outbreak could change the fate of mankind. And we knew that we have this messenger RNA technology, which was actually developed for personalized cancer therapy. But the idea of personalized cancer therapy is to get the genetic information of the patient and then make a vaccine as fast as possible. And we had now the same situation. It was not a personalized vaccine, but it was a genetic information of the virus, which was released two weeks earlier. And so this genetic information of this virus was available, and our task was to make a vaccine as fast as possible. And the challenge at that time point was, there was almost nothing known about this virus. It was a completely new virus. We had some assumptions which target which molecule encoded by the virus could be the right target. That means the molecule which can be used to precisely engineer an immune attack. This is the spike protein. It is on the surface of the virus. And there's not only one copy of the spike protein on the virus, but multiple in the range of 20, 25, 30 spike proteins. And the spike protein has two functions. One function is really to enable that the virus sticks to human cells. For example, it sticks to cells in the human lung. And the second is that the spike protein acts as a key. It allows the virus to enter into the cells. Our goal was to engineer an immune response.
ชาฮีน: ปลายเดือนมกราคม เราได้อ่านบทความวิจัยเกี่ยวกับ การระบาดในเมืองอู่ฮั่น และตระหนักว่าการระบาดใหม่นี้ มีครบทุกคุณลักษณะที่จะกลายเป็น การระบาดทั่วโลก และเราต่างกังวลว่าชีวิตของเรา จะมีการเปลี่ยนแปลง กังวลว่าการระบาดนี้จะสามารถ เปลี่ยนชะตากรรมของมนุษยชาติ และเราก็ทราบดีว่า เรามีเทคโนโลยี อาร์เอ็นเอนำรหัสนี้ ซึ่งจริง ๆ แล้วถูกพัฒนาเพื่อการบำบัดรักษา มะเร็งแบบเฉพาะบุคคล ซึ่งแนวคิดของการบำบัดรักษา มะเร็งเฉพาะบุคคล คือการนำข้อมูลทางพันธุกรรมของผู้ป่วย มาใช้ผลิตวัคซีนให้เร็วที่สุด และตอนนี้เราก็อยู่ในสถานการณ์เดียวกัน เพียงแต่มันไม่ใช่การพัฒนาวัคซีนเฉพาะบุคคล แต่เป็นการใช้ข้อมูลพันธุกรรมของไวรัส ซึ่งถูกเผยแพร่ออกมาสองสัปดาห์ก่อนหน้า และเนื่องจากเราสามารถเข้าถึง ข้อมูลทางพันธุกรรมของไวรัสนี้ งานของเราจึงเป็นการสร้างวัคซีน ให้เร็วที่สุดเท่าที่จะทำได้ และอุปสรรคในตอนนั้นคือ เราแทบไม่รู้อะไรเลยเกี่ยวกับไวรัสชนิดนี้ เป็นไวรัสที่ใหม่มาก ๆ เรามีสมมติฐานบางอย่างว่า โมเลกุลใดที่ถูกเข้ารหัสโดยไวรัส จะเป็นเป้าหมายที่ถูกต้อง หมายความว่า โมเลกุลนั้นจะสามารถนำมาใช้ เพื่อที่จะกำหนดได้อย่างแม่นยำว่า ระบบภูมิคุ้มกันจะไปจัดการมัน นี่คือภาพของโปรตีนปุ่มหนาม ที่อยู่บนผิวของไวรัส และโปรตีนปุ่มหนามก็ไม่ได้มีเพียงปุ่มเดียว แต่มีมากมายระหว่าง 20 25 หรือ 30 ปุ่มหนาม และโปรตีนปุ่มหนามก็มีหน้าที่สองประการ หน้าที่แรก คือการที่ทำให้ไวรัส สามารถเกาะกับเซลล์มนุษย์ ยกตัวอย่างเช่น การที่ไวรัสไปเกาะที่เซลล์ ในปอดของมนุษย์ และหน้าที่ที่สองของโปรตีนปุ่มหนาม คือการทำงานเหมือนกุญแจ ที่จะสามารถทำให้ไวรัส เปิดประตูเข้าไปในเซลล์ได้ เป้าหมายของเราคือการออกแบบ การตอบสนองทางภูมิคุ้มกัน
CA: You've got a slide showing the T-cell response to your vaccine. How long were you into the process before you saw this and you saw, wow, there really is a spectacular response going on here?
คริส: คุณมีสไลด์แสดงการตอบสนอง ของที-เซลล์กับวัคซีนของคุณ คุณใช้เวลาเท่าใดก่อนที่คุณจะเห็นภาพนี้ และเมื่อคุณเห็นคุณรู้สึกโอ้โห นี่มันเกิดอะไรขึ้นเนี่ย แบบนี้ไหมครับ
ÖT: We saw this already in the animal models because they are also meant to assess the immune response. And what is shown on this slide is on the left side, a lymph node from a setting where there was no RNA treatment or RNA vaccination. And on the right side, a lymph node of a treated organism, in this case, an animal. And the localization matters. And we have constructed our RNA nanoparticles, with encapsulation into lipids such that the mRNA is carried into lymph nodes, not just anywhere, it's carried into lymph nodes and in the lymph nodes it reaches a very special cell type, which is called dendritic cells, and these cells are coaches of the immune system. So they are the generals which call all the different special forces and train them on the wanted poster of attacker. And it's very important that you reach those cells. On the right side, you can see the effect of reaching those cells. You see many red dots. And these are T-cells which have been trained to recognize the antigen, the protein which mRNA has delivered, and they have expanded to a sort of army of clones, so to say. So all these red dots are an army which only knows one goal, namely attacking this specific protein encoded by the mRNA.
ทูเรชี: เราเห็นภาพนี้มาก่อนแล้วค่ะ ในสัตว์ทดลอง เพราะมันมีวัตถุประสงค์เพื่อทดสอบ การตอบสนองของภูมิคุ้มกัน และที่คุณเห็นบนสไลด์ ทางซ้ายคือภาพต่อมน้ำเหลือง ในกรณีที่ไม่มีการรักษาด้วยอาร์เอ็นเอ หรือได้รับวัคซีนอาร์เอ็นเอ และทางขวาคือภาพต่อมน้ำเหลือง ของสิ่งมีชีวิตที่ได้รับการรักษา ในกรณีนี้เป็นเซลล์ของสัตว์ และการกำหนดตำแหน่งเป็นเรื่องสำคัญ และเราได้สร้างอนุภาคอาร์เอ็นเอระดับนาโน ที่ถูกหุ้มด้วยชั้นของลิพิด เพื่อที่ว่าเอ็มอาร์เอ็นเอ จะถูกส่งไปยังต่อมน้ำเหลือง ไม่ใช่ส่งไปที่ไหนก็ได้ แต่ต้องไปที่ต่อมน้ำเหลืองเท่านั้น และภายในต่อมน้ำเหลือง มันจะเข้าไปหาเซลล์ประเภทพิเศษ ที่เรียกว่าเซลล์มีแขนง และเซลล์เหล่านี้เป็นเหมือนโค้ช ของระบบภูมิคุ้มกัน เพราะมันทำหน้าที่ในการสั่งการ ให้ระดมกำลังแบบต่าง ๆ และฝึกฝนให้สามารถจัดการกับ ศัตรูที่หมายหัวไว้ มันสำคัญมากค่ะที่คุณจะเข้าไปให้ถึง เซลล์เหล่านั้น ส่วนทางขวาคุณจะเห็นผลของ การเข้าถึงเซลล์เหล่านั้น คุณจะเห็นจุดสีแดงมากมาย และนี่คือที-เซลล์ที่ได้รับการฝึกฝน ให้สามารถระบุสารก่อภูมิต้านทานได้ เป็นโปรตีนที่เอ็มอาร์เอ็นเอได้ถูกนำไปส่ง และหากจะพูดให้ชัด มันได้ขยายตัว กลายเป็นกองทัพของโคลน จุดสีแดงเล็ก ๆ เหล่านี้คือกองทัพ ที่รู้เป้าหมายเพียงอย่างเดียว คือการจัดการโปรตีนเฉพาะตัว ที่ถูกเข้ารหัสด้วยเอ็มอาร์เอ็นเอ
CA: So it's really stunning that within just a few days of your looking at this sequence of the most dangerous pathogen to hit humanity in 100 years, I guess, that you were able to come up with these these candidate vaccines. And I guess over the course of the next weeks and months, you had growing confidence that, wow, this was going to work. It wasn't until the results of the human trials came out, I guess in November of last year, that you really knew. Tell us about that moment.
คริส: นี่มันน่าทึ่งทีเดียว ที่เพียงไม่กี่วันหลังจากที่ คุณศึกษาลำดับเหล่านี้ ซึ่งเป็นของจุลชีพก่อโรคที่อันตรายที่สุด ที่โจมตีมนุษยชาติในรอบ 100 ปี ถ้าให้ผมเดา และคุณก็สามารถที่จะคิดค้นวัคซีนตัวทดลอง และผมเดาว่าไม่กี่สัปดาห์หรือไม่กี่เดือน คุณเริ่มมีความมั่นใจว่า โอ้โห มันต้องได้ผลแน่ ๆ จนกระทั่งผลลัพธ์จากการทดลองในมนุษย์ออกมา ผมคิดว่าเป็นช่วงเดือนพฤษจิกายนปีที่แล้ว คุณรู้ว่าวันไหน เล่าให้เราฟังถึงตอนนั้นหน่อยครับ
ÖT: It was a Sunday when we were waiting for these results, which are assessed in such trials by an independent committee and Uğur said, "So let's see how the data will look like." It was not clear whether it would be a thumbs up or down. And we were very relieved. And I felt blessed to hear that the vaccine was efficacious and it was highly efficacious, over 90 percent.
ทูเรชี: วันนั้นเป็นวันอาทิตย์ค่ะ ที่เราเฝ้ารอผล ซึ่งเป็นการประเมินผลการทดลอง โดยคณะกรรมการอิสระ และอย่างที่อูกัวบอก “เรามาดูผลกันว่าจะมีหน้าตาเป็นยังไง” มันไม่แน่ชัดว่าผลจะออกมาดีหรือไม่ และสุดท้ายเราก็โล่งอก ฉันรู้สึกโชคดีที่ได้รับฟังว่า วัคซีนนั้นให้ผลตามที่ต้องการ และมีประสิทธิภาพสูง มากกว่าร้อยละ 90
CA: And that more than 90 percent almost disguises the full extent, because that's just against any kind of level of infection of COVID. Severe infection and fatalities were almost completely protected against, I think. And it must have been an ecstatic moment for you. Certainly was for so many people around the world.
คริส: และการที่มีประสิทธิภาพมากกว่า ร้อยละ 90 มันก็แทบสมบูรณ์แล้ว เพราะว่ามันก็สามารถต่อสู้ กับการติดเชื้อโควิดได้ทุกระดับ การป้องกันเกือบสมบูรณ์ต่อการติดเชื้อรุนแรง รวมไปถึงป้องกันการเสียชีวิต ผมคิดว่านะ และมันคงเป็นชั่วขณะแห่งความปีติของคุณแน่ ๆ แน่นอนสำหรับผู้คนมากมายทั่วโลกด้วย
UŞ: Yes, absolutely. So this was a Sunday evening, and there were a handful of people knowing that an effective vaccine is existing against this global pandemic. And we were so excited and so happy and we shared of course this information the next day.
ชาฮีน: ครับ เป็นเช่นนั้น ตอนนั้นคือช่วงเย็นของวันอาทิตย์ และมีเพียงไม่กี่คน ที่ทราบว่าเรามีวัคซีนที่มีประสิทธิภาพเพื่อ จัดการกับโรคระบาดที่กำลังเกิดขึ้นทั่วโลก และเราทั้งตื่นเต้นและมีความสุขมาก และแน่นอนเราก็ได้เผยแพร่ข้อมูลนั้น ในวันถัดไป
CA: So based on what's happened this time around and the amazing acceleration, compared with any other vaccine development, I mean, if we were hit by another virus, could you picture that next time we could accelerate the time line further still if need be?
คริส: หากมองสิ่งที่เกิดขึ้นในช่วงที่ผ่านมา และการเร่งการพัฒนาอย่างรวดเร็ว เมื่อเปรียบเทียบกับการพัฒนาวัคซีนในอดีต สมมติว่าถ้าเราถูกโจมตีด้วยไวรัสอีกชนิด คุณลองจินตนาการดูได้ไหมครับว่า เราจะสามารถเร่งกระบวนการเช่นนี้ได้ หากจำเป็น
UŞ: Yes, Chris, this is an excellent question. Actually, the world was not prepared to deal with such a pandemic. The science and the vaccine developers reacted in an excellent fashion. And it is incredible and wonderful that it was possible to come up with an effective vaccine while a pandemic is ongoing, in less than 12 months. But the challenges that we have at the moment is that we don't have sufficient production capacity. Ideally, we would be prepared the next time, not only to develop a vaccine in light speed, but also to to make and distribute the vaccine in light speed. So what we need now is an additional element which was not existing, is manufacturing capacity. And idle manufacturing capacity. We must be bringing us into a position that we can produce 12 billion doses of vaccine, if you consider prime boost, within less than six months. And this is technically possible. So this can be done if governments and international organizations invest into manufacturing capacity, invest into keeping this idle capacity, and also come up with a standard time span and process to enable even faster response. So we in principle, we might be able to manage to come up with a vaccine and start distribution in even less than eight months.
ชาฮีน: ครับ คริส เป็นคำถามที่เยี่ยมมากครับ จริง ๆ แล้ว ทั่วโลกไม่ได้เตรียมรับมือ กับโรคระบาดเช่นนี้ แต่นักวิทยาศาสตร์และนักพัฒนาวัคซีน ก็ได้ตอบสนองกับการระบาดได้อย่างยอดเยี่ยม มันเหลือเชื่อและน่าประหลาดใจมาก ที่เราสามารถพัฒนาวัคซีน ที่มีประสิทธิภาพได้สำเร็จ ในขณะที่กำลังเกิดโรคระบาด และภายในไม่ถึง 12 เดือน แต่อุปสรรคที่เรามีในตอนนั้น คือการที่เราไม่มีกำลังการผลิตที่เพียงพอ ดีที่สุดคือ หากเราสามารถ เตรียมการสำหรับครั้งหน้า ไม่เพียงแต่พัฒนาวัคซีนได้ระดับความเร็วแสง แต่ต้องสามารถผลิตและแจกจ่ายวัคซีน ได้ในระดับความเร็วแสงเช่นกัน เพราะฉะนั้นสิ่งที่เราต้องการในตอนนี้ คือองค์ประกอบที่ยังไม่มี ซึ่งก็คือกำลังการผลิต และกำลังการผลิตสำรอง เราต้องสามารถพาตัวเองไปยังจุด ที่เราสามารถผลิตวัคซีนได้ หนึ่งหมึ่นสองพันล้านโดส หากพิจารณาจากการเร่งผลิตในอุดมคติ ซึ่งต้องทันภายในหกเดือน และนี่ก็เป็นไปได้ในทางปฏิบัติด้วย สิ่งนี้จะเป็นไปได้ หากรัฐบาลต่าง ๆ รวมไปถึงองค์กรระหว่างประเทศ มาร่วมลงทุนกับการเพิ่มกำลังการผลิต และการลงทุนในการเพิ่มกำลังการผลิตสำรองไว้ และการออกแบบมาตรฐานกรอบเวลาและกระบวนการ ในการจัดการที่เร็วยิ่งขึ้น ในทางหลักการ เราอาจคิดค้นพัฒนาจนได้วัคซีน และเริ่มกระจายวัคซีนได้ภายในไม่ถึงแปดเดือน
CA: What does what's happened in this last year tell you now about the prospects for using mRNA to treat cancer and indeed other diseases? Where is this heading?
คริส: สิ่งที่เกิดขึ้นเมื่อปีที่แล้ว ได้บอกอะไรกับคุณในตอนนี้ ถึงแนวทางในอนาคตเกี่ยวกับ การใช้เอ็มอาร์เอ็นเอในการรักษามะเร็ง และแน่นอนโรคอื่น ๆ ด้วย สิ่งนี้จะมีทิศทางอย่างไรครับ
UŞ: What we have now is now an approved technology and a first approved product. The development of the coronavirus mRNA vaccine shows the power of the mRNA and it shows also the safety of this approach. And it shows that it opens up a door for new technology and for new type of treatments. And the mRNA molecules that we are currently using for cancer, we have more than 10 products now in clinical development, are diverse against different types of cancer. We are very confident that the success that we have generated now for our infectious disease vaccines can be continued with our cancer immunotherapies.
ชาฮีน: สิ่งที่เรามีในตอนนี้คือ เทคโนโลยีที่ได้รับการยอมรับ และผลิตภัณฑ์ที่ได้รับการยอมรับ การพัฒนาวัคซีนเอ็มอาร์เอ็นเอ เพื่อต้านเชื้อไวรัสโคโรน่า ได้แสดงถึงพลัง ของเอ็มอาร์เอ็นเอ และยืนยันว่าเป็นวิธีการที่ปลอดภัย รวมไปถึง การเปิดประตูสู่เทคโนโลยีใหม่ ๆ สำหรับการรักษาแนวใหม่ และโมเลกุลเอ็มอาร์เอ็นเอ ที่เรากำลังใช้อยู่ตอนนี้ในการรักษามะเร็ง มีจำนวนมากกว่า 10 ผลิตภัณฑ์ ที่กำลังอยู่ในขั้นการทดลองทางคลินิก ที่มีความหลากหลายเพื่อการต่อต้าน มะเร็งที่ต่างชนิดกัน เรามีความมั่นใจเป็นอย่างมากในความสำเร็จ ที่เราได้สร้างขึ้น ในการพัฒนาวัคซีนต้านโรคติดเชื้อ จะทำให้การพัฒนาการรักษามะเร็ง ด้วยการบำบัดด้วยภูมิคุ้มกัน เดินหน้าต่อได้
CA: Some people may hear this and say this is just another type of drug that's coming along. But I think on the mental model you're talking about, we should think about it as much more revolutionary than that, that typically a drug, a traditional drug, kind of changes the chemical environment, the background of an entire area of the body. But your -- If you understand the language of mRNA, you can do something much more specific and precise. Is that something like a fair way to think about it?
คริส: หลายคนฟังแล้ว อาจบอกว่านี่มันก็แค่ยาชนิดใหม่ ที่ถูกพัฒนาขึ้น แต่ผมคิดว่า ด้วยหลักคิดที่คุณกำลังสื่อสาร เราควรที่จะคิดเชิงปฏิวัติมากกว่า ผมหมายถึง ยาโดยทั่วไป เป็นการเปลี่ยนสภาพแวดล้อมทางเคมี เป็นพื้นหลังของพื้นที่ทั้งหมดของร่างกาย แต่ หากคุณเข้าใจภาษาของเอ็มอาร์เอ็นเอ คุณจะสามารถทำบางสิ่งที่จำเพาะเจาะจง และแม่นยำได้มากกว่า ผมคิดแบบนี้ถูกต้องไหมครับ
ÖT: Yes, indeed. It could be the next revolution in the biopharm landscape.
ทูเรชี: ใช่เลยค่ะ นี่จะเป็นการปฏิวัติ ที่เกิดขึ้นในวงการชีวเภสัชภัณฑ์
UŞ: At the end of the day, disease is a situation where the communication between cells is disturbed. So, for example, autoimmune disease is a disease condition where immune cells attack normal cells. And indeed, we could engineer messenger RNA therapies which could teach the immune system to stop to do that, without inhibiting the whole immune system, by just communicating with the immune cells which are attacking. We could be precise and more specific.
ชาฮีน: ท้ายที่สุดแล้ว โรคภัยไข้เจ็บเป็นสถานการณ์ ที่การสื่อสารระหว่างเซลล์ถูกรบกวน ตัวอย่างเช่น โรคภูมิต้านทานตัวเอง เป็นโรคที่มีลักษณะคือ เซลล์ภูมิคุ้มกันโจมตีเซลล์ปรกติ และแน่นอน เราสามารถออกแบบ การบำบัดด้วยอาร์เอ็นเอนำรหัส ที่สามารถสั่งให้ระบบภูมิคุ้มกัน หยุดทำเช่นนั้น โดยไม่ได้เป็นการหยุด ระบบภูมิคุ้มกันทั้งหมด แต่เป็นการสื่อสารไปที่เซลล์ภูมิคุ้มกัน ที่กำลังโจมตีอยู่ เราสามารถที่จะดำเนินการได้อย่างแม่นยำ และเฉพาะเจาะจงมากขึ้น
CA: The success of BioNTech over the last couple of years, I think the value of the company has rocketed because of the amazingness of what's happened. I mean, it's made you both extremely wealthy, I think you're both billionaires now. How have you been able to respond to that? Sometimes so much money brings its own problems with it. Is that proving a distraction?
คริส: ความสำเร็จของไบออนเทค ในช่วงไม่กี่ปีที่ผ่านมา ผมคิดว่ามูลค่าของบริษัทได้ทะยานขึ้น เพราะความน่าทึ่งที่เกิดขึ้น ผมหมายถึง มันทำให้คุณทั้งสอง ร่ำรวยขึ้นมาก ผมคิดว่าตอนนี้ พวกคุณคือเศรษฐีพันล้าน คุณคิดยังไงเหรอครับ บางครั้งการมีเงินมากก็มักนำปัญหามาให้ มันทำให้คุณไขว้เขวไหมครับ
ÖT: For a company which sees innovation as its core mission, too much money is never a problem. Because innovation really means that you have to invest. Otherwise, we will only have two type of products or incremental improvement for solutions of high medical need.
ทูเรชี: สำหรับบริษัท ที่มองนวัตกรรมเป็นแกนหลักของพันธกิจ การมีเงินมากเกินไปไม่เคยเป็นปัญหา เพราะนวัตกรรมหมายถึงการที่คุณต้องลงทุน ไม่เช่นนั้นแล้วเราก็จะมีผลิตภัณฑ์ เพียงสองสามชนิด ไม่ก็ก้าวหน้าได้เพียงเล็กน้อย สำหรับการตอบรับกับ ความต้องการทางการแพทย์ที่มีมาก
UŞ: It really gives us the chance to transform our company. So we were when we started -- When we compare ourselves with the situation we had at the beginning of 2020, we had a number of product candidates in clinical testing, but the company required funding every year or every second year. Now we have a situation to really address the full vision of the company. We started BioNTech with the idea really to provide novel treatments wherever there is a high unmet medical need. And we now can do that in a much larger and broader scale, and bring our innovations faster to patients.
ชาฮีน: มันทำให้เราได้มีโอกาส ในการเปลี่ยนแปลงบริษัทของเรา ในตอนที่เราเริ่ม หากเปรียบเทียบกับตอนนั้น ในต้นปี ค.ศ. 2020 เรามีผลิตภัณฑ์ที่อยู่ในขั้นทดลองทางคลินิก แต่บริษัทต้องการเงินทุนทุก ๆ ปี หรือสองปี ตอนนี้เราอยู่ในจุดที่สามารถตอบสนอง วิสัยทัศน์ของบริษัทได้อย่างเต็มที่ เราเริ่มต้นไบออนเทค ด้วยความคิดที่จะมอบการรักษาแบบใหม่ เพื่อตอบสนองความต้องการทางการแพทย์ ที่ยังไม่เป็นที่น่าพอใจ ตอนนี้เราสามารถทำได้แล้ว ในระดับที่ใหญ่ขึ้นและกว้างขึ้น และนำนวัตกรรมของเราไปใช้กับผู้ป่วย ได้รวดเร็วขึ้น
CA: You are both from families who immigrated from Turkey to Germany. Immigrants have faced hard times in many countries, including Germany. And yet you, I think, have helped transform the debate about immigration, in Germany and elsewhere, just by the extraordinary success that you've achieved creating this world-leading company in Germany. Do you take joy for the impact you may have had on this issue?
คริส: คุณทั้งสองมาจากครอบครัวผู้อพยพ จากตุรกีมาที่เยอรมนี ผู้อพยพต้องเผชิญกับปัญหาต่าง ๆ มาตลอด ในหลายประเทศ ซึ่งรวมถึงเยอรมนี แต่ผมคิดว่า คุณได้ช่วยแปรเปลี่ยนข้อถกเถียง เกี่ยวกับการอพยพ ทั้งในเยอรมนีและที่อื่น ๆ เพียงดูจากความสำเร็จอันน่าทึ่ง ที่คุณได้คว้ามา จากการสร้างบริษัทชั้นนำระดับโลก ในเยอรมนี คุณรู้สึกยินดีกับบทบาทของตัวเอง ที่อาจมีส่วนในประเด็นนี้ไหมครับ
UŞ: It is somehow surprising because the way how we do science, and how we recognize how people work effectively in teams together is not to us from where the person is coming, but what the person can contribute. So in our company, we have employees from more than 60 countries. So we are an international group of scientists, as any other research institution. So we have to recognize that globalization really helps to bring people, scientists or other engineers into one place, allowing to work together and to come with extraordinary results. For us, this is somehow surprising that this is seen as special. It is just the way how excellent research and science work.
ชาฮีน: มันเป็นเรื่องที่ไม่คาดคิดมาก่อน เพราะว่าวิธีที่เราทำงานด้านวิทยาศาสตร์ และวิธีที่เราตระหนักถึง การทำงานร่วมกันอย่างมีประสิทธิภาพ ไม่ได้เกี่ยวข้องกับพื้นเพของบุคคลนั้น ๆ แต่เกี่ยวข้องกับสิ่งที่พวกเขาสามารถทำได้ ในบริษัทของเราจึงมีพนักงาน ที่มาจากกว่า 60 ประเทศ เราเลยเป็นบริษัทที่เป็นกลุ่ม ของนักวิทยาศาสตร์นานาชาติ เช่นเดียวกับสถาบันวิจัยอื่น ๆ เราจะต้องตระหนักว่า โลกาภิวัฒน์นั้นมีส่วนช่วย ในการรวมผู้คน นักวิทยาศาสตร์ หรือวิศวกรด้านต่าง ๆ มาอยู่ในที่เดียวกัน ทำให้พวกเขาทำงานร่วมกันได้ และยังผลที่น่าทึ่ง สำหรับเราแล้ว มันน่าแปลกใจ ที่คนมองว่ามันเป็นสิ่งที่พิเศษ มันก็เป็นแค่วิธีการชั้นยอด สำหรับการวิจัยและการทำงานด้านวิทยาศาสตร์
CA: Well, it's extraordinary and inspiring what you've achieved, and it'll be very exciting to track progress over the coming years. Thank you so much. Thank you.
คริส: ความสำเร็จของคุณ ช่างน่าอัศจรรย์และจับใจ และมันคงน่าตื่นเต้นมากในการติดตาม ความคืบหน้าต่าง ๆ ที่จะตามมาในอนาคต ขอบคุณมากครับ ขอบคุณ