Chris Anderson: Dr. Şahin and Dr. Türeci, welcome. Such a treat to speak with you.
크리스 앤더슨: 사힌 박사님, 튀레지 박사님, 어서 오세요. 함께하게 되어 영광입니다.
Özlem Türeci: Thank you very much, Chris. It's a pleasure to be here.
외즐렘 튀레지: 감사합니다. 이곳에서 이야기하게 되어 기쁘네요.
CA: So tell me, as you think back over the last 18 months, what words pop to mind for you?
크리스: 박사님들께선 지난 18개월을 뭐라고 표현하시겠어요?
ÖT: Well, one word which comes to mind is breathless. It was indeed a breathless 16, 17 months for us. When we started in January last year, it was already at that time clear to us that we were already in a pandemic. What was not known was how fast this pandemic would evolve and whether we would have the time in the first place to have a vaccine ready soon enough in due time. And understanding this, it meant for us that there was not even one day to lose. And this was the mindset of the entire team here in Mainz and at BioNTech and later on also of our partners which were involved, Pfizer and others, to keep going and be fast.
튀레지: 음, 한마디로 표현해서 숨 막혔다고 할 수 있겠네요. 저희에겐 지난 16, 17개월이 정말 숨막히는 시간이었거든요. 저희가 작년 1월에 연구를 시작했을 땐 팬데믹과 마주하는 것이 이미 현실이 되어 있었습니다. 그때 알지 못했던 건 이 팬데믹이 얼마나 빠르게 진행될지, 그리고 시간 내에 백신을 준비해 이에 대응할 수 있을지 전혀 알 수 없었죠. 이 점을 알고 있기에 저희에겐 하루하루가 다급하고 중요했어요. 그리고 이곳 마인츠와 바이오엔테크의 모든 팀들은 그런 마음가짐으로 연구를 진행했죠. 그리고 이후에 함께하게 된 화이자와 다른 파트너들도 포기하지 않고 신속하게 연구가 진행되도록 할 수 있었죠.
CA: I mean, it's so extraordinary that the ideas and the work in your minds have now impacted hundreds of millions, perhaps billions of people. That must feel overwhelming. And yet, I know at the same time, you don't believe in this notion of a flash-in-the-pan ideas. Steven Johnson, the author, in his book "Where [Good] Ideas Come From," speaks of the slow hunch, that the best ideas happen over many years. And I know that you believe that is true in your case. I'd like us to go back a couple of decades to -- tell us how this began. How did you meet?
크리스: 두 분의 남다른 마음가짐과 노력으로 현재 수억, 어쩌면 수십억 명의 삶을 바꾸셨다는 게 정말 대단합니다. 두 분께도 큰 사건이지 않았나 싶은데요, 그럼에도 저는 두 분이 잠깐의 스치는 아이디어로 일궈낸 업적이 아니라는 걸 알고 있습니다. 작가 스티븐 존슨의 저서 “탁월한 아이디어는 어디서 오는가“에서 느린 직감에 대해 말했었죠. 최고의 생각들은 몇년에 걸쳐 떠오른다고요. 박사님들께서도 이와 같은 경우라고 느끼실 것 같아요. 이 모든 일들이 어떻게 시작되었는지, 수십 년 전의 이야기부터 해봅시다. 두 분은 어떻게 만나신 거에요?
ÖT: We met on an oncohematology ward, Uğur being a young physician, and I was still in medical school training on ward. Which means we met in one of the worlds which became important to us, the world of patient care, of treating oncohematology patients. And we soon found out that there was a second world which we liked, namely the world of science. We were haunted by the same dilemma, namely that whereas there was not much we could offer our cancer patients, there were so many potential technologies we encountered in the lab which could address this. So one of our shared visions was to bridge this dilemma by working on bringing science and technology fast. And that's an important word here. Fast to the patient's bedside to address high medical need.
튀레지: 저희는 종양혈액학 병동에서 만났어요. 당시 우구르는 젊은 내과 의사였고, 저는 아직 의과 대학에서 병동 실습을 하고 있을 때였죠. 그러니까 저희의 만남은 환자 치료, 그 중에서도 혈액종양 환자들을 돕는 거였고, 저희에게는 정말 중요한 부분이 하나로 만나게 된 것이죠. 그리고 저희는 또 하나의 소중한 접점을 발견했고, 바로 과학의 세계였어요. 당시 저희 둘은 같은 딜레마에 빠져 있었어요. 저희가 돌보는 암 환자들에게 해줄 수 있는 건 많지 않은 반면에, 실험실에는 이를 해결할 수 있는 유망한 기술들이 너무나도 많았거든요. 이 딜레마를 해결하기 위해 함께 생각해본 방법이 바로 과학과 기술을 빠르게 연결시키는 거였어요. ‘빠르게’라는 게 정말 중요했어요. 환자가 의학적 도움을 필요로 할 때 신속히 제공할 수 있도록요.
CA: So I think the first company you founded nearly 20 years ago was to use the power of the human immune system to tackle cancer.
크리스: 20년 전에 박사님들께서 설립하신 첫 번째 회사에서는 인간 면역 체계의 힘을 이용해 암에 맞서는 거였죠.
Uğur Şahin: We were always interested in using the patient's immune system to fight cancer and other type of diseases. As immunologists, we knew how powerful the human immune system is. But it was also clear that the human immune system, in the case of cancer, did not fight cancer cells. It could fight it, but it didn't. And for that, we wanted to develop immunotherapies. That means treatments that use the power of the immune system and redirect the power of the immune system to cancer cells. It was clear that in the university setting, we could not continue to develop monoclonal antibodies because the cost for development of monoclonal antibodies before you can start a clinical trial, was in the range of 20, 30 million euros, and therefore we decided to start a company to get the funding.
우구르 사힌: 저희는 환자가 이미 가지고 있는 면역 체계를 통해 암과 다른 질병들에 맞서는 데에 관심이 많았어요. 면역학자인 저희는 인간의 면역 체계가 얼마나 강력한지 알았거든요. 하지만 그 면역 체계가 암의 경우에서는 암세포에 대응하지 않는다는 점도 확실했어요. 대응할 수 있지만, 하지 않았던 거죠. 따라서 저희는 면역요법을 개발하고 싶었어요. 바로 면역체계 자체의 강력한 힘이 암세포 공격에 사용될 수 있도록 하는 치료법인 거죠. 하지만 대학교의 환경에서는 단일 클론 항체의 개발을 계속하기가 매우 어려웠어요. 단일 클론 항체 개발에 드는 비용은 임상실험을 시작하기도 전이라도 거의 2, 3백억원 정도가 들었거든요. 그래서 저희는 기업을 시작해서 자금을 마련하기로 했어요.
CA: Now, soon after you started this company, you decided to get married. Tell me about your wedding day.
크리스: 그럼 두 분은 기업을 시작하고 곧 결혼하신 거죠? 결혼식 날은 어땠는지 말해주세요.
ÖT: Day was well planned, a quick wedding. And thereafter we went back to the laboratory and our guests at our wedding, that was basically our team, our research team. So no time to lose, Chris.
튀레지: 뭐, 잘 계획된 결혼식이었죠. 금방 끝났어요. 예식 후에 바로 실험실로 돌아갔고, 결혼식에 오신 하객분들도 대부분 저희 연구팀이었어요. 고민할 시간이 없어요, 크리스.
CA: (Laughs) That was a pretty special honeymoon. I mean, it seems like your love for each other is very much bound up in your love for this work and your sense of the importance of this work. How would you characterize those intersecting relationships there?
(웃음) 크리스: 신혼여행도 특별했다죠. 제가 생각하기에 두 분의 사랑은 이 연구에 대한 사랑이나 이 일을 중요시하는 것과도 많이 엮여있는 것 같아요. 이 복합 관계를 뭐라고 표현하시겠어요?
UŞ: We are really two scientists. At the end of the day, we love what we do, and for us, we don't differentiate between work and life balance. It's for us really a privilege to be scientists, to be able to do what we love. And therefore, we combine our normal life with our professional life. And therefore, this is pretty normal for us.
사힌: 저희는 그야말로 두 명의 과학자예요. 결국 가장 중요한 것은 저희가 하는 일을 사랑하는 거고, 저희는 이 일과 삶의 균형을 따로 구분짓지 않아요. 저희가 사랑하는 연구를 할 수 있다는 거 자체만으로도 과학자로서 특권이자 영광이죠. 그래서 저희는 일상과 과학자로서의 삶을 합친답니다. 저희한테는 이 삶이 꽤 정상이 됐어요.
CA: So talk to me about this extraordinary molecule RNA, and how you got interested in it and how it became, as I understand it, an increasing focus of your work. And indeed, it led to the founding of BioNTech. Talk about that.
크리스: 그럼 이제 그 놀라운 RNA라는 분자와 여기에 관심을 갖게 되신 계기, 그리고 어떻게 연구의 핵심이 되었는지 이야기해주세요. 그리고 이 연구가 바이오엔테크의 설립으로도 이어졌죠, 이것도 이야기해주세요.
UŞ: Yeah, mRNA is a natural molecule, it's one of the first molecules of life. It is a carrier of genetic information. But in contrast to DNA, it's not stable. So it can be used to transfer information to human cells. And the human cells can use this information to build proteins, which can be used for therapeutic settings, for example, to make a protein which is a vaccine, or to make a protein which is an antibody, or to make a protein which is another type of drug. And we were fascinated by this molecule class, because it was very clear that mRNA can be produced pretty fast, within a few days. And we were, as MDs, we were particularly interested to develop personalized medicines. That means a treatment and immunotherapy specifically designed for a cancer patient, because one of the key challenges in cancer treatment, is that every patient has a different tumor. If you compare two tumors of two patients with the same type of tumor, the similarity of the tumors is less than three percent and 97 percent is really unique. And today, it's still not possible to address the uniqueness of the tumor of a patient. And therefore, we were seeking for a technology which could be used for immunotherapy and which could be used to develop a treatment within the shortest possible time. The idea to get the genetic sequence of the tumor and then make a vaccine which is personalized, within a few weeks.
사힌: 네, 먼저 mRNA는 자연적인 분자입니다. 생명에서 가장 처음 만들어지는 분자 중 하나이기도 하고요. mRNA는 유전정보의 운반자예요. 하지만 DNA와는 달리 불안정하죠. 그래서 인간 세포에게 정보를 전달할 수 있는 거에요. 정보를 받은 세포들은 그것을 기반으로 단백질을 만들 수 있고, 그 단백질들을 치료에 사용하는 겁니다. 예를 들어서 단백질로 백신을 만들거나 단백질로 항체를 만들거나, 또는 단백질로 다른 종류의 치료제를 만들 수 있어요. 저희는 이 분자의 매력에 빠질 수밖에 없었습니다. mRNA는 며칠 정도만에 빠르게 만들어질 수 있다는 확실한 장점을 갖고 있기 때문이죠. 의사로서 저희는 맞춤형 치료제에 특히 관심을 가지고 있었어요. 맞춤형 치료제는 치료와 면역요법이 특정한 암환자에게 맞춰져서 제조되는 건데요. 암 치료의 큰 과제 중 하나는 모든 환자가 각기 다른 종양을 갖고 있다는 점입니다. 같은 종류의 종양을 갖고 있는 두 환자의 종양을 비교했을 때, 그 종양들 간의 유사성은 3%도 되지 않습니다. 나머지 97%는 고유한 특징을 갖는다는 의미죠. 아직까지도 종양들의 이러한 고유성을 공략하는 해결법을 찾지 못했어요. 따라서 저희는 면역요법에 사용될 수 있는 기술과 이를 해결할 수 있는 치료법을 최대한 빠르게 찾아내고자 했습니다. 그 방법은 바로 종양의 유전자 서열을 알아내고 그에 대한 맞춤형 백신을 단 몇 주 만에 만들자는 것이었죠.
CA: Is it fair to say that almost all of the significant things that happen to us biologically are actions done by proteins, and that it's mRNA that actually makes those proteins? If you can understand the language of mRNA, you can get involved in pretty much everything of significance to the well-being of a human being.
크리스: 궁금한 게 있는데 우리 몸의 중요한 생물학적인 일들이 모두 단백질의 역할이고 mRNA가 그 단백질들을 직접 만들어내는 건가요? 그럼 mRNA의 언어를 해독하게 된다면 인간에게 중요한 모든 일들에 관여할 수 있는 거겠네요?
ÖT: Exactly. So in principle, the information instructions are in the DNA. These have to be translated into protein because proteins are the actors which keep our cells alive and our organism functional. And the way how to translate what is instructed by DNA in a fashion that it is well-timed and happens at the right places, into protein, there is messenger RNA. Messenger RNA sort of instructs when and how much of which protein has to be built in order to ensure the activity of our body.
튀레지: 맞아요. 이론적으로는, 단백질 합성의 모든 정보가 DNA에 저장되어 있습니다. 그 정보를 통해서 단백질이 만들어지죠. 왜냐하면 단백질의 역할이 세포를 유지하고 생명활동을 가능하게 해주는 것이기 때문입니다. 그리고 DNA의 지시사항이 단백질로 번역될 때 정확한 시기에, 정확한 장소에서 일어나도록 하는 게 메신저 RNA인 거죠. 메신저 RNA는 어떤 단백질이 언제, 얼만큼 만들어져야 하는지 지시를 내려서 신체의 작용을 책임집니다.
CA: So you can almost think of DNA as the sort of The Oxford English Dictionary of Language. It sort of sits there as the reference point. But for the actual living work, the living work of language out there in the world instructing things, that is done by mRNA.
크리스: 그럼 DNA는 옥스포드 영어사전 같은 거군요. 일종의 참고서 같은 것 말이죠. 반면에 생명활동, 즉 실질적인 언어를 직접 지시하는 분자는 바로 mRNA인거구요.
UŞ: Yeah, absolutely, it is possible. So the human cells, exactly, DNA is like a library. If you have the platform for the messenger RNA therapy, you can deliver any type of message and the body cells ensure that the message is translated into the right protein.
사힌: 네, 맞습니다. 인간 세포에서 DNA는 말씀하신대로 도서관 같은 거예요. 메신저 RNA 요법을 위한 플랫폼이 있다면, 우리는 어떤 메시지도 전달할 수 있고 체세포들은 이 메시지가 알맞는 단백질로 정확하게 번역될 수 있도록 하죠.
ÖT: A high advantage of mRNA is that it is so versatile. You can deliver all sorts of messages, as Uğur has called them. On the one hand, you can deliver the blueprint for the protein which you want to be produced in this cell. But you can, with the same molecule, also design into the mRNA instructions how this protein should be built, instructions to the protein factories of the cell. So you can define whether you want this protein to be built in high amounts or for a long duration, how the pharmacokinetics of this protein should be in the cell.
튀레지: mRNA의 큰 장점은 다재다능하다는 점이에요. 우구르가 말한 것처럼 어떤 메시지든 전달할 수 있는 한편, 다른 한편으로는 어떤 세포 안에서 만들고 싶은 단백질의 설계도를 전달할 수도 있는 거에요. 또는, 그 똑같은 분자로 mRNA를 설계해서 그 단백질이 어떻게 만들어지는지 설명서를 넣으면 세포의 단백질 공장에 전달할 수도 있어요. 그러니까 정의하는 것에 따라 그 단백질이 많이 만들어지도록 하거나, 오랫동안 만들어지도록 하거나, 단백질의 약물동력학 등을 결정할 수 있어요.
CA: So talk about January of last year when you first heard about this new virus that was spreading.
크리스: 그럼 작년 1월에 이 새로운 바이러스의 출현을 처음 들었을 당시에 어떠셨나요?
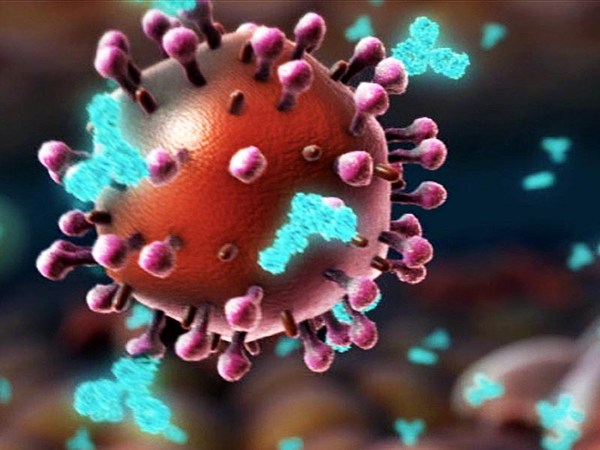
UŞ: So in the end of January, we read a paper published about this outbreak in Wuhan, and realized that this new outbreak has all features to become a global pandemic, and we were concerned that our life will change, that this outbreak could change the fate of mankind. And we knew that we have this messenger RNA technology, which was actually developed for personalized cancer therapy. But the idea of personalized cancer therapy is to get the genetic information of the patient and then make a vaccine as fast as possible. And we had now the same situation. It was not a personalized vaccine, but it was a genetic information of the virus, which was released two weeks earlier. And so this genetic information of this virus was available, and our task was to make a vaccine as fast as possible. And the challenge at that time point was, there was almost nothing known about this virus. It was a completely new virus. We had some assumptions which target which molecule encoded by the virus could be the right target. That means the molecule which can be used to precisely engineer an immune attack. This is the spike protein. It is on the surface of the virus. And there's not only one copy of the spike protein on the virus, but multiple in the range of 20, 25, 30 spike proteins. And the spike protein has two functions. One function is really to enable that the virus sticks to human cells. For example, it sticks to cells in the human lung. And the second is that the spike protein acts as a key. It allows the virus to enter into the cells. Our goal was to engineer an immune response.
사힌: 저희는 작년 1월 말에 중국 우한에서의 발발을 다룬 논문을 읽었어요. 이 새로운 바이러스가 세계적인 유행병이 될 모든 요소가 있음을, 그리고 우리의 삶이 바뀌고, 나아가 인류의 운명을 바꿀지도 모르겠다고 생각했어요. 우리는 그때 메신저 RNA 기술을 이미 갖고 있었어요. 사실 맞춤형 암 치료를 위해 개발된 것이었죠. 맟춤형 암 치료는 환자로부터 유전정보를 받아서 최대한 빠르게 백신을 만드는 기술이었고요. 그런데 비슷한 상황이었던 거죠. 다만 이번에는 맞춤형 백신이 아니라, 바이러스 유전정보가 대상이었죠. 그 정보는 2주 전에 공개되었고요. 이 유전정보가 있었기 때문에 저희는 최대한 빠르게 백신 개발에 힘쓸 수 있었죠. 이제 문제는, 바이러스에 대한 정보가 거의 없다는 거였죠. 완전히 새로운 바이러스였거든요. 그래도 바이러스가 합성하는 분자 중 어떤 분자를 목표로 삼아야 하는지는 추측을 해볼 수 있었어요. 그래서 면역체계가 그 분자에 공격을 가할 수 있도록 정밀히 설계한거죠. 여기 보이는 건 스파이크 단백질인데요. 바이러스 표면의 막 단백질이죠. 스파이크 단백질은 바이러스에 한 개만 있는 게 아니라, 20, 25, 30, 40개 정도로 여러 개가 있습니다. 스파이크 단백질에는 두 가지 기능이 있어요. 하나는 바이러스가 인간 세포와 결합하게 하는 거예요. 예를 들어서 폐 속 세포에 결합할 수 있겠죠. 두 번째 기능은 이 스파이크 단백질이 열쇠의 역할을 하는 거예요. 바이러스가 세포 안으로 진입할 수 있게 하죠. 저희의 목표는 면역반응을 설계하는 거였어요.
CA: You've got a slide showing the T-cell response to your vaccine. How long were you into the process before you saw this and you saw, wow, there really is a spectacular response going on here?
크리스: 아까 박사님들 백신의 T세포에 대한 반응을 봤는데요. 연구가 얼마나 진행됐을 때 이런 놀라운 반응이 일어나는 걸 확인하신 건가요?
ÖT: We saw this already in the animal models because they are also meant to assess the immune response. And what is shown on this slide is on the left side, a lymph node from a setting where there was no RNA treatment or RNA vaccination. And on the right side, a lymph node of a treated organism, in this case, an animal. And the localization matters. And we have constructed our RNA nanoparticles, with encapsulation into lipids such that the mRNA is carried into lymph nodes, not just anywhere, it's carried into lymph nodes and in the lymph nodes it reaches a very special cell type, which is called dendritic cells, and these cells are coaches of the immune system. So they are the generals which call all the different special forces and train them on the wanted poster of attacker. And it's very important that you reach those cells. On the right side, you can see the effect of reaching those cells. You see many red dots. And these are T-cells which have been trained to recognize the antigen, the protein which mRNA has delivered, and they have expanded to a sort of army of clones, so to say. So all these red dots are an army which only knows one goal, namely attacking this specific protein encoded by the mRNA.
튀레지: 저희는 이 반응을 이미 동물 모델에서 확인했었어요. 동물 실험에서도 면역반응을 확인해야 했거든요. 그리고 여기 보시면 왼쪽에 있는 게 림프절인데요. RNA 처치나 RNA 백신을 하지 않았을 때의 모습이죠. 그리고 오른쪽의 사진이 RNA처치가 된 개체의 림프절이고요. 이 사진은 동물에서의 반응입니다. 이제 그 RNA의 이동 위치가 중요하죠. 저희가 제작한 RNA 나노입자들은 지질에 둘러쌓여 있어 mRNA가 림프절로 이동하게 합니다. 아무 곳이나 가는 게 아니라 딱 림프절로 가는 거에요. 그래서 도착한 림프절에서는 수지상 세포라고 하는 굉장히 특별한 세포와 만나요. 수지상 세포들은 면역체계를 관리하는 사령관인데요. 다양한 특수부대 물질들을 불러모아서 침입자의 특성에 맞춘 훈련을 시킵니다. 그래서 RNA 나노 입자가 이 수지상 세포와 만나야 하죠. 오른쪽 사진이 수지상 세포와 만났을 때입니다. 빨간 점들이 많이 보이죠. 이 점들은 T세포인데요. mRNA가 전달한 단백질, 즉 항원을 인지하도록 훈련됐어요. 보시다시피 복제를 해서 T세포 군단을 만들었죠. 이제 이 빨간 점으로 보이는 군단은 오직 한 가지 목표만 가집니다. mRNA로 만들어진 특정 단백질을 인지하고 공격하는거죠.
CA: So it's really stunning that within just a few days of your looking at this sequence of the most dangerous pathogen to hit humanity in 100 years, I guess, that you were able to come up with these these candidate vaccines. And I guess over the course of the next weeks and months, you had growing confidence that, wow, this was going to work. It wasn't until the results of the human trials came out, I guess in November of last year, that you really knew. Tell us about that moment.
크리스: 정말 놀라운 것은, 단 며칠 만에 유전자 서열의 분석을 마쳤다는 것인데요. 그것도 최근 100년 간 가장 강력한 병원체의 DNA 서열을 분석해서 이런 백신 후보들을 만드신 거잖아요. 그 뒤로 몇 주, 몇 달 간은 이 백신들이 효과가 있을 거라는 기대가 컸을 거 같은데요. 그리고 작년 11월쯤에 인체실험 결과가 나왔을 때 결과를 확신할 수 있었잖아요. 이때 어떤 심정이셨나요?
ÖT: It was a Sunday when we were waiting for these results, which are assessed in such trials by an independent committee and Uğur said, "So let's see how the data will look like." It was not clear whether it would be a thumbs up or down. And we were very relieved. And I felt blessed to hear that the vaccine was efficacious and it was highly efficacious, over 90 percent.
튀레지: 그 날이 일요일이었어요. 위원회에서 실험결과들을 검정하고 저희는 그 결과들을 기다리고 있었죠. 우구르는 결과가 어떤지 확인이나 해보자고 했어요. 사실 그 전까지는 성공인지 실패인지 불확실했거든요. 그래서 정말 안도했고, 축복 받은 기분이었죠. 백신이 효과가 있고, 90% 이상의 높은 효과를 보였다는 소식을 들었을 때요.
CA: And that more than 90 percent almost disguises the full extent, because that's just against any kind of level of infection of COVID. Severe infection and fatalities were almost completely protected against, I think. And it must have been an ecstatic moment for you. Certainly was for so many people around the world.
크리스: 사실 90% 이상이면 완벽한 거나 마찬가지잖아요. 웬만한 코로나 감염 수치를 뛰어넘으니까요. 심각한 감염이나 치사율은 거의 완벽하게 예방한 것 같아요. 황홀한 순간이었을 것 같네요. 박사님들은 물론, 전세계 사람들에게도 말이에요.
UŞ: Yes, absolutely. So this was a Sunday evening, and there were a handful of people knowing that an effective vaccine is existing against this global pandemic. And we were so excited and so happy and we shared of course this information the next day.
사힌: 정말 그랬죠. 그 일요일 오후에, 몇몇 사람들은 알게 된 거죠. 이 팬데믹에 대한 효과적인 백신이 드디어 존재한다는 것을요. 저희는 정말 신나고 행복해서 다음 날 이 소식을 열심히 공유했어요.
CA: So based on what's happened this time around and the amazing acceleration, compared with any other vaccine development, I mean, if we were hit by another virus, could you picture that next time we could accelerate the time line further still if need be?
크리스: 요즘의 상황으로 감히 예상해보건대, 다른 어떤 백신 개발보다도 신속했던 이번의 엄청난 발전이 우리가 또 한번 다른 팬데믹을 맞이해도 그땐 더더욱 신속하게 대응할 수 있게 될까요?
UŞ: Yes, Chris, this is an excellent question. Actually, the world was not prepared to deal with such a pandemic. The science and the vaccine developers reacted in an excellent fashion. And it is incredible and wonderful that it was possible to come up with an effective vaccine while a pandemic is ongoing, in less than 12 months. But the challenges that we have at the moment is that we don't have sufficient production capacity. Ideally, we would be prepared the next time, not only to develop a vaccine in light speed, but also to to make and distribute the vaccine in light speed. So what we need now is an additional element which was not existing, is manufacturing capacity. And idle manufacturing capacity. We must be bringing us into a position that we can produce 12 billion doses of vaccine, if you consider prime boost, within less than six months. And this is technically possible. So this can be done if governments and international organizations invest into manufacturing capacity, invest into keeping this idle capacity, and also come up with a standard time span and process to enable even faster response. So we in principle, we might be able to manage to come up with a vaccine and start distribution in even less than eight months.
사힌: 훌륭한 질문이에요, 크리스. 솔직히 말하면 이런 팬데믹이 덮칠지 아무도 예상하지 못했었죠. 그럼에도 과학기술과 백신 개발자들은 정말 훌륭하게 대처해주었어요. 믿기지 않을 정도로 대단한 건 팬데믹이 진행되는 상황에서도 단 12개월 만에 효과적인 백신을 개발될 수 있었다는 거예요. 현재로서 넘어야 할 산은 부족한 생산능력을 보완하는 거예요. 저는 미래에 우리가 비슷한 상황에 처한다면 빠르게 백신을 개발하는 것뿐 아니라 그 백신의 생산과 유통까지도 신속하게 처리되길 희망합니다. 그러니까 이제 꼭 필요한 건 백신의 생산력이에요. 여유로운 생산력이요. 앞으로 우리는 120억 백신을 확실한 초기 대응까지 고려한다면 6개월 안에 생산할 수 있어야 해요. 이게 현재 기술로 가능합니다. 이제 세계의 정부들과 국제기구들이 생산력에 더 투자하고 이런 생산력을 유지하는 데 도움을 주면 됩니다. 생산 기간과 절차에 대한 기준도 마련해서 더 신속하게 대처할 수 있어야 하죠. 이렇게 된다면 이론적으로 백신개발은 물론 유통까지 모든 관리가 8개월 이내에 이루어질 수 있을 겁니다.
CA: What does what's happened in this last year tell you now about the prospects for using mRNA to treat cancer and indeed other diseases? Where is this heading?
크리스: 작년의 사건들을 바탕으로 전망이 바뀌었을까요? mRNA를 이용한 암이나 다른 질병들의 치료가 앞으로 어떻게 발전할까요?
UŞ: What we have now is now an approved technology and a first approved product. The development of the coronavirus mRNA vaccine shows the power of the mRNA and it shows also the safety of this approach. And it shows that it opens up a door for new technology and for new type of treatments. And the mRNA molecules that we are currently using for cancer, we have more than 10 products now in clinical development, are diverse against different types of cancer. We are very confident that the success that we have generated now for our infectious disease vaccines can be continued with our cancer immunotherapies.
사힌: 이제 우리는 입증된 기술과 첫 승인이 된 약품을 갖고 있어요. 코로나 바이러스에 대한 mRNA 백신의 개발은 mRNA의 위력을 보여주고, 이 기술의 안전성까지 보여주었어요. 이 백신으로써 우리는 새로운 문을 열게 되었습니다. 새로운 기술과 치료제의 새 장을 열게 된 것이죠. 그리고 암치료에 사용되는 mRNA 분자들로는 현재 10가지 이상의 약품이 임상 개발 중에 있어요. 그만큼 다양한 종류의 암에 맞설 수 있겠죠. 저는 앞으로 성공을 확신합니다. 이번 감염병 백신 개발로 일궈 낸 현재의 결실은 암 면역요법의 발전까지 이어지게 될 것입니다.
CA: Some people may hear this and say this is just another type of drug that's coming along. But I think on the mental model you're talking about, we should think about it as much more revolutionary than that, that typically a drug, a traditional drug, kind of changes the chemical environment, the background of an entire area of the body. But your -- If you understand the language of mRNA, you can do something much more specific and precise. Is that something like a fair way to think about it?
크리스: 이걸 보고 있는 몇몇 분들은 그저 새로운 약이 하나 더 나왔나보다라고 할 수 있잖아요. 그런데 박사님의 전망대로라면 생각보다 더 큰 혁명이라고 봐야겠어요. 기존의 약물은 화학적인 환경이나 신체의 환경을 바꾸는 거라고 한다면 박사님들의- 그러니까 mRNA의 언어를 이해할 수 있다면, 기존보다 훨씬 구체적이고 정교하게 작업할 수 있는거죠?
ÖT: Yes, indeed. It could be the next revolution in the biopharm landscape.
튀레지: 네, 그럼요. mRNA 기술은 의약계에서 하나의 혁명을 불러 올 수도 있습니다.
UŞ: At the end of the day, disease is a situation where the communication between cells is disturbed. So, for example, autoimmune disease is a disease condition where immune cells attack normal cells. And indeed, we could engineer messenger RNA therapies which could teach the immune system to stop to do that, without inhibiting the whole immune system, by just communicating with the immune cells which are attacking. We could be precise and more specific.
사힌: 질병은 결국 세포 사이의 의사소통을 방해하는 거에요. 예를 들어서, 자기 면역 질환의 경우 신체 내의 면역세포가 정상세포를 공격하는 오류가 생기죠. 그렇지만 우리는 mRNA요법을 설계함으로써 잘못된 공격을 멈추라고 면역 체계에게 가르칠 수 있어요. 면역 체계 전체를 억제하지 않고 면역 세포들과 소통해서 말이죠. 훨신 정교하고 구체적으로 접근할 수 있습니다.
CA: The success of BioNTech over the last couple of years, I think the value of the company has rocketed because of the amazingness of what's happened. I mean, it's made you both extremely wealthy, I think you're both billionaires now. How have you been able to respond to that? Sometimes so much money brings its own problems with it. Is that proving a distraction?
크리스: 최근 몇 년 바이오엔테크에서는 정말 놀라운 일들을 해내셨잖아요. 회사의 가치가 크게 높아졌을 것 같은데요. 솔직히 두 분이 이제 돈방석에 오르시지 않았나 싶은데 억만장자라고 해도 되겠어요. 이런 변화를 어떻게 받아들이셨나요. 가끔은 너무 큰 돈이 더 골칫거리일 떄도 있잖아요. 혹시 연구에 방해가 된다거나 하나요?
ÖT: For a company which sees innovation as its core mission, too much money is never a problem. Because innovation really means that you have to invest. Otherwise, we will only have two type of products or incremental improvement for solutions of high medical need.
튀레지: 기업에게 있어서 기발한 아이디어와 혁신이 핵심 목표인 이상 큰 돈이 절대 문제될 리 없죠. (웃음) 혁신이야말로 많은 투자가 필요하니까요. 그렇지 않으면 제품 개발이나 의료적 필요에 대한 해결안을 발전시키는 데 한계가 생길 거예요.
UŞ: It really gives us the chance to transform our company. So we were when we started -- When we compare ourselves with the situation we had at the beginning of 2020, we had a number of product candidates in clinical testing, but the company required funding every year or every second year. Now we have a situation to really address the full vision of the company. We started BioNTech with the idea really to provide novel treatments wherever there is a high unmet medical need. And we now can do that in a much larger and broader scale, and bring our innovations faster to patients.
사힌: 자금은 저희 기업을 변화, 성장시킬 기회를 주죠. 저희가 회사를 막 시작했을 때인 2020년 초반의 상황과 비교한다면 임상실험에 들어갈 제품 후보군들은 몇 가지 있었지만 그 해에 사용할 자금을 구하기 바빴어요. 이제는 기업의 큰 비젼을 생각할 여유가 생긴 거죠. 바이오엔테크를 설립할 때의 생각은 새로운 치료제를 제공하자는 게 목표였습니다. 의료 도움이 필요한 곳은 어디라도 말이죠. 이제는 훨씬 더 많은 곳에 더 큰 도움을 줄 수 있게 되었고, 저희의 혁신을 환자들에게 더 신속하게 제공할 수 있어요.
CA: You are both from families who immigrated from Turkey to Germany. Immigrants have faced hard times in many countries, including Germany. And yet you, I think, have helped transform the debate about immigration, in Germany and elsewhere, just by the extraordinary success that you've achieved creating this world-leading company in Germany. Do you take joy for the impact you may have had on this issue?
크리스: 두 분 모두 터키에서 독일로 이민하셨다고 알고 있는데, 독일을 포함한 많은 국가에서 이민자들의 삶이 쉽지만은 않았잖아요. 하지만 이제 두분은 두 분이 이뤄내신 놀라운 성공으로 독일이든 어디든, 이민에 대한 편견을 많이 없앴다는 생각이 들어요. 세계를 이끄는 기업을 독일에 설립하셨으니까요. 두 분이 이민 문제에 주신 좋은 영향을 어떻게 생각하시나요?
UŞ: It is somehow surprising because the way how we do science, and how we recognize how people work effectively in teams together is not to us from where the person is coming, but what the person can contribute. So in our company, we have employees from more than 60 countries. So we are an international group of scientists, as any other research institution. So we have to recognize that globalization really helps to bring people, scientists or other engineers into one place, allowing to work together and to come with extraordinary results. For us, this is somehow surprising that this is seen as special. It is just the way how excellent research and science work.
사힌: 사실 놀라운 점은 저희가 과학을 다루는 방식, 그리고 팀으로서 협력하는 사람들을 이해하는 방식은 그 사람이 어디서 왔느냐가 아니라 그 사람이 어떤 기여를 할 수 있느냐에 있습니다. 그래서 저희 회사의 직원들은 60개 이상의 국가에서 모인 국제적인 과학자 모임이에요. 다른 연구기관들과 마찬가지로요. 결국 중요한 건 세계화를 통해 사람들, 과학자들과 공학자들이 한데 모여 같이 일하고, 엄청난 결과를 얻어낸다는 거예요. 사실 과학을 하는 저희에게 이건 익숙하고 당연한 일인 것 같아요. 훌륭한 연구와 과학이란 그런 거거든요.
CA: Well, it's extraordinary and inspiring what you've achieved, and it'll be very exciting to track progress over the coming years. Thank you so much. Thank you.
크리스: 그래도 두 분의 업적은 정말 놀라운 일이에요. 미래의 과학자들에게도 가슴뛰는 일임에 분명하겠죠. 오늘 함께 해주셔서 정말 감사드립니다.