Chris Anderson: Dr. Şahin and Dr. Türeci, welcome. Such a treat to speak with you.
Chris Anderson : Dr. Şahin et Dr. Türeci, bienvenue. C’est un plaisir de discuter avec vous.
Özlem Türeci: Thank you very much, Chris. It's a pleasure to be here.
Özlem Türeci : Merci beaucoup, Chris. C’est un plaisir d’être là.
CA: So tell me, as you think back over the last 18 months, what words pop to mind for you?
CA : Alors dites-moi, quand vous repensez à ces 18 derniers mois, quels mots vous viennent à l’esprit ?
ÖT: Well, one word which comes to mind is breathless. It was indeed a breathless 16, 17 months for us. When we started in January last year, it was already at that time clear to us that we were already in a pandemic. What was not known was how fast this pandemic would evolve and whether we would have the time in the first place to have a vaccine ready soon enough in due time. And understanding this, it meant for us that there was not even one day to lose. And this was the mindset of the entire team here in Mainz and at BioNTech and later on also of our partners which were involved, Pfizer and others, to keep going and be fast.
ÖT : Ce qui me vient à l’esprit, c’est « à couper le souffle ». Nous avons en effet vécu seize ou 17 mois à couper le souffle. Lorsque nous avons commencé en janvier de l’année dernière, c’était déjà clair pour nous dès ce moment que nous affrontions une pandémie. Ce que nous ne savions pas, c’était à quelle vitesse cette pandémie évoluerait et si nous aurions le temps d’avoir un vaccin prêt en temps voulu. Et comprendre ça, cela voulait dire pour nous qu’il n’y avait pas un seul jour à perdre. Et c’était l’état d’esprit de toute l’équipe ici à Mayence et à BioNTech, et plus tard aussi chez nos partenaires, Pfizer et les autres, de persévérer et d’être rapide.
CA: I mean, it's so extraordinary that the ideas and the work in your minds have now impacted hundreds of millions, perhaps billions of people. That must feel overwhelming. And yet, I know at the same time, you don't believe in this notion of a flash-in-the-pan ideas. Steven Johnson, the author, in his book "Where [Good] Ideas Come From," speaks of the slow hunch, that the best ideas happen over many years. And I know that you believe that is true in your case. I'd like us to go back a couple of decades to -- tell us how this began. How did you meet?
CA : C’est extraordinaire que vos idées et le fruit de vos recherches aient aujourd’hui un impact sur des centaines de millions, voire des milliards de personnes. Cela doit être extraordinaire. Pourtant, je sais qu’en même temps, vous ne croyez pas à la notion d’idées miracles. Dans son livre « Where Good Ideas Come From », l’écrivain Steven Johnson parle de l’intuition lente, que les meilleures idées arrivent sur des années. Je sais que vous pensez que c’est votre cas. J’aimerais revenir quelques années en arrière pour savoir comment tout a débuté, sur votre rencontre.
ÖT: We met on an oncohematology ward, Uğur being a young physician, and I was still in medical school training on ward. Which means we met in one of the worlds which became important to us, the world of patient care, of treating oncohematology patients. And we soon found out that there was a second world which we liked, namely the world of science. We were haunted by the same dilemma, namely that whereas there was not much we could offer our cancer patients, there were so many potential technologies we encountered in the lab which could address this. So one of our shared visions was to bridge this dilemma by working on bringing science and technology fast. And that's an important word here. Fast to the patient's bedside to address high medical need.
ÖT : Nous nous sommes rencontrés dans un service d’oncohématologie, Uğur était un jeune médecin et moi j’étais encore en formation à l’école de médecine dans ce service. Nous nous sommes donc rencontrés dans un univers qui est devenu important pour nous, le monde des soins aux patients, du traitement des patients en oncohématologie. Nous avons rapidement découvert qu’un deuxième univers nous plaisait, à savoir le monde de la science. Nous étions hantés par le même dilemme : alors qu’il y avait peu de choses à offrir à nos patients atteints de cancer, on découvrait en laboratoire beaucoup de technologies potentielles pour y remédier. L’une de nos ambitions communes, c’était de résoudre ce dilemme en faisant avancer la science et la technologie rapidement. Et c’est un mot important ici. Rapidement au chevet du patient pour répondre à un besoin médical urgent.
CA: So I think the first company you founded nearly 20 years ago was to use the power of the human immune system to tackle cancer.
CA : Je crois que la première entreprise que vous avez fondée il y a près de 20 ans avait pour but d’utiliser la puissance du système immunitaire humain pour lutter contre le cancer.
Uğur Şahin: We were always interested in using the patient's immune system
Uğur Şahin : Nous avons toujours été intéressés
to fight cancer and other type of diseases. As immunologists, we knew how powerful the human immune system is. But it was also clear that the human immune system, in the case of cancer, did not fight cancer cells. It could fight it, but it didn't. And for that, we wanted to develop immunotherapies. That means treatments that use the power of the immune system and redirect the power of the immune system to cancer cells. It was clear that in the university setting, we could not continue to develop monoclonal antibodies because the cost for development of monoclonal antibodies before you can start a clinical trial, was in the range of 20, 30 million euros, and therefore we decided to start a company to get the funding.
par l’utilisation du système immunitaire du patient pour combattre le cancer et d’autres types de maladies. En tant qu’immunologistes, nous savions à quel point le système immunitaire humain est puissant. Mais il était également clair que le système immunitaire humain, dans le cas du cancer, ne combattait pas les cellules cancéreuses. Il pouvait les combattre, mais il ne le faisait pas. Et face à cela, nous avons voulu développer des immunothérapies. C’est-à-dire des traitements qui utilisent le pouvoir du système immunitaire et le redirigent vers les cellules cancéreuses. Il est apparu clairement que, dans le cadre académique, nous ne pouvions pas continuer à développer des anticorps monoclonaux, car le coût du développement d’un anticorps monoclonal avant de pouvoir commencer un essai clinique était de l’ordre de 20 à 30 millions d’euros. Nous avons donc créé une entreprise pour obtenir le financement.
CA: Now, soon after you started this company, you decided to get married. Tell me about your wedding day.
CA : Peu après avoir créé cette entreprise, vous avez décidé de vous marier. Racontez-moi le jour de votre mariage.
ÖT: Day was well planned, a quick wedding. And thereafter we went back to the laboratory and our guests at our wedding, that was basically our team, our research team. So no time to lose, Chris.
ÖT : La journée était bien préparée, un mariage rapide. Tout de suite après, nous sommes retournés au laboratoire. Les invités à notre mariage étaient essentiellement notre équipe, notre équipe de recherche. Donc pas de temps à perdre, Chris.
CA: (Laughs) That was a pretty special honeymoon. I mean, it seems like your love for each other is very much bound up in your love for this work and your sense of the importance of this work. How would you characterize those intersecting relationships there?
CA : (Rires) C’est une lune de miel assez spéciale. On dirait que votre amour pour l’autre est très lié à votre amour pour ce travail et votre conception de l’importance de ce travail. Comment décririez-vous ces relations croisées ?
UŞ: We are really two scientists. At the end of the day, we love what we do, and for us, we don't differentiate between work and life balance. It's for us really a privilege to be scientists, to be able to do what we love. And therefore, we combine our normal life with our professional life. And therefore, this is pretty normal for us.
UŞ : Nous sommes vraiment deux scientifiques. Au fond, nous aimons ce que nous faisons, et pour nous, il n’y a pas de différence dans l’équilibre entre travail et vie privée. C’est pour nous un véritable privilège d’être des scientifiques, de pouvoir faire ce que nous aimons. Nous concilions donc notre vie ordinaire avec notre vie professionnelle. Et par conséquent, c’est plutôt normal pour nous.
CA: So talk to me about this extraordinary molecule RNA, and how you got interested in it and how it became, as I understand it, an increasing focus of your work. And indeed, it led to the founding of BioNTech. Talk about that.
CA : Parlez-moi de cette extraordinaire molécule qu’est l’ARN, comment vous vous êtes intéressés à elle et comment elle est devenue visiblement un point central de votre travail. Et bien sûr, elle a mené à la création de BioNTech. Parlez-nous de cela.
UŞ: Yeah, mRNA is a natural molecule, it's one of the first molecules of life. It is a carrier of genetic information. But in contrast to DNA, it's not stable. So it can be used to transfer information to human cells. And the human cells can use this information to build proteins, which can be used for therapeutic settings, for example, to make a protein which is a vaccine, or to make a protein which is an antibody, or to make a protein which is another type of drug. And we were fascinated by this molecule class, because it was very clear that mRNA can be produced pretty fast, within a few days. And we were, as MDs, we were particularly interested to develop personalized medicines. That means a treatment and immunotherapy specifically designed for a cancer patient, because one of the key challenges in cancer treatment, is that every patient has a different tumor. If you compare two tumors of two patients with the same type of tumor, the similarity of the tumors is less than three percent and 97 percent is really unique. And today, it's still not possible to address the uniqueness of the tumor of a patient. And therefore, we were seeking for a technology which could be used for immunotherapy and which could be used to develop a treatment within the shortest possible time. The idea to get the genetic sequence of the tumor and then make a vaccine which is personalized, within a few weeks.
UŞ : L’ARN messager est une molécule naturelle, c’est l’une des premières molécules de la vie. C’est un support de l’information génétique. Mais contrairement à l’ADN, elle n’est pas stable. Elle peut être utilisée pour transférer des informations aux cellules humaines. Les cellules humaines utilisent cette information pour fabriquer des protéines, qui peuvent être utilisées à des fins thérapeutiques, par exemple pour fabriquer une protéine qui sert de vaccin, une protéine qui sert d’anticorps ou une protéine qui est un autre type de médicament. Nous avons été fascinés par cette classe de molécules, car il était évident que l’ARNm pouvait être produit assez rapidement, en quelques jours. Et en tant que médecins, nous étions très intéressés de développer des médicaments personnalisés. C’est-à-dire un traitement et une immunothérapie spécifiquement conçus pour un patient cancéreux, car l’un des principaux défis du traitement du cancer, c’est que chaque patient a une tumeur différente. Si vous comparez deux tumeurs de deux patients ayant le même type de tumeur, la similitude des tumeurs est inférieure à 3 % et 97 % de ces tumeurs est très spécifique. Aujourd’hui, il n’est toujours pas possible de tenir compte du caractère spécifique de la tumeur d’un patient. Et par conséquent, nous avons cherché une technologie utilisable pour l’immunothérapie et qui puisse être employée pour développer un traitement dans les plus brefs délais. Dans l’idée, en obtenant la séquence génétique de la tumeur pour ensuite faire un vaccin sur mesure, en quelques semaines.
CA: Is it fair to say that almost all of the significant things that happen to us biologically are actions done by proteins, and that it's mRNA that actually makes those proteins? If you can understand the language of mRNA, you can get involved in pretty much everything of significance to the well-being of a human being.
CA : Est-il juste de dire que presque toutes les choses importantes qui nous arrivent sur le plan biologique sont générées par des protéines et que c’est l’ARN messager qui fabrique ces protéines ? Si vous pouvez comprendre le langage de l’ARN messager, vous pouvez vous occuper d’à peu près tout ce qui est important pour le bien-être d’un humain.
ÖT: Exactly. So in principle, the information instructions are in the DNA. These have to be translated into protein because proteins are the actors which keep our cells alive and our organism functional. And the way how to translate what is instructed by DNA in a fashion that it is well-timed and happens at the right places, into protein, there is messenger RNA. Messenger RNA sort of instructs when and how much of which protein has to be built in order to ensure the activity of our body.
ÖT : Exactement. Donc, en principe, les directives des informations se trouvent dans l’ADN. Elles doivent être traduites en protéines car les protéines sont les acteurs qui maintiennent nos cellules en vie et notre organisme fonctionnel. Et pour traduire ce qui est indiqué par l’ADN de façon à ce que ce soit bien programmé et que cela se produise aux bons endroits, grâce aux protéines, il y a l’ARN messager. L’ARN messager indique en quelque sorte quand et quelle quantité de quelle protéine doit être construite afin d’assurer le bon fonctionnement de notre corps.
CA: So you can almost think of DNA as the sort of The Oxford English Dictionary of Language. It sort of sits there as the reference point. But for the actual living work, the living work of language out there in the world instructing things, that is done by mRNA.
CA : Donc on peut presque voir l’ADN comme une sorte de dictionnaire. Il se tient là comme un point de référence. Mais le vrai travail actif, le travail actif de traduction en dehors, pour expliquer les choses, c’est l’ARN messager qui le fait.
UŞ: Yeah, absolutely, it is possible. So the human cells, exactly, DNA is like a library. If you have the platform for the messenger RNA therapy, you can deliver any type of message and the body cells ensure that the message is translated into the right protein.
UŞ : Oui, absolument, c’est possible. Donc les cellules humaines, l’ADN en particulier est comme une bibliothèque. Si vous avez le support pour une thérapie par ARN messager, vous pouvez envoyer n’importe quel type de message et les cellules du corps s’assurent que le message soit traduit dans la bonne protéine.
ÖT: A high advantage of mRNA is that it is so versatile. You can deliver all sorts of messages, as Uğur has called them. On the one hand, you can deliver the blueprint for the protein which you want to be produced in this cell. But you can, with the same molecule, also design into the mRNA instructions how this protein should be built, instructions to the protein factories of the cell. So you can define whether you want this protein to be built in high amounts or for a long duration, how the pharmacokinetics of this protein should be in the cell.
ÖT : Un grand avantage de l’ARN messager, c’est qu’il est tellement polyvalent. On peut envoyer toutes sortes de messages, comme Uğur les a appelés. D’une part, on peut envoyer le schéma de la protéine qu’on veut voir produite dans cette cellule. Mais on peut, avec la même molécule, concevoir également dans l’ARN messager des instructions sur la façon dont cette protéine doit être fabriquée, des instructions destinées aux usines de protéines de la cellule. Ainsi, on peut définir si on veut que cette protéine soit produite en grandes quantités ou pendant une longue durée, comment la pharmacocinétique de cette protéine doit agir dans la cellule.
CA: So talk about January of last year when you first heard about this new virus that was spreading.
CA : Parlez-nous de janvier 2020 quand vous avez entendu parler pour la première fois de ce nouveau virus qui se propageait.
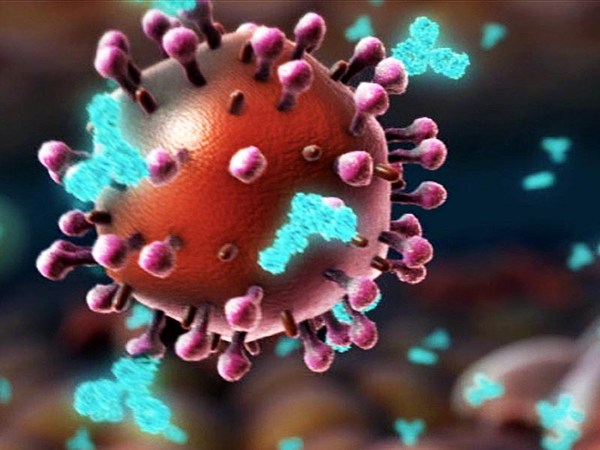
UŞ: So in the end of January, we read a paper published about this outbreak in Wuhan, and realized that this new outbreak has all features to become a global pandemic, and we were concerned that our life will change, that this outbreak could change the fate of mankind. And we knew that we have this messenger RNA technology, which was actually developed for personalized cancer therapy. But the idea of personalized cancer therapy is to get the genetic information of the patient and then make a vaccine as fast as possible. And we had now the same situation. It was not a personalized vaccine, but it was a genetic information of the virus, which was released two weeks earlier. And so this genetic information of this virus was available, and our task was to make a vaccine as fast as possible. And the challenge at that time point was, there was almost nothing known about this virus. It was a completely new virus. We had some assumptions which target which molecule encoded by the virus could be the right target. That means the molecule which can be used to precisely engineer an immune attack. This is the spike protein. It is on the surface of the virus. And there's not only one copy of the spike protein on the virus, but multiple in the range of 20, 25, 30 spike proteins. And the spike protein has two functions. One function is really to enable that the virus sticks to human cells. For example, it sticks to cells in the human lung. And the second is that the spike protein acts as a key. It allows the virus to enter into the cells. Our goal was to engineer an immune response.
UŞ : Fin janvier, nous avons lu un article sur cette épidémie à Wuhan et nous avons compris que cette nouvelle épidémie avait toutes les chances de devenir une pandémie mondiale. Nous étions inquiets que notre vie change, que cette épidémie puisse changer le destin de l’humanité. Nous savions que nous disposions de cette technologie de l’ARN messager, qui avait en réalité été développée pour la thérapie personnalisée du cancer. Le principe de cette thérapie, c’est d’obtenir les informations génétiques du patient, puis de fabriquer un vaccin aussi vite que possible. Nous étions dans la même situation. Il ne s’agissait pas d’un vaccin personnalisé, mais d’une information génétique sur un virus, qui avait été publiée deux semaines plus tôt. L’information génétique sur ce virus était disponible et notre tâche était de créer un vaccin aussi vite que possible. Le défi à ce moment-là, c’était qu’on ne connaissait presque rien sur ce virus. C’était un virus complètement nouveau. Nous avions quelques hypothèses sur quelle molécule codée par le virus pouvait être la bonne cible. C’est-à-dire la molécule à utiliser pour élaborer avec précision une attaque immunitaire. C’est le péplomère. Il se trouve à la surface du virus. Il n’y a pas qu’une seule copie de péplomère sur le virus, mais plusieurs, de l’ordre de 20, 25, 30 péplomères. Un péplomère a deux fonctions. La première est de permettre au virus de se fixer aux cellules humaines. Par exemple, il adhère aux cellules du poumon humain. Et la seconde, c’est qu’il agit comme une clé. Il permet au virus d’entrer dans les cellules. Notre objectif était de développer une réponse immunitaire.
CA: You've got a slide showing the T-cell response to your vaccine. How long were you into the process before you saw this and you saw, wow, there really is a spectacular response going on here?
CA : Une diapositive montre la réponse des lymphocytes T à votre vaccin. Combien de temps avez-vous effectué vos recherches avant de voir ça et de comprendre qu’il se produisait vraiment une réaction spectaculaire ?
ÖT: We saw this already in the animal models because they are also meant to assess the immune response. And what is shown on this slide is on the left side, a lymph node from a setting where there was no RNA treatment or RNA vaccination. And on the right side, a lymph node of a treated organism, in this case, an animal. And the localization matters. And we have constructed our RNA nanoparticles, with encapsulation into lipids such that the mRNA is carried into lymph nodes, not just anywhere, it's carried into lymph nodes and in the lymph nodes it reaches a very special cell type, which is called dendritic cells, and these cells are coaches of the immune system. So they are the generals which call all the different special forces and train them on the wanted poster of attacker. And it's very important that you reach those cells. On the right side, you can see the effect of reaching those cells. You see many red dots. And these are T-cells which have been trained to recognize the antigen, the protein which mRNA has delivered, and they have expanded to a sort of army of clones, so to say. So all these red dots are an army which only knows one goal, namely attacking this specific protein encoded by the mRNA.
ÖT : Nous l’avions déjà vu dans les modèles animaux car ils sont également destinés à évaluer la réponse immunitaire. On voit sur cette diapositive, à gauche, un ganglion lymphatique provenant d’un milieu où il n’y a pas eu de traitement ou de vaccination par ARN. Et à droite, c’est le ganglion lymphatique d’un organisme traité, en l’occurrence, un animal. La localisation est importante. Nous avons construit nos nanoparticules d’ARN en les encapsulant dans des lipides pour que l’ARN messager soit transporté dans les ganglions lymphatiques. Pas n’importe où, il est transporté dans les ganglions lymphatiques et dans ces ganglions, il atteint un type spécifique de cellules, qu’on appelle cellules dendritiques. Ces cellules sont les entraîneurs du système immunitaire. Ce sont les généraux qui appellent toutes les différentes forces spéciales et les entraînent à débusquer l’agresseur. Et c’est très important d’atteindre ces cellules. À droite, vous pouvez voir l’effet quand ces cellules sont atteintes. Vous voyez beaucoup de points rouges. Ce sont des lymphocytes T qui ont été entraînés à reconnaître l’antigène, la protéine que l’ARN messager a transmise, et ils se sont multipliés comme une sorte d’armée de clones, pour ainsi dire. Tous ces points rouges sont donc une armée qui ne connaît qu’un seul objectif, à savoir attaquer cette protéine spécifique codée par l’ARN messager.
CA: So it's really stunning that within just a few days of your looking at this sequence of the most dangerous pathogen to hit humanity in 100 years, I guess, that you were able to come up with these these candidate vaccines. And I guess over the course of the next weeks and months, you had growing confidence that, wow, this was going to work. It wasn't until the results of the human trials came out, I guess in November of last year, that you really knew. Tell us about that moment.
CA : C’est stupéfiant que quelques jours seulement après avoir examiné cette séquence de l’agent pathogène le plus dangereux pour l’humanité ces 100 dernières années, vous ayez été en mesure de proposer ces vaccins potentiels. J’imagine que dans les semaines et les mois qui ont suivi, vous aviez de plus en plus confiance que ça allait marcher. Ce n’est que lorsque les résultats des essais sur l’homme ont été publiés, en novembre de l’année dernière je crois, que vous avez su. Racontez-nous ce moment.
ÖT: It was a Sunday when we were waiting for these results, which are assessed in such trials by an independent committee and Uğur said, "So let's see how the data will look like." It was not clear whether it would be a thumbs up or down. And we were very relieved. And I felt blessed to hear that the vaccine was efficacious and it was highly efficacious, over 90 percent.
ÖT : C’était dimanche et nous attendions ces résultats, qui sont analysés dans ce type d’essais par un comité indépendant. Uğur a dit : « Voyons donc à quoi vont ressembler les données. » On ne savait pas si ce serait positif ou négatif. Et nous avons été très soulagés. Et j’ai été très heureuse d’apprendre que le vaccin était efficace et qu’il était très efficace, à plus de 90 %.
CA: And that more than 90 percent almost disguises the full extent, because that's just against any kind of level of infection of COVID. Severe infection and fatalities were almost completely protected against, I think. And it must have been an ecstatic moment for you. Certainly was for so many people around the world.
CA : Et plus de 90 % masque presque toute l’ampleur de la situation, parce que c’est contre n’importe quel niveau d’infection du COVID. Les infections sévères et les décès ont été presque entièrement couverts, je pense. Et ça a dû être un moment exaltant pour vous. Certainement pour beaucoup de gens dans le monde.
UŞ: Yes, absolutely. So this was a Sunday evening, and there were a handful of people knowing that an effective vaccine is existing against this global pandemic. And we were so excited and so happy and we shared of course this information the next day.
UŞ : Oui, absolument. C’était un dimanche soir et une poignée de gens savait qu’un vaccin efficace existait contre cette pandémie mondiale. Nous étions si enthousiastes et heureux que nous avons bien sûr partagé cette information le lendemain.
CA: So based on what's happened this time around and the amazing acceleration, compared with any other vaccine development, I mean, if we were hit by another virus, could you picture that next time we could accelerate the time line further still if need be?
CA : Donc, sur la base de ce qui s’est passé cette fois-ci et de cette incroyable accélération, par rapport à n’importe quel autre développement de vaccin, si nous étions frappés par un autre virus, imaginez-vous que la prochaine fois nous pourrions accélérer encore davantage si nécessaire ?
UŞ: Yes, Chris, this is an excellent question. Actually, the world was not prepared to deal with such a pandemic. The science and the vaccine developers reacted in an excellent fashion. And it is incredible and wonderful that it was possible to come up with an effective vaccine while a pandemic is ongoing, in less than 12 months. But the challenges that we have at the moment is that we don't have sufficient production capacity. Ideally, we would be prepared the next time, not only to develop a vaccine in light speed, but also to to make and distribute the vaccine in light speed. So what we need now is an additional element which was not existing, is manufacturing capacity. And idle manufacturing capacity. We must be bringing us into a position that we can produce 12 billion doses of vaccine, if you consider prime boost, within less than six months. And this is technically possible. So this can be done if governments and international organizations invest into manufacturing capacity, invest into keeping this idle capacity, and also come up with a standard time span and process to enable even faster response. So we in principle, we might be able to manage to come up with a vaccine and start distribution in even less than eight months.
UŞ : Oui, Chris, c’est une excellente question. En effet, le monde n’était pas préparé à affronter une telle pandémie. La science et les concepteurs de vaccins ont réagi de manière remarquable. Et c’est incroyable et merveilleux qu’il ait été possible de trouver un vaccin efficace, alors qu’une pandémie est en cours, en moins de douze mois. Mais le défi que nous avons en ce moment, c’est que nous n’avons pas de capacité de production suffisante. L’idéal serait que nous soyons prêts la prochaine fois, non seulement à développer un vaccin à la vitesse de la lumière, mais aussi à produire et distribuer ce vaccin à la vitesse de la lumière. Nous avons besoin aujourd’hui d’un élément supplémentaire qui n’existait pas : la capacité de production. Et une capacité de production inactive. Nous devons nous mettre dans la position où nous pouvons produire 12 milliards de doses de vaccin, en considérant le panachage des vaccins, en moins de six mois. Et c’est techniquement possible. Nous pouvons y arriver si les États et les organisations internationales investissent dans la capacité de production et dans le maintien de cette capacité inactive, tout en établissant un délai et un processus standard pour permettre une réponse encore plus rapide. Donc, en principe, nous pourrions arriver à mettre au point un vaccin et commencer la distribution en moins de huit mois.
CA: What does what's happened in this last year tell you now about the prospects for using mRNA to treat cancer and indeed other diseases? Where is this heading?
CA : Qu’est-ce que les événements de l’année dernière vous apprennent sur les perspectives de l’utilisation de l’ARNm pour traiter le cancer et d’autres maladies ? Vers où se dirige-t-on ?
UŞ: What we have now is now an approved technology and a first approved product. The development of the coronavirus mRNA vaccine shows the power of the mRNA and it shows also the safety of this approach. And it shows that it opens up a door for new technology and for new type of treatments. And the mRNA molecules that we are currently using for cancer, we have more than 10 products now in clinical development, are diverse against different types of cancer. We are very confident that the success that we have generated now for our infectious disease vaccines can be continued with our cancer immunotherapies.
UŞ : Ce que nous avons aujourd’hui, c’est une technologie et un premier produit approuvés. Le développement du vaccin à ARN messager contre le coronavirus montre la puissance de l’ARN messager et la fiabilité de cette méthode. Et cela ouvre la voie à de nouvelles technologies et à de nouveaux types de traitements. Les molécules d’ARN messager que nous utilisons face au cancer – nous avons plus de dix produits en cours de développement clinique – sont variées et agissent contre différents types de cancer. Nous sommes convaincus que le succès que nous avons obtenu pour nos vaccins contre les maladies infectieuses peut se poursuivre avec nos immunothérapies contre le cancer.
CA: Some people may hear this and say this is just another type of drug that's coming along. But I think on the mental model you're talking about, we should think about it as much more revolutionary than that, that typically a drug, a traditional drug, kind of changes the chemical environment, the background of an entire area of the body. But your -- If you understand the language of mRNA, you can do something much more specific and precise. Is that something like a fair way to think about it?
CA : Certains peuvent se dire qu’il ne s’agit que d’un nouveau type de médicament. Mais je pense que le modèle de réflexion dont vous parlez, nous devrions considérer qu’il est beaucoup plus révolutionnaire qu’un médicament classique, car il modifie l’environnement chimique, le contexte d’une partie entière du corps. Mais votre – Si vous comprenez le langage de l’ARN messager, vous pouvez faire quelque chose de beaucoup plus spécifique et précis. Est-ce une bonne façon de voir les choses ?
ÖT: Yes, indeed. It could be the next revolution in the biopharm landscape.
ÖT : Oui, en effet. Ce pourrait être la prochaine révolution dans le secteur biopharmaceutique.
UŞ: At the end of the day, disease is a situation where the communication between cells is disturbed. So, for example, autoimmune disease is a disease condition where immune cells attack normal cells. And indeed, we could engineer messenger RNA therapies which could teach the immune system to stop to do that, without inhibiting the whole immune system, by just communicating with the immune cells which are attacking. We could be precise and more specific.
UŞ : En fin de compte, la maladie est une situation où la communication entre les cellules est perturbée. Par exemple, une maladie auto-immune est un état pathologique où les cellules immunitaires attaquent les cellules normales. Et en effet, nous pourrions concevoir des thérapies à base d’ARN messager qui apprendraient au système immunitaire à arrêter d’agir ainsi, sans inhiber l’ensemble du système immunitaire, en communiquant uniquement avec les cellules immunitaires qui attaquent. Nous pourrions être plus précis et spécifiques.
CA: The success of BioNTech over the last couple of years, I think the value of the company has rocketed because of the amazingness of what's happened. I mean, it's made you both extremely wealthy, I think you're both billionaires now. How have you been able to respond to that? Sometimes so much money brings its own problems with it. Is that proving a distraction?
CA : Le succès de BioNTech au cours des deux dernières années – je pense que la valeur de l’entreprise a flambé en raison de l’ampleur de ce qui s’est passé. Vous êtes tous deux devenus très riches – je crois que vous êtes milliardaires. Comment avez-vous été en mesure de gérer cela ? Parfois, autant d’argent apporte son lot de problèmes. Cela vous perturbe-t-il ?
ÖT: For a company which sees innovation as its core mission, too much money is never a problem. Because innovation really means that you have to invest. Otherwise, we will only have two type of products or incremental improvement for solutions of high medical need.
ÖT : Pour une entreprise qui considère l’innovation comme sa mission principale, avoir trop d’argent n’est jamais un problème. Car l’innovation suppose en fait d’investir. Sinon, nous n’aurions que deux types de produits ou d’amélioration incrémentale pour les solutions à fort besoin médical.
UŞ: It really gives us the chance to transform our company. So we were when we started -- When we compare ourselves with the situation we had at the beginning of 2020, we had a number of product candidates in clinical testing, but the company required funding every year or every second year. Now we have a situation to really address the full vision of the company. We started BioNTech with the idea really to provide novel treatments wherever there is a high unmet medical need. And we now can do that in a much larger and broader scale, and bring our innovations faster to patients.
UŞ : Cela nous donne vraiment la chance de transformer notre entreprise. Alors que nous étions quand nous avons commencé – quand nous nous comparons avec notre situation au début de 2020, nous avions plusieurs produits candidats pour des tests cliniques, mais l’entreprise avait besoin de fonds tous les ans ou tous les deux ans. Aujourd’hui, nous sommes dans une situation où nous pouvons vraiment réaliser la vision globale de l’entreprise. Nous avons commencé BioNTech avec l’idée de fournir de nouveaux traitements partout où il y a un grand besoin médical non satisfait. Nous pouvons aujourd’hui le faire à une échelle bien plus grande, plus large et apporter nos innovations plus rapidement aux patients.
CA: You are both from families who immigrated from Turkey to Germany. Immigrants have faced hard times in many countries, including Germany. And yet you, I think, have helped transform the debate about immigration, in Germany and elsewhere, just by the extraordinary success that you've achieved creating this world-leading company in Germany. Do you take joy for the impact you may have had on this issue?
CA : Vous êtes tous deux issus de familles qui ont immigré de Turquie en Allemagne. Les immigrants ont traversé des périodes difficiles dans de nombreux pays, y compris en Allemagne. Et pourtant, vous avez, je pense, contribué à transformer le débat sur l’immigration, en Allemagne et ailleurs, rien que par l’extraordinaire succès que vous avez obtenu en créant cette entreprise de renommée mondiale en Allemagne. Vous réjouissez-vous de l’impact que vous avez pu avoir sur cette question ?
UŞ: It is somehow surprising because the way how we do science, and how we recognize how people work effectively in teams together is not to us from where the person is coming, but what the person can contribute. So in our company, we have employees from more than 60 countries. So we are an international group of scientists, as any other research institution. So we have to recognize that globalization really helps to bring people, scientists or other engineers into one place, allowing to work together and to come with extraordinary results. For us, this is somehow surprising that this is seen as special. It is just the way how excellent research and science work.
UŞ : C’est un peu surprenant parce que notre façon de pratiquer la science et de déterminer comment les gens travaillent efficacement en équipe, ne dépend pas de l’origine de la personne, mais de ce qu’elle peut apporter. Ainsi, dans notre entreprise, nos salariés viennent de plus de 60 pays. Nous sommes un groupe international de scientifiques, comme toute institution de recherche. Nous devons donc admettre que la mondialisation contribue grandement à rassembler des gens, des scientifiques ou d’autres ingénieurs dans un même lieu, ce qui nous permet de travailler ensemble et d’obtenir des résultats extraordinaires. Pour nous, c’est assez surprenant qu’on considère cela comme spécial. C’est juste la façon dont la recherche et la science de pointe fonctionnent.
CA: Well, it's extraordinary and inspiring what you've achieved, and it'll be very exciting to track progress over the coming years. Thank you so much. Thank you.
CA : Ce que vous avez accompli est extraordinairement inspirant et ce sera passionnant de suivre vos progrès ces prochaines années. Merci beaucoup. Merci à vous.