Chris Anderson: Dr. Şahin and Dr. Türeci, welcome. Such a treat to speak with you.
Chris Anderson: Dr. Şahin Dra. Türeci, bienvenidos. Es todo un placer hablar con Uds.
Özlem Türeci: Thank you very much, Chris. It's a pleasure to be here.
Özlem Türeci: Muchas gracias a ti, Chris. Es un placer estar aquí.
CA: So tell me, as you think back over the last 18 months, what words pop to mind for you?
CA: Díganme, al ver hacia atrás en los últimos 18 meses, ¿qué palabras les vienen a la cabeza?
ÖT: Well, one word which comes to mind is breathless. It was indeed a breathless 16, 17 months for us. When we started in January last year, it was already at that time clear to us that we were already in a pandemic. What was not known was how fast this pandemic would evolve and whether we would have the time in the first place to have a vaccine ready soon enough in due time. And understanding this, it meant for us that there was not even one day to lose. And this was the mindset of the entire team here in Mainz and at BioNTech and later on also of our partners which were involved, Pfizer and others, to keep going and be fast.
ÖT: Bueno, me viene a la mente el quedarse sin aliento. Definitivamente, fueron unos 16, 17 meses intensos para nosotros. Cuando comenzamos en enero del año pasado, ya resultaba evidente que estábamos en una pandemia. Lo que no se sabía era qué tan rápido se desarrollaría esta pandemia, y para empezar tampoco se sabía si tendríamos tiempo para tener lista rápidamente la vacuna cuando se necesitara. Y comprender esto para nosotros significó que no había ni un solo día que perder. Esta era la actitud de todo el equipo aquí en Mainz y en BioNTech, y más tarde, la de nuestros socios involucrados, Pfizer y otros, para seguir adelante y darnos prisa.
CA: I mean, it's so extraordinary that the ideas and the work in your minds have now impacted hundreds of millions, perhaps billions of people. That must feel overwhelming. And yet, I know at the same time, you don't believe in this notion of a flash-in-the-pan ideas. Steven Johnson, the author, in his book "Where [Good] Ideas Come From," speaks of the slow hunch, that the best ideas happen over many years. And I know that you believe that is true in your case. I'd like us to go back a couple of decades to -- tell us how this began. How did you meet?
CA: Es extraordinario que sus ideas y trabajo hasta ahora hayan impactado a cientos de millones, quizás hasta miles de millones de personas. Eso debe ser abrumador. Y aun así, sé que al mismo tiempo Uds. no creen en el concepto de “ideas de éxito pasajero”. En su libro “De dónde provienen las buenas ideas”, el escritor Steven Johnson habla de largos períodos de incubación, que las mejores ideas toman varios años. Y sé que Uds. creen que en su caso es verdad. Retrocedamos algunas décadas; cuéntennos cómo comenzó esto. ¿Cómo se conocieron?
ÖT: We met on an oncohematology ward, Uğur being a young physician, and I was still in medical school training on ward. Which means we met in one of the worlds which became important to us, the world of patient care, of treating oncohematology patients. And we soon found out that there was a second world which we liked, namely the world of science. We were haunted by the same dilemma, namely that whereas there was not much we could offer our cancer patients, there were so many potential technologies we encountered in the lab which could address this. So one of our shared visions was to bridge this dilemma by working on bringing science and technology fast. And that's an important word here. Fast to the patient's bedside to address high medical need.
ÖT: Nos conocimos en una sala de oncohematología. Uğur era un joven médico, y yo aún estaba en la facultad de medicina, haciendo guardias hospitalarias. Significa que nos conocimos en uno de los mundos que se volvieron importantes para nosotros: el mundo de la atención a pacientes, tratar a los pacientes de oncohematología. Y pronto descubrimos que había otro mundo que nos gustaba, es decir, la ciencia. Nos obsesionaba el mismo dilema, que aunque no pudiéramos ofrecer mucho a nuestros pacientes con cáncer, encontramos que en el laboratorio había muchas tecnologías potenciales que podrían resolver esto. Así, una de nuestras visiones en común era abordar este dilema trabajando para entrelazar la ciencia y la tecnología rápidamente. Y esta palabra es importante. Rápidamente para atender las necesidades médicas graves de los pacientes.
CA: So I think the first company you founded nearly 20 years ago was to use the power of the human immune system to tackle cancer.
CA: Creo que la primera compañía que fundaron hace casi 20 años era para usar el poder del sistema inmune del ser humano para combatir el cáncer.
Uğur Şahin: We were always interested in using the patient's immune system to fight cancer and other type of diseases. As immunologists, we knew how powerful the human immune system is. But it was also clear that the human immune system, in the case of cancer, did not fight cancer cells. It could fight it, but it didn't. And for that, we wanted to develop immunotherapies. That means treatments that use the power of the immune system and redirect the power of the immune system to cancer cells. It was clear that in the university setting, we could not continue to develop monoclonal antibodies because the cost for development of monoclonal antibodies before you can start a clinical trial, was in the range of 20, 30 million euros, and therefore we decided to start a company to get the funding.
Uğur Şahin: Siempre nos interesó usar el sistema inmune de los pacientes para combatir el cáncer y otras enfermedades. Como inmunólogos, sabíamos lo poderoso que es el sistema inmune del ser humano. Pero también era evidente que el sistema inmune del ser humano, en el caso del cáncer, no combatía las células cancerosas. Podría, pero no lo hacía. Y para eso, queríamos desarrollar inmunoterapias. Es decir, tratamientos que aprovechan el poder del sistema inmune y lo redirigen hacia las células cancerosas. Estaba claro que en un entorno universitario, no podríamos seguir desarrollando anticuerpos monoclonales porque el costo para desarrollarlos antes de comenzar con las pruebas clínicas, rondaba los 20 y 30 millones de euros, y por eso decidimos fundar una compañía para conseguir el financiamiento.
CA: Now, soon after you started this company, you decided to get married. Tell me about your wedding day.
CA: Después de fundar la compañía, decidieron contraer matrimonio. Cuéntenme sobre el día de su boda.
ÖT: Day was well planned, a quick wedding. And thereafter we went back to the laboratory and our guests at our wedding, that was basically our team, our research team. So no time to lose, Chris.
ÖT: Fue un día bien planeado, y una boda rápida. Y poco después, volvimos al laboratorio junto con los invitados de la boda, que eran básicamente nuestro equipo de investigación. No había tiempo que perder, Chris.
CA: (Laughs) That was a pretty special honeymoon. I mean, it seems like your love for each other is very much bound up in your love for this work and your sense of the importance of this work. How would you characterize those intersecting relationships there?
CA: (Risas) Fue una luna de miel algo especial. Es decir, parece que el amor que se tienen entre sí está muy entrelazado con su amor por este trabajo y la importancia que tiene para Uds. ¿Cómo describirían esas relaciones intrínsecas?
UŞ: We are really two scientists. At the end of the day, we love what we do, and for us, we don't differentiate between work and life balance. It's for us really a privilege to be scientists, to be able to do what we love. And therefore, we combine our normal life with our professional life. And therefore, this is pretty normal for us.
UŞ: Realmente somos dos científicos. Al final del día, amamos lo que hacemos, y para nosotros, no hay diferencia entre balancear el trabajo y la vida. Para nosotros, ser científicos es realmente un privilegio, el ser capaces de hacer lo que amamos. Y por eso, combinamos nuestras vidas cotidianas y profesionales. Por lo tanto, para nosotros es normal.
CA: So talk to me about this extraordinary molecule RNA, and how you got interested in it and how it became, as I understand it, an increasing focus of your work. And indeed, it led to the founding of BioNTech. Talk about that.
CA: Cuéntenme sobre la extraordinaria molécula ARN, cómo se interesaron en ella, y cómo se volvió, según lo veo, en el enfoque de su trabajo. Y que condujo a la fundación de BioNTech, por supuesto. Cuenten sobre eso.
UŞ: Yeah, mRNA is a natural molecule, it's one of the first molecules of life. It is a carrier of genetic information. But in contrast to DNA, it's not stable. So it can be used to transfer information to human cells. And the human cells can use this information to build proteins, which can be used for therapeutic settings, for example, to make a protein which is a vaccine, or to make a protein which is an antibody, or to make a protein which is another type of drug. And we were fascinated by this molecule class, because it was very clear that mRNA can be produced pretty fast, within a few days. And we were, as MDs, we were particularly interested to develop personalized medicines. That means a treatment and immunotherapy specifically designed for a cancer patient, because one of the key challenges in cancer treatment, is that every patient has a different tumor. If you compare two tumors of two patients with the same type of tumor, the similarity of the tumors is less than three percent and 97 percent is really unique. And today, it's still not possible to address the uniqueness of the tumor of a patient. And therefore, we were seeking for a technology which could be used for immunotherapy and which could be used to develop a treatment within the shortest possible time. The idea to get the genetic sequence of the tumor and then make a vaccine which is personalized, within a few weeks.
UŞ: Bien, el ARNm es una molécula natural, una de las primeras moléculas de la vida. Es un mensajero de información genética. Pero en comparación con el ADN, es inestable. Así que se puede usar para transferir información a las células humanas. Las células humanas pueden usar la información para producir proteínas, las cuales se pueden usar en ámbitos terapéuticos, por ejemplo, para hacer una proteína que sea una vacuna, o para hacer una proteína que sea un anticuerpo, o para hacer una proteína que sea otro tipo de fármaco. Para nosotros, este tipo de moléculas era fascinante, porque estaba muy claro que el ARNm se puede producir muy rápido, en unos pocos días. Como doctores en medicina, nos interesaba desarrollar medicamentos personalizados. Eso es, un tratamiento e inmunoterapia diseñado específicamente para un paciente con cáncer, porque uno de los retos clave de los tratamientos contra el cáncer es que cada paciente tiene un tumor distinto. Si se compara los tumores de dos pacientes que tengan el mismo tipo de tumor, la similitud de los tumores será menor al 3 % y el otro 97 % sería único. Incluso ahora, todavía no es posible atender la singularidad del tumor de un paciente. Y por lo tanto, buscamos una tecnología que se pueda usar como inmunoterapia y que se pueda usar para desarrollar un tratamiento en la menor cantidad de tiempo posible. La idea es conseguir la secuencia genética del tumor y luego fabricar una vacuna personalizada dentro de unas cuantas semanas.
CA: Is it fair to say that almost all of the significant things that happen to us biologically are actions done by proteins, and that it's mRNA that actually makes those proteins? If you can understand the language of mRNA, you can get involved in pretty much everything of significance to the well-being of a human being.
CA: ¿Es correcto decir que casi todas las cosas significativas que nos ocurren a nivel biológico son acciones realizadas por proteínas, y que el ARNm es en realidad el que produce todas esas proteínas? Si podemos entender el lenguaje del ARNm, nos podemos involucrar en casi todo lo relevante en lo que concierne al bienestar del ser humano.
ÖT: Exactly. So in principle, the information instructions are in the DNA. These have to be translated into protein because proteins are the actors which keep our cells alive and our organism functional. And the way how to translate what is instructed by DNA in a fashion that it is well-timed and happens at the right places, into protein, there is messenger RNA. Messenger RNA sort of instructs when and how much of which protein has to be built in order to ensure the activity of our body.
ÖT: Exacto. En principio, la información e instrucciones se encuentran en el ADN. Y deben ser traducidos en una proteína, porque las proteínas son los agentes que mantienen vivas a nuestras células y a nuestros organismos en óptimo funcionamiento. Y la función de traducir lo que indica el ADN, en el momento adecuado y en los lugares correctos, en una proteína es del ARN mensajero. El ARN mensajero indica cuándo y qué tanto de cuál proteína se debe producir para asegurar la actividad de nuestros organismos.
CA: So you can almost think of DNA as the sort of The Oxford English Dictionary of Language. It sort of sits there as the reference point. But for the actual living work, the living work of language out there in the world instructing things, that is done by mRNA.
CA: Así que se puede tomar al ADN en algo así como el Diccionario Oxford de la Lengua Inglesa. Está ahí como el punto de referencia. Pero en la práctica, el que está en realidad ahí afuera dando las instrucciones, es el ARNm.
UŞ: Yeah, absolutely, it is possible. So the human cells, exactly, DNA is like a library. If you have the platform for the messenger RNA therapy, you can deliver any type of message and the body cells ensure that the message is translated into the right protein.
UŞ: Sí, absolutamente, es posible. Las células humanas, específicamente, el ADN, son como una biblioteca. Si tienes la plataforma para la terapia de ARN mensajero, puedes enviar cualquier tipo de mensaje y las células del cuerpo se aseguran de que el mensaje se traduzca en la proteína correcta.
ÖT: A high advantage of mRNA is that it is so versatile. You can deliver all sorts of messages, as Uğur has called them. On the one hand, you can deliver the blueprint for the protein which you want to be produced in this cell. But you can, with the same molecule, also design into the mRNA instructions how this protein should be built, instructions to the protein factories of the cell. So you can define whether you want this protein to be built in high amounts or for a long duration, how the pharmacokinetics of this protein should be in the cell.
ÖT: Una gran ventaja del ARNm es su versatilidad. Se pueden enviar todo tipo de mensajes, así como los llamó Uğur. Por un lado, puedes mandar el manual de la proteína que quieres que se produzca en una célula. Pero con la misma molécula se pueden diseñar también en el ARNm instrucciones sobre cómo debería producirse esta proteína, instrucciones para las fábricas de proteínas de la célula. Así que puedes definir las cantidades en las que se produce esta proteína, o por cuánta duración, cómo debería ser la farmacocinética de la proteína en la célula.
CA: So talk about January of last year when you first heard about this new virus that was spreading.
CA: Cuenten sobre enero del año pasado, cuando oyeron por primera vez que este virus se estaba extendiendo.
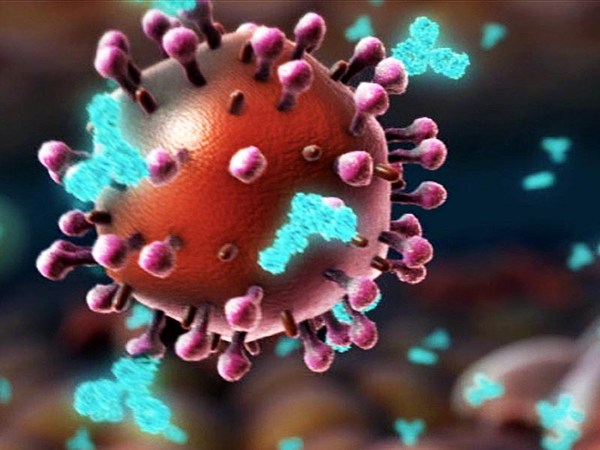
UŞ: So in the end of January, we read a paper published about this outbreak in Wuhan, and realized that this new outbreak has all features to become a global pandemic, and we were concerned that our life will change, that this outbreak could change the fate of mankind. And we knew that we have this messenger RNA technology, which was actually developed for personalized cancer therapy. But the idea of personalized cancer therapy is to get the genetic information of the patient and then make a vaccine as fast as possible. And we had now the same situation. It was not a personalized vaccine, but it was a genetic information of the virus, which was released two weeks earlier. And so this genetic information of this virus was available, and our task was to make a vaccine as fast as possible. And the challenge at that time point was, there was almost nothing known about this virus. It was a completely new virus. We had some assumptions which target which molecule encoded by the virus could be the right target. That means the molecule which can be used to precisely engineer an immune attack. This is the spike protein. It is on the surface of the virus. And there's not only one copy of the spike protein on the virus, but multiple in the range of 20, 25, 30 spike proteins. And the spike protein has two functions. One function is really to enable that the virus sticks to human cells. For example, it sticks to cells in the human lung. And the second is that the spike protein acts as a key. It allows the virus to enter into the cells. Our goal was to engineer an immune response.
UŞ: A finales de enero, leímos en un periódico sobre el brote en Wuhan, y nos dimos cuenta de que este nuevo brote era propenso a convertirse en una pandemia mundial y nos preocupaba que nuestras vidas cambiaran, que este brote pudiera cambiar el destino de la humanidad. Y sabíamos que teníamos esta tecnología de ARN mensajero, que desarrollábamos como terapia personalizada contra el cáncer. Pero la terapia personalizada para el cáncer significaba sacar la información genética del paciente y luego hacer una vacuna lo más rápido posible. Y ahora estábamos en la misma situación. No era una vacuna personalizada, sino la información genética del virus, que se había liberado dos semanas antes. La información genética del virus estaba disponible, y nuestra tarea era fabricar una vacuna lo más rápido posible. En ese tiempo, el desafío era que casi no se sabía nada de este virus. Era un virus completamente nuevo. Teníamos algunas suposiciones sobre cuál molécula codificada por el virus podría ser el objetivo correcto. Es decir, la molécula que podría usarse para inducir precisamente una respuesta inmune. Esta es la proteína spike. Está en la superficie del virus. Y no hay una sola copia de la proteína spike en el virus, sino que hay múltiples en un rango de 20, 25, 30 proteínas spike. La proteína spike tiene dos funciones. La primera es posibilitar que el virus se acople con células humanas. Por ejemplo, se acopla con las células de un pulmón humano. La segunda función es actuar como una llave. Permite al virus entrar en las células. Nuestro objetivo es diseñar una respuesta inmune.
CA: You've got a slide showing the T-cell response to your vaccine. How long were you into the process before you saw this and you saw, wow, there really is a spectacular response going on here?
CA: En una diapositiva se muestra la respuesta de los linfocitos T a su vacuna. ¿Qué tan avanzado estaba el proceso antes de que vieran esto y dijeran, “guau, realmente está ocurriendo una respuesta espectacular”?
ÖT: We saw this already in the animal models because they are also meant to assess the immune response. And what is shown on this slide is on the left side, a lymph node from a setting where there was no RNA treatment or RNA vaccination. And on the right side, a lymph node of a treated organism, in this case, an animal. And the localization matters. And we have constructed our RNA nanoparticles, with encapsulation into lipids such that the mRNA is carried into lymph nodes, not just anywhere, it's carried into lymph nodes and in the lymph nodes it reaches a very special cell type, which is called dendritic cells, and these cells are coaches of the immune system. So they are the generals which call all the different special forces and train them on the wanted poster of attacker. And it's very important that you reach those cells. On the right side, you can see the effect of reaching those cells. You see many red dots. And these are T-cells which have been trained to recognize the antigen, the protein which mRNA has delivered, and they have expanded to a sort of army of clones, so to say. So all these red dots are an army which only knows one goal, namely attacking this specific protein encoded by the mRNA.
ÖT: Ya lo habíamos visto en los modelos animales porque también debían evaluar una respuesta inmune. En esta diapositiva se muestra, del lado izquierdo, un nódulo linfático sin tratamiento ARN o vacuna ARN. En el lado derecho, un nódulo linfático de un organismo con tratamiento, en este caso, un animal. Y la ubicación es importante. Hemos construido nuestras nanopartículas de ARN, con encapsulaciones lipídicas de tal forma que el ARNm sea llevado hasta los nódulos linfáticos, no a cualquier parte, se conduce hasta los nódulos linfáticos y una vez ahí alcanza a un tipo especial de células, las células dendríticas, las cuales entrenan al sistema inmunológico. Ellas son los generales que convocan a las distintas fuerzas especiales y las entrenan para reconocer al atacante. Es muy importante alcanzar a esas células. Del lado derecho, se pueden ver los efectos de alcanzarlas. Aquí se ven muchos puntos rojos. Son los linfocitos T entrenados para reconocer el antígeno, la proteína que el ARNm ha enviado, y se han convertido en un ejército de clones, por decir algo. Los puntos rojos son un ejército que tiene un solo objetivo: atacar esta proteína específica codificada por el ARNm.
CA: So it's really stunning that within just a few days of your looking at this sequence of the most dangerous pathogen to hit humanity in 100 years, I guess, that you were able to come up with these these candidate vaccines. And I guess over the course of the next weeks and months, you had growing confidence that, wow, this was going to work. It wasn't until the results of the human trials came out, I guess in November of last year, that you really knew. Tell us about that moment.
CA: Es realmente asombroso que en tan solo unos días de observar la secuencia del patógeno más peligroso que ha golpeado a la humanidad en 100 años, creo, hayan podido desarrollar estas vacunas candidatas. Y supongo que en los siguientes meses y semanas su confianza aumentaba y pensaban “guau, esto va a funcionar”. No fue sino hasta que salieron los resultados de las pruebas en humanos, creo que en noviembre del año pasado, que lo sabían en verdad. Cuéntennos de ese momento.
ÖT: It was a Sunday when we were waiting for these results, which are assessed in such trials by an independent committee and Uğur said, "So let's see how the data will look like." It was not clear whether it would be a thumbs up or down. And we were very relieved. And I felt blessed to hear that the vaccine was efficacious and it was highly efficacious, over 90 percent.
ÖT: Fue un domingo cuando esperábamos los resultados que eran evaluados por un comité independiente y Uğur dijo: “Vamos a ver cómo se verán los datos”. No sabíamos si serían positivos o negativos. Estábamos muy aliviados. Me sentí bendecida de saber que la vacuna era eficaz, y lo era en más del 90 %.
CA: And that more than 90 percent almost disguises the full extent, because that's just against any kind of level of infection of COVID. Severe infection and fatalities were almost completely protected against, I think. And it must have been an ecstatic moment for you. Certainly was for so many people around the world.
CA: Y ese más del 90 % suele ser el 100 %, porque eso es solamente contra cualquier nivel de infección de la COVID. Eran efectivas casi por completo contra infecciones graves y mortales, creo. Debió haber sido un momento eufórico para Uds. Lo fue para muchas personas en todo el mundo.
UŞ: Yes, absolutely. So this was a Sunday evening, and there were a handful of people knowing that an effective vaccine is existing against this global pandemic. And we were so excited and so happy and we shared of course this information the next day.
UŞ: Sí, absolutamente. Eso fue una tarde de domingo, y había un montón de personas que sabían que existía una vacuna efectiva contra esta pandemia global. Estábamos muy emocionados y felices y compartimos esta información al día siguiente.
CA: So based on what's happened this time around and the amazing acceleration, compared with any other vaccine development, I mean, if we were hit by another virus, could you picture that next time we could accelerate the time line further still if need be?
CA: Con base en lo que ocurrió en esta ocasión y la impresionante rapidez, en comparación con el desarrollo de otras vacunas, quiero decir, si fuéramos atacados por otro virus, ¿creen que la próxima vez podríamos acelerar más los tiempos en caso de ser necesario?
UŞ: Yes, Chris, this is an excellent question. Actually, the world was not prepared to deal with such a pandemic. The science and the vaccine developers reacted in an excellent fashion. And it is incredible and wonderful that it was possible to come up with an effective vaccine while a pandemic is ongoing, in less than 12 months. But the challenges that we have at the moment is that we don't have sufficient production capacity. Ideally, we would be prepared the next time, not only to develop a vaccine in light speed, but also to to make and distribute the vaccine in light speed. So what we need now is an additional element which was not existing, is manufacturing capacity. And idle manufacturing capacity. We must be bringing us into a position that we can produce 12 billion doses of vaccine, if you consider prime boost, within less than six months. And this is technically possible. So this can be done if governments and international organizations invest into manufacturing capacity, invest into keeping this idle capacity, and also come up with a standard time span and process to enable even faster response. So we in principle, we might be able to manage to come up with a vaccine and start distribution in even less than eight months.
UŞ: Sí, Chris, esta es una excelente pregunta. En realidad, el mundo no estaba preparado para una pandemia así. La ciencia y desarrolladores de vacunas reaccionaron de manera excelente. Y es increíble y maravilloso que fuera posible desarrollar una vacuna efectiva con la pandemia en curso, en menos de 12 meses. Pero los desafíos de momento son que no tenemos una capacidad de producción suficiente. Idealmente, la próxima vez estaríamos preparados, no solo para desarrollar una vacuna con tal rapidez, sino que también para fabricarla y distribuirla igual de rápido. Lo que necesitamos ahora es un elemento adicional que no existía: capacidad de fabricación. Y una capacidad ociosa. Debemos situarnos en una posición en la que podamos producir 12 000 millones de dosis de vacunas, si se consideran los estímulos primarios, en menos de seis meses. Técnicamente, esto es posible. Se puede lograr si los gobiernos y organizaciones internacionales invierten en capacidad de fabricación, y en mantener la capacidad ociosa, y si también elaboran un lapso de tiempo estándar y procesos que permitan una respuesta más rápida. En principio, podríamos arreglárnoslas para desarrollar una vacuna y comenzar a distribuirla incluso en menos de ocho meses.
CA: What does what's happened in this last year tell you now about the prospects for using mRNA to treat cancer and indeed other diseases? Where is this heading?
CA: ¿Qué pueden concluir ahora de todo lo que ocurrió en el último año sobre las posibilidades de usar el ARNm para tratar el cáncer y, por supuesto, otras enfermedades? ¿Adónde conduce todo esto?
UŞ: What we have now is now an approved technology and a first approved product. The development of the coronavirus mRNA vaccine shows the power of the mRNA and it shows also the safety of this approach. And it shows that it opens up a door for new technology and for new type of treatments. And the mRNA molecules that we are currently using for cancer, we have more than 10 products now in clinical development, are diverse against different types of cancer. We are very confident that the success that we have generated now for our infectious disease vaccines can be continued with our cancer immunotherapies.
UŞ: Lo que tenemos ahora se convirtió en una tecnología aprobada y un producto aprobado por primera vez. El desarrollo de una vacuna ARNm para el coronavirus muestra el poder del ARNm y también muestra la seguridad de este enfoque. Y muestra que se abren las puertas para una nueva tecnología y para nuevos tipos de tratamientos. Y las moléculas de ARNm que usamos actualmente para el cáncer, de las que tenemos ahora más de 10 productos en desarrollo clínico, son diversas contra distintos tipos de cáncer. Confiamos mucho en que el éxito que hemos alcanzado hasta ahora para nuestras vacunas de enfermedades infecciosas sean continuadas con nuestras inmunoterapias para el cáncer.
CA: Some people may hear this and say this is just another type of drug that's coming along. But I think on the mental model you're talking about, we should think about it as much more revolutionary than that, that typically a drug, a traditional drug, kind of changes the chemical environment, the background of an entire area of the body. But your -- If you understand the language of mRNA, you can do something much more specific and precise. Is that something like a fair way to think about it?
CA: Algunos podrían oír esto y decir que es un nuevo tipo de fármaco que está por llegar. Pero creo que la imagen mental de la que están hablando debería ser tratada como algo más revolucionario que eso, más que una medicina tradicional, en algo que cambia el entorno químico, el trasfondo de un área del cuerpo entera. Pero... Si entienden el lenguaje del ARNm, pueden hacer algo más específico y preciso. ¿Es ésa una manera correcta de tomarlo?
ÖT: Yes, indeed. It could be the next revolution in the biopharm landscape.
ÖT: Sí, sin duda. Podría ser la próxima revolución del panorama biofarmacéutico.
UŞ: At the end of the day, disease is a situation where the communication between cells is disturbed. So, for example, autoimmune disease is a disease condition where immune cells attack normal cells. And indeed, we could engineer messenger RNA therapies which could teach the immune system to stop to do that, without inhibiting the whole immune system, by just communicating with the immune cells which are attacking. We could be precise and more specific.
UŞ: A fin de cuentas, una enfermedad es una situación en la que la comunicación entre las células se ve perturbada. Así, por ejemplo, una enfermedad autoinmune es una condición en la que las células inmunes atacan células normales. Y por supuesto, podríamos diseñar terapias de ARN mensajero que podrían capacitar al sistema inmune para que deje de hacer eso sin inhibirlo en su totalidad, simplemente al comunicarse con las células inmunes que son atacadas. Podríamos ser más precisos y específicos.
CA: The success of BioNTech over the last couple of years, I think the value of the company has rocketed because of the amazingness of what's happened. I mean, it's made you both extremely wealthy, I think you're both billionaires now. How have you been able to respond to that? Sometimes so much money brings its own problems with it. Is that proving a distraction?
CA: Por el éxito que BioNTech ha tenido en los últimos años, creo que el valor de la compañía se ha disparado debido a estos eventos sin precedentes. Los ha enriquecido a ambos en extremo, creo que ahora son multimillonarios. ¿Cómo han respondido a eso? A veces tanta cantidad de dinero trae problemas consigo. ¿Ha sido un distractor para Uds.?
ÖT: For a company which sees innovation as its core mission, too much money is never a problem. Because innovation really means that you have to invest. Otherwise, we will only have two type of products or incremental improvement for solutions of high medical need.
ÖT: Para una compañía cuya misión principal es la innovación, demasiado dinero nunca es un problema. Porque la innovación en realidad significa que debes invertir. De otro modo, solo tendríamos dos tipos de productos o una mejora gradual para las soluciones de necesidades médicas severas.
UŞ: It really gives us the chance to transform our company. So we were when we started -- When we compare ourselves with the situation we had at the beginning of 2020, we had a number of product candidates in clinical testing, but the company required funding every year or every second year. Now we have a situation to really address the full vision of the company. We started BioNTech with the idea really to provide novel treatments wherever there is a high unmet medical need. And we now can do that in a much larger and broader scale, and bring our innovations faster to patients.
UŞ: Realmente nos da la oportunidad de transformar nuestra compañía. Así estábamos cuando comenzamos... Cuando nos comparamos con la situación en la que estábamos a comienzos del 2020, teníamos varios productos candidatos para pruebas clínicas, pero la compañía requería financiamiento cada uno o dos años. Ahora realmente podemos abordar la visión de la compañía por completo. Fundamos BioNTech con la idea de realmente proveer tratamientos novedosos cada vez que surgieran necesidades médicas graves no atendidas. Y ahora podemos hacerlo a una escala mucho mayor, y también llevar nuestras innovaciones más rápido a los pacientes.
CA: You are both from families who immigrated from Turkey to Germany. Immigrants have faced hard times in many countries, including Germany. And yet you, I think, have helped transform the debate about immigration, in Germany and elsewhere, just by the extraordinary success that you've achieved creating this world-leading company in Germany. Do you take joy for the impact you may have had on this issue?
CA: Ambos vienen de familias que emigraron de Turquía a Alemania. Incluso en Alemania, los inmigrantes han enfrentado dificultades. Aun así, Uds., creo, han ayudado a redirigir el debate de la inmigración, en Alemania y otras partes. solo por el extraordinario éxito que han alcanzado al fundar en Alemania esta compañía líder mundial. ¿Les produce satisfacción el impacto que han causado en este asunto?
UŞ: It is somehow surprising because the way how we do science, and how we recognize how people work effectively in teams together is not to us from where the person is coming, but what the person can contribute. So in our company, we have employees from more than 60 countries. So we are an international group of scientists, as any other research institution. So we have to recognize that globalization really helps to bring people, scientists or other engineers into one place, allowing to work together and to come with extraordinary results. For us, this is somehow surprising that this is seen as special. It is just the way how excellent research and science work.
UŞ: De cierta forma es sorprendente porque en nuestra manera de hacer la ciencia, y por cómo reconocemos que las personas trabajan bien en equipo, no es relevante el país del que proviene la persona, sino las cosas que puede aportar. En nuestra compañía tenemos empleados de más de 60 países. Por lo tanto, somos un equipo de científicos internacional, como cualquier otra institución de investigación. Tenemos que reconocer que la globalización contribuye a acercar a la gente, científicos, u otros ingenieros, en un solo lugar, permitiéndonos trabajar juntos y alcanzar resultados extraordinarios. Para nosotros, es sorprendente que esto sea visto como algo excepcional. Así es como funcionan la investigación y ciencia de excelencia.
CA: Well, it's extraordinary and inspiring what you've achieved, and it'll be very exciting to track progress over the coming years. Thank you so much. Thank you.
CA: Lo que han logrado es extraordinario e inspirador, y será emocionante seguir su progreso en los próximos años. Muchas gracias. Gracias.