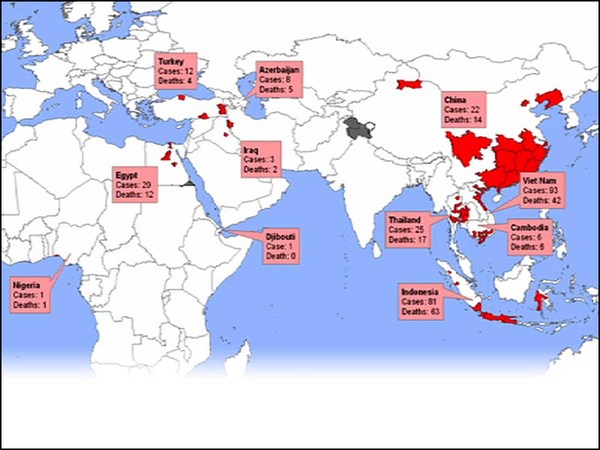
I want to tell you about a student of mine. A few weeks ago, she was on vacation when at 3am she got a phone call. It was her husband telling her that the city that she was in would be quarantined by 10am. She was in Wuhan, China. The epicenter of the coronavirus outbreak. By 8am she was on the road in a friend's car driving 500 miles to Shanghai Airport. The entire time, she was terrified the authorities would arrest her. She made it out on one of the last flights.
Vreau să vă povestesc despre o studentă de-ale mele. Acum câteva săptămâni era în vacanță, când a primit un telefon la 3 dimineața. Era soțul ei, care îi spunea că orașul în care ea se afla va fi carantinat până la 10 dimineața. Era în Wuhan, China. Epicentrul epidemiei de coronavirus. La ora 8 dimineața deja era pe drum în mașina unui prieten, parcurgând cei 800 de kilometri până la aeroportul din Shanghai. Tot drumul a fost îngrozită că autoritățile o vor aresta. A prins unul din ultimele zboruri.
So we're all relieved that she's back home, safe in the US. But what if I told you she was in this room? What if I told you she was sitting next to you? There's no vaccine. There won't be a vaccine for at least 12 months. And this virus is mutating, so there's no guarantee that the vaccine that we produce 12 months from now will match the mutated virus. We're always playing catch-up. And this is the scenario we're in every time there's an outbreak. Our quarantines are porous, our medical responses are flat-footed.
Suntem cu toții ușurați că a ajuns în siguranță înapoi în SUA. Dar dacă v-aș spune că ea se află în această încăpere? Sau dacă v-aș spune că stă chiar lângă dumneavoastră? Nu există un vaccin și nici nu va exista unul pentru cel puțin 12 luni. Iar virusul suferă mutații, așa că nu avem nicio garanție că vaccinul pe care-l vom produce peste 12 luni va mai fi eficient împotriva mutațiilor virusului. E o joacă de-a prinselea. Întotdeauna e așa când izbucnește o epidemie. Carantina e imperfectă, răspunsul medical e insuficient.
The fundamental problem that we face in controlling these outbreaks is that viruses and other infections do two things really well: they mutate and they transmit. Our medical tools do neither of these two things. Our medical tools don't mutate or transmit. We have a fundamental mismatch between our tools, which are static, and the infections, which are dynamic. This mismatch is why we're always flat-footed. This mismatch is why we're playing catch-up. And this mismatch is universal. It's the reason that we have antibiotic-resistant infections that killed 40,000 Americans last year, and it's the reason that the flu vaccine couldn't prevent the flu from killing 60,000 Americans last year. So how do we resolve this fundamental mismatch?
Problema de bază cu care ne confruntăm în controlarea epidemiilor este că virusurile și alte infecții fac două lucruri excelent: suferă mutații și se transmit. Instrumentele noastre medicale nu fac nici una, nici alta. Instrumentele noastre medicale nu se adaptează, nici nu se transmit. Avem așadar o nepotrivire de bază între instrumentele noastre, care sunt statice, și infecții, care sunt dinamice. Această nepotrivire ne face să fim mereu nepregătiți. Această nepotrivire ne face să fim mereu reactivi. Iar această nepotrivire este universală. De aceea avem infecții rezistente la antibiotice, care au omorât 40.000 de americani anul trecut, și tot de aceea avem un vaccin antigripal ce nu a împiedicat ca gripa să ucidă 60.000 de americani anul trecut. Deci, cum putem rezolva această nepotrivire fundamentală?
I've devoted my career to studying and solving this problem. For 100 years, we've used chemicals as drugs to treat infections. Chemicals will never mutate or transmit. Similarly, our vaccines are not designed to mutate or transmit. 20 years ago, I had a radical idea to use the viruses themselves as therapies -- as building blocks for therapies. To build therapies that could mutate and transmit. Let me share with you how we've had a major breakthrough, and we're already testing these new therapies.
Mi-am dedicat întreaga carieră studierii și rezolvării acestei probleme. De o sută de ani încoace, am folosit substanțe chimice drept medicamente în tratamentul infecțiilor. Dar substanțele chimice nu se modifică și nu se transmit. La fel, vaccinurile nu sunt concepute să se adapteze sau să se transmită. Acum douăzeci de ani am avut o idee revoluționară: să folosim chiar virusurile în scopuri terapeutice, incluzându-le în schemele de tratament, creând astfel tratamente capabile să se adapteze și să se transmită. Vă voi împărtăși cum am ajuns la o realizare majoră, respectiv la niște tratamente care sunt acum în testare.
HIV is the most devastating pandemic of our era. 75 million infected; 33 million dead. Most of us think that HIV is a solved problem. We have truly amazing antiviral drugs: they're safe and effective, and we've spent 15 years and billions of dollars deploying these drugs around the world. So let's look at the numbers.
HIV este cea mai devastatoare pandemie a erei noastre. 75 de milioane de infectați, 33 de milioane de decese. Mulți cred că HIV este acum o problemă rezolvată. Avem câteva antivirale cu adevărat miraculoase; sunt sigure, sunt eficiente. Am muncit cincisprezece ani și am cheltuit miliarde de dolari ca să le facem accesibile în toată lumea. Haideți să ne uităm la niște cifre.
In 2019, 1.7 million people acquired HIV. This number only hit home for me last year when I visited this rural village outside of Durban, South Africa. I was driving along this dirt road with my 10-year-old daughter in the back seat, and walking next to us on the side of the road were girls, the same age as my daughter, barefoot. My daughter asked about why these girls are barefoot and I had to explain disparity to her, which was hard. But what really shocked me was when my colleagues, the local African scientists explained to me that these young girls the same age as my daughter --
În anul 2019, 1,7 milioane de oameni s-au infectat cu HIV. Am devenit conștient de acest număr abia anul trecut, când am vizitat un sat de la marginea Durban-ului, Africa de Sud. Mergeam cu mașina pe un drum plin de praf, cu fiica mea de zece ani pe bancheta din spate. Pe marginea drumului mergeau fetițe de aceeași vârstă cu fiica mea, în picioarele goale. Fiica mea m-a întrebat de ce sunt desculțe acele fete, și a trebuit să îi explic despre prăpastia dintre civilizațiile noastre, ceea ce a fost tare greu. Dar ceea ce m-a șocat, de fapt, a fost atunci când colegii mei, oamenii de știință locali din Africa, mi-au explicat că aceste fetițe de aceeași vârstă cu fiica mea...
(Breathes)
(Suspină)
sorry -- had an 80 percent chance of acquiring HIV in their lifetime. It blew me away. How can these girls have an 80 percent risk if we have safe and effective drugs?
Mă scuzați... aveau un risc de 80% să se infecteze cu HIV pe parcursul vieții. Am rămas perplex. Cum se poate să existe un risc de 80% când noi avem medicamente sigure și eficiente?
The reason is the fundamental mismatch. It creates barriers to controlling infectious disease, particularly in resource-limited settings. The first barrier is mutation: viruses mutate, our drugs don't. The second barrier: adherence. It's really hard to get these drugs to those who need the most. I can't even adhere to a week-long antibiotic regimen in this country. We're asking those in resource-limited settings who face enormous adversity to adhere to lifelong regimens.
Iar explicația e această discrepanță fundamentală. Ea ridică obstacole în controlul bolilor infecțioase, mai ales în mediile cu resurse limitate. Primul obstacol e mutația: virusurile suferă mutații, medicamentele noastre nu. Al doilea obstacol: aderența. E foarte dificil să asiguri medicamentele celor care au cea mai mare nevoie de ele. Eu nu pot adera la un tratament antibiotic de o săptămână în această țară. Iar noi ne așteptăm ca cei din aceste zone defavorizate, care se confruntă cu nenumărate greutăți, să ia tratamente pe viață.
And the third barrier is deployment, or access. It's super hard to get these drugs to those who need them most. Not these girls but those who engage in high-risk activities, such as commercial sex work and injection drug use. In the epidemiological parlance, these groups are called "super-spreaders." And in the 1900s, a small subset of super-spreaders drove HIV along the Trans-Africa Highway and spread the virus through the continent like this. These groups are exceptionally hard to identify, they're small, they face enormous social stigma so they don't self-identify and they're the ones we need to get to the most. All of these barriers combined created the situation we have today, where greater than 15 percent of people in Southern Africa live with HIV.
Iar a treia barieră este aprovizionarea sau accesibilitatea. E foarte greu să asiguri acest tratament celor care au mai mare nevoie de el. Nu acelor fetițe, ci acelora care sunt implicați în activități cu risc crescut, cum sunt prostituția și consumul de droguri. În terminologia epidemiologică, aceste grupuri sunt denumite purtători ce transmit mult boala. În anii 1900, un grup mic de astfel de purtători au transmis virusul HIV de-a lungul autostrăzii transafricane și l-au împrăștiat astfel pe tot continentul. Aceste grupuri sunt foarte greu de identificat. Sunt mici și sunt expuse stigmatizării sociale, așa că își păstrează anonimatul. Și totuși, exact la ei trebuie să ajungem. Cumularea acestor obstacole a dus la situația actuală, în care mai mult de 15% din populația din partea de sud a Africii are HIV.
Now, conventional wisdom is: what we need to do is get more drugs to more people more effectively. I'd argue we need to solve the fundamental mismatch; we need to eliminate these barriers. If we can build therapies that mutate and transmit, we can overcome drug resistance, overcome adherence barriers, and if we do it properly, we will convert the super-spreaders from the greatest barrier to the most powerful deployment strategy that we can imagine.
Abordarea tradițională zice așa: trebuie să asigurăm mai multe medicamente, cât mai multor bolnavi, cât mai eficient. Eu aș zice că trebuie să atacăm tocmai acea discrepanță fundamentală. Trebuie să eliminăm aceste obstacole. Dacă reușim să inventăm medicamente care suferă mutații și se adaptează, putem anihila rezistența la tratamente, putem elimina barierele de aderență, și, dacă ne facem bine treaba, îi putem transforma pe purtătorii ce transmit mult boala în cea mai puternică metodă imaginabilă de răspândire a tratamentului.
This is a radical concept. It has huge potential payoff, but there's a catch. And it's serious. Before we deploy a therapy that may transmit, even if it's only in a limited population of already infected individuals, before we do this, we need to be exceptionally careful, and we need to test safety in the most rigorous ways possible. The reason I'm here today is because for the first time 20 years, we got it to work, and this is the first time I'm sharing it publicly.
E o abordare radicală. Are un potențial uriaș, dar cu o condiție. Una foarte importantă. Înainte să lansăm un tratament transmisibil, chiar și dacă vorbim de un grup mic de oameni infectați, înainte să facem asta, trebuie să fim extrem de precauți și trebuie să testăm siguranța medicamentului cu maxim de rigurozitate. Mă aflu aici deoarece, pentru prima dată în douăzeci de ani, am reușit asta și fac acest lucru public acum, pentru prima oară.
(Applause and cheers)
(Aplauze și ovații)
Last two times I did this I cried, so --
Ultimele două dăți când am spus asta am plâns, așa că...
(Laughter)
(Râsete)
So in order to help you understand this breakthrough, let me take you back 20 years to 1999. I was a graduate student in Berkeley, California, studying the biophysics of HIV. For such a complex epidemic, the simplicity of this virus fascinated me. HIV, like all viruses, is just an instruction set -- malware. It hijacks a cell and converts that cell into a factory to do one thing: single-mindedly churn out more virus. All the normal functions of the cell get wiped away. HIV infects the white blood cell that keeps us healthy. This cell has already been hijacked and converted into a factory. And if we magnify, we can see the anatomy of the virus. Those squiggly red lines in the middle? That's HIV's instruction set. Its genetic material.
Ca să înțelegeți mai bine ce înseamnă această realizare, haideți să ne întoarcem cu douăzeci de ani în urmă, în 1999. Eram absolvent al Universității Berkley, California, și studiam biofizica virusului HIV. Având în vedere complexitatea epidemiei, simplicitatea virusului mă fascina. HIV, la fel ca alte virusuri, e doar un set de instrucțiuni, un malware. Atacă celula și o transformă într-o fabrică cu un singur scop: să creeze și mai multe astfel de virusuri. Toate celelalte funcții ale celulei sunt anihilate. HIV infectează globulele albe, care ne mențin sănătoși. Această celulă a fost atacată și transformată în fabrică de HIV. Dacă mărim, putem vedea anatomia virusului. Acele liniuțe roșii din mijloc? Acela e setul de instrucțiuni HIV. Materialul genetic al virusului.
This genetic material directs the hijacking process, converting that cell into a factory first to make more copies of the instruction set, and then all the other components of the virus and assemble them into a particle. This is how the virus replicates. Each of these particles can go in and hijack a new cell. This is how the virus transmits. And every time a cell is hijacked, little mistakes are made in copying the genetic material. That's how the virus mutates. This ability to replicate, transmit and mutate is something that our current drugs cannot do.
El comandă procesul de atacare a celulelor, pe care mai întâi le transformă în fabrici, ca să asigure multiplicarea setului de instrucțiuni, apoi și a celorlalte componente ale virusului, ca la final să le asambleze într-o particulă. Așa se înmulțește virusul. Fiecare din aceste particule nou formate poate ataca mai departe o nouă celulă. Așa se transmite virusul. Și ori de câte ori o celulă e atacată, apar mici erori în copierea materialului genetic. Și astfel suferă mutații virusul. Această abilitate de a se înmulți, transmite și adapta, e ceva ce medicamentele disponibile acum nu pot face.
So, being young and naïve and a little bit ignorant, I thought: why can't we create therapies that mutate and transmit and replicate? Here was the idea. If we can take the virus and engineer it to amputate the genetic material in blue here, this amputated instruction set can no longer hijack a cell. But this amputated instruction set can do something very special. In an already infected cell, this amputated instruction set can hijack the hijacker. It can commandeer HIV's machinery to make more copies of itself, the amputated instruction set, and then each of these copies can steal all of HIV's other components so that the cell gets converted from a factory that produces virus to a factory that produces therapy. Hijackers. These carry no disease. This dramatically lowers HIV levels and keeps the cell healthier.
Așa că, tânăr, naiv și un pic ignorant fiind, m-am întrebat: de ce nu putem crea tratamente care să se adapteze, să se transmită și să se înmulțească? Aceasta era ideea: dacă putem lua virusul și să-l determinăm să-și autoelimine materialul genetic cu albastru aici, această secvență „amputată” nu mai poate ataca altă celulă. Dar tot această secvență „amputată” poate face ceva extraordinar. Într-o celulă deja infectată, ea poate ataca atacatorul. Poate comanda mecanismul HIV să o replice pe ea, secvența „amputată”, apoi fiecare din aceste copii se poate atașa la celelalte componente ale virusului, astfel încât celula atacată se transformă dintr-o fabrică de virusuri într-o fabrică de tratament. Atacatori. Aceștia nu te îmbolnăvesc. Acest proces ar scădea dramatic concentrația de HIV și ar păstra celulele mai sănătoase.
This idea consumed me for months. It was the most intense intellectual experience of my life. On every bike ride to lab, on every walk to the coffee shop, on every run in the hills above campus, the ideas, the arguments, the counterarguments, they all came so rapidly in my head, in my inner monologue, that I was physically out of breath. I thought if we can create a therapy that replicates, it would only need to be taken once. It could mutate along with the virus and possibly it could transmit between infected individuals to treat them. It was a therapy that could do all of the things that the virus could do. It solved the fundamental mismatch.
Luni de zile am fost obsedat de această idee. A fost cea mai intensă experiență intelectuală din viața mea. La fiecare drum cu bicicleta până la laborator, la fiecare drum la cafenea, la fiecare alergare pe dealurile de la marginea campusului, ideile, argumentele, contraargumentele, îmi asaltau cu atâta forță mintea, monologul interior, că rămâneam efectiv fără aer. Credeam că dacă vom putea concepe un tratament care se înmulțește, va fi suficientă o singură doză. Se va modifica apoi, la fel ca virusul, și poate se va transmite între indivizii infectați, vindecându-i. Era un tratament care putea să facă tot ce face un virus. Rezolva nepotrivirea fundamentală.
The most radical part of this concept was that the super-spreaders would also be converted from transmitting the virus to now transmitting the therapy. It was a therapy that would go viral along with the virus. This scared some people. But there's already a precedent: we already inadvertently use therapies that transmit. The vaccine that eradicated polio in the US, the oral polio vaccine, transmits between people. It's not well-known, but the fact that this vaccine transmits is part of the reason that it was chosen for the worldwide eradication effort despite its safety issues.
Cea mai radicală parte a acestui concept e faptul că purtătorii ce transmit mult boala puteau fi și ei convertiți de la a transmite virusul, la a transmite tratamentul. Un tratament care devine viral odată cu virusul. Această perspectivă i-a speriat pe unii. Dar există deja un precedent: deja am folosit, fără să ne dăm seama, tratamente care se transmit. Vaccinul care a eradicat poliomielita în SUA, vaccinul anti-poliomielitic oral, se transmite. Nu e un aspect foarte cunoscut, dar faptul că acest vaccin se transmite e parte din motivul pentru care a fost ales în demersul global de eradicare a bolii, în ciuda problemelor de siguranță a administrării.
So the bigger problem was that these hijacker therapies didn't exist. My Berkeley advisors said to me, "Lovely idea, so sad it will never work," or, "Regulators will never allow it, drop it." But the idea wouldn't drop me.
Marea problemă era că aceste tratamente „atacatoare” nu existau. Mentorii mei de la Berkley mi-au spus: „Drăguță idee, păcat că nu va funcționa niciodată.” sau: „Autoritățile n-o vor aviza niciodată, las-o baltă.” Dar ideea nu mă lăsa ea pe mine.
If it ever worked, it would solve the fundamental mismatch. So we tried for years to build it. We tried every trick in the book and failed over and over again. We -- every time we thought we had a good idea, we'd spend months, sometimes years working on it only to come up empty. We once spent five years building 150,000 versions of a hijacker therapy. Every single one failed. I once asked a really bright student what he hoped to learn from me during his PhD --
Dacă avea cea mai mică șansă de reușită, putea rezolva acea nepotrivire fundamentală. Așa că am muncit la ea ani de zile. Am testat toate strategiile și am avut eșec după eșec. Am... de câte ori ni se părea că avem o idee bună, munceam la ea luni, uneori poate chiar ani de zile, doar ca să ne întoarcem de unde am plecat. La un moment dat am petrecut cinci ani construind 150.000 de variante pentru un astfel de tratament. Absolut toate au eșuat. Odată, am întrebat un student foarte bun ce crede că va învăța de la mine în timpul doctoratului
(Laughter)
(Râsete)
And he replied, "How to keep going, how to continue moving forward despite zero evidence that there's anything there."
și mi-a spus: „Cum să perseverezi, cum să încerci din nou și din nou chiar dacă sunt zero dovezi că vei găsi ceva.
(Laughter)
(Râsete)
I wonder if he was trying to tell me something.
Mă întreb dacă bătea vreun apropo.
(Laughter)
(Râsete)
By 2018, things looked bad. There was no evidence that a hijacker therapy could be engineered. In fact, we had evidence that it might be impossible. It was time to face the hard truth. This solution that I'd wanted so badly, this hijacker therapy just didn't exist. For 20 years, I had been chasing a ghost.
Prin 2018, lucrurile nu erau prea roz. Nu aveam nicio dovadă că un astfel de tratament poate fi obținut. Dimpotrivă, aveam dovezi că așa ceva e imposibil. Venise timpul să recunosc adevărul necruțător. Această soluție pe care mi-o dorisem atât de mult, acest tratament „viral” pur și simplu nu exista. Timp de douăzeci de ani am alergat după o himeră.
Then one day, Elizabeth, a postdoc in my lab, came to me with this picture. It doesn't look like much. My wife thinks it looks like a pregnancy test.
Dar într-o zi, Elizabeth, o cercetătoare din laboratorul meu, a venit la mine cu o poză. Nu părea a fi mare lucru. Soția mea zicea că seamănă cu un test de sarcină.
(Laughter)
(Râsete)
But this little band down here -- that was the amputated genetic material that we had been looking for for 20 years. The entire time that we had been trying to build it and failing, it had evolved by itself in a flask in the back of the lab.
Dar această liniuță de aici este materialul genetic „amputat” pe care îl căutam de douăzeci de ani. În tot acest timp în care am eșuat încercând să-l construim, a evoluat de la sine într-o eprubetă uitată de prin laborator.
(Audience) What?
(Auditoriul) Poftim?
(Laughter)
(Râsete)
We finally had a foothold. And we used this to build the first hijacker. But we had no evidence that what we built was a therapy.
În sfârșit aveam ceva. Și am folosit această secvență ca să construim primul tratament. Dar nu aveam nicio dovadă că ceea ce obținusem era un tratament.
The first hurdle that any therapy has to clear is testing in a mouse. It can be risky. In our case, if our mice died, so did our funding, and with it, any hopes of this becoming a therapy, let alone a transformative one. After so many failures, we were all pretty skeptical but we didn't really have an alternative. We had to give it a shot; we had to try.
Primul hop pe care orice tratament trebuie să-l treacă e testarea pe cobai. Poate fi riscant. În cazul nostru, dacă mureau cobaii, dispărea și finanțarea proiectului și odată cu ea orice speranță de a obține vreodată un tratament, mai ales unul atât de radical cum speram. După atâtea eșecuri eram cu toții destul de neîncrezători, dar nici nu prea aveam altă șansă. Trebuia să ne asumăm riscul și să încercăm.
Amazingly, the hijacker therapy worked in a mouse, and it worked exactly as we'd predicted 20 years before. It protected the cells in a mouse from HIV. Here are the cells under a microscope. First, HIV in red infects those cells, and then the hijacker, in blue, can be activated, protects those cells and transmits to other cells. We'd finally built the hijacker after 20 years. Everyone in the lab was elated. For me, this was proof of concept. If we could do it for one virus we could do it for others.
În mod surprinzător, tratamentul radical a avut efect asupra cobaiului și a funcționat exact așa cum prezisesem acum douăzeci de ani. A protejat celulele cobaiului împotriva virusului HIV. Iată o vedere a celulelor la microscop. Mai întâi, cu roșu, vedeți HIV infectând acele celule, iar apoi, tratamentul radical, în albastru, își face efectul și protejează acele celule și se răspândește și în alte celule. În sfârșit, după douăzeci de ani, am conceput acest tratament. Toți cei care lucrau în laborator erau în extaz. Pentru mine, aceasta era dovada vie a conceptului. Dacă am putut face asta cu un virus, vom putea și cu altele.
To understand how this hijacker might impact HIV levels worldwide, we ran computer simulations. Epidemiological models. And the results were pretty amazing. If we do nothing in the hardest-hit parts of Africa, HIV prevalence will stay between 25 and 30 percent. If we manage to introduce drugs to three-quarters of the population or if we ever get the long-sought-after vaccine, we would reduce those numbers down to 20 percent. But those are best-case scenarios. If HIV evolves resistance or if people change their behaviors, these numbers could go right back up to 30 percent or even beyond. The blue is the hijacker therapy. And we've not found a way, either theoretically or experimentally, that HIV can evolve resistance to the hijacker.
Pentru a înțelege impactul global al acestui tratament asupra HIV, am rulat simulări pe calculator. Modele epidemiologice. Iar rezultatele au fost chiar uimitoare. Dacă nu luăm nicio măsură în zona cea mai afectată a Africii, infectarea cu HIV se va menține între 25 și 35 de procente. Dar dacă reușim să asigurăm medicamente pentru două treimi din populație sau dacă reușim să asigurăm mult-așteptatul vaccin, putem reduce rata la douăzeci de procente. Dar acestea sunt scenariile cele mai optimiste. Dacă HIV devine la rândul lui mai rezistent sau dacă populația își modifică comportamentul, procentul poate urca din nou la treizeci de procente sau chiar mai mult. Cu albastru e tratamentul nostru radical. Încă nu am găsit o modalitate, teoretică sau experimentală, prin care HIV să devină rezistent la acest tratament.
The reason this hijacker works so well is the super-spreaders. If the hijacker is introduced in one place over here, the super-spreaders can pick it up and transmit it through the population. Imagine if 10 years from now, HIV is no longer a pandemic.
Motivul eficacității crescute a acestui tratament sunt purtătorii. Dacă tratamentul este inoculat într-o locație aici, purtătorii îl preiau și îl împrăștie în rândul populației. Imaginați-vă că peste zece ani HIV nu mai e o pandemie.
To get there, we have to start large-scale clinical trials in five years, which means initial human tests next year. The FDA has cleared us to start testing in HIV-positive patients who have a terminal cancer and have less than a year left to live. Volunteering for this trial is their last incredibly generous gift to the world. They're called the "Last Gift cohort." And to test in these altruistic patients next year, we have to finish our preclinical tests this year ... and I think we will.
Ca să ajungem acolo, înseamnă ca peste cinci ani să demarăm testări clinice la scară largă, ceea ce înseamnă să începem la anul testările pe oameni. FDA ne-a dat avizul să începem să testăm pe pacienți seropozitivi care suferă de cancer terminal și au mai puțin de un an de trăit. Să se ofere voluntar pentru aceste testări e un ultim gest de maximă generozitate față de ceilalți. I-am numit „Cohorta Ultimului Dar”. Ca să putem începe testele cu acești pacienți altruiști trebuie să terminăm testele pre-clinice anul acesta și cred că vom reuși.
I still meet colleagues who push back and are stridently opposed to letting us move forward with testing. They say, "What if something goes wrong? You can't unrelease it." They say, "There are ethical issues; people can't consent." Well, oral polio vaccine faced similar ethical and safety concerns. In fact, oral polio vaccine faced such an effective misinformation campaign that most people still don't know that it transmits, that it successfully eradicated polio in many countries or that this vaccine is the basis for new vaccines. When we presented this hijacker therapy idea in Africa last year, the African scientists had a different response. They said, "How can you not test this?" They said it's unethical to not test it. So even though we might fail, I think the stakes are too high not to try. If we do nothing, those girls outside of Durban will acquire HIV, and the next time that there's a new virus that emerges, we'll be in the same vulnerable position that we are today with quarantines that are porous and vaccines that we need to wait months for that may not match.
Încă întâlnesc colegi care sunt împotrivă și manifestă o zgomotoasă opoziție în a fi lăsați să testăm mai departe. Ei spun: „Dacă ceva nu merge bine? Nu veți mai putea repara ce ați făcut.” Sau spun: „Există implicații etice; oamenii nu vor fi de acord cu așa ceva.” Dar și vaccinul anti-poliomielitic s-a confruntat cu o opoziție similară. De fapt, a avut parte de o așa campanie de dezinformare, încât mulți încă nu știu că el se transmite, sau că a eradicat cu succes boala în multe țări, sau că a stat la baza creării multor altor vaccinuri. Când am prezentat anul trecut în Africa conceptul acestui tratament radical, oamenii de știință africani au reacționat cu totul altfel. Au spus: „Cum să nu testați așa ceva?” Ba chiar au spus că ar fi neetic să nu îl testăm. Deci, chiar dacă vom eșua, cred că miza e mult prea mare ca să nu încercăm. Dacă nu facem nimic, acele fetițe din suburbiile Durban-ului vor contracta HIV, și cu proxima ocazie cu care va apărea un nou virus, vom fi la fel de vulnerabili precum suntem și astăzi, cu carantinele noastre precare și cu vaccinuri pentru care trebuie să așteptăm cu lunile, fără nicio garanție.
I think it's time for a new approach that's different than the static approaches of the last century. It's time for a new technology that is less reactive and more proactive. I think it's time for treatments that don't just benefit the most affluent among us but also those who face the greatest adversity. I think it's time for a new type of weapon that matches, or that solves the fundamental mismatch. I think it's time for therapies that can go viral.
Cred că a venit vremea pentru o abordare nouă, diferită de abordarea statică a ultimului secol. E timpul pentru o nouă tehnologie, mai puțin reactivă și mai degrabă proactivă. Cred că a sosit timpul pentru tratamente accesibile nu doar celor avuți, dar și celor care se confruntă cu nenumărate lipsuri. Cred că e timpul pentru un nou tip de armă care să fie pe măsură, sau să rezolve această discrepanță fundamentală. Cred că e timpul pentru tratamente care să devină virale.
Thank you very much.
Vă mulțumesc foarte mult!
(Applause)
(Aplauze)