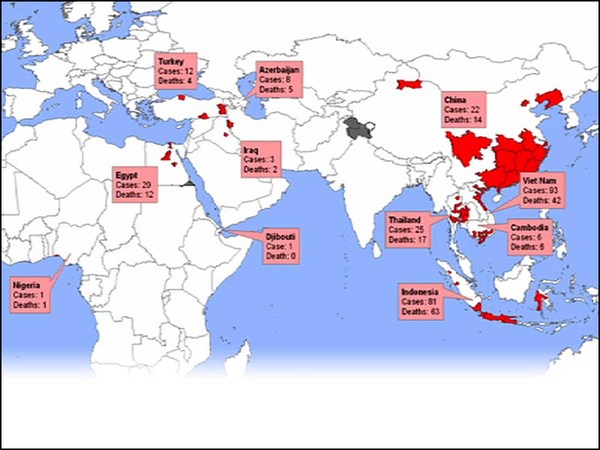
I want to tell you about a student of mine. A few weeks ago, she was on vacation when at 3am she got a phone call. It was her husband telling her that the city that she was in would be quarantined by 10am. She was in Wuhan, China. The epicenter of the coronavirus outbreak. By 8am she was on the road in a friend's car driving 500 miles to Shanghai Airport. The entire time, she was terrified the authorities would arrest her. She made it out on one of the last flights.
Ik wil jullie wat vertellen over een van mijn studenten. Enkele weken geleden was ze op vakantie toen ze om 3 uur 's nachts werd opgebeld. Haar echtgenoot zei haar dat haar stad om 10 uur onder quarantaine zou worden geplaatst. Ze was in Wuhan in China, het epicentrum van de corona-uitbraak. Om 8 uur was ze onderweg in een auto van een vriend naar Shangai Airport op 800 km afstand. De hele tijd was ze ongerust dat de autoriteiten haar zouden aanhouden. Zo kon net op tijd een van de laatste vluchten halen.
So we're all relieved that she's back home, safe in the US. But what if I told you she was in this room? What if I told you she was sitting next to you? There's no vaccine. There won't be a vaccine for at least 12 months. And this virus is mutating, so there's no guarantee that the vaccine that we produce 12 months from now will match the mutated virus. We're always playing catch-up. And this is the scenario we're in every time there's an outbreak. Our quarantines are porous, our medical responses are flat-footed.
We zijn allemaal blij dat ze terug thuis is, veilig in de Verenigde Staten. Maar wat als ik jullie zou vertellen dat ze in deze zaal zou zijn? Wat als ik zou zeggen dat ze naast je zou zitten. Er is geen vaccin. Er zal geen vaccin zijn in tenminste de eerste 12 maanden. En dit virus muteert, dus is er geen garantie dat het vaccin dat we binnen 12 maanden zullen produceren, zal passen bij het gemuteerde virus. We hinken altijd achterop. En dat scenario herhaalt zich telkens als er een uitbraak is. Onze quarantaines zijn poreus, onze medische tussenkomsten schieten altijd tekort.
The fundamental problem that we face in controlling these outbreaks is that viruses and other infections do two things really well: they mutate and they transmit. Our medical tools do neither of these two things. Our medical tools don't mutate or transmit. We have a fundamental mismatch between our tools, which are static, and the infections, which are dynamic. This mismatch is why we're always flat-footed. This mismatch is why we're playing catch-up. And this mismatch is universal. It's the reason that we have antibiotic-resistant infections that killed 40,000 Americans last year, and it's the reason that the flu vaccine couldn't prevent the flu from killing 60,000 Americans last year. So how do we resolve this fundamental mismatch?
Het fundamentele probleem bij het onder controle krijgen van deze uitbraken is dat virussen en andere infecties erg goed zijn in twee dingen: ze muteren en ze worden overgedragen. Onze medische hulpmiddelen doen geen van beide. Onze medische hulpmiddelen muteren niet en worden niet overgedragen. Er is een fundamentele onaangepastheid tussen onze hulpmiddelen, die statisch zijn, en de infecties, die dynamisch zijn. Door dit verschil komen we altijd achterop gehinkt. Door dit verschil zijn we altijd op inhalen aangewezen. En deze onaangepastheid is algemeen. Daarom krijgen we infecties waarop antibiotica geen pak hebben, en die vorig jaar 40.000 Amerikanen doodden. En het is de reden waarom het griepvaccin de griep niet kon beletten om vorig jaar 60.000 Amerikanen te doden. Hoe lossen we deze fundamentele onaangepastheid op.
I've devoted my career to studying and solving this problem. For 100 years, we've used chemicals as drugs to treat infections. Chemicals will never mutate or transmit. Similarly, our vaccines are not designed to mutate or transmit. 20 years ago, I had a radical idea to use the viruses themselves as therapies -- as building blocks for therapies. To build therapies that could mutate and transmit. Let me share with you how we've had a major breakthrough, and we're already testing these new therapies.
Ik wijdde mijn loopbaan aan het bestuderen en oplossen van dit probleem. Honderd jaar lang gebruiken we al chemicaliën als geneesmiddelen voor infecties. Chemicaliën zullen nooit muteren of worden doorgegeven. Ook onze vaccins zijn niet ontworpen om te muteren of om te worden doorgegeven. Twintig jaar terug had ik een radicaal idee om virussen zelf als therapie te gebruiken -- als bouwsteen voor een therapie. Om therapieën te maken die konden muteren en worden doorgeven. Ik vertel jullie hoe we tot een grote doorbraak kwamen en dat we deze nieuwe therapieën al aan het testen zijn.
HIV is the most devastating pandemic of our era. 75 million infected; 33 million dead. Most of us think that HIV is a solved problem. We have truly amazing antiviral drugs: they're safe and effective, and we've spent 15 years and billions of dollars deploying these drugs around the world. So let's look at the numbers.
Hiv is de meest verwoestende pandemie van onze tijd. 75 miljoen geïnfecteerden; 33 miljoen doden. De meesten van ons denken dat hiv een opgelost probleem is. We hebben al echt wonderlijke geneesmiddelen: ze zijn veilig en werkzaam, en we hadden 15 jaar en miljarden dollars nodig om deze geneesmiddelen over de wereld te verdelen. We kijken eens naar de cijfers.
In 2019, 1.7 million people acquired HIV. This number only hit home for me last year when I visited this rural village outside of Durban, South Africa. I was driving along this dirt road with my 10-year-old daughter in the back seat, and walking next to us on the side of the road were girls, the same age as my daughter, barefoot. My daughter asked about why these girls are barefoot and I had to explain disparity to her, which was hard. But what really shocked me was when my colleagues, the local African scientists explained to me that these young girls the same age as my daughter --
In 2019 werden 1,7 miljoen mensen besmet met hiv. Van dat aantal werd ik me pas echt bewust toen ik een landelijk dorp bij Durban in Zuid Afrika bezocht. Ik reed over een veldweg met mijn tien jaar oude dochter achterop. Langs de weg liepen meisjes van de leeftijd van mijn dochter, blootsvoets. Mijn dochter vroeg waarom ze blootsvoets liepen en ik moest haar ongelijkheid uitleggen, wat niet meeviel. Maar wat me echt schokte, was toen mijn collega's, de plaatselijke Afrikaanse wetenschappers, me uitlegden dat deze meisjes, even oud als mijn dochter --
(Breathes)
(Zoekt naar zijn adem)
sorry -- had an 80 percent chance of acquiring HIV in their lifetime. It blew me away. How can these girls have an 80 percent risk if we have safe and effective drugs?
sorry -- 80% kans liepen om in hun leven hiv op te lopen. Dat schokte me. Hoe kunnen deze meisjes 80% kans op hiv lopen als we veilige en werkzame geneesmiddelen hebben?
The reason is the fundamental mismatch. It creates barriers to controlling infectious disease, particularly in resource-limited settings. The first barrier is mutation: viruses mutate, our drugs don't. The second barrier: adherence. It's really hard to get these drugs to those who need the most. I can't even adhere to a week-long antibiotic regimen in this country. We're asking those in resource-limited settings who face enormous adversity to adhere to lifelong regimens.
De reden is de fundamentele onaangepastheid. Ze verhindert het in toom houden van besmettelijke ziekten, vooral waar de middelen begrensd zijn. De eerste hindernis is mutatie: virussen muteren, onze geneesmiddelen niet. De tweede hindernis: discipline. Het is echt moeilijk de geneesmiddelen te krijgen waar ze het hardst nodig zijn. Ik houdt een antibioticakuur van één week zelfs niet vol in dit land. En we vragen aan mensen met beperkte middelen en met enorme moeilijkheden om levenslange kuren vol te houden.
And the third barrier is deployment, or access. It's super hard to get these drugs to those who need them most. Not these girls but those who engage in high-risk activities, such as commercial sex work and injection drug use. In the epidemiological parlance, these groups are called "super-spreaders." And in the 1900s, a small subset of super-spreaders drove HIV along the Trans-Africa Highway and spread the virus through the continent like this. These groups are exceptionally hard to identify, they're small, they face enormous social stigma so they don't self-identify and they're the ones we need to get to the most. All of these barriers combined created the situation we have today, where greater than 15 percent of people in Southern Africa live with HIV.
En de derde hindernis is inzetbaarheid, of toegang. Het is supermoeilijk om deze geneesmiddelen te brengen bij wie ze het hardst nodig heeft. Niet deze meisjes, maar bij degenen die risicovolle activiteiten uitvoeren, zoals commercieel sekswerk of injectie van drugs. In het epidemiologisch woordgebruik heten deze groepen 'superverspreiders'. In de vorige eeuw voerden een kleine groep superverspreiders hiv met zich mee langs de Trans-Africa Highway en verspreidden zo het virus. Deze groepen zijn erg moeilijk te identificeren, ze zijn klein en dragen een enorm sociaal stigma, dus maken ze zich niet kenbaar. En net zij zijn het die we moeten vinden. Al deze hindernissen veroorzaken de situatie van vandaag, waarin meer dan 15% van de bevolking van Zuid Afrika met hiv leeft.
Now, conventional wisdom is: what we need to do is get more drugs to more people more effectively. I'd argue we need to solve the fundamental mismatch; we need to eliminate these barriers. If we can build therapies that mutate and transmit, we can overcome drug resistance, overcome adherence barriers, and if we do it properly, we will convert the super-spreaders from the greatest barrier to the most powerful deployment strategy that we can imagine.
Nu is de conventionele wijsheid: we moeten zorgen dat meer geneesmiddelen bij meer mensen effectiever terechtkomen. Ik pleit ervoor om deze fundamentele onaangepastheid op te lossen; we moeten deze hindernissen verwijderen. Als we therapieën kunnen ontwerpen die muteren en doorgegeven worden, dan verhelpen we geneesmiddelenresistentie, problemen met de discipline, en als we het goed doen, dan veranderen we de superverspreiders van de grootste hindernis in de krachtigste inzetstrategie die we kunnen bedenken.
This is a radical concept. It has huge potential payoff, but there's a catch. And it's serious. Before we deploy a therapy that may transmit, even if it's only in a limited population of already infected individuals, before we do this, we need to be exceptionally careful, and we need to test safety in the most rigorous ways possible. The reason I'm here today is because for the first time 20 years, we got it to work, and this is the first time I'm sharing it publicly.
Dat is een radicaal concept. Het heeft een enorm voordeel, maar er is een valkuil. En een serieuze. Voordat we een overdraagbare therapie gaan ontplooien, ook al is het in een beperkte populatie van al geïnfecteerde individuen, voordat we dit doen, moeten we uitzonderlijk voorzichtig zijn en de veiligheid ervan zo rigoureus mogelijk testen. In sta hier vandaag omdat we het, voor de eerste keer in 20 jaar, aan het werk kregen, en dit is ook de eerste keer dat ik het publiekelijk maak.
(Applause and cheers)
(Applaus en gejuich)
Last two times I did this I cried, so --
De twee keer dat ik dit deed, kwamen er tranen, dus --
(Laughter)
(Gelach)
So in order to help you understand this breakthrough, let me take you back 20 years to 1999. I was a graduate student in Berkeley, California, studying the biophysics of HIV. For such a complex epidemic, the simplicity of this virus fascinated me. HIV, like all viruses, is just an instruction set -- malware. It hijacks a cell and converts that cell into a factory to do one thing: single-mindedly churn out more virus. All the normal functions of the cell get wiped away. HIV infects the white blood cell that keeps us healthy. This cell has already been hijacked and converted into a factory. And if we magnify, we can see the anatomy of the virus. Those squiggly red lines in the middle? That's HIV's instruction set. Its genetic material.
Om jullie deze doorbraak te laten begrijpen, neem ik jullie 20 jaar mee terug naar 1999. Ik was afgestudeerd aan Berkeley in Californië op een studie van de biofysica van hiv. Voor zulke complexe epidemie fascineerde me de eenvoud van het virus. Hiv is, zoals alle virussen, alleen maar een verzameling instructies -- malware. Het kaapt een cel en maakt van die cel een fabriek van één ding: alleen maar meer virussen. Alle normale functies van de cel worden onderdrukt. Hiv infecteert de witte bloedcellen die ons gezond houden. Deze cel is al gekaapt en veranderd in een fabriek. Als we vergroten, kunnen we de anatomie van het virus zien. Die rode kronkels in het midden? Dat is de verzameling instructies van hiv. Het genetisch materiaal ervan.
This genetic material directs the hijacking process, converting that cell into a factory first to make more copies of the instruction set, and then all the other components of the virus and assemble them into a particle. This is how the virus replicates. Each of these particles can go in and hijack a new cell. This is how the virus transmits. And every time a cell is hijacked, little mistakes are made in copying the genetic material. That's how the virus mutates. This ability to replicate, transmit and mutate is something that our current drugs cannot do.
Dat genetisch materiaal stuurt het kapingsproces, verandert eerst de cel in een fabriek om meer kopieën van de instructieset te maken, en daarna alle andere componenten van het virus om ze dan te combineren tot een virusdeeltje. Zo plant het virus zich voort. Elk van deze deeltjes kan opnieuw andere cellen kapen. Zo wordt het virus doorgegeven. En telkens er een cel wordt gekaapt, ontstaan er foutjes bij het kopiëren van het genetisch materiaal. Zo muteert het virus. Dit voortplanten, overgaan en muteren is iets dat onze huidige geneesmiddelen niet kunnen.
So, being young and naïve and a little bit ignorant, I thought: why can't we create therapies that mutate and transmit and replicate? Here was the idea. If we can take the virus and engineer it to amputate the genetic material in blue here, this amputated instruction set can no longer hijack a cell. But this amputated instruction set can do something very special. In an already infected cell, this amputated instruction set can hijack the hijacker. It can commandeer HIV's machinery to make more copies of itself, the amputated instruction set, and then each of these copies can steal all of HIV's other components so that the cell gets converted from a factory that produces virus to a factory that produces therapy. Hijackers. These carry no disease. This dramatically lowers HIV levels and keeps the cell healthier.
Dus, jong, naïef en wat onwetend, dacht ik: waarom kunnen we geen therapieën bedenken die muteren, doorgegeven en gerepliceerd worden? Hier komt het idee. Als we het virus nemen en het bewerken om het genetisch materiaal, in blauw daar, te amputeren, dan kunnen de geamputeerde instructies de cel niet langer kapen. Maar deze geamputeerde instructies kunnen iets heel speciaals. In een reeds geïnfecteerde cel kan de geamputeerde instructieset de kaper kapen. Het kan de machinerie van hiv bevelen meer kopieën van zichzelf te maken, de geamputeerde instructies, en dan kunnen al deze kopieën alle andere hiv-componenten stelen, zodat de cel van een virusfabriek wordt veranderd in een therapiefabriek. Kapers. Deze dragen geen ziekte. Dit vermindert het hivgehalte dramatisch en houdt de cellen gezonder.
This idea consumed me for months. It was the most intense intellectual experience of my life. On every bike ride to lab, on every walk to the coffee shop, on every run in the hills above campus, the ideas, the arguments, the counterarguments, they all came so rapidly in my head, in my inner monologue, that I was physically out of breath. I thought if we can create a therapy that replicates, it would only need to be taken once. It could mutate along with the virus and possibly it could transmit between infected individuals to treat them. It was a therapy that could do all of the things that the virus could do. It solved the fundamental mismatch.
Het idee hield me maandenlang bezig. Het was de meest intense intellectuele ervaring van mijn leven. Bij elke fietsrit naar mijn lab, bij elke wandeling naar de koffieshop, bij elke run in de heuvels bij de campus buitelden de ideeën, de argumenten, de tegenargumenten, zo intens door mijn hoofd in mijn inwendige monoloog, dat ik fysisch buiten adem was. Ik dacht dat als we een therapie konden maken die repliceert, ze slechts één keer moest worden genomen. Ze kon met het virus mee muteren en mogelijks tussen geïnfecteerde individuen worden doorgegeven om ze te behandelen. Het zou een therapie zijn die alles zou kunnen wat een virus kon. Ze zou een fundamentele onaangepastheid oplossen.
The most radical part of this concept was that the super-spreaders would also be converted from transmitting the virus to now transmitting the therapy. It was a therapy that would go viral along with the virus. This scared some people. But there's already a precedent: we already inadvertently use therapies that transmit. The vaccine that eradicated polio in the US, the oral polio vaccine, transmits between people. It's not well-known, but the fact that this vaccine transmits is part of the reason that it was chosen for the worldwide eradication effort despite its safety issues.
Het ingrijpendste deel van dit concept was dat de superverspreiders ook zouden worden veranderd van virusdoorgevers naar therapiedoorgevers. Het was een therapie die viraal zou gaan samen met het virus. Dat joeg sommige mensen angst aan. Maar er was al een precedent: we gebruiken al ongewild therapieën die worden doorgegeven. Het vaccin dat polio uitroeide in de VS, het orale poliovaccin, wordt tussen mensen doorgegeven. Het is niet al te bekend, maar het feit dat het vaccin wordt overgedragen, is deels de reden dat het werd uitverkozen om het virus op wereldschaal uit te roeien ondanks de veiligheidsbezwaren.
So the bigger problem was that these hijacker therapies didn't exist. My Berkeley advisors said to me, "Lovely idea, so sad it will never work," or, "Regulators will never allow it, drop it." But the idea wouldn't drop me.
Het grotere probleem was dat deze kapertherapieën niet bestonden. Mijn raadgevers in Berkeley zegden me: "Mooi idee, spijtig dat het nooit zal werken." Of: "Regelgevers zullen het nooit toelaten, laat het los." Maar het idee liet mij niet los.
If it ever worked, it would solve the fundamental mismatch. So we tried for years to build it. We tried every trick in the book and failed over and over again. We -- every time we thought we had a good idea, we'd spend months, sometimes years working on it only to come up empty. We once spent five years building 150,000 versions of a hijacker therapy. Every single one failed. I once asked a really bright student what he hoped to learn from me during his PhD --
Als het ooit zou werken, zou het de fundamentele onaangepastheid oplossen. Dus werkten we er jaren aan om het te maken. We probeerden elke bekende truc uit en mislukten keer op keer. We -- telkens we een goed idee hadden, besteedden we maanden, soms jaren, om het uit te werken om het te zien mislukken. We besteedden ooit vijf jaren aan het bouwen van 150.000 versies van een kapertherapie. Elk ervan mislukte. Ik vroeg ooit aan een echt knappe student wat hij hoopte van me te leren tijdens zijn doctoraat
(Laughter)
(Gelach)
And he replied, "How to keep going, how to continue moving forward despite zero evidence that there's anything there."
en hij antwoordde: "Hoe te blijven doorgaan, hoe te blijven vooruitgaan ondanks nul bewijs dat er iets in zit."
(Laughter)
(Gelach)
I wonder if he was trying to tell me something.
Ik vraag me af of hij me iets probeerde te zeggen.
(Laughter)
(Gelach)
By 2018, things looked bad. There was no evidence that a hijacker therapy could be engineered. In fact, we had evidence that it might be impossible. It was time to face the hard truth. This solution that I'd wanted so badly, this hijacker therapy just didn't exist. For 20 years, I had been chasing a ghost.
Tegen 2018 zag het er slecht uit. Er was geen bewijs dat een kapertherapie kon worden gebouwd. In feite hadden we bewijs dat het wel eens onmogelijk zou kunnen zijn. Tijd om de feiten onder ogen te zien. Die oplossing die ik zo hard wilde, die kapertherapie, bestond gewoon niet. Twintig jaar lang had ik een drogbeeld nagejaagd.
Then one day, Elizabeth, a postdoc in my lab, came to me with this picture. It doesn't look like much. My wife thinks it looks like a pregnancy test.
Toen kwam op een dag Elizabeth, een postdoc in mijn lab, naar me toe met deze foto. Het lijkt op niet veel. Mijn vrouw vindt het op een zwangerschapstest lijken.
(Laughter)
(Gelach)
But this little band down here -- that was the amputated genetic material that we had been looking for for 20 years. The entire time that we had been trying to build it and failing, it had evolved by itself in a flask in the back of the lab.
Maar dat kleine streepje daar -- was het geamputeerde genetisch materiaal waar we al 20 jaar naar zochten. De hele tijd dat we het vruchteloos hadden proberen te maken, was het uit zichzelf geëvolueerd in een fles achterin het lab.
(Audience) What?
(Publiek) Wat?
(Laughter)
(Gelach)
We finally had a foothold. And we used this to build the first hijacker. But we had no evidence that what we built was a therapy.
Eindelijk hadden we een steunpunt. En daarmee bouwden we onze eerste kaper. Maar we hadden geen bewijs dat wat we maakten een therapie was.
The first hurdle that any therapy has to clear is testing in a mouse. It can be risky. In our case, if our mice died, so did our funding, and with it, any hopes of this becoming a therapy, let alone a transformative one. After so many failures, we were all pretty skeptical but we didn't really have an alternative. We had to give it a shot; we had to try.
De eerste horde die elke therapie moet nemen, is het testen met muizen. Dat is riskant. Als onze muizen doodgingen, ging onze financiering dezelfde weg en daarmee alle hoop dat dit ooit een therapie zou worden, laat staan een baanbrekende. Na zovele mislukkingen waren we allemaal nogal sceptisch, maar we hadden geen alternatief. We moesten een poging ondernemen; we moesten het proberen.
Amazingly, the hijacker therapy worked in a mouse, and it worked exactly as we'd predicted 20 years before. It protected the cells in a mouse from HIV. Here are the cells under a microscope. First, HIV in red infects those cells, and then the hijacker, in blue, can be activated, protects those cells and transmits to other cells. We'd finally built the hijacker after 20 years. Everyone in the lab was elated. For me, this was proof of concept. If we could do it for one virus we could do it for others.
Tot onze verbazing werkte de kapertherapie in een muis en wel net zoals we het 20 jaar geleden hadden voorspeld. Ze beschermde de cellen van een muis tegen hiv. Hier zie je de cellen onder de microscoop. Eerst infecteert hiv, in rood, deze cellen en dan kan de kaper, in blauw, geactiveerd worden, beschermt die cellen en wordt doorgegeven naar andere cellen. Eindelijk lukte het ons om na 20 jaar de kaper te maken. Iedereen in het lab in de wolken. Voor mij was dit het bewijs van het concept. Als we het konden met één virus, dan kon het ook met andere.
To understand how this hijacker might impact HIV levels worldwide, we ran computer simulations. Epidemiological models. And the results were pretty amazing. If we do nothing in the hardest-hit parts of Africa, HIV prevalence will stay between 25 and 30 percent. If we manage to introduce drugs to three-quarters of the population or if we ever get the long-sought-after vaccine, we would reduce those numbers down to 20 percent. But those are best-case scenarios. If HIV evolves resistance or if people change their behaviors, these numbers could go right back up to 30 percent or even beyond. The blue is the hijacker therapy. And we've not found a way, either theoretically or experimentally, that HIV can evolve resistance to the hijacker.
Om te begrijpen hoe deze kaper hiv-niveaus mondiaal kon beïnvloeden, lieten we computersimulaties lopen. Epidemiologische modellen. En de resultaten waren nogal verbazend. Als we niets doen in de hardst getroffen gebieden van Afrika, zal hiv daar tussen 25 en 30% blijven voorkomen. Als we erin slagen aan drie vierde van de bevolking geneesmiddelen te verstrekken of als we het vaccin vinden waarnaar we zolang zochten, zouden we dit kunnen herleiden tot 20%. Maar alleen in de beste gevallen. Als hiv weerstand ontwikkelt of als mensen van gedrag veranderen, kunnen deze cijfers terug stijgen naar 30% of zelfs hoger. Het blauwe is de kapertherapie. En we vonden geen enkele manier, noch theoretisch, noch experimenteel, waarop hiv weerstand tegen de kaper kan ontwikkelen.
The reason this hijacker works so well is the super-spreaders. If the hijacker is introduced in one place over here, the super-spreaders can pick it up and transmit it through the population. Imagine if 10 years from now, HIV is no longer a pandemic.
Net door de superverspreiders werkt deze kaper zo goed. Als deze kaper op één plaats hier wordt geïntroduceerd, kunnen de superverspreiders hem oppikken en het doorgeven doorheen de bevolking. Stel je voor dat in 10 jaar na nu hiv niet langer een pandemie is.
To get there, we have to start large-scale clinical trials in five years, which means initial human tests next year. The FDA has cleared us to start testing in HIV-positive patients who have a terminal cancer and have less than a year left to live. Volunteering for this trial is their last incredibly generous gift to the world. They're called the "Last Gift cohort." And to test in these altruistic patients next year, we have to finish our preclinical tests this year ... and I think we will.
Om dat te bereiken moeten we binnen vijf jaar beginnen met klinische testen op grote schaal, wat neerkomt op de eerste testen op mensen het volgende jaar. De FDA gaf ons de toelating om met testen te beginnen op hiv-positieve patiënten die een terminale kanker hebben en minder dan een jaar te leven hebben. Vrijwilliger zijn voor dit onderzoek is hun laatste ongelooflijk genereuze gift aan de wereld. Ze worden de 'Last Gift cohort' genoemd. Om deze altruïstische patiënten volgend jaar te testen, moeten we onze preklinische testen dit jaar afsluiten ... en ik denk dat dat zal lukken.
I still meet colleagues who push back and are stridently opposed to letting us move forward with testing. They say, "What if something goes wrong? You can't unrelease it." They say, "There are ethical issues; people can't consent." Well, oral polio vaccine faced similar ethical and safety concerns. In fact, oral polio vaccine faced such an effective misinformation campaign that most people still don't know that it transmits, that it successfully eradicated polio in many countries or that this vaccine is the basis for new vaccines. When we presented this hijacker therapy idea in Africa last year, the African scientists had a different response. They said, "How can you not test this?" They said it's unethical to not test it. So even though we might fail, I think the stakes are too high not to try. If we do nothing, those girls outside of Durban will acquire HIV, and the next time that there's a new virus that emerges, we'll be in the same vulnerable position that we are today with quarantines that are porous and vaccines that we need to wait months for that may not match.
Ik ontmoet nog altijd collega's die niet akkoord gaan en zich hard verzetten tegen onze plannen om te testen. Ze zeggen: "Wat als er iets misgaat? Je kan het niet terugdraaien." Ze zeggen: "Er zijn ethische bezwaren; mensen kunnen niet toestemmen." Wel, het poliovaccin stuitte op gelijkaardige ethische en veiligheidsbezwaren. In feite werd er rond het poliovaccin zo'n effectieve desinformatiecampagne gevoerd, dat de meeste mensen niet eens weten dat het overdraagbaar is, dat het polio in veel landen succesvol uitroeide of dat dit vaccin de basis is voor nieuwe vaccins. Toen we vorig jaar in Afrika de kapertherapie voorstelden, reageerden de Afrikaanse wetenschappers anders. Ze zeiden: "Hoe kun je dit niet testen?" Ze vonden het onethisch om het niet te testen. Zelfs als we zouden mislukken, is de inzet te hoog om het niet te proberen. Als we niets doen, zullen die meisjes bij Durban hiv oplopen en telkens als er een nieuw virus opduikt, zullen we ons weer in net zo'n kwetsbare positie bevinden als vandaag, met poreuze quarantaines en met vaccins waar we maanden op moeten wachten en die misschien ongeschikt zijn.
I think it's time for a new approach that's different than the static approaches of the last century. It's time for a new technology that is less reactive and more proactive. I think it's time for treatments that don't just benefit the most affluent among us but also those who face the greatest adversity. I think it's time for a new type of weapon that matches, or that solves the fundamental mismatch. I think it's time for therapies that can go viral.
Ik denk dat het tijd is voor een nieuwe benadering die anders is dan de statische benaderingen van de vorige eeuw. Tijd voor een nieuwe technologie die minder reactief en meer proactief is. Het is tijd voor behandelingen die niet alleen de rijksten onder ons bereiken, maar ook degenen die het meest hebben te lijden. Ik denk dat het tijd is voor een nieuw soort wapen dat de fundamentele onaangepastheid oplost. Het is tijd voor therapieën die viraal kunnen gaan.
Thank you very much.
Erg bedankt.
(Applause)
(Applaus)