I want to tell you about a student of mine. A few weeks ago, she was on vacation when at 3am she got a phone call. It was her husband telling her that the city that she was in would be quarantined by 10am. She was in Wuhan, China. The epicenter of the coronavirus outbreak. By 8am she was on the road in a friend's car driving 500 miles to Shanghai Airport. The entire time, she was terrified the authorities would arrest her. She made it out on one of the last flights.
Vorrei raccontarvi di una mia studentessa. Alcune settimane fa, mentre era in ferie ricevette una telefonata alle 3 di notte. Era sua marito che le diceva che la città dove si trovava sarebbe stata messa in quarantena alle 10. Lei si trovava a Wuhan, in China. L’epicentro dell’epidemia da coronavirus. Alle 8 era per strada, sull’auto di un amico, diretta a tutta velocità all’aeroporto di Shangai, col terrore di essere arrestata. Riuscì a prendere uno degli ultimi voli.
So we're all relieved that she's back home, safe in the US. But what if I told you she was in this room? What if I told you she was sitting next to you? There's no vaccine. There won't be a vaccine for at least 12 months. And this virus is mutating, so there's no guarantee that the vaccine that we produce 12 months from now will match the mutated virus. We're always playing catch-up. And this is the scenario we're in every time there's an outbreak. Our quarantines are porous, our medical responses are flat-footed.
Siamo tutti sollevati che sia di nuovo a casa, al sicuro negli Stati Uniti. Ma se vi dicessi che era in questa stanza? Che era seduta vicino a voi? Non c’è un vaccino. Non ci sarà un vaccino almeno per 12 mesi. E questo virus muta, così non ci sono garanzie che il vaccino che produrremo tra 12 mesi andrà bene per il virus mutato. Continueremo a rincorrerlo. E ci troveremo in questa situazione a ogni nuova epidemia. Le nostre quarantene sono permeabili, i nostri interventi medici sono inadeguati.
The fundamental problem that we face in controlling these outbreaks is that viruses and other infections do two things really well: they mutate and they transmit. Our medical tools do neither of these two things. Our medical tools don't mutate or transmit. We have a fundamental mismatch between our tools, which are static, and the infections, which are dynamic. This mismatch is why we're always flat-footed. This mismatch is why we're playing catch-up. And this mismatch is universal. It's the reason that we have antibiotic-resistant infections that killed 40,000 Americans last year, and it's the reason that the flu vaccine couldn't prevent the flu from killing 60,000 Americans last year. So how do we resolve this fundamental mismatch?
Il problema di fondo che dobbiamo affrontare nel controllare queste epidemie è che i virus e le altre infezioni fanno molto bene due cose: mutano e si trasmettono. I nostri strumenti sanitari non fanno nessuna di queste due cose. I nostri strumenti sanitari non mutano né si trasmettono. C’è una disparità di fondo tra i nostri strumenti, che sono statici, e le infezioni, che sono dinamiche. Questa disparità è il motivo per cui siamo sempre inadeguati. È il motivo per cui dobbiamo sempre rincorrere. E questa disparità è universale. È il motivo per cui le infezioni resistenti agli antibiotici hanno ucciso 40.000 Americani l’anno scorso, ed è il motivo per cui il vaccino antinfluenzale non ha evitato che l’influenza,l’anno scorso, uccidesse 60.000 Americani. Quindi, come risolviamo questa disparità di fondo?
I've devoted my career to studying and solving this problem. For 100 years, we've used chemicals as drugs to treat infections. Chemicals will never mutate or transmit. Similarly, our vaccines are not designed to mutate or transmit. 20 years ago, I had a radical idea to use the viruses themselves as therapies -- as building blocks for therapies. To build therapies that could mutate and transmit. Let me share with you how we've had a major breakthrough, and we're already testing these new therapies.
Ho dedicato la mia carriera a studiare come risolvere questo problema. Per cent’anni, abbiamo usato delle sostanze chimiche come farmaci per trattare le infezioni. Le sostanze chimiche non muteranno né si trasmetteranno mai. Neanche i nostri vaccini sono progettati per mutare o trasmettersi. Vent’anni fa, ebbi un’idea radicale di usare proprio i virus come terapie, come elementi di base per costruire delle terapie. Per costruire terapie in grado di mutare e trasmettersi. Vorrei raccontarvi come abbiamo fatto grandi passi avanti, e come stiamo già testando queste nuove terapie.
HIV is the most devastating pandemic of our era. 75 million infected; 33 million dead. Most of us think that HIV is a solved problem. We have truly amazing antiviral drugs: they're safe and effective, and we've spent 15 years and billions of dollars deploying these drugs around the world. So let's look at the numbers.
Quella da HIV è la pandemia più devastante della nostra epoca: 75 milioni di sieropositivi, 33 milioni di morti. La maggior parte di noi pensa che l’HIV sia un problema risolto. Abbiamo farmaci antivirali davvero fantastici: sono sicuri ed efficaci; abbiamo impiegato 15 anni e miliardi di dollari per sviluppare questi farmaci in tutto il mondo. Diamo un’occhiata ai numeri.
In 2019, 1.7 million people acquired HIV. This number only hit home for me last year when I visited this rural village outside of Durban, South Africa. I was driving along this dirt road with my 10-year-old daughter in the back seat, and walking next to us on the side of the road were girls, the same age as my daughter, barefoot. My daughter asked about why these girls are barefoot and I had to explain disparity to her, which was hard. But what really shocked me was when my colleagues, the local African scientists explained to me that these young girls the same age as my daughter --
Nel 2019, 1,7 milioni di persone hanno contratto l’HIV. Compresi la realtà di questo numero solo l’anno scorso quando andai a visitare questo villaggio rurale alla periferia di Durban, in Sud Africa. Mentre guidavo lungo questa strada polverosa con mia figlia di 10 anni sul sedile posteriore, sul lato della strada di fianco a noi c’erano delle ragazzine, della stessa età di mia figlia, che camminavano scalze. Mia figlia mi chiese come mai fossero scalze e io dovetti spiegarle cos’è la disparità, il che fu difficile. Ma ciò che mi sconvolse davvero fu quando i miei colleghi, gli scienziati africani del posto, mi spiegarono che queste ragazzine dell’età di mia figlia -
(Breathes)
(Sospiri)
sorry -- had an 80 percent chance of acquiring HIV in their lifetime. It blew me away. How can these girls have an 80 percent risk if we have safe and effective drugs?
scusate - avevano una probabilità dell’80% di contrarre l’HIV nell’arco della vita. Ero sconvolto. Com’era possibile che avessero un rischio dell’80% se abbiamo farmaci sicuri ed efficaci?
The reason is the fundamental mismatch. It creates barriers to controlling infectious disease, particularly in resource-limited settings. The first barrier is mutation: viruses mutate, our drugs don't. The second barrier: adherence. It's really hard to get these drugs to those who need the most. I can't even adhere to a week-long antibiotic regimen in this country. We're asking those in resource-limited settings who face enormous adversity to adhere to lifelong regimens.
Il motivo è la disparità di fondo. Crea ostacoli nel controllo delle malattie infettive, in particolare in contesti con risorse limitate. Il primo ostacolo è la mutazione: il virus muta, i farmaci no. Il secondo ostacolo: l’aderenza. È molto difficile far avere questi farmaci a chi ne ha più bisogno. Non si riesce ad aderire a una terapia antibiotica di una settimana in questo paese. Chiediamo a chi vive in contesti con risorse limitate che affronta enormi avversità di aderire a una terapia per tutta la vita.
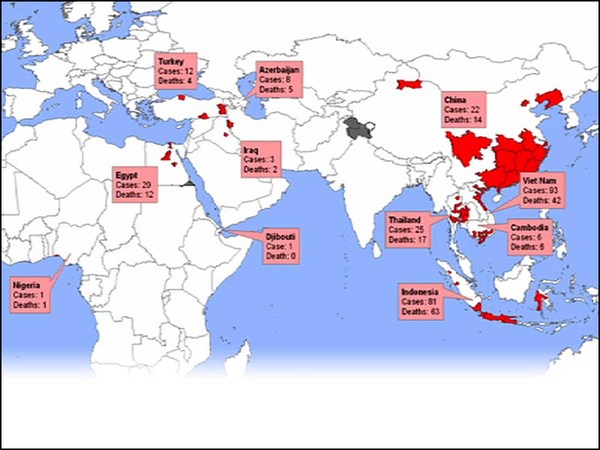
And the third barrier is deployment, or access. It's super hard to get these drugs to those who need them most. Not these girls but those who engage in high-risk activities, such as commercial sex work and injection drug use. In the epidemiological parlance, these groups are called "super-spreaders." And in the 1900s, a small subset of super-spreaders drove HIV along the Trans-Africa Highway and spread the virus through the continent like this. These groups are exceptionally hard to identify, they're small, they face enormous social stigma so they don't self-identify and they're the ones we need to get to the most. All of these barriers combined created the situation we have today, where greater than 15 percent of people in Southern Africa live with HIV.
E il terzo ostacolo è la distribuzione, o l’accesso. È difficilissimo far avere questi farmaci a chi ne ha più bisogno. Non quelle ragazzine, ma quelli impegnati in attività con rischio elevato, come la prostituzione o l’uso di droghe iniettabili. Nel linguaggio epidemiologico, questi gruppi sono definiti “superdiffusori”. E nel 1900, un piccolo gruppo di superdiffusori portò l’HIV lungo l’autostrada transafricana e diffuse così il virus in tutto il continente. È difficilissimo identificare questi gruppi, sono piccoli, devono affrontare un enorme stigma sociale per cui non si autoidentificano e sarebbero proprio quelli che più dovremmo raggiungere. La combinazione di tutti questi ostacoli ha creato l’attuale situazione, in cui più del 15% della popolazione dell’Africa meridionale convive con l’HIV.
Now, conventional wisdom is: what we need to do is get more drugs to more people more effectively. I'd argue we need to solve the fundamental mismatch; we need to eliminate these barriers. If we can build therapies that mutate and transmit, we can overcome drug resistance, overcome adherence barriers, and if we do it properly, we will convert the super-spreaders from the greatest barrier to the most powerful deployment strategy that we can imagine.
Ora, secondo l’opinione comune, la cosa da fare sarebbe far avere più farmaci a più persone in modo più efficace. Io direi che dovremmo risolvere la disparità di fondo; dobbiamo eliminare questi ostacoli. Se riusciamo a costruire terapie che mutano e si tramettono, possiamo superare la resistenza ai farmaci, gli ostacoli all’aderenza, e se lo facciamo bene, convertiremo i superdiffusori, i principali ostacoli, nella strategia di distribuzione più potente che si possa immaginare.
This is a radical concept. It has huge potential payoff, but there's a catch. And it's serious. Before we deploy a therapy that may transmit, even if it's only in a limited population of already infected individuals, before we do this, we need to be exceptionally careful, and we need to test safety in the most rigorous ways possible. The reason I'm here today is because for the first time 20 years, we got it to work, and this is the first time I'm sharing it publicly.
Si tratta di un concetto radicale. Ha un vantaggio potenziale enorme, ma c’è un inghippo. Ed è serio. Prima di distribuire una terapia che si possa trasmettere, anche solo in una ristretta popolazione di individui già infetti, prima di fare questo, dobbiamo essere estremamente attenti, e dobbiamo valutare la sicurezza in modo estremamente rigoroso. La ragione per cui sono qui oggi è che per la prima volta dopo 20 anni, l’abbiamo fatta funzionare, e questa è la prima volta che lo comunico pubblicamente.
(Applause and cheers)
(Applausi)
Last two times I did this I cried, so --
Le ultime due volte che l’ho fatto, ho pianto.
(Laughter)
(Risate)
So in order to help you understand this breakthrough, let me take you back 20 years to 1999. I was a graduate student in Berkeley, California, studying the biophysics of HIV. For such a complex epidemic, the simplicity of this virus fascinated me. HIV, like all viruses, is just an instruction set -- malware. It hijacks a cell and converts that cell into a factory to do one thing: single-mindedly churn out more virus. All the normal functions of the cell get wiped away. HIV infects the white blood cell that keeps us healthy. This cell has already been hijacked and converted into a factory. And if we magnify, we can see the anatomy of the virus. Those squiggly red lines in the middle? That's HIV's instruction set. Its genetic material.
Per farvi capire questa grande scoperta, vi riporterò indietro di 20 anni, nel 1999. Ero uno specializzando alla Berkeley, in California, studiavo la biofisica dell’HIV. Per un’epidemia tanto complessa, trovavo affascinante la semplicità di questo virus. L’HIV, come tutti i virus, è un semplice insieme di istruzioni, un malware. Dirotta una cellula e la converte in una fabbrica con un unico scopo: occuparsi esclusivamente di sfornare più virus. Tutte le normali funzioni della cellula vengono spazzate via. L’HIV infetta i globuli bianchi, le cellule che ci mantengono in salute. Questa cellula è stata dirottata e convertita in una fabbrica. Se ingrandiamo, possiamo vedere l’anatomia del virus. Quelle linee sinuose rosse nel mezzo? Quello è l’insieme delle istruzioni dell’HIV. È il suo materiale genetico.
This genetic material directs the hijacking process, converting that cell into a factory first to make more copies of the instruction set, and then all the other components of the virus and assemble them into a particle. This is how the virus replicates. Each of these particles can go in and hijack a new cell. This is how the virus transmits. And every time a cell is hijacked, little mistakes are made in copying the genetic material. That's how the virus mutates. This ability to replicate, transmit and mutate is something that our current drugs cannot do.
Questo materiale genetico dirige il processo di dirottamento, che converte quella cellula in una fabbrica per produrre altre copie di quell’insieme di istruzioni e poi tutti gli altri componenti del virus per assemblarli in una particella. Questo è il modo in cui il virus si replica. Ciascuna di queste particelle può entrare in una nuova cellula e dirottarla. Questo è il modo in cui il virus si trasmette. E ogni volta che una cellula viene dirottata, nel copiare il materiale genetico vengono commessi degli errori. Questo è il modo in cui il virus muta. Questa capacità di replicarsi, trasmettersi e mutare i farmaci attuali non ce l’hanno.
So, being young and naïve and a little bit ignorant, I thought: why can't we create therapies that mutate and transmit and replicate? Here was the idea. If we can take the virus and engineer it to amputate the genetic material in blue here, this amputated instruction set can no longer hijack a cell. But this amputated instruction set can do something very special. In an already infected cell, this amputated instruction set can hijack the hijacker. It can commandeer HIV's machinery to make more copies of itself, the amputated instruction set, and then each of these copies can steal all of HIV's other components so that the cell gets converted from a factory that produces virus to a factory that produces therapy. Hijackers. These carry no disease. This dramatically lowers HIV levels and keeps the cell healthier.
Così, essendo giovane, inesperto e un po’ ignorante, pensai: perché non possiamo creare terapie in grado di mutare, trasmettersi e replicarsi? L’idea era questa. Se riusciamo a prendere il virus e a ingegnerizzarlo per asportare il materiale genetico qui in blu, questo insieme di istruzioni asportato non può più dirottare la cellula, ma può fare una cosa molto speciale. In una cellula già infettata, questo insieme di istruzioni asportato può dirottare il dirottatore. Può dirigere il macchinario dell’HIV perché faccia più copie di sé, l’insieme di istruzioni asportato, e poi ciascuna di queste copie può rubare tutti gli altri componenti dell’HIV così la cellula viene convertita da una fabbrica che produce virus in una fabbrica che produce la terapia: dirottatori. Questi non portano alcuna malattia. Questo riduce drammaticamente i livelli di HIV e mantiene la cellula più sana.
This idea consumed me for months. It was the most intense intellectual experience of my life. On every bike ride to lab, on every walk to the coffee shop, on every run in the hills above campus, the ideas, the arguments, the counterarguments, they all came so rapidly in my head, in my inner monologue, that I was physically out of breath. I thought if we can create a therapy that replicates, it would only need to be taken once. It could mutate along with the virus and possibly it could transmit between infected individuals to treat them. It was a therapy that could do all of the things that the virus could do. It solved the fundamental mismatch.
Quest’idea mi tormentò per mesi. Fu l’esperienza intellettiva più intensa della mia vita. A ogni pedalata verso il laboratorio, a ogni camminata verso la caffetteria, a ogni corsa tra le colline vicine al campus, le idee, i ragionamenti, le controargomentazioni, nascevano nella mia testa, nei monologhi interiori, così velocemente da lasciarmi letteralmente senza fiato. Pensavo che se fossimo riusciti a creare una terapia che si replica, sarebbe stato necessario assumerla una sola volta. Sarebbe mutata insieme al virus e magari si sarebbe trasmessa tra le cellule infette dell’individuo per curarle. Era anche una terapia in grado di fare tutte le cose che può fare il virus. Avrebbe risolto la disparità di fondo.
The most radical part of this concept was that the super-spreaders would also be converted from transmitting the virus to now transmitting the therapy. It was a therapy that would go viral along with the virus. This scared some people. But there's already a precedent: we already inadvertently use therapies that transmit. The vaccine that eradicated polio in the US, the oral polio vaccine, transmits between people. It's not well-known, but the fact that this vaccine transmits is part of the reason that it was chosen for the worldwide eradication effort despite its safety issues.
L’aspetto più radicale di questo concetto era che anche i superdiffusori sarebbero stati convertiti e invece di trasmettere il virus ora avrebbero trasmesso la terapia. Era una terapia che sarebbe diventata virale insieme al virus. Questo spaventò diverse persone. Ma c’è già un precedente: usiamo già inconsapevolmente terapie che si trasmettono. Il vaccino che ha eradicato la polio negli Stati Uniti, il vaccino orale contro la polio, si trasmette tra le persone. Non è risaputo, ma il fatto che il vaccino si trasmetta è uno dei motivi per cui venne scelto per lo sforzo di eradicazione mondiale nonostante i problemi di sicurezza.
So the bigger problem was that these hijacker therapies didn't exist. My Berkeley advisors said to me, "Lovely idea, so sad it will never work," or, "Regulators will never allow it, drop it." But the idea wouldn't drop me.
Il problema maggiore era che queste terapie di dirottamento non esistevano. Il mio tutor alla Berkeley mi disse: “Una bella idea, peccato che non funzionerà mai”, o, “Gli enti di controllo non lo permetteranno mai, abbandona l'idea”. Ma l’idea non abbandonava me.
If it ever worked, it would solve the fundamental mismatch. So we tried for years to build it. We tried every trick in the book and failed over and over again. We -- every time we thought we had a good idea, we'd spend months, sometimes years working on it only to come up empty. We once spent five years building 150,000 versions of a hijacker therapy. Every single one failed. I once asked a really bright student what he hoped to learn from me during his PhD --
Se mai avesse funzionato, avrebbe risolto la disparità di fondo. Così, per anni, provammo a svilupparla. Tentammo ogni stratagemma disponibile e ogni volta fallimmo. Noi -- ogni volta, pensando di avere una buona idea, passammo mesi, a volte anni a lavorarci su solo per finire a mani vuote. Una volta impiegammo cinque anni a costruire 150.000 versioni di una terapia di dirottamento. Fallirono tutte. Chiesi a uno studente molto brillante cosa sperava di imparare da me durante il suo dottorato.
(Laughter)
(Risate)
And he replied, "How to keep going, how to continue moving forward despite zero evidence that there's anything there."
Lui mi rispose: “Come tenere duro, come continuare ad andare avanti nonostante non ci sia alcuna prova che lì ci sia qualcosa”.
(Laughter)
(Risate)
I wonder if he was trying to tell me something.
Mi chiedo se stesse cercando di dirmi qualcosa.
(Laughter)
(Risate)
By 2018, things looked bad. There was no evidence that a hijacker therapy could be engineered. In fact, we had evidence that it might be impossible. It was time to face the hard truth. This solution that I'd wanted so badly, this hijacker therapy just didn't exist. For 20 years, I had been chasing a ghost.
Nel 2018, la situazione sembrava pessima. Non vi era alcuna prova che si potesse progettare una terapia di dirottamento. Di fatto, avevamo le prove che potesse essere impossibile. Era ora di affrontare la dura verità. Questa soluzione che desideravo così tanto, questa terapia di dirottamento semplicemente non esisteva. Per 20 anni, avevo inseguito un fantasma.
Then one day, Elizabeth, a postdoc in my lab, came to me with this picture. It doesn't look like much. My wife thinks it looks like a pregnancy test.
Poi un giorno, Elizabeth, una studentessa del mio laboratorio, venne da me con questa foto. Non sembra nulla di che. Mia moglie dice che sembra un test di gravidanza.
(Laughter)
(Risate)
But this little band down here -- that was the amputated genetic material that we had been looking for for 20 years. The entire time that we had been trying to build it and failing, it had evolved by itself in a flask in the back of the lab.
Ma questa piccola banda qui in basso, quello era il materiale genetico asportato che avevamo cercato per 20 anni. In tutto quel tempo in cui noi avevamo cercato di costruirlo, fallendo, si era evoluto da solo in una beuta nel retro del laboratorio.
(Audience) What?
(Pubblico) Cosa?
(Laughter)
(Risate)
We finally had a foothold. And we used this to build the first hijacker. But we had no evidence that what we built was a therapy.
Finalmente avevamo un appiglio. E lo usammo per sviluppare il primo dirottatore. Ma non avevamo prove che quanto avevamo sviluppato fosse una terapia.
The first hurdle that any therapy has to clear is testing in a mouse. It can be risky. In our case, if our mice died, so did our funding, and with it, any hopes of this becoming a therapy, let alone a transformative one. After so many failures, we were all pretty skeptical but we didn't really have an alternative. We had to give it a shot; we had to try.
Il primo ostacolo che una terapia deve superare è la sperimentazione in un topo. Può essere rischioso. Nel nostro caso, se il topo fosse morto, avremmo perso il nostro finanziamento e ogni speranza che questa diventasse una terapia, figuriamoci una terapia rivoluzionaria. Dopo così tanti fallimenti, eravamo tutti piuttosto scettici, ma non avevamo alternative. Dovevamo somministragli una dose; dovevamo tentare.
Amazingly, the hijacker therapy worked in a mouse, and it worked exactly as we'd predicted 20 years before. It protected the cells in a mouse from HIV. Here are the cells under a microscope. First, HIV in red infects those cells, and then the hijacker, in blue, can be activated, protects those cells and transmits to other cells. We'd finally built the hijacker after 20 years. Everyone in the lab was elated. For me, this was proof of concept. If we could do it for one virus we could do it for others.
Sorprendentemente, la terapia di dirottamento funzionò in un topo, e fece esattamente quello che avevamo previsto 20 anni prima. Protesse le cellule di un topo dall’HIV. Queste sono le cellule al microscopio. Primo, l’HIV in rosso infetta queste cellule, e poi il dirottatore, in blu, può essere attivato, protegge quelle cellule e si trasmette ad altre cellule. Alla fine, dopo 20 anni, avevamo prodotto il dirottatore. Nel laboratorio eravamo tutti euforici. Per me, questa era una prova del concetto. Se potevamo farlo per un virus, avremmo potuto farlo per altri.
To understand how this hijacker might impact HIV levels worldwide, we ran computer simulations. Epidemiological models. And the results were pretty amazing. If we do nothing in the hardest-hit parts of Africa, HIV prevalence will stay between 25 and 30 percent. If we manage to introduce drugs to three-quarters of the population or if we ever get the long-sought-after vaccine, we would reduce those numbers down to 20 percent. But those are best-case scenarios. If HIV evolves resistance or if people change their behaviors, these numbers could go right back up to 30 percent or even beyond. The blue is the hijacker therapy. And we've not found a way, either theoretically or experimentally, that HIV can evolve resistance to the hijacker.
Per capire come questo dirottatore potrebbe influire sui livelli di HIV nel mondo, abbiamo fatto delle simulazioni al computer. Modelli epidemiologici. E i risultati sono stati davvero incredibili. Se non si fa nulla nelle aree dell’Africa maggiormente colpite, l’incidenza dell’infezione da HIV resterà tra il 25% e il 30%. Se riuscissimo a introdurre i farmaci nei tre quarti della popolazione o se mai riuscissimo a ottenere il vaccino a lungo ricercato, ridurremmo questo numero al 20%. Ma questi sono gli scenari più ottimistici. Se l’HIV sviluppasse una resistenza o le persone cambiassero i propri comportamenti, questi numeri potrebbero tornare subito al 30% o persino peggio. Quella blu è la terapia di dirottamento. E non abbiamo trovato un modo, sia in via teorica che sperimentale, in cui l’HIV possa sviluppare una resistenza al dirottatore.
The reason this hijacker works so well is the super-spreaders. If the hijacker is introduced in one place over here, the super-spreaders can pick it up and transmit it through the population. Imagine if 10 years from now, HIV is no longer a pandemic.
La ragione per cui questo dirottatore funziona così bene sono i superdiffusori. Se il dirottatore viene introdotto qui da qualche parte, i superdiffusori possono raccoglierlo e trasmetterlo nella popolazione. Immaginate se fra 10 anni quella dell’HIV non fosse più una pandemia.
To get there, we have to start large-scale clinical trials in five years, which means initial human tests next year. The FDA has cleared us to start testing in HIV-positive patients who have a terminal cancer and have less than a year left to live. Volunteering for this trial is their last incredibly generous gift to the world. They're called the "Last Gift cohort." And to test in these altruistic patients next year, we have to finish our preclinical tests this year ... and I think we will.
Per arrivarci, dobbiamo iniziare gli studi clinici su larga scala entro cinque anni, che significa i primi studi sull’uomo l’anno prossimo. L’FDA ha dato il via libera per iniziare gli studi su pazienti HIV positivi con un tumore allo stadio terminale e con meno di un anno di vita. La partecipazione a questi studi è il loro ultimo e generosissimo dono al mondo. Sono la “coorte dell’ultimo dono”. E per iniziare gli studi in questi pazienti altruisti l’anno prossimo, dobbiamo terminare i test preclinci quest’anno, e penso che ce la faremo.
I still meet colleagues who push back and are stridently opposed to letting us move forward with testing. They say, "What if something goes wrong? You can't unrelease it." They say, "There are ethical issues; people can't consent." Well, oral polio vaccine faced similar ethical and safety concerns. In fact, oral polio vaccine faced such an effective misinformation campaign that most people still don't know that it transmits, that it successfully eradicated polio in many countries or that this vaccine is the basis for new vaccines. When we presented this hijacker therapy idea in Africa last year, the African scientists had a different response. They said, "How can you not test this?" They said it's unethical to not test it. So even though we might fail, I think the stakes are too high not to try. If we do nothing, those girls outside of Durban will acquire HIV, and the next time that there's a new virus that emerges, we'll be in the same vulnerable position that we are today with quarantines that are porous and vaccines that we need to wait months for that may not match.
Incontro ancora colleghi che respingono e si oppongono con forza a farci andare avanti con i test. Dicono: “E se qualcosa andasse storto? Non si può tronare indietro”. Dicono: “Ci sono questioni etiche; la gente non può acconsentire”. Beh, il vaccino antipolio orale affrontò le stesse preoccupazioni sull’etica e la sicurezza. Infatti, il vaccino antipolio orale vide una campagna di disinformazione così efficace che quasi tutti non sanno che si trasmette, che ha eradicato con successo la polio in molti paesi o che questo vaccino è la base per i nuovi vaccini. Quando abbiamo presentato quest’idea della terapia di dirottamento in Africa l’anno scorso, gli scienziati africani hanno avuto una reazione diversa. Hanno detto: “Come potete non testarla?” Hanno detto che è contro l’etica non testarla. Quindi, anche se potremmo fallire, penso che la posta in gioco sia troppo alta per non provarci. Se non facciamo niente, quelle ragazzine alla periferia di Durban contrarranno l’HIV, E la prossima volta che emergerà un nuovo virus, ci troveremo indifesi come oggi con quarantene permeabili e vaccini che dovremo aspettare per mesi e che potrebbero non andar bene.
I think it's time for a new approach that's different than the static approaches of the last century. It's time for a new technology that is less reactive and more proactive. I think it's time for treatments that don't just benefit the most affluent among us but also those who face the greatest adversity. I think it's time for a new type of weapon that matches, or that solves the fundamental mismatch. I think it's time for therapies that can go viral.
Penso sia ora di avere un nuovo approccio diverso da quelli statici dell’ultimo secolo. È ora di avere una tecnologia nuova che sia meno reattiva e più proattiva. Penso sia ora di avere trattamenti che non siano a vantaggio solo dei più benestanti ma anche di quelli che affrontano le maggiori avversità. Penso sia ora di avere un nuovo tipo di arma che corrisponda, o che risolva la disparità di fondo. Penso sia ora che le terapie diventino virali.
Thank you very much.
Grazie.
(Applause)
(Applausi)