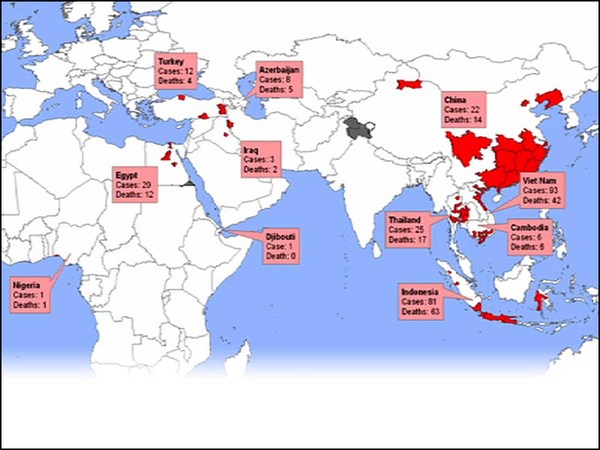
I want to tell you about a student of mine. A few weeks ago, she was on vacation when at 3am she got a phone call. It was her husband telling her that the city that she was in would be quarantined by 10am. She was in Wuhan, China. The epicenter of the coronavirus outbreak. By 8am she was on the road in a friend's car driving 500 miles to Shanghai Airport. The entire time, she was terrified the authorities would arrest her. She made it out on one of the last flights.
Saya mau bercerita soal mahasiswi saya. Beberapa minggu lalu, dia sedang berlibur dan ditelepon pukul 03.00. Suaminya memberi tahu, kota kini dia berada akan dikarantina pada pukul 10.00. Dia berada di Wuhan, China. Pusat wabah virus corona. Pukul 08.00, dia berada di mobil temannya, menyetir 500 mil ke Bandara Shanghai. Selama itu, dia takut ditangkap oleh aparat setempat. Dia berhasil ke luar dengan pesawat terakhir.
So we're all relieved that she's back home, safe in the US. But what if I told you she was in this room? What if I told you she was sitting next to you? There's no vaccine. There won't be a vaccine for at least 12 months. And this virus is mutating, so there's no guarantee that the vaccine that we produce 12 months from now will match the mutated virus. We're always playing catch-up. And this is the scenario we're in every time there's an outbreak. Our quarantines are porous, our medical responses are flat-footed.
Kami lega saat dia sudah pulang dengan aman ke Amerika Serikat. Namun, bagaimana jika saya bilang dia ada di ruangan ini? Bagaimana jika dia duduk di samping Anda? Tak ada vaksin. Tak akan ada vaksin, setidaknya 12 bulan ke depan. Dan virus ini bermutasi, jadi tak ada jaminan vaksin yang dibuat 12 bulan lalu akan cocok dengan virus yang telah bermutasi. Kita selalu berkejar-kejaran. Inilah skenario setiap ada wabah. Karantina kita lemah, respons medis juga kalah.
The fundamental problem that we face in controlling these outbreaks is that viruses and other infections do two things really well: they mutate and they transmit. Our medical tools do neither of these two things. Our medical tools don't mutate or transmit. We have a fundamental mismatch between our tools, which are static, and the infections, which are dynamic. This mismatch is why we're always flat-footed. This mismatch is why we're playing catch-up. And this mismatch is universal. It's the reason that we have antibiotic-resistant infections that killed 40,000 Americans last year, and it's the reason that the flu vaccine couldn't prevent the flu from killing 60,000 Americans last year. So how do we resolve this fundamental mismatch?
Masalah dasar dari pengendalian wabah adalah virus dan infeksi lain melakukan dua hal dengan baik, mereka bermutasi, dan menular. Alat medis kita tak bisa menangani keduanya. Alat medis tak bisa bermutasi atau menular. Ada ketidakcocokkan utama antara peralatan kita yang bersifat statis dengan infeksi yang bersifat dinamis. Inilah penyebab kita selalu kalah. Inilah penyebab kita berkejar-kejaran. Ketidakcocokkan ini universal. Inilah alasan adanya infeksi kebal antibiotik, yang membunuh 40.000 orang Amerika tahun lalu, dan juga mengapa vaksin flu tak bisa mencegah flu yang membunuh 60.000 orang Amerika tahun lalu. Jadi, bagaimana cara mengatasi ketidakcocokkan utama ini?
I've devoted my career to studying and solving this problem. For 100 years, we've used chemicals as drugs to treat infections. Chemicals will never mutate or transmit. Similarly, our vaccines are not designed to mutate or transmit. 20 years ago, I had a radical idea to use the viruses themselves as therapies -- as building blocks for therapies. To build therapies that could mutate and transmit. Let me share with you how we've had a major breakthrough, and we're already testing these new therapies.
Saya telah mengabdi untuk mempelajari dan memecahkan masalah ini. Selama 100 tahun, kita telah memakai bahan kimia sebagai obat infeksi. Bahan kimia tak akan bermutasi atau menular. Miripnya, vaksin kita tak dirancang bermutasi atau menular. 20 tahun yang lalu, saya punya ide gila memakai sistem sel virus sebagai terapi, sebagai dasar untuk terapi. Untuk membangun terapi yang bisa bermutasi dan menular. Saya akan menjelaskan bagaimana kami melakukan terobosan besar, dan telah menguji coba terapi baru ini.
HIV is the most devastating pandemic of our era. 75 million infected; 33 million dead. Most of us think that HIV is a solved problem. We have truly amazing antiviral drugs: they're safe and effective, and we've spent 15 years and billions of dollars deploying these drugs around the world. So let's look at the numbers.
HIV adalah pandemi terparah di era kita. 75 juta orang terinfeksi, 33 juta orang meninggal. Banyak dari kita berpikir masalah HIV telah diselesaikan. Kita punya obat antivirus yang bagus, mereka aman dan efektif, dan kita perlu 15 tahun dan miliaran dolar untuk mengirim obat ini ke seluruh dunia. Jadi, mari lihat datanya.
In 2019, 1.7 million people acquired HIV. This number only hit home for me last year when I visited this rural village outside of Durban, South Africa. I was driving along this dirt road with my 10-year-old daughter in the back seat, and walking next to us on the side of the road were girls, the same age as my daughter, barefoot. My daughter asked about why these girls are barefoot and I had to explain disparity to her, which was hard. But what really shocked me was when my colleagues, the local African scientists explained to me that these young girls the same age as my daughter --
Pada 2019, 1,7 juta orang tertular HIV. Angka ini menyadarkan saya saat tahun lalu, mengunjungi sebuah kampung di luar kota Durban, Afrika Selatan. Saya mengendarai mobil di jalan setapak bersama putri saya yang berumur 10 tahun di belakang, di pinggir jalan, ada gadis-gadis seumuran putri saya, tak beralas kaki. Putri saya bertanya mengapa mereka tak beralas kaki, dan saya harus menjelaskan soal kesenjangan padanya, dan itu sulit. Yang lebih mengejutkan lagi, saat rekan saya, ilmuwan lokal Afrika, menjelaskan gadis-gadis muda ini, yang seumuran putri saya,
(Breathes)
(Menghela napas)
sorry -- had an 80 percent chance of acquiring HIV in their lifetime. It blew me away. How can these girls have an 80 percent risk if we have safe and effective drugs?
maaf, kemungkinan 80% mengidap HIV seumur hidupnya. Itu mengagetkan saya. Bagaimana bisa mereka berisiko 80% padahal ada obat yang aman dan efektif?
The reason is the fundamental mismatch. It creates barriers to controlling infectious disease, particularly in resource-limited settings. The first barrier is mutation: viruses mutate, our drugs don't. The second barrier: adherence. It's really hard to get these drugs to those who need the most. I can't even adhere to a week-long antibiotic regimen in this country. We're asking those in resource-limited settings who face enormous adversity to adhere to lifelong regimens.
Alasannya adalah ketidakcocokkan utama. Itulah yang menghalangi pengendalian wabah menular, terutama di daerah yang sulit dijangkau. Halangan pertama adalah mutasi, virus bermutasi, sedangkan obat tidak. Halangan kedua, kepatuhan. Sulit sekali memberikan obat-obatan ini kepada yang paling membutuhkan. Saya pun tak bisa mematuhi aturan minum antibiotik selama seminggu di negara ini. Kami meminta mereka yang di daerah terpencil, yang menghadapi kesulitan besar, untuk mematuhi aturan seumur hidup.
And the third barrier is deployment, or access. It's super hard to get these drugs to those who need them most. Not these girls but those who engage in high-risk activities, such as commercial sex work and injection drug use. In the epidemiological parlance, these groups are called "super-spreaders." And in the 1900s, a small subset of super-spreaders drove HIV along the Trans-Africa Highway and spread the virus through the continent like this. These groups are exceptionally hard to identify, they're small, they face enormous social stigma so they don't self-identify and they're the ones we need to get to the most. All of these barriers combined created the situation we have today, where greater than 15 percent of people in Southern Africa live with HIV.
Halangan ketiga adalah penyebaran atau aksesnya. Sulit sekali memberikan obat-obatan ini kepada yang paling membutuhkan. Bukan pada gadis-gadis tadi, tapi pada mereka yang melakukan aktivitas berisiko tinggi, seperti PSK dan pengguna narkoba suntik. Istilah epidemiologisnya disebut <i>super-spreaders.</i> Di tahun 1900-an, sejumlah kecil <i>super-spreaders</i> membawa HIV sepanjang Jalan Raya Trans-Afrika, dan menyebarkannya ke seluruh benua. Seperti ini. Kelompok ini sangat sulit diidentifikasi, jumlahnya sedikit, stigma sosial buruk membuat mereka bersembunyi, dan merekalah yang perlu diobati. Semua halangan ini membentuk situasi yang kita alami saat ini, ada lebih dari 15% penduduk Afrika Selatan mengidap HIV.
Now, conventional wisdom is: what we need to do is get more drugs to more people more effectively. I'd argue we need to solve the fundamental mismatch; we need to eliminate these barriers. If we can build therapies that mutate and transmit, we can overcome drug resistance, overcome adherence barriers, and if we do it properly, we will convert the super-spreaders from the greatest barrier to the most powerful deployment strategy that we can imagine.
Pandangan umumnya adalah Kita perlu memberi lebih banyak obat ke lebih banyak orang secara lebih efisien. Kita perlu mengatasi ketidakcocokkan utama, menghapus halangan itu. Jika kita bisa membuat terapi untuk virus bermutasi dan menular, kita bisa mengatasi kekebalan obat, ketidakkepatuhan, dan jika dilakukan dengan benar, kita akan mengubah <i>super-spreaders</i> dari penghalang terbesar menjadi strategi penyebaran terkuat.
This is a radical concept. It has huge potential payoff, but there's a catch. And it's serious. Before we deploy a therapy that may transmit, even if it's only in a limited population of already infected individuals, before we do this, we need to be exceptionally careful, and we need to test safety in the most rigorous ways possible. The reason I'm here today is because for the first time 20 years, we got it to work, and this is the first time I'm sharing it publicly.
Ini adalah konsep radikal. Potensi keberhasilannya sangat tinggi, tapi ada yang perlu diperhatikan. Dan ini serius. Sebelum menerapkan terapi yang bisa menular, meski hanya pada populasi yang telah terinfeksi, sebelum melakukan ini, kami harus sangat berhati-hati, dan perlu menguji keamanannya dengan seteliti mungkin. Alasan saya di sini karena setelah 20 tahun, kami telah berhasil, dan ini pertama kalinya saya membagikannya di publik.
(Applause and cheers)
(Tepuk tangan dan bersorak)
Last two times I did this I cried, so --
Setelah dua kali melakukan ini saya menangis,
(Laughter)
So in order to help you understand this breakthrough, let me take you back 20 years to 1999. I was a graduate student in Berkeley, California, studying the biophysics of HIV. For such a complex epidemic, the simplicity of this virus fascinated me. HIV, like all viruses, is just an instruction set -- malware. It hijacks a cell and converts that cell into a factory to do one thing: single-mindedly churn out more virus. All the normal functions of the cell get wiped away. HIV infects the white blood cell that keeps us healthy. This cell has already been hijacked and converted into a factory. And if we magnify, we can see the anatomy of the virus. Those squiggly red lines in the middle? That's HIV's instruction set. Its genetic material.
Agar paham soal terobosan ini, mari kita mundur 20 tahun, ke tahun 1999. Saya seorang mahasiswa pascasarjana di Berkeley, California, mempelajari biofisika HIV. Untuk sebuah epidemi yang kompleks, virus sederhana ini membuat saya tertarik. HIV, seperti semua virus, adalah set instruksi, sebuah perusak. Virus membajak sebuah sel dan menjadikannya pabrik untuk satu hal, membuat lebih banyak virus. Semua fungsi normal sel itu hilang. HIV menyerang sel darah putih yang melindungi tubuh kita. Sel ini telah dibajak dan diubah menjadi pabrik. Jika diperbesar, kita bisa melihat anatomi virusnya. Garis merah di tengah itu adalah set intruksi HIV-nya. Material genetiknya.
This genetic material directs the hijacking process, converting that cell into a factory first to make more copies of the instruction set, and then all the other components of the virus and assemble them into a particle. This is how the virus replicates. Each of these particles can go in and hijack a new cell. This is how the virus transmits. And every time a cell is hijacked, little mistakes are made in copying the genetic material. That's how the virus mutates. This ability to replicate, transmit and mutate is something that our current drugs cannot do.
Material genetik ini memimpin proses pembajakannya, mengubah sel itu menjadi pabrik terlebih dahulu untuk membuat lebih banyak tiruan set instruksi, lalu meniru komponen lainnya dan menyusunnya menjadi sebuah partikel. Inilah cara virus mereplikasi. Setiap partikel ini bisa masuk dan membajak sel baru. Inilah cara virus menular. Tiap kali sebuah sel dibajak, kesalahan kecil terjadi saat meniru material genetiknya. Itulah cara virus bermutasi. Kemampuan mereplikasi, menularkan, dan bermutasi tak bisa dilakukan obat kita saat ini.
So, being young and naïve and a little bit ignorant, I thought: why can't we create therapies that mutate and transmit and replicate? Here was the idea. If we can take the virus and engineer it to amputate the genetic material in blue here, this amputated instruction set can no longer hijack a cell. But this amputated instruction set can do something very special. In an already infected cell, this amputated instruction set can hijack the hijacker. It can commandeer HIV's machinery to make more copies of itself, the amputated instruction set, and then each of these copies can steal all of HIV's other components so that the cell gets converted from a factory that produces virus to a factory that produces therapy. Hijackers. These carry no disease. This dramatically lowers HIV levels and keeps the cell healthier.
Karena masih muda, naif, dan tak tahu apa-apa, saya berpikir, mengapa kita tak membuat terapi yang bisa bermutasi, menular, dan mereplikasi? Inilah idenya. Jika kita ambil virusnya dan merekayasanya untuk memotong material genetik berwarna biru di sini, set instruksi yang dipotong ini tak bisa lagi membajak sel. Namun, set instruksi yang dipotong ini bisa melakukan hal spesial. Di dalam sebuah sel yang terinfeksi, set instruksi yang dipotong bisa membajak si pembajak. Ini bisa memerintah pabrik HIV-nya untuk membuat tiruan dirinya, set instruksi yang dipotong, lalu tiap tiruan ini bisa mencuri komponen lain HIV-nya, sehingga selnya berubah dari pabrik virus menjadi pabrik terapi. Pembajak. Ini tak membawa penyakit. Ini mengurangi level HIV secara dramatis dan membuat selnya tetap sehat.
This idea consumed me for months. It was the most intense intellectual experience of my life. On every bike ride to lab, on every walk to the coffee shop, on every run in the hills above campus, the ideas, the arguments, the counterarguments, they all came so rapidly in my head, in my inner monologue, that I was physically out of breath. I thought if we can create a therapy that replicates, it would only need to be taken once. It could mutate along with the virus and possibly it could transmit between infected individuals to treat them. It was a therapy that could do all of the things that the virus could do. It solved the fundamental mismatch.
Ide ini memakan waktu berbulan-bulan. Ini jadi pengalaman intelektual terintens di hidup saya. Tiap kali bersepeda ke laboratorium, berjalan ke kedai kopi, berlari di bukit di atas kampus, ide-idenya, argumennya, argumen penentangnya, semuanya muncul dalam batin saya, hingga benar-benar membuat lelah. Jika kita bisa membuat sebuah terapi replikasi, itu hanya perlu dipakai sekali. Itu bisa bermutasi bersama virusnya, dan mungkin bisa menularkan ke sesama orang yang tertular guna mengobatinya. Ini adalah terapi yang bisa melakukan hal yang sama seperti virusnya. Ini bisa mengatasi ketidakcocokkan utama.
The most radical part of this concept was that the super-spreaders would also be converted from transmitting the virus to now transmitting the therapy. It was a therapy that would go viral along with the virus. This scared some people. But there's already a precedent: we already inadvertently use therapies that transmit. The vaccine that eradicated polio in the US, the oral polio vaccine, transmits between people. It's not well-known, but the fact that this vaccine transmits is part of the reason that it was chosen for the worldwide eradication effort despite its safety issues.
Bagian paling radikal dari konsep ini adalah <i>super-spreaders</i> juga bisa diubah dari penular virus menjadi penular terapi. Ini adalah terapi yang bisa menyebar bersama virusnya. Mungkin ini menakutkan. Namun sudah ada presedennya, kami sudah secara tak langsung memakai terapi menular. Vaksin polio di AS, vaksin polio oral, menular antar manusia. Sedikit yang tahu, tapi, karena vaksin ini menular, vaksin ini dipilih untuk usaha pembasmian sedunia, meski tak sepenuhnya aman.
So the bigger problem was that these hijacker therapies didn't exist. My Berkeley advisors said to me, "Lovely idea, so sad it will never work," or, "Regulators will never allow it, drop it." But the idea wouldn't drop me.
Masalah utamanya yaitu terapi pembajak ini tak pernah ada. Penasihat saya di Berkeley berkata, "Ide bagus, sayangnya itu tak mungkin," atau, "Pemerintah tak akan mengizinkannya. Jadi, lupakan saja." Namun, saya tak menyerah.
If it ever worked, it would solve the fundamental mismatch. So we tried for years to build it. We tried every trick in the book and failed over and over again. We -- every time we thought we had a good idea, we'd spend months, sometimes years working on it only to come up empty. We once spent five years building 150,000 versions of a hijacker therapy. Every single one failed. I once asked a really bright student what he hoped to learn from me during his PhD --
Jika ini berhasil, ini akan memecahkan ketidakcocokkan utama. Jadi, kami mencobanya bertahun-tahun. Kami mencoba tiap trik yang ada di buku, dan terus saja gagal. Tiap kali ide bagus muncul, kami mengerjakannya berbulan-bulan, bahkan bertahun-tahun, tapi tak membuahkan hasil. Kami pernah menghabiskan lima tahun membuat 150.000 versi terapi pembajak. Semuanya gagal. Saya dulu bertanya pada seorang mahasiswa cerdas soal apa yang dipelajarinya dari saya selama pendidikan doktoralnya.
(Laughter)
(Tawa)
And he replied, "How to keep going, how to continue moving forward despite zero evidence that there's anything there."
Dia menjawab, "Bagaimana cara tak menyerah dan terus maju meski tak ada bukti apa pun?"
(Laughter)
(Tawa)
I wonder if he was trying to tell me something.
Saya bertanya-tanya apa maksudnya.
(Laughter)
(Tawa)
By 2018, things looked bad. There was no evidence that a hijacker therapy could be engineered. In fact, we had evidence that it might be impossible. It was time to face the hard truth. This solution that I'd wanted so badly, this hijacker therapy just didn't exist. For 20 years, I had been chasing a ghost.
Pada 2018, keadaan menjadi buruk. Tak ada bukti soal kemungkinan pembuatan terapi pembajak. Kami justru punya bukti soal ketidakmungkinannya. Itulah waktunya menerima kenyataan. Solusi yang sangat saya inginkan, terapi pembajak ini, tak pernah ada. Selama 20 tahun, saya hanya mengejar hantu.
Then one day, Elizabeth, a postdoc in my lab, came to me with this picture. It doesn't look like much. My wife thinks it looks like a pregnancy test.
Suatu hari, Elizabeth, mahasiswi pascadoktoral, mendatangi saya dengan foto ini. Ini terlihat biasa saja. Istri saya pikir ini seperti tes kehamilan.
(Laughter)
(Tawa)
But this little band down here -- that was the amputated genetic material that we had been looking for for 20 years. The entire time that we had been trying to build it and failing, it had evolved by itself in a flask in the back of the lab.
Namun, garis kecil di bawah ini adalah potongan material genetik yang telah kami cari selama 20 tahun. Selama ini, kami berusaha membuatnya dan gagal, ternyata dia berevolusi sendiri dalam tabung di belakang laboratorium.
(Audience) What?
(Tawa)
(Laughter)
Akhirnya kami punya tumpuan.
We finally had a foothold. And we used this to build the first hijacker. But we had no evidence that what we built was a therapy.
Kami memakainya untuk membuat pembajak pertama. Namun, kami tak ada bukti apakah yang kami buat itu sebuah terapi.
The first hurdle that any therapy has to clear is testing in a mouse. It can be risky. In our case, if our mice died, so did our funding, and with it, any hopes of this becoming a therapy, let alone a transformative one. After so many failures, we were all pretty skeptical but we didn't really have an alternative. We had to give it a shot; we had to try.
Kendala pertama pada uji terapi apa pun adalah saat uji coba pada tikus. Ini bisa berisiko. Pada kasus kami, jika tikusnya mati, pendanaan dihentikan. Jadi, hilanglah harapan mewujudkan terapi. Setelah sering gagal, kami merasa skeptis, tapi tak punya alternatif lain. Kami tetap harus mencobanya.
Amazingly, the hijacker therapy worked in a mouse, and it worked exactly as we'd predicted 20 years before. It protected the cells in a mouse from HIV. Here are the cells under a microscope. First, HIV in red infects those cells, and then the hijacker, in blue, can be activated, protects those cells and transmits to other cells. We'd finally built the hijacker after 20 years. Everyone in the lab was elated. For me, this was proof of concept. If we could do it for one virus we could do it for others.
Ajaibnya, terapi pembajak berhasil pada seekor tikus, dan ini berhasil seperti prediksi kami 20 tahun yang lalu. Ini melindungi sel tikus dari HIV. Inilah selnya di bawah mikroskop. Pertama, HIV yang merah menginfeksi sel itu, lalu pembajaknya yang biru diaktifkan, dan melindungi sel itu, dan menularkannya ke sel lain. Kami akhirnya membuat pembajaknya setelah 20 tahun. Semua orang di laboratorium bergembira. Bagi saya, ini adalah bukti konsep. Jika berhasil di satu virus, di lainnya juga pasti berhasil.
To understand how this hijacker might impact HIV levels worldwide, we ran computer simulations. Epidemiological models. And the results were pretty amazing. If we do nothing in the hardest-hit parts of Africa, HIV prevalence will stay between 25 and 30 percent. If we manage to introduce drugs to three-quarters of the population or if we ever get the long-sought-after vaccine, we would reduce those numbers down to 20 percent. But those are best-case scenarios. If HIV evolves resistance or if people change their behaviors, these numbers could go right back up to 30 percent or even beyond. The blue is the hijacker therapy. And we've not found a way, either theoretically or experimentally, that HIV can evolve resistance to the hijacker.
Untuk memahami dampak pembajak ini terhadap level HIV di seluruh dunia, kami menjalankan simulasi komputer. Model epidemiologis. Dan hasilnya luar biasa. Jika kami membiarkan daerah terpencil di Afrika, jumlah HIV akan ada antara 25% dan 30%. Jika kami bisa membawa obat-obatan ke tiga perempat populasi, atau memperoleh vaksin yang sudah lama dicari, kami akan menurunkan angka tadi hingga 20%. Namun, itu adalah skenario terbaik. Jika HIV menjadi kebal, atau perilaku orang berubah, angka tersebut bisa naik ke 30%, atau bahkan lebih. Yang berwarna biru adalah terapi pembajak. Dan kami belum menemukan cara, teoretis atau empiris HIV bisa kebal terhadap pembajak itu.
The reason this hijacker works so well is the super-spreaders. If the hijacker is introduced in one place over here, the super-spreaders can pick it up and transmit it through the population. Imagine if 10 years from now, HIV is no longer a pandemic.
Alasan pembajak ini bekerja baik karena <i>super-spreaders.</i> Jika pembajaknya dimasukkan di tempat ini, <i>super-spreaders </i>bisa menangkapnya dan menularkannya ke populasi. Bayangkan 10 tahun ke depan, HIV bukan lagi sebuah pandemi.
To get there, we have to start large-scale clinical trials in five years, which means initial human tests next year. The FDA has cleared us to start testing in HIV-positive patients who have a terminal cancer and have less than a year left to live. Volunteering for this trial is their last incredibly generous gift to the world. They're called the "Last Gift cohort." And to test in these altruistic patients next year, we have to finish our preclinical tests this year ... and I think we will.
Untuk mencapainya, kami harus memulai uji klinis skala besar dalam lima tahun, artinya percobaan pada manusia akan dimulai tahun depan. FDA telah mengizinkan kami untuk mengujinya pada pasien HIV yang mengidap kanker stadium akhir, dan akan meninggal dalam setahun. Menjadi sukarelawan untuk uji coba ini adalah hadiah terakhir mereka bagi dunia. Mereka disebut "The Last Gift Cohort." Agar bisa mengetesnya tahun depan, kami harus menyelesaikan uji praklinisnya tahun ini, dan saya yakin akan selesai.
I still meet colleagues who push back and are stridently opposed to letting us move forward with testing. They say, "What if something goes wrong? You can't unrelease it." They say, "There are ethical issues; people can't consent." Well, oral polio vaccine faced similar ethical and safety concerns. In fact, oral polio vaccine faced such an effective misinformation campaign that most people still don't know that it transmits, that it successfully eradicated polio in many countries or that this vaccine is the basis for new vaccines. When we presented this hijacker therapy idea in Africa last year, the African scientists had a different response. They said, "How can you not test this?" They said it's unethical to not test it. So even though we might fail, I think the stakes are too high not to try. If we do nothing, those girls outside of Durban will acquire HIV, and the next time that there's a new virus that emerges, we'll be in the same vulnerable position that we are today with quarantines that are porous and vaccines that we need to wait months for that may not match.
Masih ada rekan yang menahan saya, dan menentang tahap uji coba. Mereka berkata, "Bagaimana jika ada yang salah? Anda tak bisa meluncurkannya." Mereka bilang, "Ada masalah etika, orang tak bisa menyetujuinya." Vaksin oral polio juga punya masalah etis dan keamanan yang sama. Faktanya, vaksin polio oral pernah menghadapi disinformasi yang merugikan sehingga masyarakat masih belum tahu vaksin ini bisa menularkan virus polio, tapi berhasil membasmi polio di banyak negara, atau menjadi acuan bagi vaksin-vaksin baru. Saat menunjukkan ide terapi pembajak tahun lalu di Afrika, para ilmuwan Afrika punya respons berbeda. Mereka berkata, "Mengapa Anda tak mengujinya?" Mereka berkata, "Ini tak etis jika tak diuji." Meski ada kemungkinan gagal, taruhannya terlalu besar jika tak dicoba. Jika kami diam saja, gadis-gadis di luar Durban akan tertular HIV, dan nantinya jika ada virus baru muncul, posisi kita akan sama rentannya seperti sekarang. Dengan karantina yang lemah dan vaksin yang ditunggu berbulan-bulan mungkin tak cocok.
I think it's time for a new approach that's different than the static approaches of the last century. It's time for a new technology that is less reactive and more proactive. I think it's time for treatments that don't just benefit the most affluent among us but also those who face the greatest adversity. I think it's time for a new type of weapon that matches, or that solves the fundamental mismatch. I think it's time for therapies that can go viral.
Kita butuh pendekatan baru yang berbeda dari pendekatan statis di abad lalu. Ini waktunya bagi teknologi baru yang kurang reaktif jadi lebih proaktif. Ini waktunya untuk pengobatan tak hanya menguntungkan orang kaya, tapi juga bagi mereka yang kesulitan. Ini waktunya bagi senjata tipe baru menghapus ketidakcocokkan utama. Ini waktunya terapi dipopulerkan.
Thank you very much.
Terima kasih banyak.
(Applause)
(Tepukan tangan)