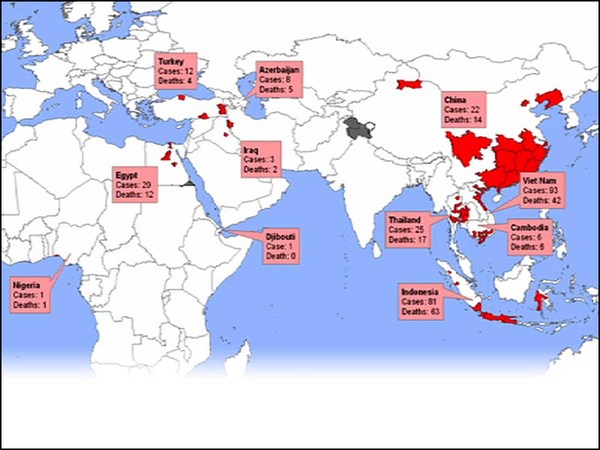
I want to tell you about a student of mine. A few weeks ago, she was on vacation when at 3am she got a phone call. It was her husband telling her that the city that she was in would be quarantined by 10am. She was in Wuhan, China. The epicenter of the coronavirus outbreak. By 8am she was on the road in a friend's car driving 500 miles to Shanghai Airport. The entire time, she was terrified the authorities would arrest her. She made it out on one of the last flights.
میخواهم در مورد یکی از دانشجوهایم بگویم. چند هفته پیش، وقتی او در تعطیلات بود در ساعت ۳ صبح یک تماس داشت. شوهرش بود که به او میگفت: شهری که در آن هستی ساعت ۱۰ قرنطینه میشود. او در شهر ووهان چین بود. مرکز شیوع ویروس کرونا. ساعت ۸ صبح او در جاده بود در اتومبیل دوستش ۸۰۰ کیلومتر را تا فرودگاه شانگهای رانندگی کرد. تمام مدت میترسید مقامات او را دستگیر کنند. بالاخره او به یکی از آخرین پروازها رسید.
So we're all relieved that she's back home, safe in the US. But what if I told you she was in this room? What if I told you she was sitting next to you? There's no vaccine. There won't be a vaccine for at least 12 months. And this virus is mutating, so there's no guarantee that the vaccine that we produce 12 months from now will match the mutated virus. We're always playing catch-up. And this is the scenario we're in every time there's an outbreak. Our quarantines are porous, our medical responses are flat-footed.
خب، خیال همه ما از بازگشتش به خانه راحت شد، امن در ایالت متحده. اما چه میشود اگر به شما بگویم او در این اتاق بود؟ چه میشود اگر به شما بگویم کنار شما نشسته بود؟ هیچ واکسنی وجود ندارد. حد اقل برای ۱۲ ماه هیچ واکسنی وجود نخواهد داشت. و این ویروس درحال جهش یافتن است، بنابراین هیچ تضمینی وجود ندارد واکسنی که ما تا ۱۲ ماه دیگر تولید میکنیم با ویروس جهش یافته مطابقت خواهد داشت. ما همیشه بازیچه میشویم. و این سناریویی است که هر زمان بیماریای شایع میشود ما در آن هستیم. قرنطینههای ما متخلخل هستند، پاسخهای پزشکی ما بدردنخور هستند.
The fundamental problem that we face in controlling these outbreaks is that viruses and other infections do two things really well: they mutate and they transmit. Our medical tools do neither of these two things. Our medical tools don't mutate or transmit. We have a fundamental mismatch between our tools, which are static, and the infections, which are dynamic. This mismatch is why we're always flat-footed. This mismatch is why we're playing catch-up. And this mismatch is universal. It's the reason that we have antibiotic-resistant infections that killed 40,000 Americans last year, and it's the reason that the flu vaccine couldn't prevent the flu from killing 60,000 Americans last year. So how do we resolve this fundamental mismatch?
مشکل اساسی که در کنترل این شیوع با آن روبرو هستیم این است که ویروسها و سایر عفونتها دو کار را به خوبی انجام میدهند: جهش پیدا میکنند و آنها را انتقال میدهند. ابزارهای پزشکی ما هیچ یک از این دو کار را انجام نمیدهند. ابزارهای پزشکی ما جهش نمییابد یا انتقال نمیپذیرد. ما بین ابزارهای خود یک عدم تطابق اساسی داریم، که ایستا هستند، و عفونتها که پویا هستند. به دلیل این عدم تطابق است ما همیشه ناکارآمد هستیم. برای همین است که ما همیشه گول میخوریم. و این عدم تطابق جهانی است. این دلیلی است که ما عفونتهای مقاوم به آنتی بیوتیک داریم که سال گذشته ۴۰,۰۰۰ آمریکایی را کشت، و این دلیلی است که واکسن آنفولانزا نمیتواند مانع از کشته شدن ۶۰،۰۰۰آمریکایی آمریکایی توسط آنفولانزا در سال گذشته گردد. خب چگونه این عدم تطابق اساسی را حل و فصل کنیم؟
I've devoted my career to studying and solving this problem. For 100 years, we've used chemicals as drugs to treat infections. Chemicals will never mutate or transmit. Similarly, our vaccines are not designed to mutate or transmit. 20 years ago, I had a radical idea to use the viruses themselves as therapies -- as building blocks for therapies. To build therapies that could mutate and transmit. Let me share with you how we've had a major breakthrough, and we're already testing these new therapies.
من کارم را برای مطالعه و حل این مشکل اختصاص دادهام. به مدت ۱۰۰ سال است که، ما از مواد شیمیایی برای درمان عفونتها به عنوان دارو استفاده کردهایم. مواد شیمیایی هرگز جهش یا انتقال نخواهند داشت. به همین ترتیب، واکسنهای ما طوری طراحی نشدهاند که جهش یا انتقال داشته باشند. ۲۰ سال پیش، من یک ایده بنیادی داشتم استفاده از خود ویروس برای درمان خودش-- به عنوان بلوکهایی برای درمان. برای ساختن روشهای درمانی که میتواند جهش و انتقال یابد. بگذارید با شما در میان بگذارم چگونه موفقیت بزرگی داشتهایم، و درحال آزمایش این روشهای درمانی جدیدهستیم.
HIV is the most devastating pandemic of our era. 75 million infected; 33 million dead. Most of us think that HIV is a solved problem. We have truly amazing antiviral drugs: they're safe and effective, and we've spent 15 years and billions of dollars deploying these drugs around the world. So let's look at the numbers.
ویروس اچ آی وی ویرانگرترین بیماری همه گیر دوران ماست. ۷۵ میلیون نفر آلوده؛ ۳۳ میلیون کشته. بیشترما فکر میکنیم که اچ آی وی یک مشکل حل شده است. ما واقعا داروهای ضد ویروسی شگفتانگیزی داریم: آنها ایمن و موثر هستند، و ما ۱۵ سال وقت صرف کردیم و همینطورمیلیاردها دلار برای بهرهبرداری از این داروها در سراسر دنیا. بنابراین بیایید به اعداد نگاه کنیم.
In 2019, 1.7 million people acquired HIV. This number only hit home for me last year when I visited this rural village outside of Durban, South Africa. I was driving along this dirt road with my 10-year-old daughter in the back seat, and walking next to us on the side of the road were girls, the same age as my daughter, barefoot. My daughter asked about why these girls are barefoot and I had to explain disparity to her, which was hard. But what really shocked me was when my colleagues, the local African scientists explained to me that these young girls the same age as my daughter --
در سال ۲۰۱۹، ۱/۷میلیون نفر به اچ آی وی مبتلا شدند. این تعداد را من فقط در سال گذشته دیدم وقتی برای بازدید از یکی از دهکدههای خارج از دوربان آفریقای جنوبی رفته بودم. داشتم در طول این جاده خاکی رانندگی میکردم با دختر ۱۰ سالهام در صندلی عقب، و در کنار ما دخترانی بودند که در کنار جاده راه میرفتند، هم سن دخترم، پابرهنه. دخترم پرسید چرا این دختران پابرهنه هستند؟ و من مجبورشدم تفاوتها را برای او توضیح دهم، که سخت بود. اما آنچه واقعاً شوکهام کرد زمانی بود که همکارم، دانشمند محلی آفریقایی به من توضیح داد که این دختران جوان هم سن دخترم --
(Breathes)
(نفس می کشد)
sorry -- had an 80 percent chance of acquiring HIV in their lifetime. It blew me away. How can these girls have an 80 percent risk if we have safe and effective drugs?
ببخشید -- به احتمال ۸۰ درصد در طول عمر خود به ایدز مبتلا میشوند. این من را تخریب کرد. چطور این دختران ۸۰ درصد در خطر هستند اگر داروهای ایمن و موثری داریم؟
The reason is the fundamental mismatch. It creates barriers to controlling infectious disease, particularly in resource-limited settings. The first barrier is mutation: viruses mutate, our drugs don't. The second barrier: adherence. It's really hard to get these drugs to those who need the most. I can't even adhere to a week-long antibiotic regimen in this country. We're asking those in resource-limited settings who face enormous adversity to adhere to lifelong regimens.
دلیل آن، عدم تطابق اساسی است. این برای کنترل بیماریهای عفونی موانعی ایجاد میکند، به خصوص در محیطهای با منابع محدود. اولین مانع جهش است: ویروسها جهش مییابند، داروهای ما اینگونه نیستند. مانع دوم: اعتقاد و تبعیت است. رسیدن این داروها به کسانی که بیشترین نیاز را دارند واقعاً سخت است. من حتی نمیتوانم یک هفته به رژیم آنتی بیوتیک در این کشور پایند باشم. در محیطهای با منابع محدود از آنها که با سختیهای زیادی مواجهاند میخواهیم به رژیمهای مادام العمر پایبند باشند.
And the third barrier is deployment, or access. It's super hard to get these drugs to those who need them most. Not these girls but those who engage in high-risk activities, such as commercial sex work and injection drug use. In the epidemiological parlance, these groups are called "super-spreaders." And in the 1900s, a small subset of super-spreaders drove HIV along the Trans-Africa Highway and spread the virus through the continent like this. These groups are exceptionally hard to identify, they're small, they face enormous social stigma so they don't self-identify and they're the ones we need to get to the most. All of these barriers combined created the situation we have today, where greater than 15 percent of people in Southern Africa live with HIV.
و مانع سوم استقرار است، یا دسترسی. رساندن این داروها به کسی که بیشترین نیاز به آن را دارد بسیار سخت است. نه این دختران بلکه کسانی که مشغول فعالیتهای پرخطر هستند، مانند کارگرهای جنسی تجاری و مصرف کنندگان مخدرهای تزریقی. در اصطلاح اپیدمیولوژیک، به این گروه ها «ابر منتشرکننده» گفته میشود. و در دهه ۱۹۰۰، یک زیرمجموعه کوچکی از ابر پخشکنندهها در گروهی در حال عبور از راههای آفریقا وجود داشت و شیوع این ویروس در این قاره صورت گرفت. شناسایی این گروهها بسیار دشوار است، آنها کوچک هستند، آنها با ننگ عظیم اجتماعی روبرو هستند بنابراین خود را شناسایی نمیکنند و کسانی هستند که باید بیشتر از همه به آنها برسیم. همه این موانع با هم ترکیب شدهاند و وضعیت امروز ما را ایجاد کردهاست، که بیش از ۱۵ درصد مردم در آفریقای جنوبی با اچ آی وی زندگی میکنند.
Now, conventional wisdom is: what we need to do is get more drugs to more people more effectively. I'd argue we need to solve the fundamental mismatch; we need to eliminate these barriers. If we can build therapies that mutate and transmit, we can overcome drug resistance, overcome adherence barriers, and if we do it properly, we will convert the super-spreaders from the greatest barrier to the most powerful deployment strategy that we can imagine.
در حال حاضر، عقل متعارف این است: آنچه باید انجام دهیم تهیه داروی بیشتر برای افراد بیشتر است. من استدلال می کنم: ما باید عدم تطابق اساسی راحل کنیم؛ ما باید این موانع را برطرف کنیم. اگر بتوانیم روشهای درمانی بسازیم که جهش و انتقال پیداکنند، ما میتوانیم بر مقاومت دارویی غلبه کنیم، غلبه برموانع پایبندی، و اگر ما آن را به درستی انجام دهیم، ما ابر پخشکنندهها را از بزرگترین مانع تبدیل خواهیم کرد به قدرتمندترین استراتژی استقراری که میتوانیم تصور کنیم.
This is a radical concept. It has huge potential payoff, but there's a catch. And it's serious. Before we deploy a therapy that may transmit, even if it's only in a limited population of already infected individuals, before we do this, we need to be exceptionally careful, and we need to test safety in the most rigorous ways possible. The reason I'm here today is because for the first time 20 years, we got it to work, and this is the first time I'm sharing it publicly.
این یک مفهوم رادیکال و بنیادی است. این بازده بالقوه زیادی دارد، اما یک چالش وجود دارد. و جدی است. قبل از اینکه ما یک روش درمانی را بخواهیم گسترش دهیم و منتقل کنیم، حتی اگر فقط در جمعیت محدودی از افراد آلوده باشد، قبل از انجام این کار، ما باید فوق العاده مراقب باشیم، و ما باید ایمنی را به سختگیرانه ترین روشهای ممکن آزمایش کنیم. دلیل اینکه امروز برای اولین بار بعد از ۲۰ سال اینجا هستم این است که، ما فهمیدیم که این کار جواب داده، و این اولین بار است که آن را به صورت عمومی به اشتراک میگذارم.
(Applause and cheers)
(تشویق و تحسین)
Last two times I did this I cried, so --
دوبار آخر که این کار را کردم گریم گرفت--
(Laughter)
(خنده)
So in order to help you understand this breakthrough, let me take you back 20 years to 1999. I was a graduate student in Berkeley, California, studying the biophysics of HIV. For such a complex epidemic, the simplicity of this virus fascinated me. HIV, like all viruses, is just an instruction set -- malware. It hijacks a cell and converts that cell into a factory to do one thing: single-mindedly churn out more virus. All the normal functions of the cell get wiped away. HIV infects the white blood cell that keeps us healthy. This cell has already been hijacked and converted into a factory. And if we magnify, we can see the anatomy of the virus. Those squiggly red lines in the middle? That's HIV's instruction set. Its genetic material.
بنابراین برای کمک به شما در درک این پیشرفت، بگذارید شما را به ۲۰ سال قبل برگردانم به سال ۱۹۹۹. وقتی از دانشگاه برکلی کالیفرنیا فارغ التحصیل شدم، در باره بیوفیزیک اچ آی وی مطالعه میکردم. برای چنین اپیدمی پیچیدهای، سادگی این ویروس من را مجذوب خود کرد. اچ آی وی، مانند همه ویروس ها، فقط یک مجموعه دستورالعمل است -- نرم افزارهای مخرب. یک سلول را ربوده و آنرا به کارخانهای مبدل میکند تا کاری انجام دهد: تمرکز بر تولید انبوه ویروس بیشتر. تمام عملکردهای طبیعی سلول از بین میرود. اچ آی وی گلبولهای سفید خون را که باعث سلامت ما میشود، آلوده میکند. این سلول قبلاً گروگان گرفته شده و به کارخانه تبدیل شده است. و اگر بزرگنمایی کنیم ، ما میتوانیم آناتومی ویروس را مشاهده کنیم. خطوط قرمز در وسط؟ اینها مجموعه دستورالعملهای اچ آی وی است. مواد ژنتیکی آن
This genetic material directs the hijacking process, converting that cell into a factory first to make more copies of the instruction set, and then all the other components of the virus and assemble them into a particle. This is how the virus replicates. Each of these particles can go in and hijack a new cell. This is how the virus transmits. And every time a cell is hijacked, little mistakes are made in copying the genetic material. That's how the virus mutates. This ability to replicate, transmit and mutate is something that our current drugs cannot do.
این ماده ژنتیکی روند گروگان گیری سلول را هدایت میکند، اول تبدیل آن سلول به یک کارخانه برای ایجاد نسخههای بیشتر از مجموعه دستور العملها، و سپس تمامی اجزای دیگر ویروس و سرهم کردن آن به صورت جزء به جرء. به این ترتیب ویروس منتقل میشود. هریک از این ذرات میتوانند وارد شوند و سلول جدیدی را بربایند. به این ترتیب ویروس تکثیر میشود. و هر بار که یک سلول ربوده میشود، در کپی کردن مواد ژنتیکی اشتباهات کمی انجام می شود. به این ترتیب ویروس جهش مییابد. این توانایی برای تکثیر، انتقال و جهش کاریاست که داروهای فعلی ما قادر به انجام آن نیست.
So, being young and naïve and a little bit ignorant, I thought: why can't we create therapies that mutate and transmit and replicate? Here was the idea. If we can take the virus and engineer it to amputate the genetic material in blue here, this amputated instruction set can no longer hijack a cell. But this amputated instruction set can do something very special. In an already infected cell, this amputated instruction set can hijack the hijacker. It can commandeer HIV's machinery to make more copies of itself, the amputated instruction set, and then each of these copies can steal all of HIV's other components so that the cell gets converted from a factory that produces virus to a factory that produces therapy. Hijackers. These carry no disease. This dramatically lowers HIV levels and keeps the cell healthier.
بنابراین، جوان و ساده لوح و کمی نادان بودن، فکر کردم: چرا ما نمیتوانیم درمانی ایجاد کنیم که جهش و انتقال و تکثیر داشته باشد؟ این ایده بود. اگر بتوانیم ویروس را برداریم و آن را مهندسی کنیم تا مواد ژنتیکی را با رنگ آبی در اینجا قطع کند، آن وقت این مجموعه دستورالعمل قطع شده دیگر نمی تواند سلول را بدزدد. اما این مجموعه دستورات قطع شده میتواند کار بسیار خاصی انجام دهد. در یک سلول قبلاً آلوده، این مجموعه دستورالعمل قطع شده میتواند گروگانگیر را بدزدد. این میتواند سازوکار اچ آی وی را برای کپی کردن از خودش به خدمت در بیاورد، مجموعه دستورات قطع شده، و سپس هریک از این کپیها میتواند تمام اجزای دیگر اچ آی وی را بدزدد به طوری که سلول از کارخانه تولید ویروس تبدیل میشود به کارخانهای که درمان ایجاد میکند. گروگانگیرها. اینها هیچ بیماری ایجاد نمیکنند. این به طور چشمگیری سطح اچ آی وی را کاهش میدهد و سلول را سالم تر نگه میدارد.
This idea consumed me for months. It was the most intense intellectual experience of my life. On every bike ride to lab, on every walk to the coffee shop, on every run in the hills above campus, the ideas, the arguments, the counterarguments, they all came so rapidly in my head, in my inner monologue, that I was physically out of breath. I thought if we can create a therapy that replicates, it would only need to be taken once. It could mutate along with the virus and possibly it could transmit between infected individuals to treat them. It was a therapy that could do all of the things that the virus could do. It solved the fundamental mismatch.
این ایده من را درگیر کرده بود. ماهها. این شدیدترین چالش فکری زندگی من بود. در هر دوچرخه سواری به آزمایشگاه، در هر پیادهروی به کافی شاپ، در هر دویدن در تپههای بالای دانشگاه، ایدهها، استدلالها، ضد استدلالها، همه آنها خیلی سریع وارد سر من شدند، در مونولوگ درونی من، از نظر جسمی من رو از نفس انداخته بود. فکرکردم اگر بتوانیم درمانی ایجاد کنیم که، فقط یکبار لازم است مصرف شود، میتواند همراه با ویروس جهش یابد و احتمالاً میتواند بین افراد آلوده منتقل شود برای درمان آنها. این درمانی بود که میتوانست همه کارهایی را که ویروس میتواند انجام دهد، انجام دهد. این عدم تطابق اساسی را برطرف کرد.
The most radical part of this concept was that the super-spreaders would also be converted from transmitting the virus to now transmitting the therapy. It was a therapy that would go viral along with the virus. This scared some people. But there's already a precedent: we already inadvertently use therapies that transmit. The vaccine that eradicated polio in the US, the oral polio vaccine, transmits between people. It's not well-known, but the fact that this vaccine transmits is part of the reason that it was chosen for the worldwide eradication effort despite its safety issues.
اساسی ترین قسمت این مفهوم این بود که ابر پخش کننده ها نیز باید تبدیل شوند از یک منتقل کننده ویروس به یک منتقل کننده درمان. این درمانی بود که همراه با سرعت ویروس منتقل و منتشر میشد. این برخی افراد رو ترسوند. اما در حال حاضر یک نمونه وجود دارد: ما پیش از این به طور ناخواسته از روشهای درمانی استفاده کردیم. واکسنی که فلج اطفال را در ایالات متحده از بین برد، واکسن خوراکی فلج اطفال، بین مردم منتقل میشد. شناخته شده و مشهور نیست، اما در واقع قابل انتقال بودن این واکسن بخشی از دلیلی است که از این واکسن برای نابودی بیماری در سراسر جهان استفاده میشد با وجود مسائل ایمنی آن.
So the bigger problem was that these hijacker therapies didn't exist. My Berkeley advisors said to me, "Lovely idea, so sad it will never work," or, "Regulators will never allow it, drop it." But the idea wouldn't drop me.
خب مشکل بزرگتر این بود که در این روشهای درمانی گروگانگیر های سلولی وجود نداشتند. مشاوران من در دانشگاه برکلی به من گفتند، « ایده خوبیاست، اما بسیار تاسف آور است که هرگز عملی نخواهد شد.» یا، « تنظیم کنندگان هرگز اجازه نمیدهند، ولش کن.» اما این ایده من را رها نمیکند.
If it ever worked, it would solve the fundamental mismatch. So we tried for years to build it. We tried every trick in the book and failed over and over again. We -- every time we thought we had a good idea, we'd spend months, sometimes years working on it only to come up empty. We once spent five years building 150,000 versions of a hijacker therapy. Every single one failed. I once asked a really bright student what he hoped to learn from me during his PhD --
اگر تا کنون جواب داده، میتواند عدم تطابق اساسی را حل کند. پس ما سالها برای ساختن آن تلاش کردیم. ما هر ترفندی را امتحان کردیم و بارها و بارها شکست خورد. ما-- هر وقت فکر میکردیم ایده خوبی داریم، ماهها، گاهی اوقات سالها، روی آن کار میکردیم تا وقتی پوچ از آب دربیاد. ما یک بار پنج سال وقت صرف کردیم ساخت ۱۵۰,۰۰۰ نسخه از گروگانگیرهای درمانی. تک تک شکست خورد. یکبار ازیک دانشجوی درخشانم پرسیدم: امیدی داری چیزی از من یاد بگیری در دوره دکترا --
(Laughter)
(خنده)
And he replied, "How to keep going, how to continue moving forward despite zero evidence that there's anything there."
و او پاسخ داد، «چگونه میتوان ادامه داد، چگونه میتوان به جلو حرکت کرد با وجود صفر دستآوردی که تاکنون کسب کردیم.»
(Laughter)
(خنده)
I wonder if he was trying to tell me something.
نمیدانم آیا او میخواست چیزی به من بگوید؟
(Laughter)
(خنده)
By 2018, things looked bad. There was no evidence that a hijacker therapy could be engineered. In fact, we had evidence that it might be impossible. It was time to face the hard truth. This solution that I'd wanted so badly, this hijacker therapy just didn't exist. For 20 years, I had been chasing a ghost.
تا سال ۲۰۱۸، اوضاع بد به نظر میرسید. هیچ مدرک و دستآوردی وجود نداشت که یک گروگانگیری درمانی میتواند مهندسی شود. در حقیقت، ما شواهدی داشتیم که ممکن است این کاری غیرممکن باشد. روبرو شدن با حقیقت زمان سختی بود. این راه حل که خیلی دوستش داشتم، این راه سلول درمانی وجود ندارد. به مدت ۲۰ سال، من دنبال سراب میدویدم.
Then one day, Elizabeth, a postdoc in my lab, came to me with this picture. It doesn't look like much. My wife thinks it looks like a pregnancy test.
سپس یک روز، الیزابت، یک فوق دکترا در آزمایشگاه من، با این تصویر پیش من آمد. زیاد شبیه به نظر نمیرسد. همسرم فکر میکند مثل آزمایش بارداری است.
(Laughter)
(خنده)
But this little band down here -- that was the amputated genetic material that we had been looking for for 20 years. The entire time that we had been trying to build it and failing, it had evolved by itself in a flask in the back of the lab.
اما این گروه کوچک این پایین -- این ماده ژنتیکی قطع شده بود که ما ۲۰ سال بدنبال آن بودیم. کل زمانی که ما برای ساختن آن تلاش کرده بودیم و شکست میخوردیم، به خودی خود در یک فلاسک در پشت آزمایشگاه تکامل یافته بود.
(Audience) What?
(مخاطبان) چی؟
(Laughter)
(خنده)
We finally had a foothold. And we used this to build the first hijacker. But we had no evidence that what we built was a therapy.
ما سرانجام سرنخی داشتیم. و ما از این برای ساخت اولین گروگانگیر سلولی استفاده کردیم. اما هیچ مدرکی دال بر اینکه آنچه ساخته بودیم یک روش درمانی بود، نداشتیم.
The first hurdle that any therapy has to clear is testing in a mouse. It can be risky. In our case, if our mice died, so did our funding, and with it, any hopes of this becoming a therapy, let alone a transformative one. After so many failures, we were all pretty skeptical but we didn't really have an alternative. We had to give it a shot; we had to try.
اولین مانعی که هر درمانی باید برطرف کند تست روی موش است. این میتواند خطرناک باشد. درمورد ما ، اگر موشهای ما میمردند، بودجه ما نیز قطع میشد، و با آن، هر گونه امید به درمان شدن ناکام میماند، چه رسد به تحول آفرینی. بعد از این همه شکست، همه ما کاملاً شک داشتیم اما در واقع گزینه دیگری نداشتیم. ما مجبور شدیم تیرآخر را شلیک کنیم. باید تلاش میکردیم.
Amazingly, the hijacker therapy worked in a mouse, and it worked exactly as we'd predicted 20 years before. It protected the cells in a mouse from HIV. Here are the cells under a microscope. First, HIV in red infects those cells, and then the hijacker, in blue, can be activated, protects those cells and transmits to other cells. We'd finally built the hijacker after 20 years. Everyone in the lab was elated. For me, this was proof of concept. If we could do it for one virus we could do it for others.
شگفت آوراست، گروگانگیری سلولی در موش کار کرد، و دقیقاً همانطور که ۲۰ سال قبل پیش بینی کرده بودیم کار کرد. از سلولهای موش در برابر اچ آی وی محافظت کرد. در اینجا سلولهای زیر میکروسکوپ را داریم. ابتدا، اچ آی وی در رنگ قرمز باعث آلوده شدن این سلولها میشود، و سپس گروگاگیر سلولی، با رنگ آبی، میتواند فعال شود، ازسلولها حفاظت میکند وبه سلولهای دیگر پخش میشود. ما سرانجام بعد از ۲۰ سال گروگانگیر سلولی را میساختیم. همه افراد در آزمایشگاه سرحال بودند. برای من، این مدرک اثبات مفهوم بود. اگر این روی یک ویروس جواب میداد، روی بقیه ویروس ها هم میشد.
To understand how this hijacker might impact HIV levels worldwide, we ran computer simulations. Epidemiological models. And the results were pretty amazing. If we do nothing in the hardest-hit parts of Africa, HIV prevalence will stay between 25 and 30 percent. If we manage to introduce drugs to three-quarters of the population or if we ever get the long-sought-after vaccine, we would reduce those numbers down to 20 percent. But those are best-case scenarios. If HIV evolves resistance or if people change their behaviors, these numbers could go right back up to 30 percent or even beyond. The blue is the hijacker therapy. And we've not found a way, either theoretically or experimentally, that HIV can evolve resistance to the hijacker.
برای درک اینکه این سلولها چگونه میتواند برسطح اچ آی وی در سراسرجهان تأثیر بگذارد، شبیه سازی رایانه ای انجام دادیم، مدلهای اپیدمیولوژیک. و نتایج بسیار شگفت انگیز بود. اگر ما در مناطق آسیب دیده آفریقا کاری انجام ندهیم، شیوع اچ آی وی بین ۲۵ تا ۳۰ درصد باقی خواهد ماند. اگر ما موفق به معرفی دارو به سه چهارم مردم شویم یا حتی اگر به واکسن با اثر طولانی مدت برسیم، میتوانیم این تعداد را به ۲۰ درصد کاهش دهیم. اما این سناریوها در بهترین حالت هستند. اگر اچ آی وی مقاومت نشاندهد یا اگر مردم رفتارهای خود را تغییر دهند، این اعداد میتوانند تا ۳۰ درصد برگردند یا حتی بیشتر. آبی، گروگان درمانی است. و هنوز راهی پیدا نکردیم، هم از لحاظ تئوری و چه از نظر تجربی، اچ آی وی میتواند تکامل پیداکند و دربرابر گروگانگیر سلولی مقاومت کند.
The reason this hijacker works so well is the super-spreaders. If the hijacker is introduced in one place over here, the super-spreaders can pick it up and transmit it through the population. Imagine if 10 years from now, HIV is no longer a pandemic.
دلیل این که این گروگانگیر سلولی بسیار خوب کار میکند سرعت پخش فوق العاده است. اگر گروگانگیر سلولی در اینجا معرفی و منتشر شود، ابر پخش کنندهها میتوانند آن را بردارند و از طریق جمعیت حاظر منتقلش کنند. تصور کنید ۱۰ سال بعد، اچ آی وی دیگر یک بیماری همه گیر نیست.
To get there, we have to start large-scale clinical trials in five years, which means initial human tests next year. The FDA has cleared us to start testing in HIV-positive patients who have a terminal cancer and have less than a year left to live. Volunteering for this trial is their last incredibly generous gift to the world. They're called the "Last Gift cohort." And to test in these altruistic patients next year, we have to finish our preclinical tests this year ... and I think we will.
برای رسیدن به آن نقطه، ما باید آزمایش های بالینی در مقیاس بزرگ را در مدت پنج سال شروع کنیم، که به معنای آزمایش های اولیه انسانی در سال آینده است. سازمان غذا و دارو ما را برای شروع آزمایش در بیماران اچ آی وی مثبت ترغیب کرده است کسانی که سرطان غیر قابل درمان دارند و کمتر از یک سال برای زندگی زمان دارند. داوطلب شدن در این آزمایش آخرین هدیه فوق العاده سخاوتمندانه آنها به جهان است. آنها « آخرین گروه هدیه» نامیده میشوند. و آزمایش در این بیماران نوع دوست سال آیندهاست، ما باید امسال آزمایشات بالینی خود را به پایان برسانیم ... و فکرکنم انجام خواهیم داد.
I still meet colleagues who push back and are stridently opposed to letting us move forward with testing. They say, "What if something goes wrong? You can't unrelease it." They say, "There are ethical issues; people can't consent." Well, oral polio vaccine faced similar ethical and safety concerns. In fact, oral polio vaccine faced such an effective misinformation campaign that most people still don't know that it transmits, that it successfully eradicated polio in many countries or that this vaccine is the basis for new vaccines. When we presented this hijacker therapy idea in Africa last year, the African scientists had a different response. They said, "How can you not test this?" They said it's unethical to not test it. So even though we might fail, I think the stakes are too high not to try. If we do nothing, those girls outside of Durban will acquire HIV, and the next time that there's a new virus that emerges, we'll be in the same vulnerable position that we are today with quarantines that are porous and vaccines that we need to wait months for that may not match.
من هنوزهمکارانی را میبینم که مخالفند و کاملاً مخالف این هستند که به ما اجازه دهند با آزمایش جلو برویم. آنها میگویند: «اگر مشکلی پیش بیاید چه؟ نمیتوانید آنها را خلاص کنید.» آنها میگویند، « مسائل اخلاقی وجود دارد؛ مردم رضایت نخواهند داد.» واکسن فلج اطفال خوراکی با نگرانیهای اخلاقی و ایمنی مشابهی روبرو شدهاست. در واقع، واکسن فلج اطفال خوراکی با چنین کمپین موثراطلاعات غلط روبرو شد که اکثر مردم هنوز نمیدانند قابللیت انتقال بود که، فلج اطفال را با موفقیت در بسیاری از کشورها ریشه کن کرد یا اینکه این واکسن اساس واکسنهای جدید است. وقتی ما سال گذشته این ایده سلول درمانی را در آفریقا ارائه دادیم، دانشمندان آفریقایی پاسخ متفاوتی داشتند. آنها گفتند: «چگونه میتوانید این را آزمایش نکنید؟» آنها گفتند که آزمایش نکردن غیراخلاقی است. حتی اگر امکان داشته باشد شکست بخوریم، من فکر میکنم مخاطرات برای تلاش زیاد نیستند. اگر کاری نکنیم، آن دختران خارج از دوربان آفریقا به اچ آی وی مبتلا میشوند، و دفعه بعدی که ویروسی جدید ظاهر شد، در همان موقعیت آسیب پذیر امروزی خواهیم بود با قرنطینههای پر از اشکال و واکسنهایی که ممکن است ماهها صبر کنیم و ممکن است مطابقت نداشته باشد.
I think it's time for a new approach that's different than the static approaches of the last century. It's time for a new technology that is less reactive and more proactive. I think it's time for treatments that don't just benefit the most affluent among us but also those who face the greatest adversity. I think it's time for a new type of weapon that matches, or that solves the fundamental mismatch. I think it's time for therapies that can go viral.
من فکر میکنم زمان یک رویکرد جدید است که متفاوت از رویکردهای ایستا در قرن گذشته است. زمان فنآوری جدیدی است که انفعال کمتری دارد و فعال تر هستند. من فکر میکنم زمان درمان رسیدهاست که فقط به نفع افراد مرفه نیست بلکه برای کسانیست که با بزرگترین ناملایمات روبرو هستند. فکر میکنم زمان نوعی سلاح جدید فرا رسیدهاست که مطابقت دارد، یا عدم تطابق اساسی را برطرف میکند. فکرمیکنم زمانش رسیده که روشهای درمانی ویروسی شوند.
Thank you very much.
بسیار از شما متشکرم.
(Applause)
(تشویق و تحسین)