Hi. So, this chap here, he thinks he can tell you the future. His name is Nostradamus, although here the Sun have made him look a little bit like Sean Connery. (Laughter)
سلام، خب، این رفیقمون اینجا اون فکر می کنه که می تونه آینده رو پیش بینی کنه. اسمش نوسترآداموس هستش، هرچند اینجا سان اون رو شبیه شان کانری کرده (صدای خنده)
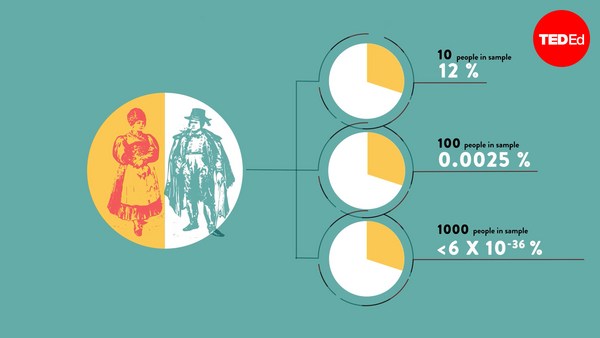
And like most of you, I suspect, I don't really believe that people can see into the future. I don't believe in precognition, and every now and then, you hear that somebody has been able to predict something that happened in the future, and that's probably because it was a fluke, and we only hear about the flukes and about the freaks. We don't hear about all the times that people got stuff wrong. Now we expect that to happen with silly stories about precognition, but the problem is, we have exactly the same problem in academia and in medicine, and in this environment, it costs lives.
و مثل خیلی از شماها، فکر کنم، من اعتقادی به این که مردم آینده رو می بینند ندارم. من اعتقادی به آیندهبینی ندارم، و هر چند وقت یک بار آدم می شنوه یه نفر تونسته یه چیزی رو پیش بینی کنه که در آینده اتفاق می افتاده، احتمالا به این دلیل هست که این یک حادثه بوده، و ما فقط در مورد حادثه ها و عجایب می شنویم. تمام اون مواردی که این آدمها اشتباه پیش بینی کردن رو نمی شنویم. ما انتظار داریم که این اتفاق احمقانه در مورد آیندهبینی بیفته، اما مشکل این هست که این مشکل عینا در محیط آکادمیک هم اتفاق می افته و در پزشکی هم٬ و در اینجا٬ به هزینه جون آدمها تموم میشه.
So firstly, thinking just about precognition, as it turns out, just last year a researcher called Daryl Bem conducted a piece of research where he found evidence of precognitive powers in undergraduate students, and this was published in a peer-reviewed academic journal and most of the people who read this just said, "Okay, well, fair enough, but I think that's a fluke, that's a freak, because I know that if I did a study where I found no evidence that undergraduate students had precognitive powers, it probably wouldn't get published in a journal. And in fact, we know that that's true, because several different groups of research scientists tried to replicate the findings of this precognition study, and when they submitted it to the exact same journal, the journal said, "No, we're not interested in publishing replication. We're not interested in your negative data." So this is already evidence of how, in the academic literature, we will see a biased sample of the true picture of all of the scientific studies that have been conducted.
پس اولا، فقط در مورد آیندهبینی، معلوم شد، پارسال محققی به نام دریل بم، تحقیق کوچکی انجام داد که تونست شواهدی از قدرت آیندهبینی توی دانشجوهای لیسانس پیدا کنه٬ و این توی یک مجله که مقاله ها بازبینی و چاپ میشن، چاپ شد و بیشتر مردمی که اون رو خوندن گفتن٬ خیلی خب٬ باشه٬ ولی من می فکر میکنم این فقط یک حادثه است و یه چیز عجیب غریبه. چونکه من می دونم اگر من تحقیقی انجام بدم که هیچ نشونهای از قدرت پیش بینی آینده تو دانشجوهای لیسانس توش پیدا نشه٬ اون احتمالا توی هیچ مجلهای چاپ نمیشه. و ما می دونیم که این یک حقیقت هستش چرا که، گروههای مختلفی از محقفین سعی کردن نتایچ این تحقیق رو در مورد آیندهگویی تکرار کنند٬ اما وقتی نتایج رو برای همون مجله فرستادن، مجله اعلام کرد ما علاقه ای به چاپ تحقیقات تکرار نتایج نداریم ما به داده های منفی شما علاقهای نداریم. بنابراین این خود نشان دهنده این است که، در دنیای آکادمیک، ما مثالی از تعصبی رو میبینیم که تمام تحقیقات علمی انجام شده بهش دچار هستند.
But it doesn't just happen in the dry academic field of psychology. It also happens in, for example, cancer research. So in March, 2012, just one month ago, some researchers reported in the journal Nature how they had tried to replicate 53 different basic science studies looking at potential treatment targets in cancer, and out of those 53 studies, they were only able to successfully replicate six. Forty-seven out of those 53 were unreplicable. And they say in their discussion that this is very likely because freaks get published. People will do lots and lots and lots of different studies, and the occasions when it works they will publish, and the ones where it doesn't work they won't. And their first recommendation of how to fix this problem, because it is a problem, because it sends us all down blind alleys, their first recommendation of how to fix this problem is to make it easier to publish negative results in science, and to change the incentives so that scientists are encouraged to post more of their negative results in public.
اما این تنها در دنیای خشک روانشناسی اتفاق نمی افته. این اتفاق در زمینه تحقیقات برای سرطان هم رخ می ده. به طور مثال در مارس ۲۰۱۲ فقط یک ماه قبل٬ تعدادی از محققین در مجله نیچر گزارش دادند که چگونه تلاش کردهاند که دادههای مربوط به ۵۳ تحقیق را بازآفرینی کنند با نگاه به درمانهای بالقوه برای درمان سرطان٬ و از مجموع ۵۳ تحقیق٬ آنها فقط توانستند دادههای مربوط به ۶ تحقیق را بازسازی کنند. ۴۷ تحقیق از مجموع ۵۳ تحقیق قابل بازسازی نبودند٬ و آنها در نتیجهگیری تحقیقشان گفتند که این احتمالا به علت این هست که چیزهای عجیب چاپ میشن. آدمها تعداد بسیار بسیار زیادی تحقیق انجام می دهند٬ و در صورتی که نتیجهای بگیرند مقاله را چاپ خواهندکرد٬ و آنها یی را که نتیجهای نداره را چاپ نمیکنند. و اولین توصیه آنها برای حل این مشکل٬ که واقعا هم یک مشکل هست٬ چراکه همه مان رو گمراه می کنه٬ این هست که باید در دانش راه رو برای چاپ نتیجه منفی هموارتر کرد٬ و راههای تشویقی را تغییر داد به صورتی که دانشمندان تشویق بشن مقدار بیشتری از دادههای منفیشون رو به صورت عمومی منتشر کنند.
But it doesn't just happen in the very dry world of preclinical basic science cancer research. It also happens in the very real, flesh and blood of academic medicine. So in 1980, some researchers did a study on a drug called lorcainide, and this was an anti-arrhythmic drug, a drug that suppresses abnormal heart rhythms, and the idea was, after people have had a heart attack, they're quite likely to have abnormal heart rhythms, so if we give them a drug that suppresses abnormal heart rhythms, this will increase the chances of them surviving. Early on its development, they did a very small trial, just under a hundred patients. Fifty patients got lorcainide, and of those patients, 10 died. Another 50 patients got a dummy placebo sugar pill with no active ingredient, and only one of them died. So they rightly regarded this drug as a failure, and its commercial development was stopped, and because its commercial development was stopped, this trial was never published.
اما این فقط در محیط خشک تحقیقات پیش بالینی ساده در مورد سرطان اتفاق نمیافته. این همچنین اتفاق می افته در دنیای کاملا واقعی پزشکی دانشگاهی هم اتفاق میافته. مثلا در سال ۱۹۸۰ تعدادی محقق در مورد داروی به نام «لورکاناید» شروع به تحقیق کردند٬ و این یک داروی ضد آریتمی بود٬ دارویی که ضربان غیرعادی قلب رو از بین میبره٬ ایده این بود که بعد از این که آدمی سکته قلبی کرد٬ به احتمال زیاد ضربان قلبش نامنظم میشه٬ پس اگر ما به اونها دارویی بدیم که ضربان غیرعادی رو از بین ببره٬ احتمال زنده موندن اون آدمها رو بالا بردیم. در همون اوایل که این درمان داشت شکل میگرفت٬ آنها تحقیق کوچکی٬ با شرکت ۱۰۰ نفر بیمار انجام دادند. ۵۰ نفر از بیماران «لورکاناید» مصرف کردند ٬ و از اونها ٬۱۰ نفر مردند. ۵۰ بیمار دیگر داروینمای ساختگی از جنس شکر مصرف کردند که هیچ ماده فعالی نداشت و فقط یک نفر از اونها مرد. پس محققین به درستی این دارو را از رده خارج کردند٬ و تولید تجاری اون متوقف شد٬ و به این دلیل که تولید تجاری این دارو متوقف شد٬ این تحقیق هیچگاه چاپ نشد.
Unfortunately, over the course of the next five, 10 years, other companies had the same idea about drugs that would prevent arrhythmias in people who have had heart attacks. These drugs were brought to market. They were prescribed very widely because heart attacks are a very common thing, and it took so long for us to find out that these drugs also caused an increased rate of death that before we detected that safety signal, over 100,000 people died unnecessarily in America from the prescription of anti-arrhythmic drugs.
متاسفانه در طول ۵ تا ۱۰ سال بعد٬ شرکتهای دیگر به همین ایده رسیدند که دارویی که باعث کنترل ضربان قلب باشه می تونه که مانع از سکته بشه. این داروها وارد بازار شدند. به صورت گسترده تجویز شدند چرا که سکته قلبی بسیار شایع بود٬ و مدتها طول کشید تا ما بفهمیم که این داروها نرخ مرگ و میر را بالا می برند. اما قبل از این که زنگ خطر به صدا بیاد٬ در آمریکا بیش از صدهزار نفر بیدلیل مردند٬ به دلیل تجویز داروهای ضد آریتمی.
Now actually, in 1993, the researchers who did that 1980 study, that early study, published a mea culpa, an apology to the scientific community, in which they said, "When we carried out our study in 1980, we thought that the increased death rate that occurred in the lorcainide group was an effect of chance." The development of lorcainide was abandoned for commercial reasons, and this study was never published; it's now a good example of publication bias. That's the technical term for the phenomenon where unflattering data gets lost, gets unpublished, is left missing in action, and they say the results described here "might have provided an early warning of trouble ahead."
حالا البته٬ در سال ۱۹۹۳ محققینی که اون تحقیق رو در سال ۱۹۸۰ انجام داده بودند٬ اون تحقیق اولیه٬ اقرار نامهای نوشتند٬ نامه عذرخواهی خطاب به جامعه علمی٬ در اون گفتند که ٬«وقتی ما تحقیمان را در سال ۱۹۸۰ انجام دادیم٬ فکر کردیم که زیاد شدن تعداد مرگ ها که در گروه «لورکاناید» اتفاق افتاد، اتفاقی بوده است.» به دلایل تجاری توسعه «لورکاناید» متوقف شد٬ و این تحقیق به این دلیل هیچگاه چاپ نشد؛ حالا این یک مثال خوب برای تعصبات چاپ و نشر است. این یک اصطلاح فنی برای مواقعی هست که دادههای دوست نداشتنی گم میشوند یا چاپ نمیشوند٬ به کار نمی روند. و آنها همچنین گفتند که نتایجشان ممکن بود «یک اخطار زودهنگام از مشکلی که پیش رو هست» میداده است.
Now these are stories from basic science. These are stories from 20, 30 years ago. The academic publishing environment is very different now. There are academic journals like "Trials," the open access journal, which will publish any trial conducted in humans regardless of whether it has a positive or a negative result. But this problem of negative results that go missing in action is still very prevalent. In fact it's so prevalent that it cuts to the core of evidence-based medicine. So this is a drug called reboxetine, and this is a drug that I myself have prescribed. It's an antidepressant. And I'm a very nerdy doctor, so I read all of the studies that I could on this drug. I read the one study that was published that showed that reboxetine was better than placebo, and I read the other three studies that were published that showed that reboxetine was just as good as any other antidepressant, and because this patient hadn't done well on those other antidepressants, I thought, well, reboxetine is just as good. It's one to try. But it turned out that I was misled. In fact, seven trials were conducted comparing reboxetine against a dummy placebo sugar pill. One of them was positive and that was published, but six of them were negative and they were left unpublished. Three trials were published comparing reboxetine against other antidepressants in which reboxetine was just as good, and they were published, but three times as many patients' worth of data was collected which showed that reboxetine was worse than those other treatments, and those trials were not published. I felt misled.
حال اینها داستانهایی هستند از دانش پایه. اینها داستانهایی هستند از۲۰ یا ۳۰ سال قبل. محیط چاپ و نشر امروزه بسیار متفاوت هست. امروز مجلات آکادمیکی مثل «ترایالز» وجود دارند٬ مجله که دسترسی به مجله برای همه آزاده. که اینها هر تحقیقی که بر روی انسانها انجام شده باشد فارغ از این که نتیجه بده یا نه رو چاپ میکنند. اما این مشکل که نتایح بد در عملاَ از بین میروند هنوز شایع هست. در حقیقت آنقدر شایع هست که تا بنیان پزشکی مبتنی بر شواهد رو درگیر خوش میکنه. خب این دارویی هست به نام «ربوکسِتین»٬ واین دارویی هست که من خودم تجویز کردم. دارویی ضد افسردگی است. من یک پزشک وسواسی هستم. پس رفتم تمام تحقیقات انجام شده روی این دارو رو مطالعه کردم. من یک تحقیقی رو خوندم که نشون می داد «ربوکسِتین» بهتر از دارونما هستش٬ و همچنین سه تحقیق دیگر رو خوندم که میگفت «ربوکسِتین» تنها مثل بقیه داروهای ضد افسردگی هستش٬ به این علت که بیمار من داروهای دیگه افسردگی روش جواب نداده٬ من گفتم حالا که «ربوکسِتین» به همون خوبی هستش٬ میارزه که امتحانش کنم اما معلوم شد که من گمراه شده بودم. در حقیقت ٬ ۷ آزمایش انجام شده بود تا «ربوکسِتین» با دارونما مقایسه کنه. یکی از اونها تایید می کرد این نظریه رو و چاپ شده بود اما شش تای دیگه نتایج منفی بود و چاپ نشده بودند. ۳ تا آزمایش چاپ شده بودند که «ربوکسِتین» را با باقی ضدافسردگیها مقایسه میکردند که نشون میدادند «ربوکسه تینمسیلات» به همون خوبی هست و آنها چاپ شده بودند٬ اما به اندازه ۳ برابر اون بیماران دیگهای که مورد آزمایش قرار گرفته بودند نشان میدادند که «ربوکسِتین» بدتر از سایر درمانهای دیگه بوده و اونها چاپ نشده بودند. من احساس کردم که گمراه شدهام.
Now you might say, well, that's an extremely unusual example, and I wouldn't want to be guilty of the same kind of cherry-picking and selective referencing that I'm accusing other people of. But it turns out that this phenomenon of publication bias has actually been very, very well studied. So here is one example of how you approach it. The classic model is, you get a bunch of studies where you know that they've been conducted and completed, and then you go and see if they've been published anywhere in the academic literature. So this took all of the trials that had ever been conducted on antidepressants that were approved over a 15-year period by the FDA. They took all of the trials which were submitted to the FDA as part of the approval package. So that's not all of the trials that were ever conducted on these drugs, because we can never know if we have those, but it is the ones that were conducted in order to get the marketing authorization. And then they went to see if these trials had been published in the peer-reviewed academic literature. And this is what they found. It was pretty much a 50-50 split. Half of these trials were positive, half of them were negative, in reality. But when they went to look for these trials in the peer-reviewed academic literature, what they found was a very different picture. Only three of the negative trials were published, but all but one of the positive trials were published. Now if we just flick back and forth between those two, you can see what a staggering difference there was between reality and what doctors, patients, commissioners of health services, and academics were able to see in the peer-reviewed academic literature. We were misled, and this is a systematic flaw in the core of medicine.
حالا ممکنه شما بگین که اون یک مورد بسیار نادر آزمایشگاهی هست و من نمیخواهم همون مصادره به مطلوبی که در مورد مطلب و منابع خودم بقیه رو متهم میکنم انجام بدم. اما ته توی قضیه در اومد که این پدیده تعصب در چاپ مقاله به صورت بسیار بسیار زیادی مورد مطالعه قرار گرفته. خب اینجا یک مورد رو مشخص میکنم که چطور میشه با این برخورد کرد. مورد کلاسیکش میشه این که شما تعدادی از آزمایشاتی که میدونید انجام شده رو جمع میکنید٬ و بعد می روید و تحقیق میکنید ببینید آیا جای معتبری چاپ شدهاند پس این شامل تمام آزمایشاتی میشه که روی داروهای ضدافسردگی شده که طی یک بازده ۱۵ ساله توسط اف دی ای(FDA سازمان دارویی آمریکا) تایید شدهاند. آنها تمام آزمایشاتی که برای تایید دارو به اف دی ای فرستاده شده بود به عنوان بسته تاییدی دارو را گرفتند. اینها پس تمام آزمایشاتی که روی این دارو ها انجام شده نیست چرا که٬ ما هرگز نخواهیم دونست که آیا همه آنها را خواهیم داشت٬ اینها آزمایشاتی هستند که انجام شدهاند تا بتونن مجوز توزیع دارو بگیرند. سپس اونها رفتند و بررسی کردند تا ببینند که شاید آزمایشات در مجلات دارای سیستم بررسی چاپ شده است. این چیزی هست که پیدا کردند. این یک نتیجه تقریبا ۵۰-۵۰ بوده. در واقعیت نصف آزمایشات مثبت و نصف دیگه اونها منفی بودند. اما وقتی که اونها رفتند و به این آزمایشات در مجلههای معتبر نگاه کردند٬ تصویری که به دست آوردند کاملا متفاوت بود. فقط ۳ تا از آزمایشات منفی چاپ شده بود٬ در حالی که همه غیر از یکی از نتایج مثبت چاپ شده بود. حالا اگه من اینو عقب و جلو کنم بین این دو٬ می بینید که چه تفاوت فاحشی هستش بین واقعیت و آن چیزی که پزشکان٬ بیماران٬ دانشگاهیان و کارمندان بخش خدمات درمانی از مجلات معتبر می تونند ببینند. ما گمراه شده بودیم٬ و این یک مشکل ساختاری در هسته پزشکی هستش.
In fact, there have been so many studies conducted on publication bias now, over a hundred, that they've been collected in a systematic review, published in 2010, that took every single study on publication bias that they could find. Publication bias affects every field of medicine. About half of all trials, on average, go missing in action, and we know that positive findings are around twice as likely to be published as negative findings.
در حقیقت میزان بسیار زیادی تحقیق در مورد تعصب انتشاراتی انجام شده. بیش از ۱۰۰تا از اونها به صورت منسجم در سال ۲۰۱۰ منتشر شد٬ که هر موردی از تعصب انتشاراتی که پیدا کردند رو شامل شد. تعصب انتشاراتی تمام زمینههای پزشکی رو تحت تاثیر قرار داده. تقریبا نیمی از آزمایشات به طور میانگین٬ دادههاشون گم میشه٬ ٬ و ما میدونیم نتایج مثبت٬ دو برابر نتایج منفی شانس چاپ شدن دارند.
This is a cancer at the core of evidence-based medicine. If I flipped a coin 100 times but then withheld the results from you from half of those tosses, I could make it look as if I had a coin that always came up heads. But that wouldn't mean that I had a two-headed coin. That would mean that I was a chancer and you were an idiot for letting me get away with it. (Laughter) But this is exactly what we blindly tolerate in the whole of evidence-based medicine. And to me, this is research misconduct. If I conducted one study and I withheld half of the data points from that one study, you would rightly accuse me, essentially, of research fraud. And yet, for some reason, if somebody conducts 10 studies but only publishes the five that give the result that they want, we don't consider that to be research misconduct. And when that responsibility is diffused between a whole network of researchers, academics, industry sponsors, journal editors, for some reason we find it more acceptable, but the effect on patients is damning.
این سرطانی هست در مرکز پزشکی تجربی. اگر من سکهای رو ۱۰۰ بار بندازم ولی نصف نتیجههای اون رو از شما مخفی کنم می تونم جوری صحنهسازی کنم انگار سکه من همیشه شیر میاد. ولی به این معنی نیست که سکه من دو روی شیر داشته٬ به این معنی هستش که من یک شیادم و شما احمقی هستین که میذارین من سرتون کلاه بذارم.(صدای خنده) اما این دقیقا چیزی هست که ما کورکورانه اجازه می دیم در قلب پزشکی تجربی بیفته. و از نظر من٬ این اشتباه انجام دادن تحقیق هستش. اگر من یک تحقیق انجام بدم و نیمی از نتایجم رو پیش خودم نگه دارم٬ شما به درستی منو متهم میکنید ٬به درستی که٬ کلاهبرداری علمی کردهام. اما ٬به هر دلیلی٬ اگر کسی ده تحقیق رو انجام بده ولی فقط نتایج ۵ تایی که دوست داره رو چاپ کنه٬ ما توجه نمیکنیم که اون تحقیق اشتباه بوده و وقتی اون مسئولیت پخش میشه بین یک شبکهای از محققین٬دانشگاهیان٬ اسپانسرهای صنعتی و سردبیران مجلات٬ما به طور کلی راحتتر قانع میشویم٬ اما تاثیر روی بیماران انکار نشدنی هستش.
And this is happening right now, today. This is a drug called Tamiflu. Tamiflu is a drug which governments around the world have spent billions and billions of dollars on stockpiling, and we've stockpiled Tamiflu in panic, in the belief that it will reduce the rate of complications of influenza. Complications is a medical euphemism for pneumonia and death. (Laughter) Now when the Cochrane systematic reviewers were trying to collect together all of the data from all of the trials that had ever been conducted on whether Tamiflu actually did this or not, they found that several of those trials were unpublished. The results were unavailable to them. And when they started obtaining the writeups of those trials through various different means, through Freedom of Information Act requests, through harassing various different organizations, what they found was inconsistent. And when they tried to get a hold of the clinical study reports, the 10,000-page long documents that have the best possible rendition of the information, they were told they weren't allowed to have them. And if you want to read the full correspondence and the excuses and the explanations given by the drug company, you can see that written up in this week's edition of PLOS Medicine.
این در حال اتفاق افتادن هستش. همین الان٬ امروز. این دارویی هستش به نام «تمیفلوTamiflu». «تمیفلو» دارویی هست که دولتها در سراسر دنیا میلیاردها میلیارد دلار صرف خریداری و انبارش کردهاند٬ و ما از روی ترس اون رو انبار میکنیم٬ به امید این که این دارو باعث کاهش «پیچیدگیهای» آنفولانزا میشه. «پیچیدگی» شکل شیک شده ذاتالریه و مرگ هستش. (خنده حضار) و حالا وقتی محققان تحقیقات ساختاری «کوچران» تلاش کردند که تمام دادهها از تمام تحقیقات که تا به حال انجام شده تا نشون بده که آیا واقعا «تمیفلو» تاثیرگذار هست یا نه آنها فهمیدند چندین تا از اون تحقیقات چاپ نشدهاند. نتایج در دسترسشون نبود. و وقتی اونها شروع کردند به دست آوردن نتایج اون تحقیقات رو از طریق روشهای مختلف٬ درخواست به دلیل آزادی اطلاعات٬ یا اذیت کردن چندین موسسه٬ چیزی که پیدا کردند متناقض بود و وقتی که سعی کردند گزارشات مربوط به آزمایشات که یه گزارش دههزار صفحهای هستش رو بگیرند که بهترین اطلاعات رو در خودش داره٬ به آنها گفته شد که آنها اجازه ندارند آنها را داشته باشند. و اگر می خواین که صورت کامل مکاتبات و بهانهها و توضیحات شرکتهای دارویی را بخوانید٬ می توانید آن را مکتوب در شماره این هفته «پلاس مدیسن» پیدا کنید.
And the most staggering thing of all of this, to me, is that not only is this a problem, not only do we recognize that this is a problem, but we've had to suffer fake fixes. We've had people pretend that this is a problem that's been fixed. First of all, we had trials registers, and everybody said, oh, it's okay. We'll get everyone to register their trials, they'll post the protocol, they'll say what they're going to do before they do it, and then afterwards we'll be able to check and see if all the trials which have been conducted and completed have been published. But people didn't bother to use those registers. And so then the International Committee of Medical Journal Editors came along, and they said, oh, well, we will hold the line. We won't publish any journals, we won't publish any trials, unless they've been registered before they began. But they didn't hold the line. In 2008, a study was conducted which showed that half of all of trials published by journals edited by members of the ICMJE weren't properly registered, and a quarter of them weren't registered at all. And then finally, the FDA Amendment Act was passed a couple of years ago saying that everybody who conducts a trial must post the results of that trial within one year. And in the BMJ, in the first edition of January, 2012, you can see a study which looks to see if people kept to that ruling, and it turns out that only one in five have done so.
و اون چیزی که بیشتر از همه هی تکرار میشه٬برای من٬ این هستش که نه تنها این یک مشکل هستش٬نه تنها ما می دونیم که این یک مشکل هستش٬ ما حتی باید از «راه حلهای الکی» بکشیم. ما آدمهایی داریم که جوری رفتار میکنند که انگار این مشکل حل شده است. اول از همه٬ ما تمام آزمایشات رو ثبت کردیم٬ وهمه میگفتند٬ آها٬ این خوبه.ما از همه میخوایم که آزمایشاتشون رو قبل از انجام ثبت کتتد٬ روششون رو خواهند گفت٬ و خواهند گفت چه میخوان بکنند قبل از این که انجام بدهند٬ در پایانش ما می تونیم بررسی کنیم که آیا همه آزمایشهای انجام شده چاپ شده است یا نه. اما مردم به خودشون زحمت ندادن که ثبت کنند آزمایشاتشون رو. بعد از اون کمیته جهانی سردبیران مجلات بهداشت وارد کار شد٬ و اونها گفتند٬ آها٬ باشه٬ این کار با ما. ما هیچ ژورنالی و هیچ آزمایشی را چاپ نمیکنیم٬ مگر این که اونها قبل از شروع ثبت شده باشند. اما اونها مبارزهای نکردند. در سال ۲۰۰۸ تحقیقی چاپ شده که نشون می داد نصف تمام مقالههای چاپ شده که توسط اعضای کمیته بررسی شده بودهاند به صورت درست حسابی ثبت نشده بودند و یکچهارم آنها اصلا ثبت نشده بودند. و در پایان اصلاحیه اف دی ای که چند سال پیس تصویب شده میگه هر کس که هر آزمایشی انجام می ده میبایست نتایج آزمایش رو تا یک سال بعد از آزمایش چاپ کنه. و در «بی ام جی» ٬در شماره یک ماه ژانویه سال ۲۰۱۲ میتونید تحقیقی رو ببینید که مردم آیا این قانون رو رعایت کردند٬ و معلوم شد به ازای هر پنج نفر ٬ تنها یک نفر رعایت کرده.
This is a disaster. We cannot know the true effects of the medicines that we prescribe if we do not have access to all of the information.
این یک افتضاح هستش. ما نمی تونیم تاثیر دارویی که تجویز میکنیم رو بدونیم اگر که به تمام اطلاعات دسترسی نداشته باشیم.
And this is not a difficult problem to fix. We need to force people to publish all trials conducted in humans, including the older trials, because the FDA Amendment Act only asks that you publish the trials conducted after 2008, and I don't know what world it is in which we're only practicing medicine on the basis of trials that completed in the past two years. We need to publish all trials in humans, including the older trials, for all drugs in current use, and you need to tell everyone you know that this is a problem and that it has not been fixed. Thank you very much. (Applause) (Applause)
این یک مشکل لاینحل نیست. ما باید مردم رو مجبور کنیم که همه آزمایشاتی که روی انسانها انجم میدن رو چاپ کنند٬ این شامل آزمایشات قدیمی هم میشه چرا که اصلاحیه اف دی ای تنها درخواستچاپ مقاله کرده از سال ۲۰۰۸ به بعد٬ و من نمیدونم چه دنیایی خواهد بود اگر ما دارویی که تجویز کنیم فقط بر اساس تحقیقاتی که در دوسال گذشته انجام شده باشه. ما باید نتایج تمام أزمایشاتی که روی انسانها شده رو چاپ کنیم٬ و این شامل آزمایشات قدیمیتر هم میشه٬برای تمام داروهایی که الان در حال استفاده هستند٬ و لازمه که شما به هر کس که میشناسید بگید: که مشکل این هست و این مشکل حل نشده است. بسیار ممنونم. (تشویق) (تشویق)