Hi. Dieser Kerl hier glaubt, er kann euch die Zukunft vorhersagen. Sein Name ist Nostradamus, auch wenn ihn die Sun hier eher ein bisschen wie Sean Connery aussehen lässt.
Hi. So, this chap here, he thinks he can tell you the future. His name is Nostradamus, although here the Sun have made him look a little bit like Sean Connery. (Laughter)
Und wie die meisten von euch glaube ich nicht so wirklich, dass Menschen in die Zukunft sehen können. Ich glaube nicht an die sogenannte Präkognition. Immer wieder hört man, dass jemand etwas vorhersagen konnte, was dann tatsächlich passierte. Das war dann wahrscheinlich bloß Zufall. Aber wir hören nur von solchen Zufällen und Glückstreffern. Wir hören nichts von all den Fällen, in denen Leute etwas Falsches behauptet haben. Das erwarten wir bei solchen albernen Geschichten über Zukunftsvorhersagen, aber das Problem ist, dass wir genau das gleiche Problem in der Wissenschaft und der Medizin haben, und dort kostet es Leben.
And like most of you, I suspect, I don't really believe that people can see into the future. I don't believe in precognition, and every now and then, you hear that somebody has been able to predict something that happened in the future, and that's probably because it was a fluke, and we only hear about the flukes and about the freaks. We don't hear about all the times that people got stuff wrong. Now we expect that to happen with silly stories about precognition, but the problem is, we have exactly the same problem in academia and in medicine, and in this environment, it costs lives.
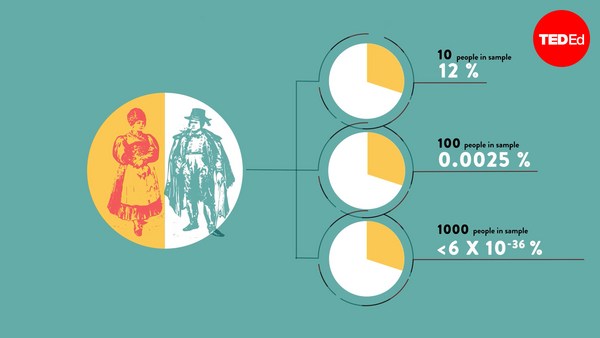
Erstens, noch zum Thema Hellsehen: Erst letztes Jahr hat tatsächlich ein Forscher namens Daryl Bem eine Studie durchgeführt und fand darin Hinweise auf hellseherische Fähigkeiten bei Studenten. Das wurde in einer wissenschaftlichen Fachzeitschrift veröffentlicht. Und die meisten Leser sagten nur: "Okay, gut und schön, aber ich denke, das ist bloß Zufall, weil ich weiß, dass eine Studie, in der keine Beweise für hellseherische Fähigkeiten unter Studenten gefunden wurden, wahrscheinlich nicht in einer Fachzeitschrift veröffentlicht werden würde. Und wir wissen tatsächlich, dass das stimmt, denn eine ganze Reihe von Forschern versuchte, die Ergebnisse dieser Hellseher-Studie zu wiederholen, und als sie das bei genau derselben Zeitschrift einreichten, sagten die: "Nein, wir sind nicht an Wiederholungsstudien interessiert. Wir wollen Ihre negativen Daten nicht." Das ist also schon ein Beweis dafür, wie wir in der akademischen Literatur ein schiefes Bild all der tatsächlich durchgeführten wissenschaftlichen Studien sehen.
So firstly, thinking just about precognition, as it turns out, just last year a researcher called Daryl Bem conducted a piece of research where he found evidence of precognitive powers in undergraduate students, and this was published in a peer-reviewed academic journal and most of the people who read this just said, "Okay, well, fair enough, but I think that's a fluke, that's a freak, because I know that if I did a study where I found no evidence that undergraduate students had precognitive powers, it probably wouldn't get published in a journal. And in fact, we know that that's true, because several different groups of research scientists tried to replicate the findings of this precognition study, and when they submitted it to the exact same journal, the journal said, "No, we're not interested in publishing replication. We're not interested in your negative data." So this is already evidence of how, in the academic literature, we will see a biased sample of the true picture of all of the scientific studies that have been conducted.
Aber das passiert nicht nur im trockenen Forschungsfeld der Psychologie. Das passiert zum Beispiel auch in der Krebsforschung. Im März 2012, vor erst einem Monat, berichteten einige Forscher in der Fachzeitschrift Nature, wie sie versucht hatten, 53 verschiedene grundlegende Studien zu wiederholen, die mögliche Behandlungsziele bei Krebs untersuchten. Von diesen 53 Studien konnten sie nur sechs erfolgreich wiederholen. 47 von diesen 53 ließen sich nicht mit denselben Ergebnissen wiederholen. Und sie sagen in ihrem Fazit, das sei auch sehr wahrscheinlich, weil außergewöhnliche Ergebnisse eben veröffentlicht werden. Menschen führen sehr viele verschiedene Studien durch und die, bei denen etwas herauskommt, veröffentlichen sie, und die, bei denen nichts herauskommt, veröffentlichen sie nicht. Ihre erste Empfehlung, wie man dieses Problem lösen könnte – und es ist ein Problem, weil es uns in die Sackgasse führt – ihre erste Empfehlung, dieses Problem zu lösen, ist, die Veröffentlichung negativer Forschungsergebnisse zu vereinfachen und die Anreize zu ändern, um Wissenschaftler dazu zu ermutigen, der Öffentlichkeit mehr negative Ergebnisse zu zeigen.
But it doesn't just happen in the dry academic field of psychology. It also happens in, for example, cancer research. So in March, 2012, just one month ago, some researchers reported in the journal Nature how they had tried to replicate 53 different basic science studies looking at potential treatment targets in cancer, and out of those 53 studies, they were only able to successfully replicate six. Forty-seven out of those 53 were unreplicable. And they say in their discussion that this is very likely because freaks get published. People will do lots and lots and lots of different studies, and the occasions when it works they will publish, and the ones where it doesn't work they won't. And their first recommendation of how to fix this problem, because it is a problem, because it sends us all down blind alleys, their first recommendation of how to fix this problem is to make it easier to publish negative results in science, and to change the incentives so that scientists are encouraged to post more of their negative results in public.
Aber das passiert nicht nur in der staubtrockenen Welt der vorklinischen Grundlagenkrebsforschung. Das passiert auch in der realen tatsächlichen klinischen Forschung. Im Jahr 1980 führten ein paar Forscher eine Studie zu einem Medikament namens Lorcainid durch. Das war ein Medikament gegen Herzrhythmusstörungen, ein Medikament, das anormale Herzrhythmen verhindert. Die Idee war, dass Menschen nach einem Herzinfarkt recht wahrscheinlich anormale Herzrhythmen haben. Wenn wir ihnen also ein Medikament geben, das anormale Rhyhmen verhindert, dann erhöht das ihre Überlebenschancen. Ganz früh in dieser Entwicklung machten sie einen sehr kleinen Versuch mit weniger als hundert Patienten. 50 Patienten bekamen Lorcainid und von denen starben zehn. 50 andere bekamen einen Placebo, ein Bonbon ohne Inhaltsstoff, und von denen starb nur einer. Also betrachteten sie aus guten Gründen dieses Medikament als gescheitert und die Entwicklung für den Markt wurde gestoppt. Da die Entwicklung für den Markt gestoppt wurde, wurde dieser Versuch nie veröffentlicht.
But it doesn't just happen in the very dry world of preclinical basic science cancer research. It also happens in the very real, flesh and blood of academic medicine. So in 1980, some researchers did a study on a drug called lorcainide, and this was an anti-arrhythmic drug, a drug that suppresses abnormal heart rhythms, and the idea was, after people have had a heart attack, they're quite likely to have abnormal heart rhythms, so if we give them a drug that suppresses abnormal heart rhythms, this will increase the chances of them surviving. Early on its development, they did a very small trial, just under a hundred patients. Fifty patients got lorcainide, and of those patients, 10 died. Another 50 patients got a dummy placebo sugar pill with no active ingredient, and only one of them died. So they rightly regarded this drug as a failure, and its commercial development was stopped, and because its commercial development was stopped, this trial was never published.
Leider hatten im Laufe der nächsten fünf bis zehn Jahre andere Firmen dieselbe Idee für ein Medikament, das Herzrhythmusstörungen bei Herzinfarktpatienten verhindern soll. Diese Medikamente wurden auf den Markt gebracht. Sie wurden sehr häufig verschrieben, weil Herzinfarkte sehr oft vorkommen. Es dauerte lange, bis wir herausfanden, dass diese Medikamente auch zu mehr Sterbefällen führten. Und dass bevor wir dieses Warnsignal hörten, mehr als 100.000 Menschen in Amerika unnötig durch die Verschreibung von Medikamenten gegen Herzrhythmusstörungen starben.
Unfortunately, over the course of the next five, 10 years, other companies had the same idea about drugs that would prevent arrhythmias in people who have had heart attacks. These drugs were brought to market. They were prescribed very widely because heart attacks are a very common thing, and it took so long for us to find out that these drugs also caused an increased rate of death that before we detected that safety signal, over 100,000 people died unnecessarily in America from the prescription of anti-arrhythmic drugs.
Im Jahr 1993 veröffentlichten die Forscher, die diese erste Studie von 1980 durchgeführt hatten, ein Mea Culpa, ein Schuldgeständnis an die wissenschaftliche Gemeinschaft, und sagten: "Als wir 1980 unsere Studie durchführten, dachten wir, dass die erhöhte Sterberate in der Lorcainid-Gruppe ein Zufallseffekt war." Die Entwicklung von Lorcainid wurde aus wirtschaftlichen Gründen aufgegeben und diese Studie wurde nie veröffentlicht; nun ist sie ein gutes Beispiel für "Publikationsbias" Das ist der Fachbegriff für das Phänomen, dass unliebsame Daten verloren gehen, nicht veröffentlicht werden, verschollen bleiben. Und sie sagen, dass die Ergebnisse, die eben beschrieben waren, "vielleicht ein erstes Warnsignal für künftige Probleme gewesen wären".
Now actually, in 1993, the researchers who did that 1980 study, that early study, published a mea culpa, an apology to the scientific community, in which they said, "When we carried out our study in 1980, we thought that the increased death rate that occurred in the lorcainide group was an effect of chance." The development of lorcainide was abandoned for commercial reasons, and this study was never published; it's now a good example of publication bias. That's the technical term for the phenomenon where unflattering data gets lost, gets unpublished, is left missing in action, and they say the results described here "might have provided an early warning of trouble ahead."
Dies sind nun Geschichten aus der Grundlagenforschung. Sie liegen 20, 30 Jahre zurück. Die Welt der wissenschaftlichen Publikationen sieht heute ganz anders aus. Es gibt wissenschaftliche Fachzeitschriften wie die Open-Access-Zeitschrift "Trials", die jeden Versuch an Menschen veröffentlicht, egal ob das Ergebnis positiv oder negativ ist. Aber das Problem, dass negative Ergebnisse verloren gehen, besteht immer noch. Es ist sogar so verbreitet, dass es auch die Grundlagen der evidenzbasierten Medizin betrifft. Es gibt ein Medikament names Reboxetin, ein Medikament, das ich selbst schon verschrieben habe, ein Antidepressivum. Ich bin ein sehr streberhafter Doktor, also las ich alle Studien, die ich zu diesem Medikament finden konnte. Ich habe eine veröffentlichte Studie gelesen, die zeigte, dass Reboxetin besser als Placebos wirkte, und ich las die drei anderen veröffentlichten Studien, die zeigten, dass Reboxetin genauso gut wie jedes andere Antodepressivum war. Weil einer meiner Patienten nicht gut auf die anderen Antidepressiva ansprach, dachte ich, okay, Reboxetin ist genauso gut. Versuchen wir's. Aber es stellte sich heraus, dass ich falsch lag. Tatsächlich wurden sieben Versuche durchgeführt, in denen Reboxetin mit einem Placebo verglichen wurde. Eine dieser Studien war positiv und wurde veröffentlicht, aber die sechs anderen waren negativ und blieben unveröffentlicht. Drei Versuche wurden veröffentlicht, in denen Reboxetin mit anderen Antidepressiva verglichen wurde, und in denen es genauso gut wirkte wie die anderen. Die wurden auch veröffentlicht. Aber dreimal mehr Patientendaten wurden erhoben, die zeigten, dass Reboxtin schlechter wirkte als diese anderen Medikamente, und diese Versuche wurden nicht veröffentlicht. Ich fühlte mich getäuscht.
Now these are stories from basic science. These are stories from 20, 30 years ago. The academic publishing environment is very different now. There are academic journals like "Trials," the open access journal, which will publish any trial conducted in humans regardless of whether it has a positive or a negative result. But this problem of negative results that go missing in action is still very prevalent. In fact it's so prevalent that it cuts to the core of evidence-based medicine. So this is a drug called reboxetine, and this is a drug that I myself have prescribed. It's an antidepressant. And I'm a very nerdy doctor, so I read all of the studies that I could on this drug. I read the one study that was published that showed that reboxetine was better than placebo, and I read the other three studies that were published that showed that reboxetine was just as good as any other antidepressant, and because this patient hadn't done well on those other antidepressants, I thought, well, reboxetine is just as good. It's one to try. But it turned out that I was misled. In fact, seven trials were conducted comparing reboxetine against a dummy placebo sugar pill. One of them was positive and that was published, but six of them were negative and they were left unpublished. Three trials were published comparing reboxetine against other antidepressants in which reboxetine was just as good, and they were published, but three times as many patients' worth of data was collected which showed that reboxetine was worse than those other treatments, and those trials were not published. I felt misled.
Nun sagen Sie vielleicht: "Naja, das ist ein extrem ungewöhnliches Beispiel", und ich will mich nicht derselben Erbsenzählerei schuldig machen, die ich an anderen kritisiere. Aber es stellt sich heraus, dass dieses Phänomen der Publikationsbias tatsächlich sehr sehr gründlich erforscht ist. Hier ist ein Beispiel, wie man das macht. Das klassische Fall ist dieser: Man nimmt sich einen Haufen Studien, von denen man weiß, dass sie vollständig durchgeführt wurden. Dann schaut man, ob sie noch woanders in der wissenschaftlichen Literatur veröffentlicht wurden. Eine dieser Untersuchungen betrachtete alle Versuche, die jemals zu Antidepressiva durchgeführt wurden und die über einen Zeitraum von 15 Jahren von der FDA, der US-Arzneimittelbehörde, zugelassen wurden. Sie nahmen sich alle Versuche vor, die im Zuge ihrer Zulassung bei der FDA eingereicht wurden. Das sind nicht alle Versuche, die jemals zu diesen Medikamenten durchgeführt wurden, weil wir nie wissen können, ob die vorliegen, aber wir haben die, die durchgeführt wurden, um die Zulassung für den Markt zu bekommen. Und dann schauten sie, ob diese Versuche alle in der etablierten geprüften wissenschaftlichen Literatur veröffentlicht wurden. Und dabei fanden sie Folgendes heraus: Es war ungefähr 50-50. In Wahrheit war die Hälfte dieser Versuche positiv, die Hälfte negativ. Aber als sie diese Versuche in den großen Veröffentlichungen suchten, fanden Sie ein ganz anderes Bild vor. Nur drei der negativen Versuche waren veröffentlicht worden, aber bis auf einen alle positiven Versuche. Wenn wir jetzt zwischen diesen beiden Darstellungen hin und her springen, sehen Sie den riesigen Unterschied zwischen der Realität und dem was Ärzte, Patienten, Verantwortliche im Gesundheitswesen und Akademiker in der Fachliteratur sehen konnten. Wir wurden getäuscht und dies ist ein systematischer Fehler mitten im Herzen der Medizin.
Now you might say, well, that's an extremely unusual example, and I wouldn't want to be guilty of the same kind of cherry-picking and selective referencing that I'm accusing other people of. But it turns out that this phenomenon of publication bias has actually been very, very well studied. So here is one example of how you approach it. The classic model is, you get a bunch of studies where you know that they've been conducted and completed, and then you go and see if they've been published anywhere in the academic literature. So this took all of the trials that had ever been conducted on antidepressants that were approved over a 15-year period by the FDA. They took all of the trials which were submitted to the FDA as part of the approval package. So that's not all of the trials that were ever conducted on these drugs, because we can never know if we have those, but it is the ones that were conducted in order to get the marketing authorization. And then they went to see if these trials had been published in the peer-reviewed academic literature. And this is what they found. It was pretty much a 50-50 split. Half of these trials were positive, half of them were negative, in reality. But when they went to look for these trials in the peer-reviewed academic literature, what they found was a very different picture. Only three of the negative trials were published, but all but one of the positive trials were published. Now if we just flick back and forth between those two, you can see what a staggering difference there was between reality and what doctors, patients, commissioners of health services, and academics were able to see in the peer-reviewed academic literature. We were misled, and this is a systematic flaw in the core of medicine.
Tatsächlich wurden mittlerweile so viele Studien zur Publikationsbias gemacht, über 100, dass sie inzwischen in einer systematischen Übersicht gesammelt und im Jahr 2010 veröffentlicht wurden. Hier ist jede einzelne Studie über Publikationsbias erfasst, die sie finden konnten. Publikationsbias betrifft jeden Bereich der Medizin. Durchschnittlich etwa die Hälfte aller Studien geht unter und wir wissen, dass positive Ergebnisse etwa zweimal so oft veröffentlicht werden wie negative.
In fact, there have been so many studies conducted on publication bias now, over a hundred, that they've been collected in a systematic review, published in 2010, that took every single study on publication bias that they could find. Publication bias affects every field of medicine. About half of all trials, on average, go missing in action, and we know that positive findings are around twice as likely to be published as negative findings.
Das ist ein Geschwür inmitten der evidenzbasierten Medizin. Wenn ich hundertmal eine Münze werfe, aber dann jedes zweite Ergebnis für mich behalte, dann kann ich so tun, als lande meine Münze immer mit dem Kopf nach oben. Aber das hieße nicht, dass ich eine Münze mit Kopf auf beiden Seiten habe. Sondern das hieße, dass ich ein Hallodri bin, und dass ihr Idioten seid, weil ihr es mir durchgehen lasst. Aber genau das lassen wir blind durchgehen, in der gesamten evidenzbasierten Medizin. Und für mich ist das wissenschaftliches Fehlverhalten. Wenn ich eine Studie durchführe und die Hälfte der Datenpunkte aus dieser einen Studie vorenthalten würde, dann würdet ihr mich zu Recht des wissenschaftlichen Betrugs beschuldigen. Aber wenn aus irgendeinem Grund jemand zehn Studien durchführt, aber nur die fünf davon veröffentlicht, die die gewünschten Ergebnisse hervorbringen, dann betrachten wir das nicht als wissenschaftliches Fehlverhalten. Und wenn diese Verantwortung dann auch noch unter einem ganzen Netzwerk von Forschern, Akademikern, Industriesponsoren, Herausgebern verteilt ist, dann finden wir es irgendwie eher vertretbar. Aber die Auswirkungen für die Patienten sind vernichtend.
This is a cancer at the core of evidence-based medicine. If I flipped a coin 100 times but then withheld the results from you from half of those tosses, I could make it look as if I had a coin that always came up heads. But that wouldn't mean that I had a two-headed coin. That would mean that I was a chancer and you were an idiot for letting me get away with it. (Laughter) But this is exactly what we blindly tolerate in the whole of evidence-based medicine. And to me, this is research misconduct. If I conducted one study and I withheld half of the data points from that one study, you would rightly accuse me, essentially, of research fraud. And yet, for some reason, if somebody conducts 10 studies but only publishes the five that give the result that they want, we don't consider that to be research misconduct. And when that responsibility is diffused between a whole network of researchers, academics, industry sponsors, journal editors, for some reason we find it more acceptable, but the effect on patients is damning.
Und das passiert jetzt gerade, heute. Das ist ein Medikament namens Tamiflu. Tamiflu ist ein Medikament, für das Regierungen auf der ganzen Welt viele Milliarden auf Vorrat ausgegeben haben. Wir haben Tamiflu in Panik gehortet, im Glauben, dass es die Häufigkeit von Komplikationen bei Grippeerkrankungen reduziert. Komplikationen ist der medizinische Euphemismus für Lungenentzündung und Tod. (Lachen) Als nun die Cochrane-Gutachter für ihre systematische Übersicht versuchten, alle Daten aus allen Versuchen zusammen zu bekommen, die jemals zur Wirkung von Tamiflu durchgeführt worden waren, fanden sie heraus, dass einige dieser Versuche nie veröffentlicht wurden. Die Ergebnisse waren ihnen nicht zugänglich. Und als sie anfingen, die Berichte zu diesen Versuchen über viele verschiedene Wege zu bekommen, durch das Gesetz über die Auskunftspflicht öffentlicher Einrichtungen, durch Bedrängen diverser Organisationen, waren ihre Erkenntnisse widersprüchlich. Und als sie versuchten, an die klinischen Versuchsberichte zu kommen, diese 10.000-Seiten langen Dokumente, die die bestmögliche Darstellung der Informationen liefern, sagte man ihnen, dass sie sie nicht einsehen dürften. Wenn Sie den kompletten Austausch und die Entschuldigungen und Erklärungen der Pharmafirmen lesen wollen, können Sie das in der dieswöchigen Ausgabe von PLOS Medicine lesen.
And this is happening right now, today. This is a drug called Tamiflu. Tamiflu is a drug which governments around the world have spent billions and billions of dollars on stockpiling, and we've stockpiled Tamiflu in panic, in the belief that it will reduce the rate of complications of influenza. Complications is a medical euphemism for pneumonia and death. (Laughter) Now when the Cochrane systematic reviewers were trying to collect together all of the data from all of the trials that had ever been conducted on whether Tamiflu actually did this or not, they found that several of those trials were unpublished. The results were unavailable to them. And when they started obtaining the writeups of those trials through various different means, through Freedom of Information Act requests, through harassing various different organizations, what they found was inconsistent. And when they tried to get a hold of the clinical study reports, the 10,000-page long documents that have the best possible rendition of the information, they were told they weren't allowed to have them. And if you want to read the full correspondence and the excuses and the explanations given by the drug company, you can see that written up in this week's edition of PLOS Medicine.
Das Erstaunlichste an all dem ist für mich Folgendes: Dies ist nicht nur ein erkennbares und erkanntes Problem, sondern wir mussten bisher mit wirkungslosen Lösungen dafür leben. Wir ließen die Menschen so tun, als sei das ein gelöstes Problem. Erst hatten wir Versuchsregister und jeder sagte: "Oh, Problem gelöst. Wir lassen alle ihre Versuche registrieren, sie veröffentlichen den Bericht, sie sagen, was sie vorhaben, bevor sie damit anfangen, und nachher können wir prüfen, ob alle Versuche, die komplett durchgeführt wurden, auch veröffentlicht wurden. Aber niemand hatte Lust auf diese Register. Also kam das Internationale Komitee der Herausgeber medizinischer Fachzeitschriften daher und sagte: "Naja, wir bleiben da weiter dran. Wir veröffentlichen in unseren Zeitschriften keine Versuche, die nicht vorher registriert wurden." Aber sie blieben nicht dran. 2008 wurde eine Studie durchgeführt, die zeigte, dass die Hälfte aller Versuche, die in Zeitschriften veröffentlicht wurden, die von Mitgliedern dieses Komitees, des ICMJE, herausgegen werden, nicht ordentlich registriert worden waren. Und dass ein Viertel davon überhaupt nicht registriert war. Und dann schließlich wurde die FDA-Gesetzesnovellierung verabschiedet – vor ein paar Jahren – die besagte, dass jeder, der einen Versuch durchführt, die Ergebnisse innerhalb eines Jahres veröffentlichen muss. Im British Medical Journal, in der ersten Ausgabe vom Januar 2012, können Sie eine Studie darüber lesen, ob sich jemand an diese Regel gehalten hat, und es stellt sich heraus, dass nur jeder fünfte das getan hat.
And the most staggering thing of all of this, to me, is that not only is this a problem, not only do we recognize that this is a problem, but we've had to suffer fake fixes. We've had people pretend that this is a problem that's been fixed. First of all, we had trials registers, and everybody said, oh, it's okay. We'll get everyone to register their trials, they'll post the protocol, they'll say what they're going to do before they do it, and then afterwards we'll be able to check and see if all the trials which have been conducted and completed have been published. But people didn't bother to use those registers. And so then the International Committee of Medical Journal Editors came along, and they said, oh, well, we will hold the line. We won't publish any journals, we won't publish any trials, unless they've been registered before they began. But they didn't hold the line. In 2008, a study was conducted which showed that half of all of trials published by journals edited by members of the ICMJE weren't properly registered, and a quarter of them weren't registered at all. And then finally, the FDA Amendment Act was passed a couple of years ago saying that everybody who conducts a trial must post the results of that trial within one year. And in the BMJ, in the first edition of January, 2012, you can see a study which looks to see if people kept to that ruling, and it turns out that only one in five have done so.
Das ist ein Desaster. Wir können die wahren Auswirkungen der Medikamente, die wir verschreiben nicht kennen, wenn wir keinen Zugang zu all diesen Informationen haben.
This is a disaster. We cannot know the true effects of the medicines that we prescribe if we do not have access to all of the information.
Es ist nicht schwer, dieses Problem zu lösen. Wir müssen die Leute dazu zwingen, alle Versuche an Menschen zu veröffentlichen, einschließlich der älteren Versuche, weil das FDA-Gesetz das nur für die Versuche nach 2008 verlangt. Ich weiß nicht, in was für einer Welt wir leben, in der wir nur Medizin auf der Basis von Versuchen der letzten zwei Jahre praktizieren. Wir müssen alle Versuche an Menschen veröffentlichen, einschließlich der älteren Versuche, für alle Medikamente, die zur Zeit in Gebrauch sind. Sie sollten jedem, den Sie kennen, sagen, dass wir hier ein Problem haben, das noch nicht gelöst ist. Vielen vielen Dank. (Applaus.) (Applaus.)
And this is not a difficult problem to fix. We need to force people to publish all trials conducted in humans, including the older trials, because the FDA Amendment Act only asks that you publish the trials conducted after 2008, and I don't know what world it is in which we're only practicing medicine on the basis of trials that completed in the past two years. We need to publish all trials in humans, including the older trials, for all drugs in current use, and you need to tell everyone you know that this is a problem and that it has not been fixed. Thank you very much. (Applause) (Applause)