Ahoj. Tenhle chlápek si myslí, že umí předpovídat budoucnost. Jmenuje se Nostradamus, ačkoliv podle „The Sun“ vypadá spíš jako Sean Connery. (Smích)
Hi. So, this chap here, he thinks he can tell you the future. His name is Nostradamus, although here the Sun have made him look a little bit like Sean Connery. (Laughter)
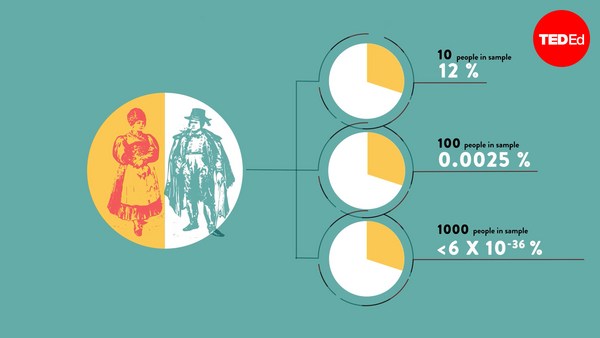
Asi jako většina z vás, ani já nevěřím, že lidé mohou předpovídat budoucnost. Nevěřím na předtuchy, ale čas od času zaslechnete, že někdo někdy předpověděl něco, co se pak v budoucnosti stalo, což byla nejspíš šťastná náhoda a my holt slýcháme pouze o náhodách a o podivnostech. O případech, kdy se lidé spletli, se nedozvídáme. To se dá čekat u hloupých historek o předpovědích, ale problém je, že přesně tomu samému čelíme v akademické obci a v medicíně, v prostředí, kde to stojí životy.
And like most of you, I suspect, I don't really believe that people can see into the future. I don't believe in precognition, and every now and then, you hear that somebody has been able to predict something that happened in the future, and that's probably because it was a fluke, and we only hear about the flukes and about the freaks. We don't hear about all the times that people got stuff wrong. Now we expect that to happen with silly stories about precognition, but the problem is, we have exactly the same problem in academia and in medicine, and in this environment, it costs lives.
Předně, pokud jde čistě o předvídání budoucnosti, zrovna minulý rok vědec Daryl Bem prováděl výzkum, během kterého našel důkazy o schopnostech vysokoškoláků předvídat budoucnost, otiskli mu to v akademickém časopise a většina lidí, kteří to četli, si řekli: „OK, fajn,“ ale myslím, že je to náhoda, abnormalita, protože vím, že kdybych já udělal studii, ve které bych nenašel žádné důkazy o schopnosti studentů věštit, nejspíš by to žádný časopis neotiskl. A my víme, že je to pravda, protože se několik různých vědeckých skupin pokusilo opakovat výsledky této studie o předpovídání budoucna a když je zaslali tomu samému časopisu, dostalo se jim odpovědi: „Nemáme zájem publikovat to samé. Vaše negativní výsledky nás nezajímají.“ Už to je důkazem, že v odborné literatuře najdeme zkreslený vzorek skutečného souhrnu všech vědeckých studií, které kdy byly uskutečněny.
So firstly, thinking just about precognition, as it turns out, just last year a researcher called Daryl Bem conducted a piece of research where he found evidence of precognitive powers in undergraduate students, and this was published in a peer-reviewed academic journal and most of the people who read this just said, "Okay, well, fair enough, but I think that's a fluke, that's a freak, because I know that if I did a study where I found no evidence that undergraduate students had precognitive powers, it probably wouldn't get published in a journal. And in fact, we know that that's true, because several different groups of research scientists tried to replicate the findings of this precognition study, and when they submitted it to the exact same journal, the journal said, "No, we're not interested in publishing replication. We're not interested in your negative data." So this is already evidence of how, in the academic literature, we will see a biased sample of the true picture of all of the scientific studies that have been conducted.
To se ovšem neděje pouze v ryze akademickém oboru psychologie. Například se to také stává při výzkumu rakoviny. V březnu 2012, jen před měsícem, popisovali vědci v časopise Nature, jak se pokoušeli zopakovat 53 studií základního výzkumu zaměřených na potenciální cíle léčby rakoviny a z těchto 53 studií se jim povedlo úspěšně zopakovat 6. 47 z 53 se nedalo zopakovat. A v diskusi uvádějí, že je to velmi pravděpodobně proto, že se do tisku dostávají jen nevysvětlitelné náhody. Dělá se velké množství nejrůznějších studií, z nichž se publikují ty případy, které vyjdou, a ty, které se nezdaří, se nepublikují. Jejich první doporučení, jak tenhle problém napravit, a je to problém, protože nás zavádí do slepých uliček, tedy jejich první doporučení k nápravě je usnadnit lidem publikování negativních výsledků ve vědě, změnit pobídky a povzbudit vědce, aby zveřejňovali více negativních výsledků.
But it doesn't just happen in the dry academic field of psychology. It also happens in, for example, cancer research. So in March, 2012, just one month ago, some researchers reported in the journal Nature how they had tried to replicate 53 different basic science studies looking at potential treatment targets in cancer, and out of those 53 studies, they were only able to successfully replicate six. Forty-seven out of those 53 were unreplicable. And they say in their discussion that this is very likely because freaks get published. People will do lots and lots and lots of different studies, and the occasions when it works they will publish, and the ones where it doesn't work they won't. And their first recommendation of how to fix this problem, because it is a problem, because it sends us all down blind alleys, their first recommendation of how to fix this problem is to make it easier to publish negative results in science, and to change the incentives so that scientists are encouraged to post more of their negative results in public.
Ale nestává se to jen v suchopárném světě základního, předklinického výzkumu rakoviny. Běžně se to děje i v samém srdci akademické medicíny. V roce 1980 vědci vypracovali studii o léku lorcainide, což je antiarytmikum, léčivo potlačující srdeční arytmie. Myšlenka spočívala v tom, že lidé po infarktu mají často větší tendence k arytmiím, takže když jim podáte lék proti arytmii, zvýší se jejich šance na přežití. Na začátku vývoje provedli velmi malou studii na zhruba 100 pacientech. 50 dostalo lorcainide a 10 z nich zemřelo. Dalších 50 dostalo placebo pilulku bez účinné látky a zemřel pouze 1. Po právu považovali tento lék za neúspěšný, jeho komerční vývoj byl zastaven, a protože byl zastaven, jejich studie nebyla nikdy publikována.
But it doesn't just happen in the very dry world of preclinical basic science cancer research. It also happens in the very real, flesh and blood of academic medicine. So in 1980, some researchers did a study on a drug called lorcainide, and this was an anti-arrhythmic drug, a drug that suppresses abnormal heart rhythms, and the idea was, after people have had a heart attack, they're quite likely to have abnormal heart rhythms, so if we give them a drug that suppresses abnormal heart rhythms, this will increase the chances of them surviving. Early on its development, they did a very small trial, just under a hundred patients. Fifty patients got lorcainide, and of those patients, 10 died. Another 50 patients got a dummy placebo sugar pill with no active ingredient, and only one of them died. So they rightly regarded this drug as a failure, and its commercial development was stopped, and because its commercial development was stopped, this trial was never published.
Bohužel, během dalších 5 až 10 let měli ostatní výrobci stejný nápad vyrábět antiarytmika pro pacienty po infarktu. Tyto léky se dostaly na trh a byly hromadně předepisovány, protože infarkt myokardu je velmi častá věc. A dlouho nám pak trvalo, než jsme zjistili, že i ony zvyšují míru úmrtnosti, a než jsme si všimli varovného signálu, zemřelo v Americe zbytečně přes 100 000 lidí kvůli užívání antiarytmik.
Unfortunately, over the course of the next five, 10 years, other companies had the same idea about drugs that would prevent arrhythmias in people who have had heart attacks. These drugs were brought to market. They were prescribed very widely because heart attacks are a very common thing, and it took so long for us to find out that these drugs also caused an increased rate of death that before we detected that safety signal, over 100,000 people died unnecessarily in America from the prescription of anti-arrhythmic drugs.
V roce 1993 uveřejnili autoři té původní studie z roku 1980 „mea culpa“, omluvu vědecké komunitě, ve které stálo: „Když jsme prováděli naši studii v roce 1980, mysleli jsme si, že zvýšená úmrtnost, která se objevila u skupiny užívající lorcainide, je vliv náhody.“ Vývoj lorcainidu byl opuštěn z komerčních důvodů a tato studie nebyla nikdy publikována. Teď slouží jako výborný příklad publikačního bias (zkreslení výsledků). Jde o terminus technicus pro fenomén, kdy se nelichotivá data ztrácejí, nepublikují se, jsou ponechána svému osudu, ačkoli výsledky zmíněné studie „mohly poskytnout včasné varování před nadcházejícími problémy.“
Now actually, in 1993, the researchers who did that 1980 study, that early study, published a mea culpa, an apology to the scientific community, in which they said, "When we carried out our study in 1980, we thought that the increased death rate that occurred in the lorcainide group was an effect of chance." The development of lorcainide was abandoned for commercial reasons, and this study was never published; it's now a good example of publication bias. That's the technical term for the phenomenon where unflattering data gets lost, gets unpublished, is left missing in action, and they say the results described here "might have provided an early warning of trouble ahead."
Tyhle historky souvisejí se základním výzkumem. Jsou 20, 30 let staré. Dnes jsou podmínky publikování v akademické obci úplně jiné. Existují volně přístupné časopisy jako jsou „Trials“ (Studie), které publikují jakékoli studie na lidech bez ohledu na to, jestli přinesly pozitivní nebo negativní výsledky. Problém s negativními výsledky, o které jsme přišli, je stále velmi rozšířený. Je tak rozšířený, že proniká do jádra medicíny založené na důkazech. Tohle je lék reboxetine, který jsem sám předepisoval. Jde o antidepresivum. Jsem velmi důkladný doktor, takže jsem si přečetl veškeré studie, které o tomto přípravku vyšly. Jedna z nich prokazovala, že reboxetine je lepší než placebo a v dalších 3 publikovaných studiích, které jsem četl, vyšel reboxetine srovnatelně se všemi ostatními antidepresivy. Mému pacientovi nedělala ostatní antidepresiva dobře, tak jsem si řekl, proč nezkusit reboxetine, když je stejně účinný. Ale ukázalo se, že mě uvedli v omyl. Ve skutečnosti bylo provedeno 7 studií srovnávajících reboxetine s placebem. Jediný pozitivní byl publikován, ale 6 z nich vyšlo negativně a publikovány nebyly. Byly publikovány 3 studie srovnávající reboxetine s ostatními antidepresivy, ve kterých byl stejně dobrý, a ty byly otištěny, ale data od trojnásobného počtu pacientů naznačovala, že reboxetine je horší než ostatní léky, a tyto studie uveřejněny nebyly. Cítil jsem se oklamán.
Now these are stories from basic science. These are stories from 20, 30 years ago. The academic publishing environment is very different now. There are academic journals like "Trials," the open access journal, which will publish any trial conducted in humans regardless of whether it has a positive or a negative result. But this problem of negative results that go missing in action is still very prevalent. In fact it's so prevalent that it cuts to the core of evidence-based medicine. So this is a drug called reboxetine, and this is a drug that I myself have prescribed. It's an antidepressant. And I'm a very nerdy doctor, so I read all of the studies that I could on this drug. I read the one study that was published that showed that reboxetine was better than placebo, and I read the other three studies that were published that showed that reboxetine was just as good as any other antidepressant, and because this patient hadn't done well on those other antidepressants, I thought, well, reboxetine is just as good. It's one to try. But it turned out that I was misled. In fact, seven trials were conducted comparing reboxetine against a dummy placebo sugar pill. One of them was positive and that was published, but six of them were negative and they were left unpublished. Three trials were published comparing reboxetine against other antidepressants in which reboxetine was just as good, and they were published, but three times as many patients' worth of data was collected which showed that reboxetine was worse than those other treatments, and those trials were not published. I felt misled.
Teď byste asi mohli říct, že jde o extrémně neobvyklý případ a já bych se nechtěl dopustit toho stejného výběrového odkazování jen na to, co se mi hodí, ze kterého obviňuji ostatní. Faktem ale je, že fenomén publikačního bias byl opravdu velmi dobře prostudován. Tady je jeden příklad možného přístupu. Klasický model je, že máte hromadu studií, o kterých víte, že se uskutečnily a byly dokončeny a pak hledáte, zda byly publikovány kdekoli v odborné literatuře. Zde se zabývali všemi studiemi, které byly o antidepresivech provedeny a schváleny FDA v období 15 let. Jde o studie předložené FDA jako součást žádostí o schválení. Takže to nejsou všechny studie, které kdy byly s těmi léky prováděny, protože skutečný počet nezjistíme, ale byly to ty, které byly prováděny za účelem povolení prodeje. Pak se zjišťovalo, jestli byly všechny tyto studie uveřejněny v peer-review odborné literatuře. A zjistilo se následující. Skóre bylo přibližně 50 na 50. Polovina studií byla ve skutečnosti pozitivní a polovina negativní. Když po nich ale pátrali v odborném tisku, obraz byl velmi rozdílný. Z negativních studií byly uveřejněny pouze tři, z pozitivních všechny, kromě jediné. Když se nad těmi čísly zamyslíme, uvidíme ten zarážející rozdíl mezi realitou a tím, co mohli doktoři, pacienti, poskytovatelé zdravotní péče a akademici vidět na stránkách peer-review odborné literatury. Byli jsme klamáni, jedná se o systematickou chybu v samém srdci medicíny.
Now you might say, well, that's an extremely unusual example, and I wouldn't want to be guilty of the same kind of cherry-picking and selective referencing that I'm accusing other people of. But it turns out that this phenomenon of publication bias has actually been very, very well studied. So here is one example of how you approach it. The classic model is, you get a bunch of studies where you know that they've been conducted and completed, and then you go and see if they've been published anywhere in the academic literature. So this took all of the trials that had ever been conducted on antidepressants that were approved over a 15-year period by the FDA. They took all of the trials which were submitted to the FDA as part of the approval package. So that's not all of the trials that were ever conducted on these drugs, because we can never know if we have those, but it is the ones that were conducted in order to get the marketing authorization. And then they went to see if these trials had been published in the peer-reviewed academic literature. And this is what they found. It was pretty much a 50-50 split. Half of these trials were positive, half of them were negative, in reality. But when they went to look for these trials in the peer-reviewed academic literature, what they found was a very different picture. Only three of the negative trials were published, but all but one of the positive trials were published. Now if we just flick back and forth between those two, you can see what a staggering difference there was between reality and what doctors, patients, commissioners of health services, and academics were able to see in the peer-reviewed academic literature. We were misled, and this is a systematic flaw in the core of medicine.
Už bylo provedeno mnoho studií o publikačním bias, více než 100, jejich systematický přehled byl zveřejněn v roce 2010, zahrnoval každičkou studii o publikačním bias, kterou se podařilo nalézt. Publikační bias ovlivňuje všechny obory medicíny. Průměrně polovina studií je pro praxi ztracena, a víme, že pozitivní výsledky mají dvojnásobnou pravděpodobnost publikování než výsledky negativní.
In fact, there have been so many studies conducted on publication bias now, over a hundred, that they've been collected in a systematic review, published in 2010, that took every single study on publication bias that they could find. Publication bias affects every field of medicine. About half of all trials, on average, go missing in action, and we know that positive findings are around twice as likely to be published as negative findings.
Jedná se o rakovinu v samotném srdci medicíny založené na důkazech. Pokud bych si 100krát hodil mincí, ale zamlčel vám výsledky poloviny hodů, mohlo by to vypadat, že mince vždy dopadne pannou nahoru. Ale neznamenalo by to, že panna je na obou stranách mince. Znamenalo by to, že jsem podvodník a vy idioti, u kterých mi to hladce prošlo. (Smích) Ale přesně to slepě tolerujeme v celé vědecky založené medicíně. Podle mě je to vědecký podvod. Pokud bych provedl jednu studii a z té studie zamlčel polovinu dat, oprávněně byste mě nařkli z vědeckého podvodu. A přesto, z nějakého důvodu, pokud někdo provede 10 studií, ale publikuje pouze těch 5, které ukazují požadované výsledky, nepovažujeme to za vědecký podvod. A když je zodpovědnost rozptýlena v celé síti vědců, akademiků, sponzorských firem, redaktorů v časopisech, zdá se nám to z nějakého důvodu přijatelné, ale důsledky pro pacienty jsou zničující.
This is a cancer at the core of evidence-based medicine. If I flipped a coin 100 times but then withheld the results from you from half of those tosses, I could make it look as if I had a coin that always came up heads. But that wouldn't mean that I had a two-headed coin. That would mean that I was a chancer and you were an idiot for letting me get away with it. (Laughter) But this is exactly what we blindly tolerate in the whole of evidence-based medicine. And to me, this is research misconduct. If I conducted one study and I withheld half of the data points from that one study, you would rightly accuse me, essentially, of research fraud. And yet, for some reason, if somebody conducts 10 studies but only publishes the five that give the result that they want, we don't consider that to be research misconduct. And when that responsibility is diffused between a whole network of researchers, academics, industry sponsors, journal editors, for some reason we find it more acceptable, but the effect on patients is damning.
A děje se to stále, i dnes. Tento lék se jmenuje Tamiflu. Vlády celého světa utratily za předzásobení se Tamiflu miliardy a miliardy dolarů, v panice jsme hromadili zásoby Tamiflu a věřili jsme, že sníží míru komplikací při chřipce. Komplikace je lékařským eufemismem pro zápal plic a smrt. (Smích) Systematičtí revizoři z Cochrane se snažili shromáždit veškerá data ze všech studií, které byly provedeny bez ohledu na to, zda to Tamiflu dokáže nebo ne, a zjistili, že několik studií publikováno nebylo. Výsledky nebyly volně dostupné. Když začali různými prostředky získávat přístup k těmto studiím, žádostmi podle Zákona o svobodném přístupu k informacím a dotíráním na různé další organizace, došli k nesourodým zjištěním. Když se pokusili sehnat zprávy o průběhu klinických studií, dokumenty o desetitisících stranách, poskytující nejlepší možný souhrn informací, bylo jim řečeno, že je nelze vydat. Pokud chcete číst celou korespondenci, výmluvy a vysvětlování farmaceutické firmy, můžete si to přečíst tento týden v „PLOS Medicine“.
And this is happening right now, today. This is a drug called Tamiflu. Tamiflu is a drug which governments around the world have spent billions and billions of dollars on stockpiling, and we've stockpiled Tamiflu in panic, in the belief that it will reduce the rate of complications of influenza. Complications is a medical euphemism for pneumonia and death. (Laughter) Now when the Cochrane systematic reviewers were trying to collect together all of the data from all of the trials that had ever been conducted on whether Tamiflu actually did this or not, they found that several of those trials were unpublished. The results were unavailable to them. And when they started obtaining the writeups of those trials through various different means, through Freedom of Information Act requests, through harassing various different organizations, what they found was inconsistent. And when they tried to get a hold of the clinical study reports, the 10,000-page long documents that have the best possible rendition of the information, they were told they weren't allowed to have them. And if you want to read the full correspondence and the excuses and the explanations given by the drug company, you can see that written up in this week's edition of PLOS Medicine.
Podle mě je nejvíce šokující nejen to, že je to problém a my ho dokážeme rozpoznat, ale že musíme snášet pokusy o jeho falešnou nápravu. Našli se tací, kteří předstírali, že tento problém již byl odstraněn. Nejprve se zavedly registry studií a všichni říkali: „Ano, to je OK. Všichni zaregistrují své studie, zašlou protokol, uvedou, co budou dělat předtím, než to udělají, a pak bude možné zkontrolovat, zda byly publikovány všechny studie, které byly provedeny a dokončeny.“ Ale nikdo se neobtěžoval tyto registry používat. Proto nastoupil ICMJE, Mezinárodní výbor editorů lékařských časopisů, a uvedl: „My to ohlídáme. Nezveřejníme žádné studie, které nebudou předem zaregistrovány.“ Ale nic neohlídali. Studie z roku 2008 ukázala, že polovina studií zveřejněných v časopisech redigovaných členy ICMJE, nebyla řádně registrována, a čtvrtina nebyla registrována vůbec. A tak byl nakonec před pár lety schválen dodatek k zákonu o FDA, který stanovil, že kdokoli, kdo provádí studii, musí její výsledky zveřejnit do jednoho roku. V prvním lednovém čísle časopisu BMJ v roce 2012 je studie, která sleduje, zda bylo toto pravidlo dodrženo, a ukazuje se, že se tak stalo pouze v jednom z pěti případů.
And the most staggering thing of all of this, to me, is that not only is this a problem, not only do we recognize that this is a problem, but we've had to suffer fake fixes. We've had people pretend that this is a problem that's been fixed. First of all, we had trials registers, and everybody said, oh, it's okay. We'll get everyone to register their trials, they'll post the protocol, they'll say what they're going to do before they do it, and then afterwards we'll be able to check and see if all the trials which have been conducted and completed have been published. But people didn't bother to use those registers. And so then the International Committee of Medical Journal Editors came along, and they said, oh, well, we will hold the line. We won't publish any journals, we won't publish any trials, unless they've been registered before they began. But they didn't hold the line. In 2008, a study was conducted which showed that half of all of trials published by journals edited by members of the ICMJE weren't properly registered, and a quarter of them weren't registered at all. And then finally, the FDA Amendment Act was passed a couple of years ago saying that everybody who conducts a trial must post the results of that trial within one year. And in the BMJ, in the first edition of January, 2012, you can see a study which looks to see if people kept to that ruling, and it turns out that only one in five have done so.
To je katastrofa. Nemůžeme znát skutečné účinky léků, které předepisujeme, pokud nemáme přístup k veškerým informacím.
This is a disaster. We cannot know the true effects of the medicines that we prescribe if we do not have access to all of the information.
Tento problém není těžké napravit. Je třeba vynutit zveřejnění všech studií prováděných na lidech, včetně starších studií, protože Dodatek k zákonu o FDA požaduje zveřejnění jen studií provedených po roce 2008, a já nechápu, proč bychom měli praktikovat medicínu pouze na základě studií dokončených v posledních 2 letech. Musíme zveřejnit veškeré studie na lidech, včetně starších studií, týkajících se aktuálně používaných léků, a je třeba, aby všichni věděli, že zde máme problém a že nebyl vyřešen. Děkuji vám. (Potlesk) (Potlesk)
And this is not a difficult problem to fix. We need to force people to publish all trials conducted in humans, including the older trials, because the FDA Amendment Act only asks that you publish the trials conducted after 2008, and I don't know what world it is in which we're only practicing medicine on the basis of trials that completed in the past two years. We need to publish all trials in humans, including the older trials, for all drugs in current use, and you need to tell everyone you know that this is a problem and that it has not been fixed. Thank you very much. (Applause) (Applause)