I'm going to talk to you today about hopefully converting fear into hope. When we go to the physician today -- when we go to the doctor's office and we walk in, there are words that we just don't want to hear. There are words that we're truly afraid of. Diabetes, cancer, Parkinson's, Alzheimer's, heart failure, lung failure -- things that we know are debilitating diseases, for which there's relatively little that can be done.
Я расскажу вам сегодня, о превращении страха в надежду. Когда сегодня мы идем к врачу, когда мы идем к кабинету и входим, есть слова, которые мы просто не хотим слышать. Есть слова, которых мы искренне боимся. Диабет, рак, болезнь Паркинсона, болезнь Альцгеймера, сердечная недостаточность, лёгочная недостаточность. Болезни, известные как истощающие заболевания. С которыми почти ничего нельзя сделать.
And what I want to lay out for you today is a different way of thinking about how to treat debilitating disease, why it's important, why without it perhaps our health care system will melt down if you think it already hasn't, and where we are clinically today, and where we might go tomorrow, and what some of the hurdles are. And we're going to do all of that in 18 minutes, I promise.
И то, чем я хочу сегодня поделиться - это другой взгляд на то как лечить истощающие болезни, почему это важно. Почему без этого возможно, наша система здравоохранения растает, если вы считаете, что этого ещё не произошло. Что уже сделано на сегодня с клинической точки зрения, что может быть сделано завтра, и что нам мешает двигаться дальше. И всё это мы сделаем за 18 минут, я обещаю.
I want to start with this slide, because this slide sort of tells the story the way Science Magazine thinks of it. This was an issue from 2002 that they published with a lot of different articles on the bionic human. It was basically a regenerative medicine issue. Regenerative medicine is an extraordinarily simple concept that everybody can understand. It's simply accelerating the pace at which the body heals itself to a clinically relevant timescale. So we know how to do this in many of the ways that are up there. We know that if we have a damaged hip, you can put an artificial hip in. And this is the idea that Science Magazine used on their front cover.
Я хочу начать с этого слайда, потому, что этот слайд, как бы, рассказывает историю так, как это представляет Science Magazine. Это было в издании 2002 года, которое они опубликовали с большим количеством статей об искусственном человеке. В основном, это было издание о регенеративной медицине. Регенеративная медицина - это чрезвычайно простая идея, которое каждый может понять. Это просто увеличение темпа, с которым тело лечит себя в клинически значимом масштабе времени. Итак, мы знаем как это сделать разными существующими способами. Мы знаем, что если у нас поврежден тазобедренный сустав, можно вставить искусственный. И эту идею Science Magazine использовали для обложки.
This is the complete antithesis of regenerative medicine. This is not regenerative medicine. Regenerative medicine is what Business Week put up when they did a story about regenerative medicine not too long ago. The idea is that instead of figuring out how to ameliorate symptoms with devices and drugs and the like -- and I'll come back to that theme a few times -- instead of doing that, we will regenerate lost function of the body by regenerating the function of organs and damaged tissue. So that at the end of the treatment, you are the same as you were at the beginning of the treatment.
Это полная противоположность регенеративной медицины. Это не регенеративная медицина. Регенеративная медицина - это то, что напечатали в Business Week когда они подготовили статью о регенеративной медицине не так давно. Идея заключается в том, чтобы вместо того, чтобы выяснять как бороться с симптомами с помощью устройств и лекарств и тому подобного - и я ещё вернусь к этой теме несколько раз - вместо этого, мы будем регенеровать утраченные функции тела, регенерируя функции органов и поврежденных тканей. Таким образом, что к окончанию лечения, вы будете таким же каким и были в начале лечения.
Very few good ideas -- if you agree that this is a good idea -- very few good ideas are truly novel. And this is just the same. If you look back in history, Charles Lindbergh, who was better known for flying airplanes, was actually one of the first people along with Alexis Carrel, one of the Nobel Laureates from Rockefeller, to begin to think about, could you culture organs? And they published this book in 1937, where they actually began to think about, what could you do in bio-reactors to grow whole organs? We've come a long way since then. I'm going to share with you some of the exciting work that's going on.
Мало хороших идей - если вы согласны, что это хорошая идея - очень мало действительно новых идей. И эта точно такая же. Если мы заглянем в историю, Чарльз Линдберг - кто был более известен как летчик - был фактически одним из первых людей, вместе с Алексисом Каррелом, один из нобелевских лауреатов от Рокафеллера, кто начал думать о том, можно ли выращивать органы? И они опубликовали книгу в 1937, где они фактически начали думать о том, что можно сделать в био-реакторе, чтобы вырастить органы? С тех пор прошло много времени. Я поделюсь с вами частью захватывающей работы, которая сейчас ведется.
But before doing that, what I'd like to do is share my depression about the health care system and the need for this with you. Many of the talks yesterday talked about improving the quality of life, and reducing poverty, and essentially increasing life expectancy all around the globe. One of the challenges is that the richer we are, the longer we live. And the longer we live, the more expensive it is to take care of our diseases as we get older.
Но перед этим, я бы хотел поделиться с вами унынием по поводу системы здравоохранения и потребности в ней. На вчерашних выступлениях говорили об улучшении качества жизни и уменьшении бедности. И по существу - увеличение продолжительности жизни по всей планете. Одна из проблем - чем мы богаче, тем дольше мы живем. И чем дольше мы живем, тем дороже становится лечение наших болезней пока мы стареем.
This is simply the wealth of a country versus the percent of population over the age of 65. And you can basically see that the richer a country is, the older the people are within it. Why is this important? And why is this a particularly dramatic challenge right now? If the average age of your population is 30, then the average kind of disease that you have to treat is maybe a broken ankle every now and again, maybe a little bit of asthma. If the average age in your country is 45 to 55, now the average person is looking at diabetes, early-onset diabetes, heart failure, coronary artery disease -- things that are inherently more difficult to treat, and much more expensive to treat.
Это простое соотношение богатства страны и процента населения старше 65 лет. В основном можно увидеть, что чем богаче страна, тем старее люди в ней. Почему это важно? И почему это особенно волнующая проблема именно сейчас? Если средний возраст вашего населения - 30, тогда средний вид болезни который вам приходится лечить - может быть сломанная лодыжка время от времени, может быть немного астмы. Если средний возраст в стране от 45 до 55, тогда у среднего человека диабет, ранний диабет, сердечная недостаточность, ишемическая болезнь сердца. Болезни, которые по определению тяжелее лечить, и гораздо дороже лечить.
Just have a look at the demographics in the U.S. here. This is from "The Untied States of America." In 1930, there were 41 workers per retiree. 41 people who were basically outside of being really sick, paying for the one retiree who was experiencing debilitating disease. In 2010, two workers per retiree in the U.S. And this is matched in every industrialized, wealthy country in the world. How can you actually afford to treat patients when the reality of getting old looks like this?
Просто взгляните сюда на демографию в США. Это из книги "Разъединенные Штаты Америки". В 1930-м году, на 1 пенсионера приходился 41 рабочий. 41 человек, которые не были очень сильно больны, платили за одного пенсионера, который болел истощающим заболеванием. В 2010, 2 рабочих на одного пенсионера в США. И тоже самое в каждой развитой, богатой стране в мире. Как фактически можно позволить лечить пациентов, когда реальность старения выглядит так?
This is age versus cost of health care. And you can see that right around age 45, 40 to 45, there's a sudden spike in the cost of health care. It's actually quite interesting. If you do the right studies, you can look at how much you as an individual spend on your own health care, plotted over your lifetime. And about seven years before you're about to die, there's a spike. And you can actually -- (Laughter) -- we won't get into that. (Laughter)
Это соотношение возраста к затратам на лечение. И можно увидеть, что около 45, от 40 до 45 лет, резкий рост в стоимости лечения. Это на самом деле очень интересно - если хорошо разобраться, можно посмотреть на график ваших тратит на медицинское обслуживание, в течении жизни. Примерно за семь лет до смерти будет резкий скачок. И фактически можно - (Смех) - не будем в это углубляться. (Смех)
There are very few things, very few things that you can really do that will change the way that you can treat these kinds of diseases and experience what I would call healthy aging. I'd suggest there are four things, and none of these things include an insurance system or a legal system. All those things do is change who pays. They don't actually change what the actual cost of the treatment is.
Очень мало, очень мало что можно сделать чтобы изменить способ лечения таких болезней и испытывать то, что я бы назвал здоровое старение. Я бы предположил, что есть 4 способа. И один из них не включает систему страхования или правовую систему. Они всего-лишь определяют, кто платит. Они на самом деле не меняют фактическую стоимость лечения.
One thing you can do is not treat. You can ration health care. We won't talk about that anymore. It's too depressing. You can prevent. Obviously a lot of monies should be put into prevention.
Ещё можно не лечить. Можно нормировать лечение. Но мы об этом больше не будем говорить. Это слишком грустно. Можно предотвращать. Очевидно, что много денег должно тратиться на профилактику.
But perhaps most interesting, to me anyway, and most important, is the idea of diagnosing a disease much earlier on in the progression, and then treating the disease to cure the disease instead of treating a symptom. Think of it in terms of diabetes, for instance. Today, with diabetes, what do we do? We diagnose the disease eventually, once it becomes symptomatic, and then we treat the symptom for 10, 20, 30, 40 years. And we do OK. Insulin's a pretty good therapy. But eventually it stops working, and diabetes leads to a predictable onset of debilitating disease.
Но возможно самой интересной и самой важной, по крайне мере для меня, является идея диагностирования болезни на ранних стадиях развития, и затем лечение болезни чтобы вылечить болезнь, а не лечение симптомов. Подумайте об этом в применении к диабету, например. Что мы сегодня делаем с диабетом? Мы диагностируем болезнь со временем, как только она становится симптоматической, и затем мы лечим симптомы 10, 20, 30, 40 лет. И мы в порядке. Инсулин - вполне нормальное лекарство. Но внезапно он перестает работать. и диабет ведет к предсказуемому возникновению истощающей болезни.
Why couldn't we just inject the pancreas with something to regenerate the pancreas early on in the disease, perhaps even before it was symptomatic? And it might be a little bit expensive at the time that we did it, but if it worked, we would truly be able to do something different.
Почему бы нам не вводить в поджелудочную железу вещество для регенерации поджелудочной железы на ранних стадиях болезни, возможно даже до того, как она стало симптоматической? И это могло бы быть чуть дороже, когда мы бы это делали, но если бы это сработало, это было бы безусловно большим достижением.
This video, I think, gets across the concept that I'm talking about quite dramatically. This is a newt re-growing its limb. If a newt can do this kind of thing, why can't we? I'll actually show you some more important features about limb regeneration in a moment. But what we're talking about in regenerative medicine is doing this in every organ system of the body, for tissues and for organs themselves. So today's reality is that if we get sick, the message is we will treat your symptoms, and you need to adjust to a new way of life.
На мой взгляд, это видео дает очень эффектное представление о том, о чем я говорю. Это тритон, заново отращивает свою конечность. Если это может тритон, почему не можем мы? Я на самом деле покажу вам более важные моменты о регенерации конечности через секунду. Но то, о чем мы сейчас говорим в регенеративной медицине - делать тоже самое в каждом системе органов тела, с тканями и самими органами. Итак, настоящая реальность - если мы заболели, идея в том, что мы лечим симптомы, и вам нужно привыкнуть к новым условиям жизни.
I would pose to you that tomorrow -- and when tomorrow is we could debate, but it's within the foreseeable future -- we will talk about regenerative rehabilitation. There's a limb prosthetic up here, similar actually one on the soldier that's come back from Iraq. There are 370 soldiers that have come back from Iraq that have lost limbs. Imagine if instead of facing that, they could actually face the regeneration of that limb. It's a wild concept. I'll show you where we are at the moment in working towards that concept.
Я бы предположил, что завтра - а когда будет завтра можно поспорить, но это уже в обозримом будущем - мы будем говорить о регенеративном восстановлении. Это протез конечности, так наверху. практически такой же как у солдата, который вернулся с Ирака ... 370 солдат, которые вернулись из Ирака потеряли конечности. Представьте, что если бы вместо того, чтобы столкнуться с этим они бы могли столкнуться с регенерацией этой конечности. Это сумасшедшая идея. Я покажу вам, где мы сейчас находимся в работе над этой идеей.
But it's applicable, again, to every organ system. How can we do that? The way to do that is to develop a conversation with the body. We need to learn to speak the body's language. And to switch on processes that we knew how to do when we were a fetus. A mammalian fetus, if it loses a limb during the first trimester of pregnancy, will re-grow that limb. So our DNA has the capacity to do these kinds of wound-healing mechanisms. It's a natural process, but it is lost as we age. In a child, before the age of about six months, if they lose their fingertip in an accident, they'll re-grow their fingertip. By the time they're five, they won't be able to do that anymore.
Но она применима, опять же, к каждой системе органов. Как мы это можем сделать? Это можно сделать наладив общение с телом. Нам предстоит научиться говорить на языке тела. И включить процессы, которые мы умели включать когда были зародышем. Зародыш млекопитающего, потеряв конечность в первом триместре беременности, отрастит конечность вновь. Таким образом, наша ДНК обладает способностью к таким рано-исцеляющим механизмам. Это естественный процесс, но он исчезает когда мы взрослеем. У ребенка, примерно до 6 месяцев, если он случайно лишится кончика пальца, ребенок отрастит заново кончик пальца. К пяти годам, ребенок уже так не сможет.
So to engage in that conversation with the body, we need to speak the body's language. And there are certain tools in our toolbox that allow us to do this today. I'm going to give you an example of three of these tools through which to converse with the body.
Так чтобы начать этот диалог с телом, нам нужно говорить на языке тела. И у нас в запасе есть инструменты которые позволяют нам делать это сегодня. Я приведу примеры трех таких инструментов с помощью которых можно говорить с телом.
The first is cellular therapies. Clearly, we heal ourselves in a natural process, using cells to do most of the work. Therefore, if we can find the right cells and implant them in the body, they may do the healing. Secondly, we can use materials. We heard yesterday about the importance of new materials. If we can invent materials, design materials, or extract materials from a natural environment, then we might be able to have those materials induce the body to heal itself. And finally, we may be able to use smart devices that will offload the work of the body and allow it to heal.
Первая - клеточная терапия. Очевидно, мы лечимся в естественных условиях, используя клетки, чтобы сделать большую часть работы. Таким образом, если мы найдем правильные клетки и вживим их в тело, они могут исцелить. Во-вторых, мы можем использовать материалы. Вчера мы слышали о важности новых материалов. Если бы мы могли изобрести материалы, разработать материалы, или извлечь материалы из естественной среды, тогда мы бы смогли заставить эти материалы убедить тело исцелить себя. И наконец, мы смогли бы использовать умные устройства которые разгрузят работу тела и позволят ему исцелять.
I'm going to show you an example of each of these, and I'm going to start with materials. Steve Badylak -- who's at the University of Pittsburgh -- about a decade ago had a remarkable idea. And that idea was that the small intestine of a pig, if you threw away all the cells, and if you did that in a way that allowed it to remain biologically active, may contain all of the necessary factors and signals that would signal the body to heal itself. And he asked a very important question. He asked the question, if I take that material, which is a natural material that usually induces healing in the small intestine, and I place it somewhere else on a person's body, would it give a tissue-specific response, or would it make small intestine if I tried to make a new ear?
Я покажу вам пример каждого из этих примеров, и я начну с материалов. У Стива Бадыляка - что из Университета Питтсбурга - около декады назад была замечательная идея. И эта идея заключалась в том, что маленький кишечник свиньи, если выкинуть все клетки, и если это сделать так чтобы он остался биологически активным, может содержать все необходимые факторы и сигналы Которые бы просигнализировали телу излечиться. И он задал важный вопрос. Он задал вопрос, если взять такой материал, который является природным материалом, который обычно вызывает заживление в маленьком кишечнике, и поместить его куда-нибудь ещё на тело человека, даст ли это тканеспецифичную реакцию, или получиться маленький желудок когда я пытась сделать новое ухо?
I wouldn't be telling you this story if it weren't compelling. The picture I'm about to show you is a compelling picture. (Laughter) However, for those of you that are even the slightest bit squeamish -- even though you may not like to admit it in front of your friends -- the lights are down. This is a good time to look at your feet, check your Blackberry, do anything other than look at the screen. (Laughter)
Я бы не рассказывал эту историю, если бы она не была убедительной. Картинка которую я собираюсь показать - (Смех) - убедительная картинка. Однако, для тех из вас, кто хоть немножко подвержен тошноте - даже если вы бы не хотели признаваться в этом друзьям - свет выключен. Самое время посмореть на ваши ноги, проверить смартфон, поделать что-нибудь и не смотреть на экран. (Смех)
What I'm about to show you is a diabetic ulcer. And although -- it's good to laugh before we look at this. This is the reality of diabetes. I think a lot of times we hear about diabetics, diabetic ulcers, we just don't connect the ulcer with the eventual treatment, which is amputation, if you can't heal it. So I'm going to put the slide up now. It won't be up for long. This is a diabetic ulcer. It's tragic. The treatment for this is amputation. This is an older lady. She has cancer of the liver as well as diabetes, and has decided to die with what' s left of her body intact.
То что я собираюсь показать - это диабетическая язва. И тем не менее - лучше посмеяться до того как мы посмотрим на это. Это реальность диабета. Я думаю когда мы часто слышим о диабетиках, о диабетических язвах, мы просто не связываем язву с возможным лечением, то есть ампутацией, если нельзя вылечить. Я сейчас покажу слайд. Это не на долго. Это диабетическая язва. Это ужасно. Лечение - ампутация. Это пожилая женщина. У ней рак печении вместе с диабетом, и решила умирать с тем что осталось от её тела нетронутым.
And this lady decided, after a year of attempted treatment of that ulcer, that she would try this new therapy that Steve invented. That's what the wound looked like 11 weeks later. That material contained only natural signals. And that material induced the body to switch back on a healing response that it didn't have before.
И эта женщина решила, после года попыток лечения язвы, что она попробует новое лечение, изобретенное Стивом. Вот как выглядела рана 11 недель спустя. Этот материал содержал только природные сигналы. И этот материал побудил тело включить лечащую реакцию которой не было до этого.
There's going to be a couple more distressing slides for those of you -- I'll let you know when you can look again. This is a horse. The horse is not in pain. If the horse was in pain, I wouldn't show you this slide. The horse just has another nostril that's developed because of a riding accident. Just a few weeks after treatment -- in this case, taking that material, turning it into a gel, and packing that area, and then repeating the treatment a few times -- and the horse heals up. And if you took an ultrasound of that area, it would look great.
Будет ещё пара более печальных слайдов для тех из вас - Я вам скажу когда можно будет смотреть. Это лошадь. Лошади не больно. Если бы лошади было больно, я бы показывал вам этот слайд. У лошади просто развилась ещё одна ноздря из-за происшествия при езде. Буквально несколько недель после лечения - в этом случае, взяли этот материал, превратили в гель, заполнили это место и затем повторяли лечение несколько раз - и лошадь излечивается. И если сделать УЗИ этого места, всё будет в порядке.
Here's a dolphin where the fin's been re-attached. There are now 400,000 patients around the world who have used that material to heal their wounds. Could you regenerate a limb? DARPA just gave Steve 15 million dollars to lead an eight-institution project to begin the process of asking that question.
Здесь дельфин, которому прикрепили плавник. На текущий момент 400 000 пациентов по всему миру использовали этот материал для заживления ран. Можно ли регенерировать конечность? DARPA выдала Стиву 15 миллионов долларов на проведение проекта, чтобы начать процесс поиска ответа на этот вопрос.
And I'll show you the 15 million dollar picture. This is a 78 year-old man who's lost the end of his fingertip. Remember that I mentioned before the children who lose their fingertips. After treatment that's what it looks like. This is happening today. This is clinically relevant today. There are materials that do this. Here are the heart patches.
И я покажу вам картинку на 15 миллионов долларов. Это человек 78 лет, потерявший кончик пальца. Помните, я упоминал ранее детей, потерявших кончики пальцев. И после лечения вот как это выглядит. Это происходит сегодня. Сегодня это клинически доказано. Есть материалы, которые это делают. Есть заплатки для сердца.
But could you go a little further? Could you, say, instead of using material, can I take some cells along with the material, and remove a damaged piece of tissue, put a bio-degradable material on there? You can see here a little bit of heart muscle beating in a dish. This was done by Teruo Okano at Tokyo Women's Hospital. He can actually grow beating tissue in a dish. He chills the dish, it changes its properties and he peels it right out of the dish. It's the coolest stuff.
Но можно ли пойти немножко дальше? Можно ли, скажем, вместо использования материалов взять несколько клеток вместе с материалом, и удалить поврежденные части ткани, а поместить био-разлагаемый материал? Здесь можно увидеть маленький кусочек сердечной мышцы в чаше. Это сделал Теруо Окано в токийской женской больнице. Он фактически может выращивать бьющиеся ткани в чаше. Он охлаждает чашу, она меняет свои свойства, и он отрывает её слоем от чаши. Это обалденно.
Now I'm going to show you cell-based regeneration. And what I'm going to show you here is stem cells being removed from the hip of a patient. Again, if you're squeamish, you don't want to watch. But this one's kind of cool. So this is a bypass operation, just like what Al Gore had, with a difference. In this case, at the end of the bypass operation, you're going to see the stem cells from the patient that were removed at the beginning of the procedure being injected directly into the heart of the patient. And I'm standing up here because at one point I'm going to show you just how early this technology is. Here go the stem cells, right into the beating heart of the patient. And if you look really carefully, it's going to be right around this point you'll actually see a back-flush. You see the cells coming back out. We need all sorts of new technology, new devices, to get the cells to the right place at the right time.
А сейчас я вам покажу регенерацию на основе клеток. И то что я покажу здесь - это стволовые клетки взятые с бедра пациента. Опять же если не можете, не смотрите. Но это клёво. Это операция шунтирования, такую делелали Элу Гору с небольшим отличием. В этом случае, в конце шунтирования, вы увидите стволовые клетки пацинта ,которые были извлечены в начале процедуры, введеные прямо в сердце пациента. И я стою здесь потому, что в один момент я покажу вам насколько ещё молода эта технология. Вот пошли стволовые клетки, прямо в бьющееся сердце пациента. И если внимательно посмотреть, это должно быть где-то в этот момент, фактически можно увидеть противоток. Видно вытекающие стволовые клетки. Нам нужны различные новые технологии, новые устройства, чтобы поместить стволовые клетки в нужное место в нужное время.
Just a little bit of data, a tiny bit of data. This was a randomized trial. At this time this was an N of 20. Now there's an N of about 100. Basically, if you take an extremely sick patient and you give them a bypass, they get a little bit better. If you give them stem cells as well as their bypass, for these particular patients, they became asymptomatic. These are now two years out. The coolest thing would be is if you could diagnose the disease early, and prevent the onset of the disease to a bad state.
Просто немного информации, маленькая порция информации. Это был случайный эксперимент. Тогда это было 1 из 20-ти. Сейчас 1 из примерно 100. В общем, если взять очень больного пациента и сделать ему шунтирование, ему станет немного легче. Если использовать стволовые клетки вместе с шунтированием, этим конкретным пациентам, симптомы больше не проявляются. Это было уже 2 года назад. было бы здорово если можно было диагностировать эти заболевания заранее, и предупреждать развитие болезни с осложнениями.
This is the same procedure, but now done minimally invasively, with only three holes in the body where they're taking the heart and simply injecting stem cells through a laparoscopic procedure. There go the cells. We don't have time to go into all of those details, but basically, that works too. You can take patients who are less sick, and bring them back to an almost asymptomatic state through that kind of therapy.
Это та же процедура, но уже с минимальным хирургическим вмешательством, всего лишь 3 надреза на теле, находим сердце и просто вживляем стволовые клетки с Вот клетки. У нас нет времени погружаться во все эти детали, тем не менее это тоже работотает. Можно взять менее больного пациента и вернуть его почти к бессимптомному состоянию с помощью такого лечения.
Here's another example of stem-cell therapy that isn't quite clinical yet, but I think very soon will be. This is the work of Kacey Marra from Pittsburgh, along with a number of colleagues around the world. They've decided that liposuction fluid, which -- in the United States, we have a lot of liposuction fluid. (Laughter) It's a great source of stem cells. Stem cells are packed in that liposuction fluid. So you could go in, you could get your tummy-tuck. Out comes the liposuction fluid, and in this case, the stem cells are isolated and turned into neurons. All done in the lab. And I think fairly soon, you will see patients being treated with their own fat-derived, or adipose-derived, stem cells.
Вот ещё один пример лечения стволовыми клетками, но ещё пока не до конца отработный, но скоро уже будет. Это работа Кейси Мара из Питсбурга, с группой коллега по всего света. Они решили, что жидкость после липосакции, а у нас в США очень часто делают липосакцию. (Смех) Это хороший источник стволовых клеток. Их полно в этой жидкости. Так что можно прийти, подтянуть животик. Получается жидкость, в этом случае, стволовые клетки изолированы и превращены в нейроны. Всё делается в лаборатории. И, я думаю, очень скоро мы увидим лечение пациентов их же стоволовыми клетками, полученными из их жира или липоцитов.
I talked before about the use of devices to dramatically change the way we treat disease. Here's just one example before I close up. This is equally tragic. We have a very abiding and heartbreaking partnership with our colleagues at the Institute for Surgical Research in the US Army, who have to treat the now 11,000 kids that have come back from Iraq. Many of those patients are very severely burned.
Я уже говорил о том, что использование устройств может существенно изменить то, как мы лечим болезни. Это ещё один пример перед тем, как я закончу. Это столь же трагично. У нас очень прочное и огорчительное сотрудничество с нашими коллегами из института хирургических исследований ВВС США, которым приходится лечить 11 000 ребят вернувшихся из Ирака. Многие из этих пациенотов имею очень сильные ожоги.
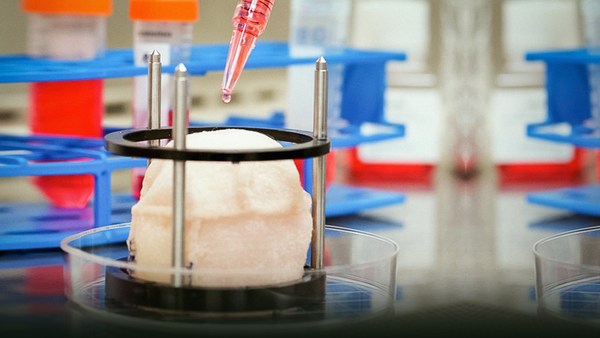
And if there's anything that's been learned about burn, it's that we don't know how to treat it. Everything that is done to treat burn -- basically we do a sodding approach. We make something over here, and then we transplant it onto the site of the wound, and we try and get the two to take. In this case here, a new, wearable bio-reactor has been designed -- it should be tested clinically later this year at ISR -- by Joerg Gerlach in Pittsburgh. And that bio-reactor will lay down in the wound bed. The gun that you see there sprays cells. That's going to spray cells over that area. The reactor will serve to fertilize the environment, deliver other things as well at the same time, and therefore we will seed that lawn, as opposed to try the sodding approach. It's a completely different way of doing it.
И если и есть что-то, что мы узнали об ожогах, так это то, что мы не знаем как их лечить. Всё, что сделано для лечения ожогов - В основном мы используем подход задернения. Мы делаем что-то здесь, затем мы пересаживаем это на поверхность раны, и мы пытаемся, и получается чтобы они срастались. В этом случае, здесь, был придуман новый носимый био-реактор - он позже будет испытываться в этом году в институте хирургических исследований - Йоргом Герлахом из Питсбурга. И этот био-реактор кладется на поверхность раны. Пистолет, который вы там видите, распыляет клетки. Он распыляет клетки по поверхности. Реактор послужит для того, чтобы удобрить среду, и выполняет другие функции в то же время, и таким образом мы засеваем эту лужайку, в противоположность подходу задернения. Это совершенно другой способ.
So my 18 minutes is up. So let me finish up with some good news, and maybe a little bit of bad news. The good news is that this is happening today. It's very powerful work. Clearly the images kind of get that across. It's incredibly difficult because it's highly inter-disciplinary. Almost every field of science engineering and clinical practice is involved in trying to get this to happen.
Итак, мои 18 минут подходят к концу. Позвольте мне закончить с хорошими новостями, и может быть немножко плохих новостей. Хорошая новость - это то, что это происходит сегодня. Это значительная работа. Изображения, вроде бы, дают четкое представление от этом. Это невероятно сложно из-за высокой степени междицсциплинарности. Почти каждая область знаний и клинической практики задействована в попытке это реализовать.
A number of governments, and a number of regions, have recognized that this is a new way to treat disease. The Japanese government were perhaps the first, when they decided to invest first 3 billion, later another 2 billion in this field. It's no coincidence. Japan is the oldest country on earth in terms of its average age. They need this to work or their health system dies. So they're putting a lot of strategic investment focused in this area. The European Union, same thing. China, the same thing. China just launched a national tissue-engineering center. The first year budget was 250 million US dollars.
Некоторые правительства и группа регионов признали, что это новый способ лечения болезней. Японское правительство было пожалуй первым, когад они решили инвестировать 3 миллиарда, позднее ещё 2 миллиарда в эту область. Это не совпадение. Япония - самая старая страна на земле если судить по среднему возрасту. Им это нужно, иначе их система здравоохранения умрет. Поэтому они делают большие капиталовложения в эту область. Европейский союз - тоже самое. Китай - тоже самое. Китай только-что запустил национальный центр по исследованию тканей. Бюджет на первый год составил 250 миллионов долларов.
In the United States we've had a somewhat different approach. (Laughter) Oh, for Al Gore to come and be in the real world as president. We've had a different approach. And the approach has basically been to just sort of fund things as they come along. But there's been no strategic investment to bring all of the necessary things to bear and focus them in a careful way.
В США у нас как-бы другой подход. Мы - (Смех) Чтобы Элу Гору прийти и стать президентом в действительности. У нас другой подход. И подход в основном заключался в виде простой поддержки проектов, по ходу возникновения. Но не было долгосрочных инвестиций чтобы создать всё необходимое и направить в нужное русло.
And I'm going to finish up with a quote, maybe a little cheap shot, at the director of the NIH, who's a very charming man. Myself and Jay Vacanti from Harvard went to visit with him and a number of his directors of his institute just a few months ago, to try and convince him that it was time to take just a little piece of that 27.5 billion dollars that he's going to get next year and focus it, in a strategic way, to make sure we can accelerate the pace at which these things get to patients. And at the end of a very testy meeting, what the NIH director said was, "Your vision is larger than our appetite." I'd like to close by saying that no one's going to change our vision, but together we can change his appetite. Thank you.
Я собираюсь закончить цитатой, которая может ударить по больному месту директора национального института здоровья, очаровательного человека. Я и Джей Ваканти из Гарварда отправились к нему и ещё группе директоров его института с визитом всего несколько месяцев назад, и попытались убедить его в том, что уже самое время взять малую часть от 27.5 миллиардов долларов которые он получит в следующем году и направить их стратегически, чтобы убедиться, что мы можем ускорить процесс, чтобы эта технология быстрее дошла до пациентов. И в конце этой очень раздражительной встречи, Директор института сказал: "Ваше видение больше чем наш аппетит". Я бы хотел завершиться со словами, что никто не изменит наше видение, но вместе мы можем изменить его аппетит. Спасибо.