I'm going to talk to you today about hopefully converting fear into hope. When we go to the physician today -- when we go to the doctor's office and we walk in, there are words that we just don't want to hear. There are words that we're truly afraid of. Diabetes, cancer, Parkinson's, Alzheimer's, heart failure, lung failure -- things that we know are debilitating diseases, for which there's relatively little that can be done.
Ik ga het hopelijk met jullie vandaag hebben over het omzetten van angst naar hoop. Als wij heden ten dage naar een arts gaan naar zijn praktijk en daar naar binnen lopen zijn er woorden die wij echt niet willen horen. Er zijn uitspraken die wij echt niet willen horen. Uitspraken als Diabetes, Parkinson, Alzheimer hartfalen of longziekten. Dit zijn ziekten die je aantasten, ziekten waartegen weinig te doen is.
And what I want to lay out for you today is a different way of thinking about how to treat debilitating disease, why it's important, why without it perhaps our health care system will melt down if you think it already hasn't, and where we are clinically today, and where we might go tomorrow, and what some of the hurdles are. And we're going to do all of that in 18 minutes, I promise.
En wat ik vandaag aan jullie wil duidelijk maken is een andere manier van denken over hoe je deze ziekten kunt behandelen, waarom dit zo belangrijk is. Waarom zonder deze manier van denken onze gezondheidszorg mogelijk onbetaalbaar word,. als dat nu al niet het geval is. Maar ook waar wij in de geneeskunde nu staan en waar wij in de toekomst mogelijk kunnen komen, maar ook welke opstakels er zijn. Dat allemaal gaan wij doen in 18 minuten, dat beloof ik.
I want to start with this slide, because this slide sort of tells the story the way Science Magazine thinks of it. This was an issue from 2002 that they published with a lot of different articles on the bionic human. It was basically a regenerative medicine issue. Regenerative medicine is an extraordinarily simple concept that everybody can understand. It's simply accelerating the pace at which the body heals itself to a clinically relevant timescale. So we know how to do this in many of the ways that are up there. We know that if we have a damaged hip, you can put an artificial hip in. And this is the idea that Science Magazine used on their front cover.
Ik wil met deze sheet beginnen, omdat deze ongeveer het verhaal vertelt hoe Science Magazine hierover denkt. Dit gaat over een thema uit 2002 die zij met een aantal verschillende artikelen over de bionische mens hebben gepubliceerd. In de kern ging het over regeneratieve geneeskunde. Regeneratieve geneeskunde is een buitengewoon eenvoudig concept dat iedereen kan begrijpen. Het is eenvoudigweg het versnellen van het tempo waarin het lichaam zich herstelt tot binnen een klinisch relevante tijdspanne. Wij weten dus hoe wij dit moeten doen in heel veel voorkomende gevallen. Wij weten dat als een heup beschadigd is, je er een kunstmatige heup voor in de plaats kunt zetten. En dat is het idee dat Science Magazine op de omslag van het blad gebruikte.
This is the complete antithesis of regenerative medicine. This is not regenerative medicine. Regenerative medicine is what Business Week put up when they did a story about regenerative medicine not too long ago. The idea is that instead of figuring out how to ameliorate symptoms with devices and drugs and the like -- and I'll come back to that theme a few times -- instead of doing that, we will regenerate lost function of the body by regenerating the function of organs and damaged tissue. So that at the end of the treatment, you are the same as you were at the beginning of the treatment.
Dit is volledig tegengesteld aan regeneratieve geneeskunde. Dit is zeker geen regeneratieve geneeskunde. Regeneratieve geneeskunde is waar Business Week het over had toen zij nog niet zo lang geleden een verhaal hielden over regeneratieve geneeskunde. Het idee is om in plaats van uit te zoeken hoe je symptomen kunt bestrijden met techniek en medicijnen en dergelijke en op dat thema kom ik nog een paar keer terug-- in plaats van die richting in te slaan, gaan wij het functieverlies van het lichaam herstellen door de functies van organen en het beschadigde weefsel te regenereren. Waardoor je aan het einde van de behandeling, hetzelfde bent als voor de start van de symptomen.
Very few good ideas -- if you agree that this is a good idea -- very few good ideas are truly novel. And this is just the same. If you look back in history, Charles Lindbergh, who was better known for flying airplanes, was actually one of the first people along with Alexis Carrel, one of the Nobel Laureates from Rockefeller, to begin to think about, could you culture organs? And they published this book in 1937, where they actually began to think about, what could you do in bio-reactors to grow whole organs? We've come a long way since then. I'm going to share with you some of the exciting work that's going on.
Erg weinig goede ideeën -- als je dit ook een goed idee vindt -- erg weinig goede ideeën zijn echt nieuw. En met dit idee is het niet anders. Als je terugkijkt in de geschiedenis, Charles Lindbergh -- die vooral bekend is door het besturen van vliegtuigen -- was eigenlijk één van de eerste mensen, samen met Alexis Carrel, een van de Nobelprijswinnaars van Rockefeller die begon na te denken over, kun je organen kweken? En zij hebben een boek uitgegeven in 1937, waar zij in feite begonnen na te denken over, wat kun je in bio-reactoren doen om hele organen te laten groeien? Wij hebben sindsdien een hele weg afgelegd. Ik ga met jullie iets van het enerverende werk dat aan de gang is delen.
But before doing that, what I'd like to do is share my depression about the health care system and the need for this with you. Many of the talks yesterday talked about improving the quality of life, and reducing poverty, and essentially increasing life expectancy all around the globe. One of the challenges is that the richer we are, the longer we live. And the longer we live, the more expensive it is to take care of our diseases as we get older.
Maar voor ik dat doe, wil ik graag mijn negatieve gevoel delen over het systeem van de gezondheidszorg en waarom dat voor jullie belangrijk is. Veel van de verhalen van gisteren gaan over het verbeteren van de kwaliteit van het leven en het verminderen van armoede. En eigenlijk over het verbeteren van de levensverwachting overal ter wereld. Een van de uitdagingen is dat hoe rijker wij zijn hoe langer wij leven. Des te langer wij leven des te duurder wordt het om onze ziektes te behandelen, naarmate wij ouder worden.
This is simply the wealth of a country versus the percent of population over the age of 65. And you can basically see that the richer a country is, the older the people are within it. Why is this important? And why is this a particularly dramatic challenge right now? If the average age of your population is 30, then the average kind of disease that you have to treat is maybe a broken ankle every now and again, maybe a little bit of asthma. If the average age in your country is 45 to 55, now the average person is looking at diabetes, early-onset diabetes, heart failure, coronary artery disease -- things that are inherently more difficult to treat, and much more expensive to treat.
Dit is eenvoudig de welvaart van een land in relatie tot het percentage van de bevolking boven de 65 jaar. En je kunt in feite zien dat naarmate een land welvarender is, de gemiddelde leeftijd van de bevolking hoger is. Waarom is dit belangrijk? En waarom is dit juist nu een speciaal dramatisch uitdaging? Als de gemiddelde leeftijd van de bevolking 30 is, dan is het soort gemiddeld te behandelen aandoening misschien af en toe een gebroken enkel, misschien een beetje asthma. Als de gemiddelde leeftijd van de bevolking tussen de 45 en 55 ligt, is er vooral diabetes, vroege diabetes, hartfalen, ziekte van de kransslagader. Dat zijn zaken die als zodanig moeilijker te behandelen zijn, en ook veel duurder.
Just have a look at the demographics in the U.S. here. This is from "The Untied States of America." In 1930, there were 41 workers per retiree. 41 people who were basically outside of being really sick, paying for the one retiree who was experiencing debilitating disease. In 2010, two workers per retiree in the U.S. And this is matched in every industrialized, wealthy country in the world. How can you actually afford to treat patients when the reality of getting old looks like this?
Kijk even naar de demografische gegevens van de VS hier. Deze zijn van de "Verenigde Staten van Amerika". In 1930, met 41 werkenden op 1 gepensioneerde. 41 Mensen die eigenlijk niet ziek zijn betalen voor 1 gepensioneerde die leed aan een chronische ziekte. In 2010 zijn dat twee werkenden per gepensioneerde in de VS. En dat is net zo in elk geïndustrialiseerd, welvarend land in de wereld. Hoe kan het je in werkelijkheid je permitteren patienten te behandelen, wanneer de werkelijkheid van het ouder worden er zo uit ziet?
This is age versus cost of health care. And you can see that right around age 45, 40 to 45, there's a sudden spike in the cost of health care. It's actually quite interesting. If you do the right studies, you can look at how much you as an individual spend on your own health care, plotted over your lifetime. And about seven years before you're about to die, there's a spike. And you can actually -- (Laughter) -- we won't get into that. (Laughter)
Dit is leeftijd ten opzichte van kosten. En je kunt zien dat rond de leeftijd van 45 jaar, tussen 40 en 45, een plotselinge piek aanwezig is in de kosten van de gezondheidszorg. Het is eigenlijk best interessant - als je het juiste onderzoek doet- om te zien hoeveel je als individu uitgeeft aan je eigen zorg, op ieder moment van je leven. En ongeveer 7 jaar voordat je dood zou gaan, is er een piek. En je kunt daarmee in feite -- (gelach) -- daar zullen wij niet op ingaan. (gelach)
There are very few things, very few things that you can really do that will change the way that you can treat these kinds of diseases and experience what I would call healthy aging. I'd suggest there are four things, and none of these things include an insurance system or a legal system. All those things do is change who pays. They don't actually change what the actual cost of the treatment is.
Er zijn heel weinig zaken, heel weinig zaken die je werkelijk kunt doen om de manier van behandelen van dit soort ziekten te veranderen en te ervaren wat ik noem " gezond ouder worden" . Ik denk dat er vier zaken zijn. En geen hiervan houdt een verzekeringssysteem of wettelijk systeem in. Al wat deze oplossingen doen is het veranderen van wie betaalt. Zij veranderen in feite niet wat de actuele kosten van de behandeling zijn.
One thing you can do is not treat. You can ration health care. We won't talk about that anymore. It's too depressing. You can prevent. Obviously a lot of monies should be put into prevention.
Een ding wat je kunt doen is niet behandelen. Je kunt gezondheidszorg rantsoeneren. Hier praten wij maar niet meer over. Dat is te deprimerend. Je kunt ook aan preventie doen. Het is duidelijk dat veel geld in preventie gestoken zou moeten worden.
But perhaps most interesting, to me anyway, and most important, is the idea of diagnosing a disease much earlier on in the progression, and then treating the disease to cure the disease instead of treating a symptom. Think of it in terms of diabetes, for instance. Today, with diabetes, what do we do? We diagnose the disease eventually, once it becomes symptomatic, and then we treat the symptom for 10, 20, 30, 40 years. And we do OK. Insulin's a pretty good therapy. But eventually it stops working, and diabetes leads to a predictable onset of debilitating disease.
Maar misschien het meest interessante, voor mij zeker, en het belangrijkste, is het idee om het diagnosticeren van een ziekte in een veel eerder stadium te doen, en dan de ziekte behandelen om de ziekte te genezen in plaats van een symptoom te behandelen. Denk bijvoorbeeld aan diabetes. Wat doen wij op dit moment met diabetes? Wij diagnosticeren uiteindelijk de ziekte, wanneer het symptomatisch wordt, en dan behandelen wij het symptoom gedurende 10, 20, 30, 40 jaar. En dat doen wij goed. Insuline is een behoorlijk goede therapie. Maar tenslotte werkt het niet meer, en leidt diabetes tot een voorspelbaar begin van een chronisch verloop.
Why couldn't we just inject the pancreas with something to regenerate the pancreas early on in the disease, perhaps even before it was symptomatic? And it might be a little bit expensive at the time that we did it, but if it worked, we would truly be able to do something different.
Waarom zouden wij de pancreas niet met iets kunnen injecteren om deze pancreas te regenereren in een vroeg stadium van de ziekte, mogelijk zelfs voor dat deze symptomatisch wordt? En mogelijk zou het een beetje duur kunnen zijn op het moment dat wij dat deden, maar als het werkte, zouden wij werkelijk in staat zijn iets anders te doen.
This video, I think, gets across the concept that I'm talking about quite dramatically. This is a newt re-growing its limb. If a newt can do this kind of thing, why can't we? I'll actually show you some more important features about limb regeneration in a moment. But what we're talking about in regenerative medicine is doing this in every organ system of the body, for tissues and for organs themselves. So today's reality is that if we get sick, the message is we will treat your symptoms, and you need to adjust to a new way of life.
Deze video, denk ik, gaat behoorlijk heftig verder dan het concept waar ik het nu over heb. Dit is een salamander, waarbij een poot opnieuw groeit. Als een salamander dat kan, waarom wij niet? Ik zal je nu enkele andere nog belangrijkere kenmerken laten zien over regeneratie van ledematen. Maar waar wij het in regeneratieve geneeskunde over hebben is de toepassing hiervan bij elk orgaan van het lichaam, bij weefsels en bij de organen zelf. Dus, de realiteit van vandaag is dat als wij ziek worden, de boodschap is: wij behandelen uw symptomen, en je moet je aanpassen aan een nieuwe manier van leven.
I would pose to you that tomorrow -- and when tomorrow is we could debate, but it's within the foreseeable future -- we will talk about regenerative rehabilitation. There's a limb prosthetic up here, similar actually one on the soldier that's come back from Iraq. There are 370 soldiers that have come back from Iraq that have lost limbs. Imagine if instead of facing that, they could actually face the regeneration of that limb. It's a wild concept. I'll show you where we are at the moment in working towards that concept.
Mijn stelling is dat morgen-- en wanneer morgen is, daar kunnen wij het over hebben, maar het is wel in de nabije toekomst--- zullen wij praten over regeneratieve rehabilitatie. Hier is een beenprothese, ongeveer gelijk aan die van de soldaat die uit Irak terugkwam ... er zijn 370 soldaten die teruggekomen zijn uit Irak en ledematen hebben verloren. Stel je voor dat zij in plaats van dit onder ogen te moeten zien een regeneratie van het ledemaat mochten ervaren. Het is een uitdagend concept. Ik zal u laten zien waar wij op dit moment zijn in ons werk richting dit concept.
But it's applicable, again, to every organ system. How can we do that? The way to do that is to develop a conversation with the body. We need to learn to speak the body's language. And to switch on processes that we knew how to do when we were a fetus. A mammalian fetus, if it loses a limb during the first trimester of pregnancy, will re-grow that limb. So our DNA has the capacity to do these kinds of wound-healing mechanisms. It's a natural process, but it is lost as we age. In a child, before the age of about six months, if they lose their fingertip in an accident, they'll re-grow their fingertip. By the time they're five, they won't be able to do that anymore.
Maar het is toepasbaar, nogmaals, bij elk orgaansysteem. Hoe kunnen wij dat doen? De manier om dat te doen is in gesprek proberen te komen met het lichaam. Wij moeten de taal leren spreken van het lichaam. En processen aanzetten die dat konden toen wij nog een foetus waren. Een zoogdierfoetus zal, als deze een ledemaat verliest in de eerste drie maanden van de zwangerschap, deze opnieuw laten ontstaan. Dus ons DNA heeft de capaciteit om dit soort wond-herstellende mechanismen uit te voeren. Het is een natuurlijk proces, maar het verdwijnt tijdens het ouder worden. Bij een kind, voor de leeftijd van 6 maanden, als zij een topje van een vinger bij een ongeval verliezen, zal deze vingertop weer aangroeien. Als kinderen een jaar of 5 zijn, zullen zij niet meer in staat zijn dat te doen.
So to engage in that conversation with the body, we need to speak the body's language. And there are certain tools in our toolbox that allow us to do this today. I'm going to give you an example of three of these tools through which to converse with the body.
Dus om mee te kunnen doen aan deze conversatie met het lichaam, moeten wij de taal van het lichaam spreken. En wij hebben bepaalde gereedschappen in onze kist die ons dat mogelijk maken. Ik ga u een voorbeeld geven van drie van deze gereedshappen waarmee wij in gesprek komen met het lichaam.
The first is cellular therapies. Clearly, we heal ourselves in a natural process, using cells to do most of the work. Therefore, if we can find the right cells and implant them in the body, they may do the healing. Secondly, we can use materials. We heard yesterday about the importance of new materials. If we can invent materials, design materials, or extract materials from a natural environment, then we might be able to have those materials induce the body to heal itself. And finally, we may be able to use smart devices that will offload the work of the body and allow it to heal.
Het eerste gereedschap is cellulaire therapie. Het is duidelijk, wij genezen onszelf in een natuurlijk proces, met gebruik van cellen, die het meeste werk doen. Dus, als wij de juiste cellen kunnen vinden en in het lichaam kunnen inbrengen, zouden zij voor de genezing kunnen zorgen. Ten tweede kunnen wij bepaalde materialen gebruiken. Wij hebben gisteren het een en ander gehoord over hoe belangrijk nieuwe materialen zijn. Als wij materialen kunnen verzinnen, materialen kunnen ontwerpen of materialen kunnen extraheren uit een natuurlijke omgeving, dan zouden wij in staat kunnen zijn deze materialen het lichaam te laten aanzetten tot zelfgenezing. En ten derde zouden wij slimme apparaatjes kunnen gebruiken die werk van het lichaam kunnen overnemen en het in staat stellen te helen.
I'm going to show you an example of each of these, and I'm going to start with materials. Steve Badylak -- who's at the University of Pittsburgh -- about a decade ago had a remarkable idea. And that idea was that the small intestine of a pig, if you threw away all the cells, and if you did that in a way that allowed it to remain biologically active, may contain all of the necessary factors and signals that would signal the body to heal itself. And he asked a very important question. He asked the question, if I take that material, which is a natural material that usually induces healing in the small intestine, and I place it somewhere else on a person's body, would it give a tissue-specific response, or would it make small intestine if I tried to make a new ear?
Ik zal u een voorbeeld geven van elk van deze mogelijkheden, en ik start met materialen. Steve Badylak - werkzaam op de University of Pittsburgh -- had een decennium geleden een opmerkelijk idee. En dat idee was dat de dunnedarm van een varken, als je alle cellen weggooide, en dat zo deed dat de darm biologisch actief bleef, alle noodzakelijke factoren en signalen zou bevatten om het lichaam aan te zetten zichzelf te helen. En hij stelde zich een erg belangrijke vraag. Hij vroeg zich af, als ik dat materiaal, wat natuurlijk materiaal is dat gewoonlijk genezing induceert in de dunne darm, ergens anders op het menselijk lichaam plaats, zou dit dan een weefsel-specifieke reactie geven, of zou het dunnedarmweefsel vormen terwijl ik een nieuw oor wilde maken?
I wouldn't be telling you this story if it weren't compelling. The picture I'm about to show you is a compelling picture. (Laughter) However, for those of you that are even the slightest bit squeamish -- even though you may not like to admit it in front of your friends -- the lights are down. This is a good time to look at your feet, check your Blackberry, do anything other than look at the screen. (Laughter)
Ik zou u dit verhaal niet vertellen als het niet zo fascinerend was. Het plaatje dat ik u ga laten zien -- (gelach) -- is een fascinerend plaatje. Maar, voor diegenen onder jullie die ook maar een beetje overgevoelig zijn, ook als je dat niet wil toegeven ten opzichte van je vrienden -- het licht gaat uit. Een goed moment om naar je voeten te kijken, je Blackberry te controleren, doe iets anders dan naar het scherm kijken. (gelach)
What I'm about to show you is a diabetic ulcer. And although -- it's good to laugh before we look at this. This is the reality of diabetes. I think a lot of times we hear about diabetics, diabetic ulcers, we just don't connect the ulcer with the eventual treatment, which is amputation, if you can't heal it. So I'm going to put the slide up now. It won't be up for long. This is a diabetic ulcer. It's tragic. The treatment for this is amputation. This is an older lady. She has cancer of the liver as well as diabetes, and has decided to die with what' s left of her body intact.
Wat ik u laat zien is een diabetisch ulcer en hoewel - het is goed even te lachen voor wij hiernaar kijken. Dit is de realiteit van diabetes. Ik denk dat wij vaak horen over diabetes, diabetische ulcera maar wij verbinden de ulcer niet met de eventuele behandeling daarvan, en dat is amputatie, als je de ulcer niet kunt genezen. Dus ik laat u nu de sheet zien. Het duurt maar even. Dit is een diabetisch ulcer. Tragisch. De behandeling hiervoor is amputatie. Dit is een oudere dame. Zij heeft leverkanker en diabetes, en heeft besloten te sterven met wat nog over is van haar lichaam.
And this lady decided, after a year of attempted treatment of that ulcer, that she would try this new therapy that Steve invented. That's what the wound looked like 11 weeks later. That material contained only natural signals. And that material induced the body to switch back on a healing response that it didn't have before.
En deze dame nam de beslissing na een jaar mislukte behandeling van dit ulcer, om de nieuwe therapie die Steven heeft ontwikkeld uit te proberen. Zo ziet de wond er uit na 11 weken behandeling. Dat materiaal bevatte alleen natuurlijke signalen. En dat materiaal zette het lichaam aan om terug te keren naar een genezende reactie die het ervoor niet had.
There's going to be a couple more distressing slides for those of you -- I'll let you know when you can look again. This is a horse. The horse is not in pain. If the horse was in pain, I wouldn't show you this slide. The horse just has another nostril that's developed because of a riding accident. Just a few weeks after treatment -- in this case, taking that material, turning it into a gel, and packing that area, and then repeating the treatment a few times -- and the horse heals up. And if you took an ultrasound of that area, it would look great.
Er komen nog een paar angstwekkende sheets voor diegenen onder jullie die --- Ik geef wel aan wanneer jullie weer kunnen kijken. Dit is een paard. Het paard heeft geen pijn. Als het paard pijn zou lijden zou ik de sheet niet hebben laten zien. Het paard heeft een nieuwe neusvleugel ontwikkeld noodzakelijk door een ruiterongeluk. Slechts enkele weken na behandeling -- in dit geval, door dat materiaal te gebruiken, omgevormd tot een gel, en door dat gebied daarmee in te pakken, en dit enige malen te herhalen -- en het paard herstelde. En als je een ultrasound opname zou maken van dat gebied, zou het er fantastisch uitzien.
Here's a dolphin where the fin's been re-attached. There are now 400,000 patients around the world who have used that material to heal their wounds. Could you regenerate a limb? DARPA just gave Steve 15 million dollars to lead an eight-institution project to begin the process of asking that question.
Hier zie je een dolfijn waarbij de vin opnieuw is aangebracht. Op dit moment zijn er wereldwijd 400.000 patiënten die dat materiaal hebben gebruikt om hun wonden te laten genezen. Kun je een ledemaat regenereren? DARPA gaf Steve 15 miljoen dollars om een project met 8 instituten te leiden om het proces te starten hierop een antwoord te geven.
And I'll show you the 15 million dollar picture. This is a 78 year-old man who's lost the end of his fingertip. Remember that I mentioned before the children who lose their fingertips. After treatment that's what it looks like. This is happening today. This is clinically relevant today. There are materials that do this. Here are the heart patches.
En ik laat u het 15 miljoen dollar plaatje zien. Dit is een 78 jarige man die het laatste stukje van de top van zijn vinger kwijt is. Herinner u even dat ik eerder het voorbeeld gaf van de kinderen die een vingertop verloren hadden. Na behandeling ziet het er zo uit. Dit is wat er heden ten dage gebeurt. Dit is op dit moment klinisch relevant. Er zijn materialen die dit kunnen. Dit geeft de burger moed.
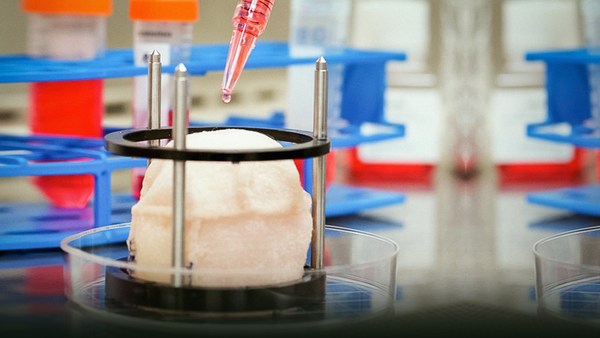
But could you go a little further? Could you, say, instead of using material, can I take some cells along with the material, and remove a damaged piece of tissue, put a bio-degradable material on there? You can see here a little bit of heart muscle beating in a dish. This was done by Teruo Okano at Tokyo Women's Hospital. He can actually grow beating tissue in a dish. He chills the dish, it changes its properties and he peels it right out of the dish. It's the coolest stuff.
Maar kun je nog iets verder gaan? Kun je, zeg, in plaats van materiaal te gebruiken, kan ik enkele cellen met het materiaal mee opnemen, en een stuk beschadigd weefsel verwijderen, en er een bio-afbreekbaar materiaal op leggen? Hier kun je een klein stukje hartspier zien kloppen in een schaal. Dit is gedaan door Teruo Okano in het Tokyo Women's Hospital. Hij kan echt kloppend weefsel in een schaal laten groeien. Hij koelt de schaal af, waardoor de eigenschappen veranderen en hij pelt het direct uit de schaal. Dit is zeer bijzonder.
Now I'm going to show you cell-based regeneration. And what I'm going to show you here is stem cells being removed from the hip of a patient. Again, if you're squeamish, you don't want to watch. But this one's kind of cool. So this is a bypass operation, just like what Al Gore had, with a difference. In this case, at the end of the bypass operation, you're going to see the stem cells from the patient that were removed at the beginning of the procedure being injected directly into the heart of the patient. And I'm standing up here because at one point I'm going to show you just how early this technology is. Here go the stem cells, right into the beating heart of the patient. And if you look really carefully, it's going to be right around this point you'll actually see a back-flush. You see the cells coming back out. We need all sorts of new technology, new devices, to get the cells to the right place at the right time.
Nu laat ik u op cellen gebaseerde regeneratie zien. En wat ik u ga laten zien zijn stamcellen die uit de heup van een patiënt zijn gehaald. En nogmaals, als u heel gevoelig bent, hoeft u niet te kijken. Maar dit is wel bijzonder. Dus, dit is een bypassoperatie, net zoals Al Gore heeft gehad, met een verschil. In dit geval, aan het einde van de bypassoperatie, zult u zien dat de stamcellen van de patiënt die aan het begin van de procedure zijn verwijderd direct geïnjecteerd worden in het hart van de patiënt. En ik sta even hierop omdat op dit punt ik u ga laten zien hoe jong deze technologie is. Hier gaan de stamcellen, direct het kloppend hart van de patiënt in. En als je heel precies kijkt, gaat het direct om dit punt heen je ziet feitelijk een terugvloed. Je ziet de cellen er weer uitkomen. Wij hebben allerlei nieuwe soorten technologie nodig, nieuwe apparaten, om de cellen naar de juiste plek op het juiste tijdstip in te kunnen brengen.
Just a little bit of data, a tiny bit of data. This was a randomized trial. At this time this was an N of 20. Now there's an N of about 100. Basically, if you take an extremely sick patient and you give them a bypass, they get a little bit better. If you give them stem cells as well as their bypass, for these particular patients, they became asymptomatic. These are now two years out. The coolest thing would be is if you could diagnose the disease early, and prevent the onset of the disease to a bad state.
Nog een beetje statistiek, een klein beetje data. Dit was een gerandomiseerde proef. Op dit tijdstip was er een N van 20. Nu is er een N van ongeveer 100. Eigenlijk is het zo; als je een extreem zieke patiënt hebt en je geeft hem een bypass, dan wordt hij een beetje beter. Als je hen zowel stamcellen als een bypass geeft, bij deze patiënten, dan hebben ze geen symptomen meer. Deze zijn nu twee jaar verder. Het meest fascinerende is als je de diagnose vroeg kan stellen, en het begin van de ziekte kan tegenhouden in zijn ontwikkeling.
This is the same procedure, but now done minimally invasively, with only three holes in the body where they're taking the heart and simply injecting stem cells through a laparoscopic procedure. There go the cells. We don't have time to go into all of those details, but basically, that works too. You can take patients who are less sick, and bring them back to an almost asymptomatic state through that kind of therapy.
Dit is dezelfde procedure, maar minder invasief, met slechts drie gaatjes in het lichaam bij het hart en simpel via een laparoscopie de stamcellen injecteren. Daar gaan de cellen. Wij hebben geen tijd om op alle details in te gaan, maar in de kern, dat werkt ook. Je kunt ook minder zieke patiënten nemen, en hen terugbrengen naar een bijna symptoomloze toestand door dit soort therapie.
Here's another example of stem-cell therapy that isn't quite clinical yet, but I think very soon will be. This is the work of Kacey Marra from Pittsburgh, along with a number of colleagues around the world. They've decided that liposuction fluid, which -- in the United States, we have a lot of liposuction fluid. (Laughter) It's a great source of stem cells. Stem cells are packed in that liposuction fluid. So you could go in, you could get your tummy-tuck. Out comes the liposuction fluid, and in this case, the stem cells are isolated and turned into neurons. All done in the lab. And I think fairly soon, you will see patients being treated with their own fat-derived, or adipose-derived, stem cells.
Hier is nog een voorbeeld van stamceltherapie welke nog niet in klinische fase is, maar naar mijn idee wel spoedig zal komen. Dit is het werk van Kacey Marra uit Pittsburgh, samen met een aantal collega's uit de hele wereld. Zij hebben besloten dat vloeistof van een liposuctie, wat -- in de VS hebben wij veel vloeistof uit liposuctie. (gelach) Het is een grote bron aan stamcellen. Stamcellen zitten verpakt in de liposuctievloeistof. Dus je kunt naar binnen, en neemt je buikplooi. Daar heb je de liposuctievloeistof en in dit geval, worden de stamcellen geïsoleerd en omgevormd naar neuronen. Allemaal in het laboratorium. En ik denk dat je behoorlijk snel patiënten zult zien, die behandeld worden met hun eigen uit vet afkomstige, of uit hun adipositas verkregen, stamcellen.
I talked before about the use of devices to dramatically change the way we treat disease. Here's just one example before I close up. This is equally tragic. We have a very abiding and heartbreaking partnership with our colleagues at the Institute for Surgical Research in the US Army, who have to treat the now 11,000 kids that have come back from Iraq. Many of those patients are very severely burned.
Eerder heb ik gesproken over het gebruik van apparatuur om de manier waarop wij de ziekte behandelen enorm te veranderen. Hier is slechts één voorbeeld voordat ik afsluit. Dit is net zo tragisch. Wij hebben een erg duurzaam en hartverscheurende relatie met onze collega's van het instituut voor Chirurgisch Onderzoek in de US Army, die 11,000 kinderen moeten behandelen die terug zijn gekomen uit Irak. Veel van die patiënten zijn zeer ernstig verbrand.
And if there's anything that's been learned about burn, it's that we don't know how to treat it. Everything that is done to treat burn -- basically we do a sodding approach. We make something over here, and then we transplant it onto the site of the wound, and we try and get the two to take. In this case here, a new, wearable bio-reactor has been designed -- it should be tested clinically later this year at ISR -- by Joerg Gerlach in Pittsburgh. And that bio-reactor will lay down in the wound bed. The gun that you see there sprays cells. That's going to spray cells over that area. The reactor will serve to fertilize the environment, deliver other things as well at the same time, and therefore we will seed that lawn, as opposed to try the sodding approach. It's a completely different way of doing it.
En als wij iets hebben geleerd van brandwonden dan is het wel dat wij niet weten hoe deze te behandelen. Alles wat is geprobeerd om brandwonden te behandelen --- in de kern gebruiken wij een toedekkende benadering. Wij halen iets op deze plaats, en wij transplanteren het op de plek van de wond, en wij proberen beide plaatsen het te laten accepteren. In dit voorbeeld hier, is een nieuw, draagbare bio-reactor ontworpen -- het moet nog klinisch getest worden later dit jaar bij ISR -- door Joerg Gerlach in Pittsburgh. En deze bio-reactor wordt in het wondbed gelegd. Het pistool wat je ziet sproeit cellen. Het sproeit cellen over dat gebied. De reactor dient om de omgeving vruchtbaar te maken, en levert ook nog andere zaken op hetzelfde moment, en daarom bezaaien wij die baan, als tegengestelde aan de toedekkende benadering. Het is een totaal andere manier van werken.
So my 18 minutes is up. So let me finish up with some good news, and maybe a little bit of bad news. The good news is that this is happening today. It's very powerful work. Clearly the images kind of get that across. It's incredibly difficult because it's highly inter-disciplinary. Almost every field of science engineering and clinical practice is involved in trying to get this to happen.
Nou mijn 18 minuten zijn om. Dus laat ik maar eindigen met wat goed nieuws, en misschien een klein beetje slecht nieuws. Het goede nieuws is dat dit op dit moment gebeurt. Het is heel erg sterk werk. Zeker als je kijkt naar de beelden die zijn langs gekomen. Het is ongelooflijk moeilijk, want er zijn veel disciplines bij betrokken. Bijna elk terrein van de technische wetenschap en de klinische praktijk is betrokken om dit te laten gebeuren.
A number of governments, and a number of regions, have recognized that this is a new way to treat disease. The Japanese government were perhaps the first, when they decided to invest first 3 billion, later another 2 billion in this field. It's no coincidence. Japan is the oldest country on earth in terms of its average age. They need this to work or their health system dies. So they're putting a lot of strategic investment focused in this area. The European Union, same thing. China, the same thing. China just launched a national tissue-engineering center. The first year budget was 250 million US dollars.
Een aantal overheidsinstellingen, een aantal regio's hebben onderkend dat dit een nieuwe manier is om ziekte te behandelen. De Japanse overheid was misschien de eerste, toen zij 3 biljoen besloten te investeren, en later nog eens 2 biljoen hierin. Het is geen toeval. Japan is het oudste land op aarde in termen van de leeftijd van de bevolking. Zij hebben dit nodig anders sterft hun gezondheidszorgsysteem. Dus stoppen zij heel veel strategische investeringen in dit gebied. De Europese Unie, hetzelfde. China, net zo. China heeft net een nationaal weefsel-ontwikkelingscentrum opgericht. Het budget voor het eerste jaar was 250 miljoen Amerikaanse dollar.
In the United States we've had a somewhat different approach. (Laughter) Oh, for Al Gore to come and be in the real world as president. We've had a different approach. And the approach has basically been to just sort of fund things as they come along. But there's been no strategic investment to bring all of the necessary things to bear and focus them in a careful way.
In de VS hebben wij een iets andere benadering gehad. Wij -- (gelach) -- oh, stel je voor, Al Gore als president in de echte wereld. Wij hebben een andere benadering gehad. En deze ging in essentie over het ondersteunen van zaken met een fonds wanneer deze langskwamen. Maar er is geen strategisch investeringsbeleid om alle noodzakelijke elementen op te pakken en ze zorgvuldig te focussen.
And I'm going to finish up with a quote, maybe a little cheap shot, at the director of the NIH, who's a very charming man. Myself and Jay Vacanti from Harvard went to visit with him and a number of his directors of his institute just a few months ago, to try and convince him that it was time to take just a little piece of that 27.5 billion dollars that he's going to get next year and focus it, in a strategic way, to make sure we can accelerate the pace at which these things get to patients. And at the end of a very testy meeting, what the NIH director said was, "Your vision is larger than our appetite." I'd like to close by saying that no one's going to change our vision, but together we can change his appetite. Thank you.
En ik eindig met een citaat, misschien een goedkope steek, naar de directeur van de NIH, die een zeer charmante man is. Ikzelf en Jay Vacanti van Harvard bezochten hem en een aantal van zijn directeuren van zijn instituut enkele maanden geleden, om hem te proberen te overtuigen dat het tijd werd om, al was het maar een klein stukje van die 27,5 miljard dollars die hij volgend jaar gaat krijgen, te gaan besteden op een strategisch wijze, om er voor te zorgen dat wij het tempo kunnen versnellen om deze zaken bij de patiënt te brengen. En aan het einde van een erg kritische bijeenkomst is dit wat de NIH directeur zei: "Uw visie is groter dan onze maag". Ik sluit af met de woorden dat niemand onze visie kan veranderen, maar samen kunnen wij wel zijn maag vergroten. Dank u.