I'm going to talk to you today about hopefully converting fear into hope. When we go to the physician today -- when we go to the doctor's office and we walk in, there are words that we just don't want to hear. There are words that we're truly afraid of. Diabetes, cancer, Parkinson's, Alzheimer's, heart failure, lung failure -- things that we know are debilitating diseases, for which there's relatively little that can be done.
Aion puhua teille tänään pelon kääntämisestä toivoksi. Kun nykyään menee lääkärille, kun menee vastaanotolle, on sanoja, joita ei yksinkertaisesti halua kuulla. On sanoja, joita todella pelkäämme. Diabetes, syöpä, Parkinsonin tauti, Alzheimer, sydämen tai keuhkojen vajaatoiminta. Ne ovat heikentäviä sairauksia, joille ei voida tehdä juuri mitään.
And what I want to lay out for you today is a different way of thinking about how to treat debilitating disease, why it's important, why without it perhaps our health care system will melt down if you think it already hasn't, and where we are clinically today, and where we might go tomorrow, and what some of the hurdles are. And we're going to do all of that in 18 minutes, I promise.
Haluan näyttää teille tänään erilaisen ajattelutavan, miten heikentäviä tauteja voidaan hoitaa, ja miksi se on tärkeää. Koska ilman sitä, kenties, meidän terveydenhuoltojärjestelmämme hajoaa, jos se ei ole sitä jo tehnyt. Ja missä olemme kliinisellä tasolla, minne olemme menossa, ja mitä esteitä matkalla on. Ja kaikki tämä 18 minuutissa, sen lupaan.
I want to start with this slide, because this slide sort of tells the story the way Science Magazine thinks of it. This was an issue from 2002 that they published with a lot of different articles on the bionic human. It was basically a regenerative medicine issue. Regenerative medicine is an extraordinarily simple concept that everybody can understand. It's simply accelerating the pace at which the body heals itself to a clinically relevant timescale. So we know how to do this in many of the ways that are up there. We know that if we have a damaged hip, you can put an artificial hip in. And this is the idea that Science Magazine used on their front cover.
Aloitetaan tästä. Tämä kertoo Science-lehden käsityksen asiasta. Tässä numerossa vuodelta 2002 heillä oli useita artikkeleita bionisesta ihmisestä. Se oli käytännössä regeneratiivisen lääketieteen numero. Regeneratiivinen lääketiede on epätavallisen yksinkertainen käsite, jonka kuka tahansa ymmärtää. Se yksinkertaisesti nopeuttaa kehon omaa paranemista kliinisesti relevantissa ajassa. Osaamme jo hoitaa tavoilla, jotka on kuvattu tuossa ylhäällä. Osaamme laittaa tekonivelen vaurioituneeseen lonkkaan. Ja tätä ideaa Science-lehti esitteli etusivullaan.
This is the complete antithesis of regenerative medicine. This is not regenerative medicine. Regenerative medicine is what Business Week put up when they did a story about regenerative medicine not too long ago. The idea is that instead of figuring out how to ameliorate symptoms with devices and drugs and the like -- and I'll come back to that theme a few times -- instead of doing that, we will regenerate lost function of the body by regenerating the function of organs and damaged tissue. So that at the end of the treatment, you are the same as you were at the beginning of the treatment.
Tämä on regeneratiivisen lääketieteen täydellinen vastakohta. Tämä ei ole regeneratiivista lääketiedettä. Business Week -lehdessä se on esitetty oikein, kun he tekivät asiasta jutun melko vähän aikaa sitten. Sen sijaan, että parantaisimme oireita laitteiden ja lääkkeiden avulla -- palaan tähän teemaan myöhemmin -- sen sijaan uudistamme kehon menetetyn toimintakyvyn regeneroimalla elimien toiminnan ja vahingoittuneen kudoksen. Joten hoidon loputtua henkilö ei ole muuttunut hoidon alkuun verrattuna.
Very few good ideas -- if you agree that this is a good idea -- very few good ideas are truly novel. And this is just the same. If you look back in history, Charles Lindbergh, who was better known for flying airplanes, was actually one of the first people along with Alexis Carrel, one of the Nobel Laureates from Rockefeller, to begin to think about, could you culture organs? And they published this book in 1937, where they actually began to think about, what could you do in bio-reactors to grow whole organs? We've come a long way since then. I'm going to share with you some of the exciting work that's going on.
Hyvin harvat ideat -- jos olette samaa mieltä tämän idean hyvyydestä -- hyvin harvat ideat ovat todella uusia. Tämä on juuri sellainen. Aiemmin historiassa Charles Lindbergh -- joka on paremmin tunnettu lentäjänä -- oli yksi ensimmäisistä, joka Nobel-palkitun Alexis Carrelin tavoin pohti, voisiko elimiä viljellä? He julkaisivat kirjan 1937. Siinä he pohtivat mahdollisuutta kasvattaa kokonaisia elimiä bioreaktoreissa. Olemme edistyneet. Aion kertoa teille jännittävästä työstä, joka nyt on meneillään.
But before doing that, what I'd like to do is share my depression about the health care system and the need for this with you. Many of the talks yesterday talked about improving the quality of life, and reducing poverty, and essentially increasing life expectancy all around the globe. One of the challenges is that the richer we are, the longer we live. And the longer we live, the more expensive it is to take care of our diseases as we get older.
Mutta ennen sitä haluaisin jakaa huoleni terveydenhuoltojärjestelmästämme ja työmme tärkeydestä. Useat eilisistä puheista käsittelivät sitä, miten elämänlaatua parannetaan köyhyyttä vähentämällä. Se siis lisää elinajanodotetta ympäri maapalloa. Yksi haasteista on se, että mitä rikkaampia olemme, sitä pidempään elämme. Ja mitä pidempään elämme, sitä kalliimmaksi tulee sairauksiemme hoito, kun vanhenemme.
This is simply the wealth of a country versus the percent of population over the age of 65. And you can basically see that the richer a country is, the older the people are within it. Why is this important? And why is this a particularly dramatic challenge right now? If the average age of your population is 30, then the average kind of disease that you have to treat is maybe a broken ankle every now and again, maybe a little bit of asthma. If the average age in your country is 45 to 55, now the average person is looking at diabetes, early-onset diabetes, heart failure, coronary artery disease -- things that are inherently more difficult to treat, and much more expensive to treat.
Tämä on maan varallisuus ja yli 65-vuotiaiden prosentuaalinen osuus väestöstä. Mitä rikkaampi maa on, sitä vanhempia ihmisiä siellä on. Miksi tämä on tärkeää? Ja miksi tämä on erityisen dramaattinen haaste juuri nyt? Jos populaation ikäkeskiarvo on 30, silloin keskimääräinen hoitoa kaipaava sairaus on kenties nilkan murtuma silloin tällöin, ehkä vähän astmaa. Jos ikäkeskiarvo maassa on 45:stä 55:een, keskimääräinen ihminen saa diabeteksen, sydämen vajaatoimintaa, sepelvaltimotaudin. Näitä on väistämättä vaikeampi hoitaa, ja hoitaminen on paljon kalliimpaa.
Just have a look at the demographics in the U.S. here. This is from "The Untied States of America." In 1930, there were 41 workers per retiree. 41 people who were basically outside of being really sick, paying for the one retiree who was experiencing debilitating disease. In 2010, two workers per retiree in the U.S. And this is matched in every industrialized, wealthy country in the world. How can you actually afford to treat patients when the reality of getting old looks like this?
Katsokaa näitä Yhdysvaltain väestötietoja. Tämä on kirjasta "The Untied States of America". Vuonna 1930 oli 41 työntekijää yhtä eläkeläistä kohti. 41 käytännössä tervettä henkilöä kustansi yhden eläkeläisen, jolla oli heikentävä sairaus. Vuonna 2010 Yhdysvalloissa on kaksi työntekijää eläkeläistä kohti. Sama toistuu kaikissa teollistuneissa, varakkaissa maissa ympäri maailman. Miten meillä on varaa hoitaa potilaita, kun vanheneminen näyttää tältä?
This is age versus cost of health care. And you can see that right around age 45, 40 to 45, there's a sudden spike in the cost of health care. It's actually quite interesting. If you do the right studies, you can look at how much you as an individual spend on your own health care, plotted over your lifetime. And about seven years before you're about to die, there's a spike. And you can actually -- (Laughter) -- we won't get into that. (Laughter)
Tässä ikä verrattuna hoitokustannuksiin. Katsokaa kuinka suunnilleen 45-vuotiaana, 40:stä 45:een, hoitokustannukset äkisti kasvavat. On aika mielenkiintoista -- tutkimuksista selviää, miten paljon kukin henkilö käyttää rahaa terveydenhoitoon elämänsä aikana. Noin seitsemän vuotta ennen kuolemaa kustannuksissa on piikki. On siis mahdollista -- (Naurua) -- ei siitä sen enempää. (Naurua)
There are very few things, very few things that you can really do that will change the way that you can treat these kinds of diseases and experience what I would call healthy aging. I'd suggest there are four things, and none of these things include an insurance system or a legal system. All those things do is change who pays. They don't actually change what the actual cost of the treatment is.
On hyvin vähän asioita, joita voi tehdä muuttaakseen tämän kaltaisten sairausten hoitoa, ja saavuttaa niin kutsutun terveen ikääntymisen. On neljä asiaa. Mikään näistä ei sisällä vakuutus- tai oikeusjärjestelmää. Ne ainoastaan muuttavat maksajaa. Ne eivät muuta itse hoitojen kustannuksia.
One thing you can do is not treat. You can ration health care. We won't talk about that anymore. It's too depressing. You can prevent. Obviously a lot of monies should be put into prevention.
Voidaan olla hoitamatta. Terveydenhuoltoa voidaan rajoittaa. Ei puhuta siitä. Se olisi liian masentavaa. Voidaan ennaltaehkäistä. Suuria rahasummia tulisi laittaa ennaltaehkäisyyn.
But perhaps most interesting, to me anyway, and most important, is the idea of diagnosing a disease much earlier on in the progression, and then treating the disease to cure the disease instead of treating a symptom. Think of it in terms of diabetes, for instance. Today, with diabetes, what do we do? We diagnose the disease eventually, once it becomes symptomatic, and then we treat the symptom for 10, 20, 30, 40 years. And we do OK. Insulin's a pretty good therapy. But eventually it stops working, and diabetes leads to a predictable onset of debilitating disease.
Ehkä mielenkiintoisinta ja tärkeintä olisi diagnosoida sairaus paljon aiemmin, ja hoitaa sairaus oireiden hoitamisen sijaan. Ajatelkaa esimerkiksi diabetestä. Miten me nykyään hoidamme diabetestä? Me diagnosoimme sairauden sen oireiden ilmaannuttua, ja hoidamme sen oireita 10, 20, 30, 40 vuotta. Ja se toimii. Insuliini on melko hyvä hoito. Mutta lopulta se lakkaa toimimasta, ja diabetes johtaa ennustettaviin heikentäviin sairauksiin.
Why couldn't we just inject the pancreas with something to regenerate the pancreas early on in the disease, perhaps even before it was symptomatic? And it might be a little bit expensive at the time that we did it, but if it worked, we would truly be able to do something different.
Miksi emme vain ruiskuttaisi haimaan jotain, mikä parantaisi haiman sairauden alkuvaiheessa, jopa ennen kuin se oireilisi? Se saattaisi olla tuolloin kallista, mutta jos se toimisi, se olisi todella jotain uutta.
This video, I think, gets across the concept that I'm talking about quite dramatically. This is a newt re-growing its limb. If a newt can do this kind of thing, why can't we? I'll actually show you some more important features about limb regeneration in a moment. But what we're talking about in regenerative medicine is doing this in every organ system of the body, for tissues and for organs themselves. So today's reality is that if we get sick, the message is we will treat your symptoms, and you need to adjust to a new way of life.
Tämä video kertoo mielestäni aika hyvin -- ja dramaattisesti -- mistä on kyse. Tässä vesilisko kasvattaa uudelleen raajansa. Jos vesilisko voi tehdä tuon, miksemme me voi? Näytän teille muita esimerkkejä raajojen regeneroinnista pian. Regeneroivassa lääketieteessä me haluamme tehdä saman kaikissa kehon elimissä, kudoksissa ja elimissä itsessään. Nykyään jos tulee sairaaksi, voimme hoitaa oireita, ja henkilön tulee omaksua uusi elämäntapa.
I would pose to you that tomorrow -- and when tomorrow is we could debate, but it's within the foreseeable future -- we will talk about regenerative rehabilitation. There's a limb prosthetic up here, similar actually one on the soldier that's come back from Iraq. There are 370 soldiers that have come back from Iraq that have lost limbs. Imagine if instead of facing that, they could actually face the regeneration of that limb. It's a wild concept. I'll show you where we are at the moment in working towards that concept.
Ehdotan teille, että tulevaisuudessa -- voimme keskustella milloin se on, mutta se on nähtävissä -- me tulemme puhumaan regeneroivasta kuntouttamisesta. Tuolla on raajaproteesi, samanlainen kuin sotilaiden saama, kun he tulevat takaisin Irakista ... 370 sotilasta on tullut takaisin Irakista ilman raajaa tai raajoja. Kuvitelkaa, jos he proteesin sijaan voisivat saada raajansa takaisin regeneraatiolla. Se on hurja ajatus. Näytän teille miten lähellä olemme tuota ajatusta.
But it's applicable, again, to every organ system. How can we do that? The way to do that is to develop a conversation with the body. We need to learn to speak the body's language. And to switch on processes that we knew how to do when we were a fetus. A mammalian fetus, if it loses a limb during the first trimester of pregnancy, will re-grow that limb. So our DNA has the capacity to do these kinds of wound-healing mechanisms. It's a natural process, but it is lost as we age. In a child, before the age of about six months, if they lose their fingertip in an accident, they'll re-grow their fingertip. By the time they're five, they won't be able to do that anymore.
Mutta se toimii kaikkiiin elimiin. Kuinka me teemme sen? Kehitämme keskustelun kehon kanssa. Meidän tulee oppia kehon kieltä. Ja käynnistää prosesseja, jotka tunsimme ollessamme sikiöitä. Jos nisäkkään sikiö menettää raajan raskauden ensimmäisellä kolmanneksella, se kasvattaa sen uudelleen. Meidän DNA:ssamme on kyky tällaisiin parannusmekanismeihin. Se on luonnollinen prosessi, mutta menetämme sen ikääntyessämme. Lapsi, ennen kuuden kuukauden ikää, jos menettää sormenpäänsä, kasvattaa sen takaisin. Viisivuotiaina he eivät pysty enää tekemään sitä.
So to engage in that conversation with the body, we need to speak the body's language. And there are certain tools in our toolbox that allow us to do this today. I'm going to give you an example of three of these tools through which to converse with the body.
Voidaksemme keskustella kehon kanssa, meidän on osattava kehon kieltä. Meillä on muutamia työkaluja siihen nykyään. Annan teille kolme esimerkkiä näistä työkaluista, joiden kautta keskustelemme kehon kanssa.
The first is cellular therapies. Clearly, we heal ourselves in a natural process, using cells to do most of the work. Therefore, if we can find the right cells and implant them in the body, they may do the healing. Secondly, we can use materials. We heard yesterday about the importance of new materials. If we can invent materials, design materials, or extract materials from a natural environment, then we might be able to have those materials induce the body to heal itself. And finally, we may be able to use smart devices that will offload the work of the body and allow it to heal.
Ensimmäinen on soluterapia. Parannamme itsemme luonnollisessa prosessissa solujen tehdessä suurimman työn. Jos voimme löytää oikeat solut ja istuttaa ne kehoon, ne saattavat parantaa. Toisena, voimme käyttää materiaaleja. Kuulimme eilen uusien materiaalien tärkeydestä. Jos voimme keksiä, suunnitella materiaaleja, tai eristää materiaaleja luonnosta, nuo materiaalit saattavat saada kehon parantamaan itsensä. Lopuksi, voimme käyttää fiksuja laitteita, jotka tekemällä osan kehon työstä, antavat sen parantua.
I'm going to show you an example of each of these, and I'm going to start with materials. Steve Badylak -- who's at the University of Pittsburgh -- about a decade ago had a remarkable idea. And that idea was that the small intestine of a pig, if you threw away all the cells, and if you did that in a way that allowed it to remain biologically active, may contain all of the necessary factors and signals that would signal the body to heal itself. And he asked a very important question. He asked the question, if I take that material, which is a natural material that usually induces healing in the small intestine, and I place it somewhere else on a person's body, would it give a tissue-specific response, or would it make small intestine if I tried to make a new ear?
Näytän teille esimerkin jokaisesta näistä, ja aloitan materiaaleista. Steve Badylak -- Pittsburghin yliopistosta -- sai noin 10 vuotta sitten loistavan idean. Hänen ideansa oli, että sian ohutsuoli, jos heitetään mäkeen kaikki solut, ja jos se tehdään niin, että se pysyy biologisesti aktiivisena, voi sisältää kaikki tarvittavat tekijät ja signaalit, jotka signaloivat kehon parantamaan itsensä. Hän kysyi hyvin tärkeän kysymyksen. Hän kysyi, jos otetaan tämä luonnollinen materiaali, joka yleensä aikaan saa parantumista ohutsuolessa, ja se laitetaan jonnekin muualle henkilön kehoon, antaako se kudosspesifisen vasteen vai yrittäisikö se tehdä ohutsuolta uuden korvan sijaan?
I wouldn't be telling you this story if it weren't compelling. The picture I'm about to show you is a compelling picture. (Laughter) However, for those of you that are even the slightest bit squeamish -- even though you may not like to admit it in front of your friends -- the lights are down. This is a good time to look at your feet, check your Blackberry, do anything other than look at the screen. (Laughter)
En kertoisi teille tätä tarinaa, jos se ei olisi voimallinen. Kuva, jonka aion näyttää teille -- (Naurua) -- on voimallinen kuva. Ne teistä, jotka ovat edes hitusen herkkähermoisia -- vaikka eivät myöntäisi sitä julkisesti -- Nyt on hyvä hetki katsella jalkojanne, tarkistaa Blackberry, tehdä mitä tahansa muuta kuin katsoa valkokangasta. (Naurua)
What I'm about to show you is a diabetic ulcer. And although -- it's good to laugh before we look at this. This is the reality of diabetes. I think a lot of times we hear about diabetics, diabetic ulcers, we just don't connect the ulcer with the eventual treatment, which is amputation, if you can't heal it. So I'm going to put the slide up now. It won't be up for long. This is a diabetic ulcer. It's tragic. The treatment for this is amputation. This is an older lady. She has cancer of the liver as well as diabetes, and has decided to die with what' s left of her body intact.
Aion näyttää teille diabeettisen haavauman. Ja vaikka -- on hyvä nauraa ennen kuin katsomme tätä. Tämä on todellisuutta diabeteksessä. Usein kun kuulemme diabeteksestä ja sen haavaumista, emme yhdistä haavaumaa sen lopulliseen hoitoon, amputaatioon, jos sitä ei voida parantaa. Laitan kuvan nyt vähäksi aikaa esille. Tämä on diabeetikon haavauma. Hoitona on amputaatio. Tämä on vanhempi rouva. Hänellä on maksasyöpä diabeteksen lisäksi, ja hän on päättänyt kuolla jättäen jälkeensä kehonsa sellaisena kuin se on.
And this lady decided, after a year of attempted treatment of that ulcer, that she would try this new therapy that Steve invented. That's what the wound looked like 11 weeks later. That material contained only natural signals. And that material induced the body to switch back on a healing response that it didn't have before.
Tämä rouva päätti, kun haavaumaa oli yritetty hoitaa vuoden ajan, että hän kokeilisi Steven keksimää uutta terapiaa. Tältä haava näytti 11 viikkoa myöhemmin. Tämä materiaali sisältää vain luonnollisia signaaleja. Materiaali sai kehon taas parannusvasteeseen, mitä sillä ei ollut aiemmin.
There's going to be a couple more distressing slides for those of you -- I'll let you know when you can look again. This is a horse. The horse is not in pain. If the horse was in pain, I wouldn't show you this slide. The horse just has another nostril that's developed because of a riding accident. Just a few weeks after treatment -- in this case, taking that material, turning it into a gel, and packing that area, and then repeating the treatment a few times -- and the horse heals up. And if you took an ultrasound of that area, it would look great.
Nyt tulee vielä pari ahdistavaa kuvaa teille, jotka -- Kerron kun voitte taas katsoa. Tässä on hevonen. Hevosella ei ole kipuja. Jos hevosella olisi kipuja, en näyttäisi teille tätä kuvaa. Hevosella on vain ylimääräinen sierain ratsastusonnettomuuden takia. Muutama viikko hoidon jälkeen -- tässä tapauksessa, materiaalista tehtiin geeliä, ja se laitettiin tuolle alueelle, ja toistettiin muutaman kerran -- ja hevonen parantui. Jos tuosta ottaisi ultraäänikuvan, se näyttäisi hyvältä.
Here's a dolphin where the fin's been re-attached. There are now 400,000 patients around the world who have used that material to heal their wounds. Could you regenerate a limb? DARPA just gave Steve 15 million dollars to lead an eight-institution project to begin the process of asking that question.
Delfiini, jonka evä on kiinnittynyt takaisin. Yhteensä 400 000 potilasta on käyttänyt tätä materiaalia haavojensa parantamiseen. Voimmeko regeneroida raajan? DARPA antoi juuri Stevelle 15 milj. dollaria kahdeksan instituutin projektiin, jotta tuo kysymys voidaan kysyä.
And I'll show you the 15 million dollar picture. This is a 78 year-old man who's lost the end of his fingertip. Remember that I mentioned before the children who lose their fingertips. After treatment that's what it looks like. This is happening today. This is clinically relevant today. There are materials that do this. Here are the heart patches.
Näytän teille nyt 15 miljoonan dollarin kuvan. Tämä on 78-vuotias mies, joka menetti sormenpäänsä. Mainitsin aiemmin lapset, jotka menettivät sormenpäänsä. Hoidon jälkeen se näyttää tältä. Tämä tapahtuu nyt. Tämä on kliinisesti relevanttia jo nyt. On olemassa materiaaleja, jotka toimivat. Sydämellekin.
But could you go a little further? Could you, say, instead of using material, can I take some cells along with the material, and remove a damaged piece of tissue, put a bio-degradable material on there? You can see here a little bit of heart muscle beating in a dish. This was done by Teruo Okano at Tokyo Women's Hospital. He can actually grow beating tissue in a dish. He chills the dish, it changes its properties and he peels it right out of the dish. It's the coolest stuff.
Mutta voimmeko mennä pidemmälle? Voisimmeko materiaalien sijaan ottaa joitain soluja materiaalin lisäksi, ja poistaa vaurioituneen kudoksen, laittaa biohajoavan materiaalin tilalle? Tässä näette palan sydänlihasta sykkimässä maljalla. Tämän on tehnyt Teruo Okano Tokion naisten sairaalassa. Hän kasvattaa sykkivää kudosta maljalla. Hän viilentää maljaa, se muuttaa ominaisuuksiaan ja hän kuorii sen maljalta. Siistiä.
Now I'm going to show you cell-based regeneration. And what I'm going to show you here is stem cells being removed from the hip of a patient. Again, if you're squeamish, you don't want to watch. But this one's kind of cool. So this is a bypass operation, just like what Al Gore had, with a difference. In this case, at the end of the bypass operation, you're going to see the stem cells from the patient that were removed at the beginning of the procedure being injected directly into the heart of the patient. And I'm standing up here because at one point I'm going to show you just how early this technology is. Here go the stem cells, right into the beating heart of the patient. And if you look really carefully, it's going to be right around this point you'll actually see a back-flush. You see the cells coming back out. We need all sorts of new technology, new devices, to get the cells to the right place at the right time.
Nyt näytän solupohjaisen regeneraation. Seuraavassa kantasoluja otetaan potilaan lonkasta. Taas, heikkohermoiset älkööt katsoko. Tosin tämä on aika siistiä. Tämä on ohitusleikkaus, samanlainen kuin Al Goren, mutta erilainen. Tässä tapauksessa leikkauksen lopussa näette kuinka kantasolut, jotka otettiin talteen operaation alussa, ruiskutetaan suoraan potilaan sydämeen. Yhdessä kohdassa näytän teille miten alkutekijöissään tämä teknologia vielä on. Tässä kantasolut menevät suoraan potilaan sykkivään sydämeen. Katsokaa tarkasti, suunnilleen näillä kohdin, näette takaisinvirtauksen. Solut tulevat takaisin ulos. Tarvitsemme uutta teknologiaa, laitteita, saadaksemme solut oikeaan paikkaan ajallaan.
Just a little bit of data, a tiny bit of data. This was a randomized trial. At this time this was an N of 20. Now there's an N of about 100. Basically, if you take an extremely sick patient and you give them a bypass, they get a little bit better. If you give them stem cells as well as their bypass, for these particular patients, they became asymptomatic. These are now two years out. The coolest thing would be is if you could diagnose the disease early, and prevent the onset of the disease to a bad state.
Hitusen dataa. Tämä oli satunnaiskoe. Tuolloin N oli 20. Nykyään N on noin 100. Erittäin sairas potilas, saatuaan ohitusleikkauksen, paranee vähän. Jos heille annetaan kantasoluja leikkauksen lisäksi, nämä kyseiset potilaat, heidän oireensa katosivat. Tämä oli kaksi vuotta sitten. Siisteintä olisi, jos sairauden voisi diagnosoida aikaisin, ja estää sairauden pahentuminen.
This is the same procedure, but now done minimally invasively, with only three holes in the body where they're taking the heart and simply injecting stem cells through a laparoscopic procedure. There go the cells. We don't have time to go into all of those details, but basically, that works too. You can take patients who are less sick, and bring them back to an almost asymptomatic state through that kind of therapy.
Sama operaatio minimi-invasiivisena, vain kolmen kehoon tehdyn reiän avulla he ottavat sydämen, ja injektoivat kantasolut käyttämällä vatsaontelotähystintä. Siinä menevät solut. Emme ehdi katsoa kaikkia yksityiskohtia, mutta tämä toimii. Vähemmän sairaat potilaat voidaan saada takaisin lähes oireettomaan tilaan tämän kaltaisella hoidolla.
Here's another example of stem-cell therapy that isn't quite clinical yet, but I think very soon will be. This is the work of Kacey Marra from Pittsburgh, along with a number of colleagues around the world. They've decided that liposuction fluid, which -- in the United States, we have a lot of liposuction fluid. (Laughter) It's a great source of stem cells. Stem cells are packed in that liposuction fluid. So you could go in, you could get your tummy-tuck. Out comes the liposuction fluid, and in this case, the stem cells are isolated and turned into neurons. All done in the lab. And I think fairly soon, you will see patients being treated with their own fat-derived, or adipose-derived, stem cells.
Tässä toinen esimerkki kantasoluterapiasta, joka ei ole vielä kliininen, mutta tulee pian olemaan. Tämän on tehnyt Kacey Marra Pittsburghista eri puolilta maailmaa olevien kollegoiden kanssa. He päättivät, että rasvaimuneste, jota -- Yhdysvalloissa meillä on paljon rasvaimunestettä. (Naurua) Se on loistava kantasolujen lähde. Kantasoluja on rasvaimunesteessä paljon. Joten kun menee teettämään vatsan muotoilun ulos tulee rasvaimunestettä, ja tässä tapauksessa kantasolut ovat erotettu ja muutettu neuroneiksi. Laboratoriossa. Uskon, että melko pian tulette näkemään potilaita hoidettavan heidän omasta ihrastaan erotetuilla kantasoluilla.
I talked before about the use of devices to dramatically change the way we treat disease. Here's just one example before I close up. This is equally tragic. We have a very abiding and heartbreaking partnership with our colleagues at the Institute for Surgical Research in the US Army, who have to treat the now 11,000 kids that have come back from Iraq. Many of those patients are very severely burned.
Puhuin aiemmin laitteiden käyttämisestä hoitojen muuttamiseksi dramaattisesti. Tässä yksi esimerkki ennen kuin lopetan. Tämäkin on traaginen. Meillä on pitkäkestoinen ja sydäntäsärkevä yhteistyö Yhdysvaltain armeijan Kirurgisen tutkimuksen instituutin kanssa. He hoitavat 11 000 poikaamme, jotka ovat tulleet takaisin Irakista. Useat potilaista ovat pahoin palaneita.
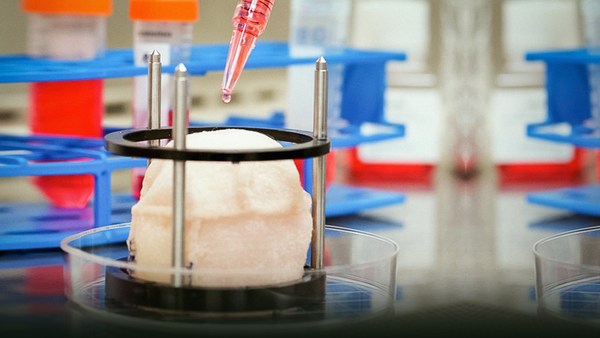
And if there's anything that's been learned about burn, it's that we don't know how to treat it. Everything that is done to treat burn -- basically we do a sodding approach. We make something over here, and then we transplant it onto the site of the wound, and we try and get the two to take. In this case here, a new, wearable bio-reactor has been designed -- it should be tested clinically later this year at ISR -- by Joerg Gerlach in Pittsburgh. And that bio-reactor will lay down in the wound bed. The gun that you see there sprays cells. That's going to spray cells over that area. The reactor will serve to fertilize the environment, deliver other things as well at the same time, and therefore we will seed that lawn, as opposed to try the sodding approach. It's a completely different way of doing it.
Ja jos olemme jotain oppineet palovammoista, niin sen, ettemme tiedä miten niitä tulee hoitaa. Hoidamme palovammoja siirteitä käyttämällä. Teemme jotain toisaalla, ja istutamme sen vamman alueelle, ja yritämme saada ne hyväksymään toisensa. Uusi puettava bioreaktori on suunniteltu -- sitä testataan kliinisesti myöhemmin tänä vuonna ISR:ssä -- Joerg Gerlachin toimesta Pittsburghissa. Bioreaktori asennetaan loukkaantuneen sängylle. Näkemänne pistooli suihkuttaa soluja. Se suihkuttaa soluja tuon alueen ylle. Reaktori lannoittaa ympäristön, ja tekee muutakin, ja siten me istutamme nurmikon, emmekä yritä kasvattaa sitä siirteillä. Se on täysin uudenlainen menetelmä.
So my 18 minutes is up. So let me finish up with some good news, and maybe a little bit of bad news. The good news is that this is happening today. It's very powerful work. Clearly the images kind of get that across. It's incredibly difficult because it's highly inter-disciplinary. Almost every field of science engineering and clinical practice is involved in trying to get this to happen.
Olen käyttänyt 18 minuuttiani. Haluan lopettaa hyvillä uutisilla, ja ehkä vähän huonoillakin. Hyvä uutinen on, että tämä kaikki tapahtuu nyt. Se on mahtava työ. Kuvat kertovat sen aika hyvin. Se on hyvin vaikeaa, koska se vaatii yhteistyötä monilta tieteenaloilta. Melkein kaikki tekniikan ja kliinisen työn alat ovat tässä mukana.
A number of governments, and a number of regions, have recognized that this is a new way to treat disease. The Japanese government were perhaps the first, when they decided to invest first 3 billion, later another 2 billion in this field. It's no coincidence. Japan is the oldest country on earth in terms of its average age. They need this to work or their health system dies. So they're putting a lot of strategic investment focused in this area. The European Union, same thing. China, the same thing. China just launched a national tissue-engineering center. The first year budget was 250 million US dollars.
Useat valtiot ja alueet ovat löytäneet tämän uuden tavan hoitaa. Japanin hallitus oli ehkä ensimmäinen, kun he päättivät investoida 3 miljardia, ja myöhemmin 2 miljardia lisää tähän alaan. Se ei ole sattumaa. Japanilaisten keskimääräinen ikä on vanhin maailmassa. He tarvitsevat tätä tai heidän terveydenhuoltojärjestelmänsä hajoaa. Joten he ovat strategisesti keskittäneet rahaa tälle alalle. Euroopan unionissa, sama juttu. Kiina, sama juttu. Kiina käynnisti juuri kansallisen kudostekniikan keskuksen. Ensimmäisen vuoden budjetti oli 250 miljoonaa dollaria.
In the United States we've had a somewhat different approach. (Laughter) Oh, for Al Gore to come and be in the real world as president. We've had a different approach. And the approach has basically been to just sort of fund things as they come along. But there's been no strategic investment to bring all of the necessary things to bear and focus them in a careful way.
Meillä Yhdysvalloissa on vähän erilainen lähestymistapa. Me -- (Naurua) -- olisipa Al Gore oikeasti presidentti. Meillä on ollut erillainen lähestymistapa. Meillä rahoitus tulee sitä mukaa, kun asioita ilmenee. Mutta strategisia investointeja ei ole tehty, jolloin olisi voitu keskittyä tiettyihin aiheisiin huolellisesti.
And I'm going to finish up with a quote, maybe a little cheap shot, at the director of the NIH, who's a very charming man. Myself and Jay Vacanti from Harvard went to visit with him and a number of his directors of his institute just a few months ago, to try and convince him that it was time to take just a little piece of that 27.5 billion dollars that he's going to get next year and focus it, in a strategic way, to make sure we can accelerate the pace at which these things get to patients. And at the end of a very testy meeting, what the NIH director said was, "Your vision is larger than our appetite." I'd like to close by saying that no one's going to change our vision, but together we can change his appetite. Thank you.
Aion lopettaa ehkä vähän epäreiluun lainaukseen NIH:n johtajalta, joka on erittäin miellyttävä mies. Minä ja Jay Vacanti Harvardista menimme tapaamaan häntä ja muita hänen instituuttinsa johtajia vain muutama kuukausi sitten, yritimme taivuttaa hänet antamaan vain vähän 27,5 miljardista dollarista, jotka hän saa ensi vuonna, ja keskittämään sen strategisesti, jotta nopeuttaisimme näiden keksintöjen päätymistä potilaille. Koettelevan tapaamisen päätteeksi NIH:n johtaja sanoi: "Teidän visionne on isompi kuin meidän ruokahalumme." Kukaan ei voi muuttaa meidän visiotamme, mutta yhdessä voimme muuttaa hänen ruokahaluaan. Kiitos.