Σήμερα θα σας μιλήσω για την προσδοκία της μετατροπής του φόβου σε ελπίδα. Όταν πηγαίνουμε στο γιατρό σήμερα, όταν μπαίνουμε στο γραφείο του γιατρού και καθόμαστε, υπάρχουν λέξεις που δεν θέλουμε να ακούσουμε. Υπάρχουν λέξεις που πραγματικά φοβόμαστε. Διαβήτης, καρκίνος, Πάρκινσον, Αλτσχάιμερ, καρδιακή ανεπάρκεια, πνευμονική ανεπάρκεια Ασθένειες που ξέρουμε ότι είναι εξουθενωτικές για το σώμα και για της οποίες υπάρχουν σχετικά λίγα πράγματα που μπορούμε να κάνουμε.
I'm going to talk to you today about hopefully converting fear into hope. When we go to the physician today -- when we go to the doctor's office and we walk in, there are words that we just don't want to hear. There are words that we're truly afraid of. Diabetes, cancer, Parkinson's, Alzheimer's, heart failure, lung failure -- things that we know are debilitating diseases, for which there's relatively little that can be done.
Και αυτό που θα ήθελα να σας παρουσιάσω σήμερα είναι ένας διαφορετικός τρόπος σκέψης για να αντιμετωπίσουμε αυτές τις εξουθενωτικές ασθένειες, και γιατί είναι σημαντικός. Γιατί χωρίς αυτόν, πιθανότατα, το σύστημα υγείας θα καταρρεύσει, εάν δεν πιστεύετε ότι έχει ήδη καταρρεύσει. Και που βρισκόμαστε κλινικά σήμερα, και που ίσως να βρισκόμαστε αύριο, και ποια είναι κάποια από τα εμπόδια. Και θα τα κάνουμε όλα αυτά σε 18 λεπτά, το υπόσχομαι.
And what I want to lay out for you today is a different way of thinking about how to treat debilitating disease, why it's important, why without it perhaps our health care system will melt down if you think it already hasn't, and where we are clinically today, and where we might go tomorrow, and what some of the hurdles are. And we're going to do all of that in 18 minutes, I promise.
Θέλω να αρχίσω με αυτή την διαφάνεια, διότι δείχνει την ιστορία με τον τρόπο που τη βλέπει το περιοδικό "Science" (Σάιενς). Αυτό είναι ένα τεύχος από το 2002 που εκδόθηκε με πολλά διαφορετικά άρθρα για τον βιονικό άνθρωπο. Ήταν βασικά ένα τεύχος για την αναγεννητική ιατρική. Η αναγεννητική ιατρική είναι μια εξαιρετικά απλή έννοια που όλοι μπορούν να καταλάβουν. Είναι πολύ απλά, η επιτάχυνση του ρυθμού με τον όποιο το σώμα μας αυτοθεραπεύεται ώστε να έχει κλινική εφαρμογή Ξέρουμε πως να το επιτύχουμε αυτό με πολλούς από τους τρόπους που βλέπετε εκεί πάνω. Ξέρουμε ότι αν έχετε ένα κατεστραμμένο γοφό, μπορούμε να βάλουμε ένα τεχνητό γοφό. Και αυτή είναι η ιδέα που χρησιμοποίησε το περιοδικό "Science" για εξώφυλλο.
I want to start with this slide, because this slide sort of tells the story the way Science Magazine thinks of it. This was an issue from 2002 that they published with a lot of different articles on the bionic human. It was basically a regenerative medicine issue. Regenerative medicine is an extraordinarily simple concept that everybody can understand. It's simply accelerating the pace at which the body heals itself to a clinically relevant timescale. So we know how to do this in many of the ways that are up there. We know that if we have a damaged hip, you can put an artificial hip in. And this is the idea that Science Magazine used on their front cover.
Και αυτό είναι το ακριβώς αντίθετο από την αναγεννητική ιατρική. Αυτό δεν είναι αναγεννητική ιατρική. Αναγεννητική ιατρική είναι αυτό που έδειξε το περιοδικό "Business Week" όταν έκαναν ένα άρθρο για την αναγεννητική ιατρική πριν λίγο καιρό. Η λογική είναι ότι αντί να προσπαθούμε να βελτιώσουμε τα συμπτώματα με συσκευές, φάρμακα και λοιπά -- και θα ξαναμιλήσω για αυτό το θέμα αρκετές φόρες -- αντί λοιπόν να προσπαθούμε αυτό, θα αναγεννήσουμε τη χαμένη λειτουργία του σώματος αναγεννώντας τη λειτουργία των οργάνων και του κατεστραμμένου ιστού. Έτσι ώστε στο τέλος της θεραπείας, να είσαι ακριβώς ο ίδιος που ήσουν και στην αρχή της θεραπείας.
This is the complete antithesis of regenerative medicine. This is not regenerative medicine. Regenerative medicine is what Business Week put up when they did a story about regenerative medicine not too long ago. The idea is that instead of figuring out how to ameliorate symptoms with devices and drugs and the like -- and I'll come back to that theme a few times -- instead of doing that, we will regenerate lost function of the body by regenerating the function of organs and damaged tissue. So that at the end of the treatment, you are the same as you were at the beginning of the treatment.
Πολύ λίγες καλές ιδέες -- αν συμφωνείτε ότι αυτή είναι καλή ιδέα -- πολύ λίγες καλές ιδέες είναι πραγματικά καινοτόμες. Όπως και σ' αυτή την περίπτωση. Αν κοιτάξουμε στην ιστορία, ο Τσαρλς Λίντμπεργκ -- που είναι πιο γνωστός ως πιλότος -- ήταν ένας από του πρώτους ανθρώπους, μαζί με τον Αλέξις Καρελ, έναν δαφνοστεφανωμένο νομπελίστα από το ινστιτούτο Ροκφελερ, οι όποιοι άρχισαν να σκέφτονται, πως θα μπορούσαμε να καλλιεργήσουμε όργανα; Εξέδωσαν ένα βιβλίο το 1937, όπου όντως άρχισαν να σκέφτονται, πώς θα μπορούσαμε να μεγαλώσουμε ολόκληρα όργανα σε βίο-αντιδραστήρες Έχουμε προχωρήσει πολύ από τότε. Θα μοιραστώ μαζί σας κάποια από την συναρπαστική δουλεία που συντελείται.
Very few good ideas -- if you agree that this is a good idea -- very few good ideas are truly novel. And this is just the same. If you look back in history, Charles Lindbergh, who was better known for flying airplanes, was actually one of the first people along with Alexis Carrel, one of the Nobel Laureates from Rockefeller, to begin to think about, could you culture organs? And they published this book in 1937, where they actually began to think about, what could you do in bio-reactors to grow whole organs? We've come a long way since then. I'm going to share with you some of the exciting work that's going on.
Πριν πάμε σε αυτό, αυτό που θα ήθελα είναι να μοιραστώ την θλίψη μου για το σύστημα υγείας και το λόγο αυτής της θλίψης. Πολλές ομιλίες χθες, μιλούσαν για τη βελτίωση της ποιότητας της ζωής και μείωση της ανέχειας. Και ουσιαστικά την αύξηση της διάρκειας ζωής σε όλη τη γη. Μια από τις προκλήσεις είναι ότι όσο πιο πλούσιοι είμαστε, τόσο περισσότερο ζούμε. Όσο περισσότερο ζούμε, τόσο πιο ακριβό είναι να φροντίσουμε τις ασθένειές μας όσο γερνάμε.
But before doing that, what I'd like to do is share my depression about the health care system and the need for this with you. Many of the talks yesterday talked about improving the quality of life, and reducing poverty, and essentially increasing life expectancy all around the globe. One of the challenges is that the richer we are, the longer we live. And the longer we live, the more expensive it is to take care of our diseases as we get older.
Αυτό είναι απλά ο πλούτος μιας χώρας συναρτήσει του ποσοστού το πληθυσμού πάνω από 65 Και βασικά βλέπεις ότι όσο πιο πλούσια είναι μια χώρα, τόσο πιο ηλικιωμένοι είναι οι άνθρωποι σε αυτή. Γιατί είναι τόσο σημαντικό αυτό; Και γιατί είναι τόσο δραματική πρόκληση σήμερα; Αν η μέση ηλικία του πληθυσμού σου είναι 30, η μέση ασθένεια που θα πρέπει να φροντίσεις είναι ίσως ένας σπασμένος αστράγαλος πότε-πότε, ίσως και λίγο άσθμα. Αν η μέση ηλικία του πληθυσμού της χώρας σου είναι 45 με 55, τώρα ο μέσος πολίτης πρέπει αντιμετωπίσει διαβήτη, νεανικό διαβήτη, καρδιακή ανεπάρκεια, στεφανιαία νόσο. Πράγματα που είναι από τη φύση τους, πιο δύσκολα και πολύ πιο ακριβά να θεραπευτούν.
This is simply the wealth of a country versus the percent of population over the age of 65. And you can basically see that the richer a country is, the older the people are within it. Why is this important? And why is this a particularly dramatic challenge right now? If the average age of your population is 30, then the average kind of disease that you have to treat is maybe a broken ankle every now and again, maybe a little bit of asthma. If the average age in your country is 45 to 55, now the average person is looking at diabetes, early-onset diabetes, heart failure, coronary artery disease -- things that are inherently more difficult to treat, and much more expensive to treat.
Δείτε τα δημογραφικά εδώ στις Η.Π.Α. και αυτό είναι από το "Οι Διαιρεμένες Πολιτείες Αμερικής" (The Untied States of America) Το 1930, υπήρχαν 41 εργαζόμενοι για κάθε συνταξιούχο 41 εργαζόμενοι οι όποιοι ήταν βασικά εκτός οποιασδήποτε σοβαρής ασθένειας και πλήρωναν για ένα συνταξιούχο ο οποίος είχε κάποια εξουθενωτική ασθένεια Το 2010, δυο εργαζόμενοι για κάθε συνταξιούχο στις Η.Π.Α. Και αντίστοιχα στοιχεία έχει κάθε βιομηχανική, πλούσια χώρα στον κόσμο. Πως να αντέξεις το οικονομικό βάρος της θεραπείας, όταν αυτή είναι η πραγματικότητα του γήρατος;
Just have a look at the demographics in the U.S. here. This is from "The Untied States of America." In 1930, there were 41 workers per retiree. 41 people who were basically outside of being really sick, paying for the one retiree who was experiencing debilitating disease. In 2010, two workers per retiree in the U.S. And this is matched in every industrialized, wealthy country in the world. How can you actually afford to treat patients when the reality of getting old looks like this?
Γήρας εναντίον κόστους υγειονομικής περίθαλψης. Και μπορείτε να δείτε ότι στις ηλικίες μεταξύ 45, 40 με 45, υπάρχει μια οξεία άνοδος στο κόστος της υγειονομικής περίθαλψης. Είναι πραγματικά αρκετά ενδιαφέρον -- αν κάνεις τις κατάλληλες μελέτες, μπορείς να κάνεις ένα σχεδιάγραμμα για να εξετάσεις πόσο ξοδεύεις ως άτομο στην υγειονομική περίθαλψή σου, κατά τη διάρκεια της ζωής σου. Και περίπου στα επτά χρόνια πριν το θάνατο, υπάρχει μια οξεία αύξηση. Και βασικά μπορείς -- (Γέλια) -- άσε ας μην το πάμε εκεί. (Γέλια)
This is age versus cost of health care. And you can see that right around age 45, 40 to 45, there's a sudden spike in the cost of health care. It's actually quite interesting. If you do the right studies, you can look at how much you as an individual spend on your own health care, plotted over your lifetime. And about seven years before you're about to die, there's a spike. And you can actually -- (Laughter) -- we won't get into that. (Laughter)
Υπάρχουν πολύ λίγα πράγματα, πολύ λίγα πράγματα να κάνεις που θα αλλάξουν τον τρόπο να θεραπεύσεις τέτοιες ασθένειες και να βιώσεις αυτό που θα αποκαλούσα υγιή γήρανση. Πιστεύω πως υπάρχουν τέσσερα πράγματα Και κανένα δεν περιλαμβάνει το ασφαλιστικό ή το νομικό σύστημα. Αυτά το μόνο που κάνουν είναι να αλλάζουν το ποιος πληρώνει. Στην πραγματικότητα δεν αλλάζουν το κόστος της θεραπείας.
There are very few things, very few things that you can really do that will change the way that you can treat these kinds of diseases and experience what I would call healthy aging. I'd suggest there are four things, and none of these things include an insurance system or a legal system. All those things do is change who pays. They don't actually change what the actual cost of the treatment is.
Ένα πράγμα που μπορείς να κάνεις είναι να μην κάνεις θεραπεία. Να βάλεις δελτίο στην περίθαλψη. Δεν θα το συζητήσουμε άλλο. Είναι πολύ καταθλιπτικό Μπορείς να προλαμβάνεις. Και σίγουρα πολλά χρήματα πρέπει να διατεθούν για την πρόληψη.
One thing you can do is not treat. You can ration health care. We won't talk about that anymore. It's too depressing. You can prevent. Obviously a lot of monies should be put into prevention.
Αλλά ίσως πιο ενδιαφέρον, για εμένα τουλάχιστον, και το πιο σημαντικό, είναι η ιδέα της διάγνωσης της ασθένειας πολύ νωρίτερα στην πορεία της, και μετά η αγωγή με σκοπό τη θεραπεία της ασθένειας και όχι του συμπτώματος. Σκεφτείτε το σε σχέση με το διαβήτη, για παράδειγμα. Σήμερα, τι κάνουμε με το διαβήτη; Διαγνώσκουμε την ασθένεια τελικά, μόνο όταν αρχίζει και έχει συμπτώματα και μετά θεραπεύουμε τα συμπτώματα για 10, 20, 30, 40 χρόνια. Και τα πάμε καλά. Η ινσουλίνη είναι καλή θεραπεία. Τελικά όμως σταματά να δουλεύει, και ο διαβήτης οδηγεί στην προβλέψιμη έναρξη εξουθενωτικής ασθένειας.
But perhaps most interesting, to me anyway, and most important, is the idea of diagnosing a disease much earlier on in the progression, and then treating the disease to cure the disease instead of treating a symptom. Think of it in terms of diabetes, for instance. Today, with diabetes, what do we do? We diagnose the disease eventually, once it becomes symptomatic, and then we treat the symptom for 10, 20, 30, 40 years. And we do OK. Insulin's a pretty good therapy. But eventually it stops working, and diabetes leads to a predictable onset of debilitating disease.
Γιατί να μην μπορούμε να κάνουμε μια ένεση στο πάγκρεας με κάτι για να αναγεννηθεί το πάγκρεας νωρίς στην πορεία της ασθένειας. ίσως πριν καν αρχίσουν τα συμπτώματα; Και ίσως να είναι λίγο ακριβό την ώρα που θα το κάναμε, αλλά αν δούλευε, θα μπορούσαμε πραγματικά να είμαστε σε θέση να κάνουμε διαφορά.
Why couldn't we just inject the pancreas with something to regenerate the pancreas early on in the disease, perhaps even before it was symptomatic? And it might be a little bit expensive at the time that we did it, but if it worked, we would truly be able to do something different.
Αυτό το βίντεο, πιστεύω, δείχνει το νόημα αυτού που λέω αρκετά εντυπωσιακά. Εδώ είναι μια σαλαμάνδρα, που ξανά-φυτρώνει το άκρο της. Αν μια σαλαμάνδρα μπορεί να κάνει κάτι τέτοιο, γιατί όχι και εμείς; Θα σας δείξω μερικά από τα πιο σημαντικά χαρακτηριστικά για την αναγέννηση άκρων σε λίγο. Αλλά για αυτό που μιλάμε στην αναγεννητική ιατρική είναι να γίνεται αυτό σε κάθε σύστημα οργάνων του σώματος, για ιστούς και για τα ίδια τα όργανα. Έτσι, η σημερινή πραγματικότητα είναι ότι όταν αρρωστήσεις, το μήνυμα είναι ότι θα αντιμετωπίσουμε τα συμπτώματά σου, και εσύ θα πρέπει να προσαρμοστείς σε ένα νέο τρόπο ζωής.
This video, I think, gets across the concept that I'm talking about quite dramatically. This is a newt re-growing its limb. If a newt can do this kind of thing, why can't we? I'll actually show you some more important features about limb regeneration in a moment. But what we're talking about in regenerative medicine is doing this in every organ system of the body, for tissues and for organs themselves. So today's reality is that if we get sick, the message is we will treat your symptoms, and you need to adjust to a new way of life.
Θα ήθελα να σας θέσω ότι αύριο -- και πότε είναι αυτό το αύριο είναι συζητήσιμο αλλά είναι στο ορατό μέλλον -- θα μιλήσουμε για την αναγεννητική αποκατάσταση. Υπάρχει ένα προσθετικό άκρο εδώ, παρόμοιο με εκείνο του στρατιώτη που επέστρεψε από το Ιράκ ... υπάρχουν 370 στρατιώτες που έχουν επιστρέψει από το Ιράκ και χάσει άκρα. Φανταστείτε αν αντί να έχουν να αντιμετωπίσουν αυτό, θα μπορούσαν να έχουν να αντιμετωπίσουν την αναγέννηση αυτού του άκρου. Είναι τρελή σύλληψη. Θα σου δείξω πού βρισκόμαστε αυτή τη στιγμή στον αγώνα μας προς τα εκεί.
I would pose to you that tomorrow -- and when tomorrow is we could debate, but it's within the foreseeable future -- we will talk about regenerative rehabilitation. There's a limb prosthetic up here, similar actually one on the soldier that's come back from Iraq. There are 370 soldiers that have come back from Iraq that have lost limbs. Imagine if instead of facing that, they could actually face the regeneration of that limb. It's a wild concept. I'll show you where we are at the moment in working towards that concept.
Και μπορεί να εφαρμοστεί, όπως είπα, σε κάθε σύστημα οργάνων. Πώς το κάνουμε αυτό; Ο τρόπος για να γίνει είναι να αναπτυχθεί μια συνομιλία με το σώμα. Πρέπει να μάθουμε να μιλάμε τη γλώσσα του σώματος. Και να ενεργοποιήσουμε τις διαδικασίες που ξέραμε πώς να το κάνουμε όταν ήμασταν έμβρυο. Ένα έμβρυο θηλαστικού, όταν χάνει ένα άκρο κατά τη διάρκεια του πρώτου τριμήνου της εγκυμοσύνης, το άκρο θα ξαναφυτρώσει Οπότε, το DNA μας έχει την ήδη την ικανότητα αυτών των μηχανισμών επούλωσης. Είναι μια φυσική διαδικασία, αλλά χάνεται καθώς μεγαλώνουμε. Ένα παιδί, πριν από την ηλικία των έξι περίπου μηνών, εάν χάσει την άκρη του δακτύλου του σε ατύχημα, θα ξαναφυτρώσει η άκρη του δακτύλου. Όταν γίνουν πέντε χρονών, δεν είναι πλέον σε θέση να το κάνουν αυτό.
But it's applicable, again, to every organ system. How can we do that? The way to do that is to develop a conversation with the body. We need to learn to speak the body's language. And to switch on processes that we knew how to do when we were a fetus. A mammalian fetus, if it loses a limb during the first trimester of pregnancy, will re-grow that limb. So our DNA has the capacity to do these kinds of wound-healing mechanisms. It's a natural process, but it is lost as we age. In a child, before the age of about six months, if they lose their fingertip in an accident, they'll re-grow their fingertip. By the time they're five, they won't be able to do that anymore.
Έτσι για να συμμετάσχουμε στην εν λόγω συνομιλία με το σώμα, θα πρέπει να μιλάμε τη γλώσσα του σώματος. Και υπάρχουν ορισμένα εργαλεία στην εργαλειοθήκη μας που μας επιτρέπουν να κάνουμε αυτό σήμερα. Θα σας δώσω τρία παράδειγμα αυτών των εργαλείων μέσω των οποίων συνομιλούμε με το σώμα.
So to engage in that conversation with the body, we need to speak the body's language. And there are certain tools in our toolbox that allow us to do this today. I'm going to give you an example of three of these tools through which to converse with the body.
Το πρώτο είναι η κυτταρική θεραπεία. Είναι σαφές ότι, το σώμα μας επουλώνεται με φυσική διαδικασία, και χρησιμοποιούμε κύτταρα για να κάνουν την περισσότερη δουλειά. Άρα, αν μπορούμε να βρούμε τα σωστά κύτταρα και τα εμφυτεύσουμε στο σώμα, μπορούν να κάνουν τη θεραπεία. Δεύτερον, μπορούμε να χρησιμοποιήσουμε υλικά. Ακούσαμε χθες σχετικά με τη σημασία των νέων υλικών. Αν μπορούμε να εφεύρουμε υλικά, να σχεδιάσουμε υλικά, ή να εξάγουμε υλικά από ένα φυσικό περιβάλλον, τότε ίσως μπορούμε να βάλουμε αυτά τα υλικά να ωθήσουν το σώμα να επουλωθεί μόνο του. Και τέλος, μπορεί να είμαστε σε θέση να χρησιμοποιήσουμε έξυπνες συσκευές που θα απαλλάξουν από το έργο του το σώμα και θα του επιτρέψουν να επουλωθεί
The first is cellular therapies. Clearly, we heal ourselves in a natural process, using cells to do most of the work. Therefore, if we can find the right cells and implant them in the body, they may do the healing. Secondly, we can use materials. We heard yesterday about the importance of new materials. If we can invent materials, design materials, or extract materials from a natural environment, then we might be able to have those materials induce the body to heal itself. And finally, we may be able to use smart devices that will offload the work of the body and allow it to heal.
Θα σας δείξω ένα παράδειγμα για κάθε ένα από αυτά, και θα ξεκινήσω με τα υλικά. Ο Στιβ Μπαντιλακ- που είναι στο Πανεπιστήμιο του Πίτσμπουργκ -- πριν από περίπου μια δεκαετία πριν είχε μια εξαιρετική ιδέα. Και η ιδέα ήταν ότι το λεπτό έντερο του χοίρου, εάν πετάξεις όλα τα κύτταρα, και αν το έκανες αυτό με τρόπο που του επέτρεπε να παραμείνει βιολογικά ενεργό, μπορεί να περιέχει όλα τα απαραίτητα στοιχεία και τα σήματα που θα σηματοδοτήσουν την αρχή της επούλωσής του. Και έκανε μια πολύ σημαντική ερώτηση. Ρώτησε, αν πάρω αυτό το υλικό, το οποίο είναι ένα φυσικό υλικό που συνήθως ωθεί την επούλωση στο λεπτό έντερο, και το βάλω σε ένα άλλο μέρος στο σώμα ενός ανθρώπου, θα δώσει συγκεκριμένη ιστολογική αντίδραση, ή θα φτιάξει λεπτό έντερο αν προσπάθησα να φτιάξω καινούριο αυτί;
I'm going to show you an example of each of these, and I'm going to start with materials. Steve Badylak -- who's at the University of Pittsburgh -- about a decade ago had a remarkable idea. And that idea was that the small intestine of a pig, if you threw away all the cells, and if you did that in a way that allowed it to remain biologically active, may contain all of the necessary factors and signals that would signal the body to heal itself. And he asked a very important question. He asked the question, if I take that material, which is a natural material that usually induces healing in the small intestine, and I place it somewhere else on a person's body, would it give a tissue-specific response, or would it make small intestine if I tried to make a new ear?
Δεν θα σας έλεγα αυτή την ιστορία αν δεν ήταν πειστική. Η εικόνα που είμαι έτοιμος να σας παρουσιάσω -- (Γέλια) -- είναι μια συναρπαστική εικόνα. Ωστόσο, όσοι από εσάς είναι αηδιάζετε εύκολα -- ακόμα και αν δεν το παραδέχεστε στους φίλους σας -- τα φώτα είναι σβηστά. Είναι μια καλή στιγμή για να κοιτάξετε τα πόδια σας, να ελέγξετε το κινητό σας, να κάνετε οτιδήποτε άλλο από το να κοιτάτε την οθόνη. (Γέλια)
I wouldn't be telling you this story if it weren't compelling. The picture I'm about to show you is a compelling picture. (Laughter) However, for those of you that are even the slightest bit squeamish -- even though you may not like to admit it in front of your friends -- the lights are down. This is a good time to look at your feet, check your Blackberry, do anything other than look at the screen. (Laughter)
Αυτό που θα σας δείξω είναι ένα διαβητικό έλκος. Και παρόλο -- είναι καλό να γελάμε πριν το δούμε αυτό. Αυτή είναι η πραγματικότητα του διαβήτη. Νομίζω ότι πολλές φορές ακούμε για διαβητικούς, διαβητικά έλκη, και απλά δεν συνδέουμε το έλκος με την τελική θεραπεία, που είναι ο ακρωτηριασμός, αν δεν μπορεί να επουλωθεί. Γι 'αυτό θα δείξω τη διαφάνεια τώρα. Όχι για πολύ. Αυτό είναι ένα διαβητικό έλκος. Είναι τραγικό. Η θεραπεία για αυτό είναι ο ακρωτηριασμός. Είναι μια μεγαλύτερη κυρία. Έχει καρκίνο του ήπατος, καθώς και διαβήτη, και αποφάσισε να πεθάνει με ότι έχει απομείνει από το σώμα της ανέπαφο.
What I'm about to show you is a diabetic ulcer. And although -- it's good to laugh before we look at this. This is the reality of diabetes. I think a lot of times we hear about diabetics, diabetic ulcers, we just don't connect the ulcer with the eventual treatment, which is amputation, if you can't heal it. So I'm going to put the slide up now. It won't be up for long. This is a diabetic ulcer. It's tragic. The treatment for this is amputation. This is an older lady. She has cancer of the liver as well as diabetes, and has decided to die with what' s left of her body intact.
Και αυτή η κυρία αποφάσισε, μετά από ένα χρόνο θεραπείας αυτού του έλκους, ότι θα δοκιμάσει αυτή τη νέα θεραπεία που επινόησε ο Στιβ. Έτσι έγινε το τραύμα 11 εβδομάδες αργότερα. Το υλικό αυτό περιλάμβανε μόνο τα φυσικά σήματα. Και αυτό το υλικό προκάλεσε το σώμα να επιστρέψει σε μια επουλωτική στάση την οποία δεν είχε πριν.
And this lady decided, after a year of attempted treatment of that ulcer, that she would try this new therapy that Steve invented. That's what the wound looked like 11 weeks later. That material contained only natural signals. And that material induced the body to switch back on a healing response that it didn't have before.
Τώρα θα έχουμε κάνα-δυό ακόμα οδυνηρές διαφάνειες για όσους από εσάς -- Θα σας πω όταν μπορείτε να ξανακοιτάξετε. Αυτό είναι ένα άλογο. Το άλογο αυτό δεν πονάει. Αν το άλογο πονούσε, δεν θα σας έδειχνα αυτή τη διαφάνεια. Το άλογο έχει απλώς ένα τρίτο ρουθούνι, που ανέπτυξε εξαιτίας ενός ατυχήματος. Μόλις λίγες εβδομάδες μετά τη θεραπεία -- σε αυτήν την περίπτωση, πήραμε το υλικό, το μετατρέψαμε σε ζελέ, και γεμίσαμε την περιοχή, και επαναλάβαμε τη θεραπεία αρκετές φορές -- και το άλογο θεραπεύτηκε. Και αν κάναμε υπερηχογράφημα στην περιοχή, θα ήταν μια χαρά.
There's going to be a couple more distressing slides for those of you -- I'll let you know when you can look again. This is a horse. The horse is not in pain. If the horse was in pain, I wouldn't show you this slide. The horse just has another nostril that's developed because of a riding accident. Just a few weeks after treatment -- in this case, taking that material, turning it into a gel, and packing that area, and then repeating the treatment a few times -- and the horse heals up. And if you took an ultrasound of that area, it would look great.
Εδώ είναι ένα δελφίνι που επανασύνδεσαν το πτερύγιο του. Υπάρχουν 400.000 οι ασθενείς σε όλο τον κόσμο που έχουν χρησιμοποιήσει αυτό υλικό για να επουλωθούν τις πληγές τους. Θα μπορούσαμε να αναγεννήσουμε ένα άκρο; Ο Οργανισμός Ανώτερων Ερευνητικών Αμυντικών Έργων (DARPA) μόλις έδωσε στον Στιβ 15 εκατ. δολάρια για να επιβλέπει το έργο οκτώ ινστιτούτων να ξεκινήσει τη διαδικασία αυτής ακριβώς της ερώτησης.
Here's a dolphin where the fin's been re-attached. There are now 400,000 patients around the world who have used that material to heal their wounds. Could you regenerate a limb? DARPA just gave Steve 15 million dollars to lead an eight-institution project to begin the process of asking that question.
Και θα σας δείξω την εικόνα 15 εκατ. δολαρίων. Αυτό είναι 78χρονος ο ποιος έχασε την άκρη του δάκτυλό του. Θυμάστε τι ανέφερα πριν για τα παιδιά που χάνουν τα δάχτυλά τους. Μετά από την θεραπεία αυτό είναι το δάχτυλό του. Αυτό συμβαίνει σήμερα. Αυτό είναι κλινικά εφικτό σήμερα. Υπάρχουν υλικά που το κάνουν αυτό. Υπάρχουν μπαλώματα για την καρδιά.
And I'll show you the 15 million dollar picture. This is a 78 year-old man who's lost the end of his fingertip. Remember that I mentioned before the children who lose their fingertips. After treatment that's what it looks like. This is happening today. This is clinically relevant today. There are materials that do this. Here are the heart patches.
Αλλά θα μπορούσαμε να πάμε και πιο μακριά; Θα μπορούσαμε, ας πούμε, αντί της χρησιμοποίησης υλικού, να πάρουμε και κάποια κύτταρα μαζί με το υλικό, και να αφαιρέσουμε τον κατεστραμμένο ιστό, να βάλουμε βιοδιασπώμενο υλικό εκεί πάνω; Μπορείτε να δείτε εδώ ένα μικρό κομμάτι της καρδιακού μυός. Αυτό έγινε από τον Τέρουο Οκάνο στο Νοσοκομείο Γυναικών του Τόκιο . Πραγματικά καλλιεργεί καρδιακό ιστό με σφυγμό στο εργαστήριο. Εάν ψυχράνει το δοχείο, αλλάζει τις ιδιότητες του και έτσι ξεκολλά εύκολα από το δοχείο Είναι πολύ πρώτο.
But could you go a little further? Could you, say, instead of using material, can I take some cells along with the material, and remove a damaged piece of tissue, put a bio-degradable material on there? You can see here a little bit of heart muscle beating in a dish. This was done by Teruo Okano at Tokyo Women's Hospital. He can actually grow beating tissue in a dish. He chills the dish, it changes its properties and he peels it right out of the dish. It's the coolest stuff.
Τώρα θα σας παρουσιάσω αναγέννηση με βάση τα κύτταρα Και αυτό που θα σας δείξω είναι βλαστικά κύτταρα που έχουν αφαιρεθεί από το ισχίο του ασθενούς. Και πάλι, αν αηδιάζετε εύκολα, μη κοιτάτε. Αυτό όμως είναι ωραίο. Αυτό λοιπόν είναι ένα μπάι πας, όπως του Αλ Γκορ, με μια διαφορά. Σε αυτη την περίπτωση, στο τέλος του μπάι πας, θα δείτε τα βλαστικά κύτταρα του ασθενούς τα οποία πήραμε στην αρχή της εγχείρησης να δίνονται πίσω ενέσιμα στην καρδία του ασθενούς. Και στέκομαι εδώ πάνω επειδή σε ένα σημείο Θα σας δείξω πόσο καινούρια είναι αυτή η τεχνολογία. Εδώ είναι τα βλαστικά κύτταρα, πάνε μέσα στην καρδία του ασθενούς Και αν δείτε προσεκτικά περίπου σε αυτό το σημείο μπορείτε να δείτε ότι ξεχειλίζουν Τα κύτταρα χύνονται έξω Χρειαζόμαστε όλων των ειδών νέες τεχνολογίες, νέες συσκευές, για να βάλουμε κύτταρα στο σωστό μέρος τη σωστή στιγμή.
Now I'm going to show you cell-based regeneration. And what I'm going to show you here is stem cells being removed from the hip of a patient. Again, if you're squeamish, you don't want to watch. But this one's kind of cool. So this is a bypass operation, just like what Al Gore had, with a difference. In this case, at the end of the bypass operation, you're going to see the stem cells from the patient that were removed at the beginning of the procedure being injected directly into the heart of the patient. And I'm standing up here because at one point I'm going to show you just how early this technology is. Here go the stem cells, right into the beating heart of the patient. And if you look really carefully, it's going to be right around this point you'll actually see a back-flush. You see the cells coming back out. We need all sorts of new technology, new devices, to get the cells to the right place at the right time.
Μόνο ένα μικρό κομμάτι των δεδομένων, ένα μικρό κομμάτι των δεδομένων. Αυτή ήταν μια μελέτη με τυχαίες παραμέτρους. Αυτή τη φορά το δείγμα ήταν 20 ασθενείς. Τώρα υπάρχει μια έρευνα με 100. Βασικά, αν πάρεις ένα εξαιρετικά άρρωστο ασθενή και του κάνεις μπάι πας, θα τα πάει λίγο καλύτερα. Αν τους δώσεις και βλαστικά κύτταρα, μαζί με το μπάι πας, αυτοί οι συγκεκριμένοι ασθενείς, έγιναν ασυμπτωματικοί. Αυτοί έχουν βγει εδώ και δύο χρόνια. Το πιο φανταστικό θα ήταν να μπορούσαμε να διαγνώσουμε την ασθένεια σε πρώιμο στάδιο, και να προλάβουμε την εκδήλωση της σε κακό στάδιο.
Just a little bit of data, a tiny bit of data. This was a randomized trial. At this time this was an N of 20. Now there's an N of about 100. Basically, if you take an extremely sick patient and you give them a bypass, they get a little bit better. If you give them stem cells as well as their bypass, for these particular patients, they became asymptomatic. These are now two years out. The coolest thing would be is if you could diagnose the disease early, and prevent the onset of the disease to a bad state.
Αυτή είναι η ίδια ακριβώς διαδικασία, αλλά τώρα γίνεται με πολύ λιγότερη χειρουργική παρέμβαση, με μόνο τρεις τρύπες στο σώμα παίρνουν την καρδιά και κάνουν απλά μια ένεση βλαστοκυττάρων λαπαροσκοπικά. Να τα κύτταρα Δεν έχουμε χρόνο να μπούμε σε όλες τις λεπτομέρειες, αλλά βασικά, και αυτό δουλεύει. Μπορείς να πάρεις λιγότερο άρρωστους ασθενείς, και να τους φέρεις σε μια σχεδόν ασυμπτωματική κατάσταση μέσω αυτής της θεραπείας.
This is the same procedure, but now done minimally invasively, with only three holes in the body where they're taking the heart and simply injecting stem cells through a laparoscopic procedure. There go the cells. We don't have time to go into all of those details, but basically, that works too. You can take patients who are less sick, and bring them back to an almost asymptomatic state through that kind of therapy.
Εδώ είναι ένα άλλο παράδειγμα θεραπείας με βλαστοκύτταρα που δεν είναι ακόμα σε κλινικό στάδιο, αλλά πιστεύω ότι πολύ σύντομα θα είναι. Αυτό είναι το έργο της Κέισι Μάρα από το Πιτσμπουργκ, και ορισμένων συναδέλφων της σε όλο τον κόσμο. Αποφάσισαν ότι το υγρό από τη λιποαναρρόφηση, -- και στις ΗΠΑ έχουμε πολύ υγρό από λιποαναρροφήσεις. (Γέλια) Είναι πολύ καλή πηγή βλαστοκυττάρων. Το υγρό αυτό είναι γεμάτο βλαστοκύτταρα. Οπότε, θα μπορούσες να πας, να κάνεις μια λιποαναρρόφηση στην κοιλιά. Να βγάλεις το υγρό σου, και σ' αυτή την περίπτωση, να απομονώσεις τα βλαστοκύτταρα και να τα μετατρέψεις σε νευρώνες. Όλα στο εργαστήριο. Και νομίζω ότι πολύ σύντομα, θα δείτε τους ασθενείς να υποβάλλονται σε θεραπεία με τα δικά τους βλαστοκύτταρα από λίπος, ή αλλιώς το λιπώδη ιστό τους.
Here's another example of stem-cell therapy that isn't quite clinical yet, but I think very soon will be. This is the work of Kacey Marra from Pittsburgh, along with a number of colleagues around the world. They've decided that liposuction fluid, which -- in the United States, we have a lot of liposuction fluid. (Laughter) It's a great source of stem cells. Stem cells are packed in that liposuction fluid. So you could go in, you could get your tummy-tuck. Out comes the liposuction fluid, and in this case, the stem cells are isolated and turned into neurons. All done in the lab. And I think fairly soon, you will see patients being treated with their own fat-derived, or adipose-derived, stem cells.
Μίλησα και πριν για τη χρήση συσκευών για να αλλάξει δραματικά ο τρόπος θεραπείας των νόσων. Θα σας δείξω ένα μόνο παράδειγμα, πριν κλείσω. Εξίσου τραγικό. Έχουμε μια πολύ στενή και συναισθηματική συνεργασία με τους συναδέλφους μας στο Ινστιτούτο Ερευνών για την Χειρουργική στον αμερικανικό στρατό, που τώρα έχουν να θεραπεύσουν, 11.000 παιδιά που έχουν γυρίσει από το Ιράκ. Πολλοί από αυτούς τους ασθενείς έχουν πολύ σοβαρά εγκαύματα.
I talked before about the use of devices to dramatically change the way we treat disease. Here's just one example before I close up. This is equally tragic. We have a very abiding and heartbreaking partnership with our colleagues at the Institute for Surgical Research in the US Army, who have to treat the now 11,000 kids that have come back from Iraq. Many of those patients are very severely burned.
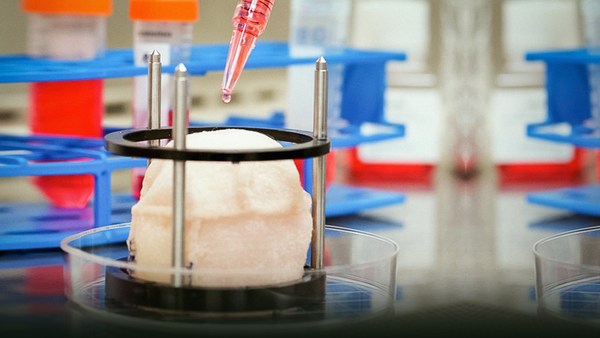
Και αν υπάρχει κάτι που μάθαμε για τα εγκαύματα, είναι ότι δεν ξέρουμε πώς να τα θεραπεύσουμε. Ό,τι γίνεται για τη θεραπεία του εγκαύματος -- βασικά το κάνουμε σα να στρώνουμε χλοοτάπητα. Φτιάχνουμε κάτι εδώ, και μετά το μεταμοσχεύουμε πάνω στην πληγή, και προσπαθήσουμε να κάνουμε δυο μέρη να κολλήσουν μεταξύ τους. Στην περίπτωση αυτή, έχει σχεδιαστεί ένας καινούριος "φορετός" βίο-αντιδραστήρας -- ο οποίος σκοπεύεται να δοκιμαστεί κλινικά εντός του έτους στο ISR -- από τον Γιοργκ Γκέρλατς στο Πίτσμπουργκ. Και αυτός ο βίο-αντιδραστήρας θα απλωθεί πάνω στην πληγή. Το όπλο που βλέπετε εκεί ψεκάζει κύτταρα. Θα ψεκάσει κύτταρα σε όλη την περιοχή. Ο αντιδραστήρας θα κάνει γόνιμη αυτή την περιοχή, και την ίδια στιγμή θα προσθέσει και άλλα κατάλληλα υλικά, έτσι ώστε να "φυτρώσει" δέρμα στην περιοχή, και όχι να στρωθούν κομμάτια δέρματος από πάνω. Είναι ένας εντελώς διαφορετικός τρόπος προσέγγισης.
And if there's anything that's been learned about burn, it's that we don't know how to treat it. Everything that is done to treat burn -- basically we do a sodding approach. We make something over here, and then we transplant it onto the site of the wound, and we try and get the two to take. In this case here, a new, wearable bio-reactor has been designed -- it should be tested clinically later this year at ISR -- by Joerg Gerlach in Pittsburgh. And that bio-reactor will lay down in the wound bed. The gun that you see there sprays cells. That's going to spray cells over that area. The reactor will serve to fertilize the environment, deliver other things as well at the same time, and therefore we will seed that lawn, as opposed to try the sodding approach. It's a completely different way of doing it.
Κι έτσι τελείωσαν τα 18 λεπτά μου. Οπότε, ας τελειώσω με τα καλά νέα, και ίσως με λίγα άσχημα νέα. Τα καλά νέα είναι ότι αυτά συμβαίνουν σήμερα. Είναι πολύ δυναμική δουλειά. Είναι σαφές αυτό από τις εικόνες που είδαμε. Είναι απίστευτα δύσκολη δουλειά γιατί είναι εξαιρετικά διεπιστημονική. Σχεδόν κάθε τομέας της επιστημονικής μηχανικής και της κλινικής πρακτικής συμμετέχει στην προσπάθεια για να μπορέσουν να συμβούν αυτά.
So my 18 minutes is up. So let me finish up with some good news, and maybe a little bit of bad news. The good news is that this is happening today. It's very powerful work. Clearly the images kind of get that across. It's incredibly difficult because it's highly inter-disciplinary. Almost every field of science engineering and clinical practice is involved in trying to get this to happen.
Ορισμένες κυβερνήσεις, καθώς και ορισμένες περιφέρειες, έχουν αναγνωρίσει ότι πρόκειται για ένα νέο τρόπο θεραπείας. Η ιαπωνική κυβέρνηση ήταν ίσως η πρώτη, όταν αποφάσισαν να επενδύσουν πρώτα 3 δισ., και αργότερα ακόμα 2 δισ. σε αυτόν τον τομέα. Δεν είναι τυχαίο. Η Ιαπωνία είναι η γηραιότερη χώρα στη γη από την άποψη μέσης ηλικίας. Πρέπει να το κάνουν να δουλέψει ή το σύστημα υγείας τους θα καταρρεύσει. Έτσι κάνουν πολλές στρατηγικές επενδύσεις επικεντρώνοντας σε αυτόν τον τομέα Η Ευρωπαϊκή Ένωση, το ίδιο. Η Κίνα, το ίδιο. Η Κίνα μόλις ξεκίνησε ένα Εθνικό Κέντρο Ιστομηχανικής. Το πρώτο έτος o προϋπολογισμός του ήταν 250 εκατ. δολάρια ΗΠΑ.
A number of governments, and a number of regions, have recognized that this is a new way to treat disease. The Japanese government were perhaps the first, when they decided to invest first 3 billion, later another 2 billion in this field. It's no coincidence. Japan is the oldest country on earth in terms of its average age. They need this to work or their health system dies. So they're putting a lot of strategic investment focused in this area. The European Union, same thing. China, the same thing. China just launched a national tissue-engineering center. The first year budget was 250 million US dollars.
Στις Ηνωμένες Πολιτείες είχαμε μια κάπως διαφορετική προσέγγιση. Εμείς -- (Γέλια) -- α, ο Αλ Γκορ να ερχόταν και να ήταν πρόεδρος στον πραματικό κόσμο. Είχαμε μια διαφορετική προσέγγιση. Και η προσέγγιση είναι βασικά να χρηματοδοτούνται έρευνες γενικά. Αλλά δεν υπάρχει στρατηγική επένδυση ώστε να φέρει προσεκτικά όλα τα απαραίτητα στοιχεία μαζί και να τα εστιάσει.
In the United States we've had a somewhat different approach. (Laughter) Oh, for Al Gore to come and be in the real world as president. We've had a different approach. And the approach has basically been to just sort of fund things as they come along. But there's been no strategic investment to bring all of the necessary things to bear and focus them in a careful way.
Και θα κλείσω με μια φράση, ίσως είναι λίγο χτύπημα κάτω απ' τη ζώνη, προς το διευθυντή του Εθνικού Ινστιτούτου Υγείας, ο οποίος είναι ένα πολύ γοητευτικός άνθρωπος. Εγώ και ο Τζέι Βακάντι από το Χάρβαρντ πήγαμε να επισκεφτούμε αυτόν και μια σειρά στελεχών του ιδρύματός του πριν από μόλις λίγους μήνες, για να προσπαθήσουμε να τον πείσουμε ότι είναι καιρός να πάρει μόνο ένα μικρό κομματάκι από τα 27.5 δισ. δολάρια που πρόκειται να λάβει το επόμενο έτος και να το εστιάσει, με στρατηγικό τρόπο, για να επιβεβαιώσει την επιτάχυνση του ρυθμού με τον οποίο αυτά τα πράγματα περνούν στους τους ασθενείς. Και στο τέλος μιας πολύ δύσκολης συνάντησης, αυτό που είπε ο διευθυντής το ΕΙΥ είναι, "Το όραμά σας είναι μεγαλύτερο από την όρεξή μας." Θα ήθελα να κλείσω λέγοντας ότι κανείς δεν πρόκειται να αλλάξει το όραμά μας, αλλά μαζί μπορούμε να αλλάξουμε την όρεξή του. Ευχαριστώ.
And I'm going to finish up with a quote, maybe a little cheap shot, at the director of the NIH, who's a very charming man. Myself and Jay Vacanti from Harvard went to visit with him and a number of his directors of his institute just a few months ago, to try and convince him that it was time to take just a little piece of that 27.5 billion dollars that he's going to get next year and focus it, in a strategic way, to make sure we can accelerate the pace at which these things get to patients. And at the end of a very testy meeting, what the NIH director said was, "Your vision is larger than our appetite." I'd like to close by saying that no one's going to change our vision, but together we can change his appetite. Thank you.