Dnes budu mluvit o tom, co doufám promění strach v naději. Když jdeme ke svému lékaři, když vstoupíme do jeho ordinace jsou slova, která prostě nechceme slyšet. Jsou to slova, kterých se opravdu obáváme. Cukrovka, rakovina, Parkinsonova nebo Alzheimerova choroba, selhání srdce, selhání plic. Víme, že to jsou oslabující nemoci s nimiž můžeme udělat relativně málo.
I'm going to talk to you today about hopefully converting fear into hope. When we go to the physician today -- when we go to the doctor's office and we walk in, there are words that we just don't want to hear. There are words that we're truly afraid of. Diabetes, cancer, Parkinson's, Alzheimer's, heart failure, lung failure -- things that we know are debilitating diseases, for which there's relatively little that can be done.
Dnes Vám chci představit jiný způsob myšlení o tom, jak zacházet s takovými nemocemi a a vysvětlit proč je takové myšlení důležité. Bez toho se možná náš systém zdravotní péče může zhroutit, tedy pokud nemyslíte, že se to již stalo. Řeknu kde jsme klinicky dnes, a kam bychom mohli jít zítra, a jaké jsou překážky. A slibuji, že vše zvládneme probrat v 18 minutách.
And what I want to lay out for you today is a different way of thinking about how to treat debilitating disease, why it's important, why without it perhaps our health care system will melt down if you think it already hasn't, and where we are clinically today, and where we might go tomorrow, and what some of the hurdles are. And we're going to do all of that in 18 minutes, I promise.
Chtěl bych začít s tímto diapositivem protože nám ukazuje jak to vidí časopis Science Magazine. Bylo to číslo z roku 2002, v němž uveřejnili mnoho různých článků o bionické lidské bytosti. Byla to číslo o regenerativním lékařství. Regenerativní lékařství je mimořádně jednoduchý pojem, kterému každý rozumí. Je to jednoduše urychlení tempa, kterým se tělo samo hojí takže se hojení proběhne v klinicky významném čase. Takže víme, jak to udělat různými způsoby, které již existují. Víme, že když máme poškozený kyčel, můžeme vložit kyčel umělý. A to je myšlenka, kterou časopis Science Magazine použil na hlavní straně.
I want to start with this slide, because this slide sort of tells the story the way Science Magazine thinks of it. This was an issue from 2002 that they published with a lot of different articles on the bionic human. It was basically a regenerative medicine issue. Regenerative medicine is an extraordinarily simple concept that everybody can understand. It's simply accelerating the pace at which the body heals itself to a clinically relevant timescale. So we know how to do this in many of the ways that are up there. We know that if we have a damaged hip, you can put an artificial hip in. And this is the idea that Science Magazine used on their front cover.
To je ale úplný protiklad regenerativního lékařství. To totiž není regenerativní lékařství. Regenerativní lékařství je to, co uvedl časopis Business Week ve svém nedávném článku. Myšlenka je taková, že místo abychom odstraňovali příznaky s pomocí protéz, drog a tak podobně -- k tomuto se několikrát vrátím -- místo toho, znovuvytvoříme ztracenou funkci těla zregenerováním funkce orgánů a poškozené tkáně. Takže na konci léčby, jste tím, kým jste byli na začátku léčby.
This is the complete antithesis of regenerative medicine. This is not regenerative medicine. Regenerative medicine is what Business Week put up when they did a story about regenerative medicine not too long ago. The idea is that instead of figuring out how to ameliorate symptoms with devices and drugs and the like -- and I'll come back to that theme a few times -- instead of doing that, we will regenerate lost function of the body by regenerating the function of organs and damaged tissue. So that at the end of the treatment, you are the same as you were at the beginning of the treatment.
Málo dobrých nápadů -- pokud souhlasíte, že to je dobrý nápad -- velmi málo dobrých nápadů je opravdu nových. Přesně tak je tomu i zde. Když se podíváte do historie, Charles Lindbergh, který byl víc známý díky letectví - byl ve skutečnosti jeden z prvních lidí, spolu s Alexis Carrel, jedna z nositelek Nobelovy ceny z Rockefellerova ústavu, kteří začali přemýšlet o tom, zda je možné orgány vypěstovat. A v roce 1937 uveřejnili tuto knihu, ve které vskutku začali přemýšlet o tom, co by se mohlo udělat v bio-reaktoru, aby vyrostl celý orgán. Od té doby jsme došli daleko. Podělím se s vámi o některé fascinující práce, které se nyní dějí.
Very few good ideas -- if you agree that this is a good idea -- very few good ideas are truly novel. And this is just the same. If you look back in history, Charles Lindbergh, who was better known for flying airplanes, was actually one of the first people along with Alexis Carrel, one of the Nobel Laureates from Rockefeller, to begin to think about, could you culture organs? And they published this book in 1937, where they actually began to think about, what could you do in bio-reactors to grow whole organs? We've come a long way since then. I'm going to share with you some of the exciting work that's going on.
Ale předtím, než to udělám, chtěl bych se podělit s mými depresemi nad systémem zdravotní péče a potřebě vám to sdělit. Mnoho přednášek ze včerejška se týkalo zlepšení kvality života a snížení chudoby. A podstaného zvýšení průměrné délky života na celém světě. Jedna z výzev je, že čím jsme bohatší, tím déle žijeme. A čím déle žijeme, tím dražší je pečovat o naše nemoci, když stárneme.
But before doing that, what I'd like to do is share my depression about the health care system and the need for this with you. Many of the talks yesterday talked about improving the quality of life, and reducing poverty, and essentially increasing life expectancy all around the globe. One of the challenges is that the richer we are, the longer we live. And the longer we live, the more expensive it is to take care of our diseases as we get older.
Jednoduše řečeno, jde o bohatství země ve srovnání s procentem populace nad 65 let věku. A v podstatě můžete vidět, že čím je země bohatší, tím více starších lidí v ní žije. Proč je to důležité? A proč je to obzvláště právě teď tak dramatická výzva? Jestliže je průměrný věk naší populace 30 let, potom je takové průměrné onemocnění, které musíte léčit tu a tam zlomený kotník, možná trochu astma. Jestliže je průměrný věk ve vaší zemi od 45 do 55 let, průměrný člověk bere v úvahu cukrovku, juvenilní cukrovku, selhání srdce, choroby srdeční tepny. To vše je neodmyslitelně obtížnější léčit, a tedy hodně nákladnější .
This is simply the wealth of a country versus the percent of population over the age of 65. And you can basically see that the richer a country is, the older the people are within it. Why is this important? And why is this a particularly dramatic challenge right now? If the average age of your population is 30, then the average kind of disease that you have to treat is maybe a broken ankle every now and again, maybe a little bit of asthma. If the average age in your country is 45 to 55, now the average person is looking at diabetes, early-onset diabetes, heart failure, coronary artery disease -- things that are inherently more difficult to treat, and much more expensive to treat.
Jen se podívejte na demografii zde v USA. Toto je ze "Spojených států Amerických". V roce 1930 bylo 41 pracovníků na jednoho důchodce. 41 lidí, kteří v podstatě nebyli vážně nemocní, platili na jednoho důchodce, který prodělával oslabující onemocnění. V roce 2010 na jednoho důchodce jsou dva pracující. A tak tomu je v každé vyvinuté, bohaté zemi. Jak si vlastně můžete dovolit platit léčbu pacientů, když realita stárnutí vypadá právě takto?
Just have a look at the demographics in the U.S. here. This is from "The Untied States of America." In 1930, there were 41 workers per retiree. 41 people who were basically outside of being really sick, paying for the one retiree who was experiencing debilitating disease. In 2010, two workers per retiree in the U.S. And this is matched in every industrialized, wealthy country in the world. How can you actually afford to treat patients when the reality of getting old looks like this?
Je to případ věku versus náklady na zdravotní péči. A vidíte, že právě okolo věku 45 let, 40 až 45, zde je náhlý zlom v nákladech na zdravotní péči. Je to ve skutečnosti velice zajímavé - jestliže to správně analyzujete, uvažte kolik vy jako jednotlivec vynaložíte na svoji vlastní zdravotní péči, během celého vašeho života. Asi 7 let předtím než umřete je vrchol. A vlastně můžete - (smích) - tím se nebudeme zabývat. (smích)
This is age versus cost of health care. And you can see that right around age 45, 40 to 45, there's a sudden spike in the cost of health care. It's actually quite interesting. If you do the right studies, you can look at how much you as an individual spend on your own health care, plotted over your lifetime. And about seven years before you're about to die, there's a spike. And you can actually -- (Laughter) -- we won't get into that. (Laughter)
Je zde pár věcí, velmi málo věcí, které se dají udělat, které by změnily způsob léčení takových onemocnění a umožnily zažít co bych nazval zdravé stárnutí. Řekl bych, že se jedná o 4 věci. A ani jedna se netýká systému pojištění nebo právního systému. Změna je v tom, kdo platí. Změna vlastně není ve skutečných nákladech léčby.
There are very few things, very few things that you can really do that will change the way that you can treat these kinds of diseases and experience what I would call healthy aging. I'd suggest there are four things, and none of these things include an insurance system or a legal system. All those things do is change who pays. They don't actually change what the actual cost of the treatment is.
Jedna z možností je, že nebudete léčit. Můžete zdravotní péči udělovat na příděl. Nebudeme o této metodě dál mluvit. Je to příliš depresivní. Onemocněním můžete předcházet. Samozřejmě, spousta peněz by se mělo vkládat do prevence.
One thing you can do is not treat. You can ration health care. We won't talk about that anymore. It's too depressing. You can prevent. Obviously a lot of monies should be put into prevention.
Ale snad nejzajímavější, v každém případě pro mě, nejzajímavější je myšlenka diagnostikování onemocnění v ranném stádiu, s následnou léčbou toho onemocnění místo léčení příznaků. Jako přiklad uvažme cukrovku. Co dnes můžem dělat s cukrovkou? Onemocnění diagnostikujeme, když se projeví příznaky. a posléze je léčíme 10, 20, 30, 40 let. A funguje to. Inzulín je docela dobrá terapie.™ Ale nakonec přestane fungovat, a cukrovka vede k předpovídatelnému počátku oslabující nemoci.
But perhaps most interesting, to me anyway, and most important, is the idea of diagnosing a disease much earlier on in the progression, and then treating the disease to cure the disease instead of treating a symptom. Think of it in terms of diabetes, for instance. Today, with diabetes, what do we do? We diagnose the disease eventually, once it becomes symptomatic, and then we treat the symptom for 10, 20, 30, 40 years. And we do OK. Insulin's a pretty good therapy. But eventually it stops working, and diabetes leads to a predictable onset of debilitating disease.
Proč nestačí pouze stříknout něco do slinivky, aby se ta slinivka zregenerovala v počátku nemoci, možná i dříve než se ukáží příznaky nemoci? A možná by to bylo trochu nákladnější v té době kdy bychom to udělali, ale kdyby to fungovalo, tak jsme dokázali něco zcela jiného.
Why couldn't we just inject the pancreas with something to regenerate the pancreas early on in the disease, perhaps even before it was symptomatic? And it might be a little bit expensive at the time that we did it, but if it worked, we would truly be able to do something different.
Myslím, že toto video objasňuje myšlenku o které zde mluvím docela dramaticky. Toto je čolek, kterému dorůstá končetina. Když to dokáže čolek, proč ne my? Dokonce vám za chvíli ukáži nějaké zajímavé charakteristiky o regeneraci končetin. Ale to, o čem mluvíme v regenerativní medicíně, je dokázat tohle s každým orgánovým systémem našeho těla, s tkáněmi a samotnými orgány. Dnešní realitou je, že když onemocníme, zpráva pro Vás je léčba vašich příznaků po níž se holt přizpůsobíte novému způsobu života.
This video, I think, gets across the concept that I'm talking about quite dramatically. This is a newt re-growing its limb. If a newt can do this kind of thing, why can't we? I'll actually show you some more important features about limb regeneration in a moment. But what we're talking about in regenerative medicine is doing this in every organ system of the body, for tissues and for organs themselves. So today's reality is that if we get sick, the message is we will treat your symptoms, and you need to adjust to a new way of life.
Já tvrdím, že zítra -- a kdy ten zítřek nastane, o tom můžeme diskutovat, ale bude v dohledné budoucnosti -- zítra budem mluvit o regenerativní rehabilitaci. Zde vidíte protézu, je velice podobná té, kterou má voják, který se vrátil z Iráku... 370 vojáků, kteří se z Iráku vrátili, přišli o končetiny. Představte si, že by místo žitím s tím, mohli by čekat regeneraci této končetiny. Je to odvážná představa. Ukáži vám, kde se momentálně nacházíme při práci na tomto konceptu.
I would pose to you that tomorrow -- and when tomorrow is we could debate, but it's within the foreseeable future -- we will talk about regenerative rehabilitation. There's a limb prosthetic up here, similar actually one on the soldier that's come back from Iraq. There are 370 soldiers that have come back from Iraq that have lost limbs. Imagine if instead of facing that, they could actually face the regeneration of that limb. It's a wild concept. I'll show you where we are at the moment in working towards that concept.
Znovu podotýkám, že je to aplikovatelné na každý orgán. Jak toho můžeme dosáhnout? Udělat to lze tak, že rozvineme konverzaci s naším tělem. Je potřeba, abychom se naučili řeč těla. A zapnout procesy, které jsme uměli , když jsme byli zárodkem. Savčí zárodek, který přijde o končeninu během prvního trimestru v těhotenství, si ji znovu nechá narůst. Takže naše DNA má schopnost řídit takové mechanismy hojení ran. Je to přirozený proces., ale s věkem se ztrácí. Dítěti, které je mladší než šest měsíců a které přijde náhodou o špičku prstu špicka prstu mu zase doroste. Jakmile dosáhne věku pěti let, pak už to nebude možné.
But it's applicable, again, to every organ system. How can we do that? The way to do that is to develop a conversation with the body. We need to learn to speak the body's language. And to switch on processes that we knew how to do when we were a fetus. A mammalian fetus, if it loses a limb during the first trimester of pregnancy, will re-grow that limb. So our DNA has the capacity to do these kinds of wound-healing mechanisms. It's a natural process, but it is lost as we age. In a child, before the age of about six months, if they lose their fingertip in an accident, they'll re-grow their fingertip. By the time they're five, they won't be able to do that anymore.
Takže abychom se mohli zabývat konverzací s naším tělem, potřebujeme se naučit mluvit řečí těla. A my už dnes máme jisté nástroje, které nám dovolí toho dosáhnout. Dám vám příklad tří takových nástrojů, díky kterým můžem rozmlouvat s naším tělem.
So to engage in that conversation with the body, we need to speak the body's language. And there are certain tools in our toolbox that allow us to do this today. I'm going to give you an example of three of these tools through which to converse with the body.
Prvním nástrojem je buňková terapie. Jasně, léčíme se přírodním postupem, používáním buněk, které udělají nějvětší kus práce. Tudíž, pokud můžeme najít ty správné buňky a vpravit je do těla, ty tam mohou léčit. Za druhé, můžeme použít jisté materiály. Včera jsme slyšeli o důležitosti nových materiálů. Když můžeme vymyslet a navrhnout látky, nebo extrahovat látky z přírodního prostředí, potom můžeme být schopni touto látkou přimět tělo, aby se samo vyléčilo. A nakonec, můžeme využít chytrých přístrojů, které tělo zbaví těžké práce a umožní mu se léčit.
The first is cellular therapies. Clearly, we heal ourselves in a natural process, using cells to do most of the work. Therefore, if we can find the right cells and implant them in the body, they may do the healing. Secondly, we can use materials. We heard yesterday about the importance of new materials. If we can invent materials, design materials, or extract materials from a natural environment, then we might be able to have those materials induce the body to heal itself. And finally, we may be able to use smart devices that will offload the work of the body and allow it to heal.
Ukáži vám příklad každého z těchto tři a začnu s materiály. Steve Badylak - který je na Univerzitě v Pittsburgu - měl, asi před deseti lety, pozoruhodný nápad. Myšlenka byla, že prasečí tenké střevo, ze kterého vyhodíte všechny buňky, a když to uděláte způsobem, které mu dovoluje zůstat biologicky aktivní, může obsahovat všechny důležité faktory a signály, které signalizují tělu, ze se má hojit. A položil si velmi důležitou otázku. Zeptal se, když vezmu tento materiál, který je přírodní látkou, a který obvykle vyvolává hojení v tenkém střevě, a umístím ho někam jinam na těle člověka, dostanu stejnou odpověď, ale specifickou pro takovou jinou tkáň, a nebo se vytvoří tenké střevo, když jsem zkusil udělat nové ucho?
I'm going to show you an example of each of these, and I'm going to start with materials. Steve Badylak -- who's at the University of Pittsburgh -- about a decade ago had a remarkable idea. And that idea was that the small intestine of a pig, if you threw away all the cells, and if you did that in a way that allowed it to remain biologically active, may contain all of the necessary factors and signals that would signal the body to heal itself. And he asked a very important question. He asked the question, if I take that material, which is a natural material that usually induces healing in the small intestine, and I place it somewhere else on a person's body, would it give a tissue-specific response, or would it make small intestine if I tried to make a new ear?
Neříkal bych vám tento příběh, pokud by nebyl přesvědčivý, Obrázek, který vám chci ukázat - (smích) je přesvědčivým obrázkem. Nicméně, pro ty, kteří jsou, třeba jen trošicku choulostiví, i když by to nechtěli nepřiznat před svými přáteli -- osvětlení je ztlumeno a toto je vhodný čas aby jste se podívali dolů, na své nohy, zkontrolovali svoje Blackberry, prostě dělali něco jiného než sledování obrazovky. (smích)
I wouldn't be telling you this story if it weren't compelling. The picture I'm about to show you is a compelling picture. (Laughter) However, for those of you that are even the slightest bit squeamish -- even though you may not like to admit it in front of your friends -- the lights are down. This is a good time to look at your feet, check your Blackberry, do anything other than look at the screen. (Laughter)
To co vám chci ukázat je diabetický vřed. Ačkoli, je dobré se zasmát předtím než se na to podíváte. Toto je skutečnost cukrovky. Myslím, že o cukrovce a vředech jsme slyšeli mnohokrát, ale nespojili jsme si vřed s eventuální léčbou, kterou je amputace, pokud se vřed nedá vyléčit. Takže zde ho vidíte, nebojte, nebude tam dlouho. Toto je diabetický vřed. Je to tragické. Léčbou je amputace. Tato starší žena, která má vedle cukrovky i rakovinu jater se rozhodla zemřít s tělem jaké má.
What I'm about to show you is a diabetic ulcer. And although -- it's good to laugh before we look at this. This is the reality of diabetes. I think a lot of times we hear about diabetics, diabetic ulcers, we just don't connect the ulcer with the eventual treatment, which is amputation, if you can't heal it. So I'm going to put the slide up now. It won't be up for long. This is a diabetic ulcer. It's tragic. The treatment for this is amputation. This is an older lady. She has cancer of the liver as well as diabetes, and has decided to die with what' s left of her body intact.
Tato paní se rozhodla, že po roce, během kterého pokoušela o léčbu tohoto vředu, že by zkusila novou terapii, kterou vynalezl Steve. Toto je rána o 11 týdnů později. Tato látka obsahovala pouze přírodní signály. A tato látka donutila tělo, aby přepla zpět na léčebný proces, který předtím tělo nemělo.
And this lady decided, after a year of attempted treatment of that ulcer, that she would try this new therapy that Steve invented. That's what the wound looked like 11 weeks later. That material contained only natural signals. And that material induced the body to switch back on a healing response that it didn't have before.
Teď bude ještě pár hrozných obrázků - pro ty otrlé - Řeknu Vám, kdy se můžete zase začít dívat. Toto je kůň. Kůň se není v bolestech. Kdyby kůň byl v bolestech , neukazoval bych vám tento obrázek. Kůň má pouze další nosní dírku, která se vyvinula po jezdecké nehodě. Pouze několik týdnů po léčbě -- v tomto případě jsme vzali látku, přeměnili ji na gel, a zabalili zraněnou oblast, a poté jsme tuto léčbu několikrát opakovali -- a kůň se uzdravil. Utrazvukový snímek této oblasti, vypadá to výborně.
There's going to be a couple more distressing slides for those of you -- I'll let you know when you can look again. This is a horse. The horse is not in pain. If the horse was in pain, I wouldn't show you this slide. The horse just has another nostril that's developed because of a riding accident. Just a few weeks after treatment -- in this case, taking that material, turning it into a gel, and packing that area, and then repeating the treatment a few times -- and the horse heals up. And if you took an ultrasound of that area, it would look great.
Zde je delfín, jehož ploutev byla pře-připevněna a přirostla. Na světě je okolo 400.000 pacientů, kteří používají tuto látku k léčení jejich zranění. Mohl byste regenerovat končetinu? Agentura pro výzkum pokročilých obranných projektů právě dala Stevovi 15 milionů dolarů, aby koordinoval výzkum osmi ústavů který by tuto otázku zodpověděl.
Here's a dolphin where the fin's been re-attached. There are now 400,000 patients around the world who have used that material to heal their wounds. Could you regenerate a limb? DARPA just gave Steve 15 million dollars to lead an eight-institution project to begin the process of asking that question.
A ukážu vám obrázek 15 milionů dolarů. Toto je 78-letý muž, který přišel o špičku prstu. Pamatujete si, co jsem říkal o tom, když děti přijou o jejich špičky prstů. Takhle to vypadá po léčbě. A to je dnes. Dnes je to již klinicky významné. Látky, které to dokáží. Srdeční záplaty.
And I'll show you the 15 million dollar picture. This is a 78 year-old man who's lost the end of his fingertip. Remember that I mentioned before the children who lose their fingertips. After treatment that's what it looks like. This is happening today. This is clinically relevant today. There are materials that do this. Here are the heart patches.
Ale mohli bychom jít ještě dále? Mohli byste, řekněme, namísto použití této látky, mohu vzít nějaké buňky spolu s tou látkou a odstranit poškozený kus tkáně, a dát na to biologicky rozložitelnou látku? Zde můžete vidět kousek srdečního svalu bijícího v misce. To bylo provedeno v tokijské ženské nemocnici panem Teruo Okano. On umí vypěstovat bijící srdeční sval v misce. Zchladí misku a to způsobí změnu jejích vlastností pak odloupne tkáň od misky. Je to ta nejlepší věc.
But could you go a little further? Could you, say, instead of using material, can I take some cells along with the material, and remove a damaged piece of tissue, put a bio-degradable material on there? You can see here a little bit of heart muscle beating in a dish. This was done by Teruo Okano at Tokyo Women's Hospital. He can actually grow beating tissue in a dish. He chills the dish, it changes its properties and he peels it right out of the dish. It's the coolest stuff.
Nyní vám ukáži regeneraci založenou na buňkách. A to co vám zde ukáži jsou kmenové buňky vyjmuté z kyčle pacienta. Znovu podotýkám, že jestli máte slabý žaludek, nedívejte se. Ale tenhle je docela fajn. Takže toto je bypass operace, kterou měl i Al Gore, s jedním rozdílem. V tomto případě, na konci operace, uvidíte kmenové buňky pacienta, které byli odejmuty na začátku procedury jak jsou vstříknuté přímo do srdce pacienta. A já tady stojím na podiu, protože vám chci ukázat, jak tato technologie je ve svých začátcích. Zse jsou kmenové buňky, přímo do bijícího srdce pacienta. A když se pozorně podíváte, bude to právě kolem tohoto bodu kde uvidíte zpětný tok. Vidítě ty buňky, jak se vracejí zpět. Potřebujeme nové druhy technologií, nové přístroje, abychom dostali buňky na správné místo ve správný čas.
Now I'm going to show you cell-based regeneration. And what I'm going to show you here is stem cells being removed from the hip of a patient. Again, if you're squeamish, you don't want to watch. But this one's kind of cool. So this is a bypass operation, just like what Al Gore had, with a difference. In this case, at the end of the bypass operation, you're going to see the stem cells from the patient that were removed at the beginning of the procedure being injected directly into the heart of the patient. And I'm standing up here because at one point I'm going to show you just how early this technology is. Here go the stem cells, right into the beating heart of the patient. And if you look really carefully, it's going to be right around this point you'll actually see a back-flush. You see the cells coming back out. We need all sorts of new technology, new devices, to get the cells to the right place at the right time.
Trochu údajů, malý kousek informací. To byla randomizovaná zkouška. V té době to byla zkouška s N= 20. Nyní máme zkoušku s N= 100. V podstatě, když vezmete extrémně nemocného pacienta a uděláte mu bypass, jeho stav se zlepší. Když mu dáte i kmenové buňky během jeho bypass operace, v těchto speciálních případech příznaky pacienta zmizí. Tito už jsou bez příznaků dva 2 roky . Nejlepší věc by byla, kdyby se diagnóza nemoci provedla dříve a předešlo se onemocnění a vzniku vážného stavu.
Just a little bit of data, a tiny bit of data. This was a randomized trial. At this time this was an N of 20. Now there's an N of about 100. Basically, if you take an extremely sick patient and you give them a bypass, they get a little bit better. If you give them stem cells as well as their bypass, for these particular patients, they became asymptomatic. These are now two years out. The coolest thing would be is if you could diagnose the disease early, and prevent the onset of the disease to a bad state.
Toto je ten samý proces, ale nyní méně agresivní, pouze se třemi otvory v těle, kde se operuje srdce a jednoduše se do něj vstříknou kmenové buňky díky laparoskopii. Tady jdou ty buňky. Nemáme čas zacházet do dalších podrobností, ale v zásadě, také to funguje. Pacienti, kteří jsou nemocní méně, jsou přivedeni tuto téměř bezpříznakového stavu tímto druhem terapie.
This is the same procedure, but now done minimally invasively, with only three holes in the body where they're taking the heart and simply injecting stem cells through a laparoscopic procedure. There go the cells. We don't have time to go into all of those details, but basically, that works too. You can take patients who are less sick, and bring them back to an almost asymptomatic state through that kind of therapy.
Další příklad terapie kmenovými buňkami, která ještě není docela klinická, ale myslím, že brzy bude. Práce Kacey Marra z Pittsburghu, spolu s množstvím kolegů z celého světa. Rozhodli se, že tekutina z liposukce, a že v USA máme hodně této tekutiny z kosmetických úprav. (smích) Je to vynikající zdroj kmenových buněk. Kmenové buňky jsou součástí této kapaliny. Takže můžete jít na plastiku břicha. Ven se dostane tekutina z liposukce, a v tomto případě, kmenové buňky jsou oddělené a mění se v nervové buňky. Vše je uděláno v laboratoři. A myslím, že docela brzy uvidíte pacienty, kteří se tak budou léčit touto metodou odebrání vlastního tuku, kmenovými buňkami.
Here's another example of stem-cell therapy that isn't quite clinical yet, but I think very soon will be. This is the work of Kacey Marra from Pittsburgh, along with a number of colleagues around the world. They've decided that liposuction fluid, which -- in the United States, we have a lot of liposuction fluid. (Laughter) It's a great source of stem cells. Stem cells are packed in that liposuction fluid. So you could go in, you could get your tummy-tuck. Out comes the liposuction fluid, and in this case, the stem cells are isolated and turned into neurons. All done in the lab. And I think fairly soon, you will see patients being treated with their own fat-derived, or adipose-derived, stem cells.
Předtím jsem mluvil o použití přístrojů, aby se výrazně změnil způsob jakým léčíme nemoci. Než uzavřeme toto téma, mám tu jeden příklad. Je to stejně tragické. Máme dlouhodobou a srdcervoucí spolupráci s našimi kolegy z Institutu pro lékařský výzkum v armádě USA, kteří musí vyléčit 11.000 hochů, kteří se vrátili z Iráku. Mnoho z těchto pacientů bylo hrozně popálených.
I talked before about the use of devices to dramatically change the way we treat disease. Here's just one example before I close up. This is equally tragic. We have a very abiding and heartbreaking partnership with our colleagues at the Institute for Surgical Research in the US Army, who have to treat the now 11,000 kids that have come back from Iraq. Many of those patients are very severely burned.
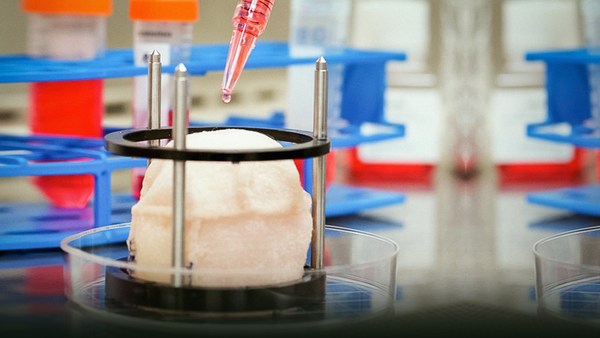
A pokud jsme se něco naučili o popáleninách, bylo to. že nevíme, jak je léčit. Vše co se doposud dělalo pro léčbu spálenin - byl přístup podobný přikládání drnů na poškozený trávník. Něco necháme vyrůst na jednom místě a poté to přeneseme na místo kde je zranění a zkusíme zařídit, aby se to uchytilo. Zde v tomto případě se vytvořil nový, nositelný biologický stabilizátor - který by měl být klinicky testován na konci tohoto roku na ISR - Joergem Gerlachem v Pitsburgu. A tento biologický stabilizátor se vsadí do lůžka zranění. Pistolkou, kterou vidíte, se stříkají buňky. Tímto způsobem se postříkají buňky po celé ploše. Stabilizátor slouží jako hnojivo v prostředí, dodává vše současně. a proto oséváme tento trávník jako alternativa k drnovému přístupu. Je to kompletně odlišný způsob provedení.
And if there's anything that's been learned about burn, it's that we don't know how to treat it. Everything that is done to treat burn -- basically we do a sodding approach. We make something over here, and then we transplant it onto the site of the wound, and we try and get the two to take. In this case here, a new, wearable bio-reactor has been designed -- it should be tested clinically later this year at ISR -- by Joerg Gerlach in Pittsburgh. And that bio-reactor will lay down in the wound bed. The gun that you see there sprays cells. That's going to spray cells over that area. The reactor will serve to fertilize the environment, deliver other things as well at the same time, and therefore we will seed that lawn, as opposed to try the sodding approach. It's a completely different way of doing it.
Takže, mých 18 minut řečnění je u konce. Dokončím tuto prezentaci nějakými dobrými novinkami, a možná i trochu špatnými zprávami. Dobrá zpráva je, že to o čem jsem dnes mluvil se dnes již děje. Je to velmi efektní práce. Je zřejmé, že pomocí obrázků jsme si to objasnili. Je to neuvěřitelně těžké, protože jde o velice inter-disciplinární vědu. Téměř každy obor vědy z oblasti techniky a klinické praxe se podílí ve snaze, aby se toto vše stalo.
So my 18 minutes is up. So let me finish up with some good news, and maybe a little bit of bad news. The good news is that this is happening today. It's very powerful work. Clearly the images kind of get that across. It's incredibly difficult because it's highly inter-disciplinary. Almost every field of science engineering and clinical practice is involved in trying to get this to happen.
Množství vlád a regionů rozpoznali, že to je nový způsob jak léčit nemoci. Japonská vláda byla snad první, když se rozhodli investovat první 3 miliardy, později další 2 miliardy do této oblasti. Není to náhoda. Japonsko je nejstarší stát na Zemi pokud jde o průměrný věk. Potřebují, aby to fungovalo, jinak jejich zdravotní systém zkolabuje. Takže proto se strategicky soustřeďují na investice do této oblasti. To samé dělá Evropská Unie. Čína - to samé. Čína zrovna rozeběhla národní centrum technické tkáně. Rozpočet pro první rok byl 250 milionů amerických dolarů.
A number of governments, and a number of regions, have recognized that this is a new way to treat disease. The Japanese government were perhaps the first, when they decided to invest first 3 billion, later another 2 billion in this field. It's no coincidence. Japan is the oldest country on earth in terms of its average age. They need this to work or their health system dies. So they're putting a lot of strategic investment focused in this area. The European Union, same thing. China, the same thing. China just launched a national tissue-engineering center. The first year budget was 250 million US dollars.
V USA máme poněkud jiný přístup. My - (smích) - uh, čekáme na Al Gora až se stane prezidentem světa. Máme odlišný přístup. Tento přístup je, že do toho vrazíme peníze, když to vypadá naléhavé. Ale žádné strategické investice, které by přinesly nezbytné věci, které by se pak soustředily pečlivým způsobem.
In the United States we've had a somewhat different approach. (Laughter) Oh, for Al Gore to come and be in the real world as president. We've had a different approach. And the approach has basically been to just sort of fund things as they come along. But there's been no strategic investment to bring all of the necessary things to bear and focus them in a careful way.
Nakonec budu citovat, možná laciná střela, ale je od ředitele NIH, velice šarmantního muže. Já a Jay Vacanti z Harvardu jsme s dalšími řediteli jeho institutu jeli navštívit jen před pár měsíci, zkusit ho přesvědčit, že teš je pravý čas vzít alespoň kousek z těch 27.5 miliard dolarů, které dostanou příští rok a zaměřit je strategickým způsobem tak, aby bylo jisté, že můžeme zrychlit tempo, kterým se tyto terapie dostanou k pacientům. Na konci rozhádané schůze ředitel NIH řekl, "Vaše vize je větší než náš apetit." Chtěl bych uzavřít tuto přednášku tím, že nikdo nám naši vizi nezmění, ale společně můžeme zvýšit jeho apetit. Děkuji vám.
And I'm going to finish up with a quote, maybe a little cheap shot, at the director of the NIH, who's a very charming man. Myself and Jay Vacanti from Harvard went to visit with him and a number of his directors of his institute just a few months ago, to try and convince him that it was time to take just a little piece of that 27.5 billion dollars that he's going to get next year and focus it, in a strategic way, to make sure we can accelerate the pace at which these things get to patients. And at the end of a very testy meeting, what the NIH director said was, "Your vision is larger than our appetite." I'd like to close by saying that no one's going to change our vision, but together we can change his appetite. Thank you.