Днес ще ви говоря за надеждата да се превърне страхът в надежда. Когато отиваме на лекар днес, когато отиваме в кабинета на доктора и влизаме вътре, има думи, които просто не искаме да чуваме. Има думи, от които истински се страхуваме. Диабет, рак, Паркинсон, Алцхаймер, отказ на сърцето, отказ на белия дроб. Неща, за които знаем, че са изтощителни болести, за които може да се направи относително малко.
I'm going to talk to you today about hopefully converting fear into hope. When we go to the physician today -- when we go to the doctor's office and we walk in, there are words that we just don't want to hear. There are words that we're truly afraid of. Diabetes, cancer, Parkinson's, Alzheimer's, heart failure, lung failure -- things that we know are debilitating diseases, for which there's relatively little that can be done.
Онова, което искам да ви изложа днес, е различен начин на мислене за това как да се лекуват изтощителни болести, защо това е важно. Защо без това вероятно здравната ни система ще се стопи, ако мислите, че това вече не се е случило. Къде сме клинично днес, къде може да отидем утре и какви са някои от препятствията. Ще направим всичко това за 18 минути, обещавам.
And what I want to lay out for you today is a different way of thinking about how to treat debilitating disease, why it's important, why without it perhaps our health care system will melt down if you think it already hasn't, and where we are clinically today, and where we might go tomorrow, and what some of the hurdles are. And we're going to do all of that in 18 minutes, I promise.
Искам да започна с този кадър, тъй като той един вид разказва историята по начина, по който списание Science (Наука) мисли за нея. Това е един брой от 2002 г., в който са публикували много различни статии за бионичния човек. По същество това е брой за регенеративна медицина. Регенеративната медицина е една изключително проста концепция, която всеки може да разбере. Това е просто ускоряване на скоростта, с която тялото изцелява само себе си към клинично приложима времева рамка. Знаем как да правим това по много от съществуващите начини. Знаем, че ако имаме увредено бедро, в него може да се присади изкуствено бедро. Това е идеята, която списание Science са използвали на първа корица.
I want to start with this slide, because this slide sort of tells the story the way Science Magazine thinks of it. This was an issue from 2002 that they published with a lot of different articles on the bionic human. It was basically a regenerative medicine issue. Regenerative medicine is an extraordinarily simple concept that everybody can understand. It's simply accelerating the pace at which the body heals itself to a clinically relevant timescale. So we know how to do this in many of the ways that are up there. We know that if we have a damaged hip, you can put an artificial hip in. And this is the idea that Science Magazine used on their front cover.
Това е пълната антитеза на регенеративната медицина. Това не е регенеративна медицина. Регенеративна медицина е онова, за което говорят BusinessWeek, когато публикуваха статия за регенеративна медицина неотдавна. Идеята е, че вместо да се търси как да се облекчат системите с устройства, лекарства и подобни... ще се върна върху тази тема след няколко минути... вместо да правим това, ще регенерираме изгубената функция на тялото чрез регенериране функцията на органи и увредена тъкан. Така че в края на лечението сте същите, каквито сте били в началото на лечението.
This is the complete antithesis of regenerative medicine. This is not regenerative medicine. Regenerative medicine is what Business Week put up when they did a story about regenerative medicine not too long ago. The idea is that instead of figuring out how to ameliorate symptoms with devices and drugs and the like -- and I'll come back to that theme a few times -- instead of doing that, we will regenerate lost function of the body by regenerating the function of organs and damaged tissue. So that at the end of the treatment, you are the same as you were at the beginning of the treatment.
Много малко добри идеи - ако сте съгласни, че това е добра идея - много малко добри идеи са истински новаторски. Съвсем същото е с това. Ако погледнете назад в историята, Чарлз Линдберг - по-добре известен с това, че е управлявал самолети - всъщност бил един от първите хора, наред с Алексис Карел, един от нобеловите лауреати от Рокфелер, да започне да мисли за това - могат ли да се култивират органи? Издали тази книга през 1937 г., където всъщност започнали да мислят за това какво може да се направи в био-реактори, за да се отглежат цели органи? Изминали сме дълъг път оттогава. Ще споделя с вас част от вълнуващата работа, която се върши.
Very few good ideas -- if you agree that this is a good idea -- very few good ideas are truly novel. And this is just the same. If you look back in history, Charles Lindbergh, who was better known for flying airplanes, was actually one of the first people along with Alexis Carrel, one of the Nobel Laureates from Rockefeller, to begin to think about, could you culture organs? And they published this book in 1937, where they actually began to think about, what could you do in bio-reactors to grow whole organs? We've come a long way since then. I'm going to share with you some of the exciting work that's going on.
Но преди това бих искал да споделя депресията си относно системата за здравеопазване и нуждата от това с вас. В много от разговорите вчера стана дума за подобряване качеството на живота и намаляване на бедността. И по същество удължаване на продължителността на живота по цял свят. Едно от предизвикателствата е, че колкото сме по-богати, толкова по-дълго живеем. А колкото по-дълго живеем, толкова по-скъпо е да се грижим за болестите си с остаряването ни.
But before doing that, what I'd like to do is share my depression about the health care system and the need for this with you. Many of the talks yesterday talked about improving the quality of life, and reducing poverty, and essentially increasing life expectancy all around the globe. One of the challenges is that the richer we are, the longer we live. And the longer we live, the more expensive it is to take care of our diseases as we get older.
Това просто е богатството на една страна срещу процента население над 65-годишна възраст. По същество се вижда, че колкото по-богата е една страна, толкова по-стари са хората в нея. Защо това е важно? И защо това е особено драматично предизвикателство в момента? Ако средната възраст на населението е 30 години, тогава средностатистическият вид болест, който трябва да се лекува, е може би счупен глезен от време на време, може би малко астма. Ако средната възраст във вашата страна е от 45 до 55 години, средностатистическият човек е изправен пред диабет, ранно атакуващ диабет, сърдечни заболявания, коронарно-артериални заболявания. Неща, които са по същество по-трудни за лекуване и много по-скъпи за лекуване.
This is simply the wealth of a country versus the percent of population over the age of 65. And you can basically see that the richer a country is, the older the people are within it. Why is this important? And why is this a particularly dramatic challenge right now? If the average age of your population is 30, then the average kind of disease that you have to treat is maybe a broken ankle every now and again, maybe a little bit of asthma. If the average age in your country is 45 to 55, now the average person is looking at diabetes, early-onset diabetes, heart failure, coronary artery disease -- things that are inherently more difficult to treat, and much more expensive to treat.
Само погледнете демографските данни в САЩ тук. Това е от "Съединени американски щати". През 1930 г. е имало по 41 работници на един пенсионер. 41 души, които по същество са били извън истинска болест, плащащи за единствения пенсионер, който е преживявал изтощителна болест. През 2010 г. - двама работещи на пенсионер в САЩ. Така е и във всяка индустриализирана, богата страна в света. Как всъщност може да си позволиш да лекуваш пациенти, щом реалността на остаряването изглежда така?
Just have a look at the demographics in the U.S. here. This is from "The Untied States of America." In 1930, there were 41 workers per retiree. 41 people who were basically outside of being really sick, paying for the one retiree who was experiencing debilitating disease. In 2010, two workers per retiree in the U.S. And this is matched in every industrialized, wealthy country in the world. How can you actually afford to treat patients when the reality of getting old looks like this?
Това е възрастта срещу цената на здравеопазването. И виждате, че около 45-годишна възраст, 40 до 45 има внезапен скок в цената на здравеопазването. Всъщност е твърде интересно - ако се правят правилните проучвания, може да се разгледа колко харчите вие като индивид за собственото си здравеопазване, разпределено през живота ви. Около седем години преди да сте на път да умрете, има скок. И всъщност може... (Смях) ...няма да навлизаме в това. (Смях)
This is age versus cost of health care. And you can see that right around age 45, 40 to 45, there's a sudden spike in the cost of health care. It's actually quite interesting. If you do the right studies, you can look at how much you as an individual spend on your own health care, plotted over your lifetime. And about seven years before you're about to die, there's a spike. And you can actually -- (Laughter) -- we won't get into that. (Laughter)
Има много малко неща - много малко неща, които всъщност могат да се направят, които биха променили начина, по който може да се лекуват тези типове болести и да се преживее онова, което бих нарекъл здравословно остаряване. Бих предположил, че има четири неща. И нито едно от тези неща не включва застрахователна система или законова система. Всичко, което правят тези неща, е да променят това кой плаща. Те всъщност не променят онова, което е същинската стойност на лечението.
There are very few things, very few things that you can really do that will change the way that you can treat these kinds of diseases and experience what I would call healthy aging. I'd suggest there are four things, and none of these things include an insurance system or a legal system. All those things do is change who pays. They don't actually change what the actual cost of the treatment is.
Едно нещо, което може да се направи, е да не се лекува. Може да се въведе режим за здравеопазване. Вече няма да говорим за това. Твърде потискащо е. Може да се предотвратява. Очевидно, много средства трябва да се вложат за превенция.
One thing you can do is not treat. You can ration health care. We won't talk about that anymore. It's too depressing. You can prevent. Obviously a lot of monies should be put into prevention.
Но вероятно най-интересна, поне за мен, и най-важна е идеята да се диагностицира една болест на много по-ранен етап от развитието й, а после да се третира болестта, за да се лекува, вместо да се третира симптом. Мислете за това с оглед на диабета, например. Какво правим с диабета днес? Диагностицираме болестта в крайна сметка, щом веднъж стане симптоматична, а после третираме симптома 10, 20, 30, 40 години. Справяме се добре. Инсулинът е доста добра терапия. Но в крайна сметка той спира да действа, и диабетът води до предвидима атака на изтощителна болест.
But perhaps most interesting, to me anyway, and most important, is the idea of diagnosing a disease much earlier on in the progression, and then treating the disease to cure the disease instead of treating a symptom. Think of it in terms of diabetes, for instance. Today, with diabetes, what do we do? We diagnose the disease eventually, once it becomes symptomatic, and then we treat the symptom for 10, 20, 30, 40 years. And we do OK. Insulin's a pretty good therapy. But eventually it stops working, and diabetes leads to a predictable onset of debilitating disease.
Защо не можем просто да инжектираме панкреаса с нещо, за да регенерираме панкреаса на ранен етап от болестта, вероятно дори преди да стане симптоматичен? Може да е малко скъпо по времето, когато го правим, но ако подейства, наистина ще можем да направим нещо различно.
Why couldn't we just inject the pancreas with something to regenerate the pancreas early on in the disease, perhaps even before it was symptomatic? And it might be a little bit expensive at the time that we did it, but if it worked, we would truly be able to do something different.
Според мен това видео предава понятието, за което говоря, доста драматично. Това е тритон, чийто крайник израства повторно. Ако един тритон може да прави такова нещо, защо ние да не можем? Всъщност ще ви покажа някои по-важни детайли за регенерацията на крайници след малко. Но онова, за което говорим в регенеративната медицина, е да правим това във всяка органова система от тялото, за тъкани и за самите органи. И така, днешната реалност е, че ако се разболеем, посланието е - ще третираме симптомите ти, а ти трябва да се приспособиш към нов начин на живот.
This video, I think, gets across the concept that I'm talking about quite dramatically. This is a newt re-growing its limb. If a newt can do this kind of thing, why can't we? I'll actually show you some more important features about limb regeneration in a moment. But what we're talking about in regenerative medicine is doing this in every organ system of the body, for tissues and for organs themselves. So today's reality is that if we get sick, the message is we will treat your symptoms, and you need to adjust to a new way of life.
Ще поставя това пред вас утре, а утре вече можем да спорим, но е в рамките на предвидимото бъдеще... ще говорим за регенеративна рехабилитация. Тук горе има протеза за крайник, всъщност подобна на онази, която войникът, завърнал се от Ирак... има 370 войници, върнали се от Ирак, които са изгубили крайници. Представете си, ако вместо да се сблъскат с това, те всъщност можеха да се изправят пред регенерация на този крайник. Това е налудничава представа. Ще ви покажа къде сме в момента в работата към тази представа.
I would pose to you that tomorrow -- and when tomorrow is we could debate, but it's within the foreseeable future -- we will talk about regenerative rehabilitation. There's a limb prosthetic up here, similar actually one on the soldier that's come back from Iraq. There are 370 soldiers that have come back from Iraq that have lost limbs. Imagine if instead of facing that, they could actually face the regeneration of that limb. It's a wild concept. I'll show you where we are at the moment in working towards that concept.
Но тя е приложима, отново, към всяка органова система. Как можем да направим това? Начинът да се направи това е да се развие разговор с тялото. Нужно е да се научим да говорим езика на тялото. И да включваме процеси, които сме знаели как да извършваме, когато сме били фетус. При фетуса на един бозайник, ако изгуби крайник през първия триместър на бременност, този крайник отново ще израстне. Значи нашата ДНК има капацитета да изпълнява този вид заздравителни механизми. Това е естествен процес, но е изгубен с остаряването ни. При едно дете, преди около шестмесечна възраст, ако изгуби върха на пръста си при инцидент, върхът на пръста отново израства. Докато станат петгодишни, вече няма да са в състояние да направят това.
But it's applicable, again, to every organ system. How can we do that? The way to do that is to develop a conversation with the body. We need to learn to speak the body's language. And to switch on processes that we knew how to do when we were a fetus. A mammalian fetus, if it loses a limb during the first trimester of pregnancy, will re-grow that limb. So our DNA has the capacity to do these kinds of wound-healing mechanisms. It's a natural process, but it is lost as we age. In a child, before the age of about six months, if they lose their fingertip in an accident, they'll re-grow their fingertip. By the time they're five, they won't be able to do that anymore.
Значи, за да влезем в този разговор с тялото, е нужно да говорим езика на тялото. Има дадени инструменти в нашата кутия, които ни позволяват да правим това днес. Ще ви дам един пример за три от тези инструменти, чрез които да се разговаря с тялото.
So to engage in that conversation with the body, we need to speak the body's language. And there are certain tools in our toolbox that allow us to do this today. I'm going to give you an example of three of these tools through which to converse with the body.
Първият са клетъчните терапии. Явно се изцеляваме при естествен процес, използвайки клетки, за да вършат повечето от работата. Поради това, ако можем да открием правилните клетки и да ги имплантираме в тялото, те може да извършат изцелението. Второ, можем да използваме материали. Чухме вчера за важността на новите материали. Ако можем да изобретяваме материали, разработваме материали, или да извличаме материали от една естествена околна среда, тогава може да сме в състояние чрез тези материали да склоним тялото да се изцелява само. И най-сетне, може да сме в състояние да използваме "умни" устройства, които да свалят товара на работата от тялото и да му позволят да се изцелява.
The first is cellular therapies. Clearly, we heal ourselves in a natural process, using cells to do most of the work. Therefore, if we can find the right cells and implant them in the body, they may do the healing. Secondly, we can use materials. We heard yesterday about the importance of new materials. If we can invent materials, design materials, or extract materials from a natural environment, then we might be able to have those materials induce the body to heal itself. And finally, we may be able to use smart devices that will offload the work of the body and allow it to heal.
Ще ви покажа пример за всеки от тези, и ще започна с материалите. Стив Бадилак - който е в Университета в Питсбърг - преди около десетилетие имал забележителна идея. Идеята била, че тънкото черво на едно прасе, ако изхвърлиш всички клетки и ако го направиш по начин, който му позволява да остави биологично активно, може да съдържа всички необходими фактори и сигнали, които биха сигнализирали на тялото да се изцелява само. И задал много важен въпрос. Задал въпроса: ако взема този материал, който е естествен материал, обикновено причиняващ изцеление в тънкото черво, и го поставя някъде другаде върху тялото на едно лице, дали той би дал тъканно-специфичен отклик, или би направил тънко черво, ако се опитам да направя ново ухо?
I'm going to show you an example of each of these, and I'm going to start with materials. Steve Badylak -- who's at the University of Pittsburgh -- about a decade ago had a remarkable idea. And that idea was that the small intestine of a pig, if you threw away all the cells, and if you did that in a way that allowed it to remain biologically active, may contain all of the necessary factors and signals that would signal the body to heal itself. And he asked a very important question. He asked the question, if I take that material, which is a natural material that usually induces healing in the small intestine, and I place it somewhere else on a person's body, would it give a tissue-specific response, or would it make small intestine if I tried to make a new ear?
Не бих ви разказвал тази история, ако не беше завладяваща. Снимката, която съм на път да ви покажа... (Смях) ...е завладяваща снимка. Но за онези от вас, които са дори най-леко гнусливи... дори да не ви харесва да го признаете пред приятелите си... светлините са угасени. Това е добър момент да погледнете към краката си, да проверите своето "Блекбери", да правите каквото и да е друго, освен да гледате екрана. (Смях)
I wouldn't be telling you this story if it weren't compelling. The picture I'm about to show you is a compelling picture. (Laughter) However, for those of you that are even the slightest bit squeamish -- even though you may not like to admit it in front of your friends -- the lights are down. This is a good time to look at your feet, check your Blackberry, do anything other than look at the screen. (Laughter)
Онова, което ще ви покажа, е диабетична язва. И въпреки че... добре е да се посмеем, преди да погледнем това. Това е реалността на диабета. Мисля, че много пъти, щом чуем за диабетици, диабетични язви, просто не свързваме язвата с окончателното лечение, което е ампутация, ако тя не може да се излекува. И така, сега ще пусна кадъра. Няма да е за дълго. Това е диабетична язва. Трагично е. Лечението за това е ампутация. Това е една възрастна дама. Тя има рак на черния дроб, както и диабет, и е решила да умре с онова, което е останало от тялото й, непокътнато.
What I'm about to show you is a diabetic ulcer. And although -- it's good to laugh before we look at this. This is the reality of diabetes. I think a lot of times we hear about diabetics, diabetic ulcers, we just don't connect the ulcer with the eventual treatment, which is amputation, if you can't heal it. So I'm going to put the slide up now. It won't be up for long. This is a diabetic ulcer. It's tragic. The treatment for this is amputation. This is an older lady. She has cancer of the liver as well as diabetes, and has decided to die with what' s left of her body intact.
Тази дама решила, след години опити за лечение на тази язва, че ще опита тази нова терапия, изобретена от Стив. Така изглеждала раната 11 седмици по-късно. Този материал съдържал само натурални сигнали. И този материал е подтикнал тялото да превключи отново към изцелителен отклик, който не е имало преди.
And this lady decided, after a year of attempted treatment of that ulcer, that she would try this new therapy that Steve invented. That's what the wound looked like 11 weeks later. That material contained only natural signals. And that material induced the body to switch back on a healing response that it didn't have before.
Ще има още един-два мъчителни кадъра за онези от вас... ще ви кажа кога може да погледнете отново. Това е кон. Конят не изпитва болка. Ако конят изпитваше болка, не бих ви показвал този кадър. Конят просто има още една ноздра, която се е развила заради инцидент при яздене. Само няколко седмици след лечение... в този случай вземане на този материал, превръщането му в гел и покриване на тази област, а после повтаряне на лечението няколко пъти... и раната на коня зараства. Ако прегледате тази област с ултразвук, би изглеждала страхотно.
There's going to be a couple more distressing slides for those of you -- I'll let you know when you can look again. This is a horse. The horse is not in pain. If the horse was in pain, I wouldn't show you this slide. The horse just has another nostril that's developed because of a riding accident. Just a few weeks after treatment -- in this case, taking that material, turning it into a gel, and packing that area, and then repeating the treatment a few times -- and the horse heals up. And if you took an ultrasound of that area, it would look great.
Ето един делфин, при който перката е била повторно прикачена. Сега има 400 000 пациенти по света, които са използвали този материал за зарастване на раните си. Би ли могло да се регенерира крайник? DARPA току-що дадоха на Стив 15 милиона долара, за да води проект с осем институции, да започне процеса на задаване на този въпрос.
Here's a dolphin where the fin's been re-attached. There are now 400,000 patients around the world who have used that material to heal their wounds. Could you regenerate a limb? DARPA just gave Steve 15 million dollars to lead an eight-institution project to begin the process of asking that question.
Ще ви покажа снимката за 15 милиона долара. Това е 78-годишен мъж, изгубил върха на пръста си. Помните, че споменах преди за децата, които губят върховете на пръстите си. Ето така изглежда след лечение. Това се случва днес. Това е клинично приложимо днес. Има материали, които правят това. Това са кръпките на сърцето.
And I'll show you the 15 million dollar picture. This is a 78 year-old man who's lost the end of his fingertip. Remember that I mentioned before the children who lose their fingertips. After treatment that's what it looks like. This is happening today. This is clinically relevant today. There are materials that do this. Here are the heart patches.
Но може ли да се отиде малко по-далеч? Може ли, да кажем, вместо използване на материал, мога ли да взема някои клетки наред с материала и да премахна повредено парче тъкан, да поставя био-разграждащ се материал там? Виждате тук малко парченце сърдечен мускул, биещо в съд. Това е било направено от Теруо Окано в Женската болница в Токио. Той всъщност може да отглежда биеща тъкан в съд. Охлажда съда, той променя свойствата си и я обелва направо от съда. Направо страхотно.
But could you go a little further? Could you, say, instead of using material, can I take some cells along with the material, and remove a damaged piece of tissue, put a bio-degradable material on there? You can see here a little bit of heart muscle beating in a dish. This was done by Teruo Okano at Tokyo Women's Hospital. He can actually grow beating tissue in a dish. He chills the dish, it changes its properties and he peels it right out of the dish. It's the coolest stuff.
Сега ще ви покажа клетъчно-базирана регенерация. Онова, което ще ви покажа тук, са стволови клетки, отстранявани от бедрото на пациент. Отново, ако сте гнусливи, няма да искате да гледате. Но това е някак страхотно. Това е байпас операция, точно като онази, направена на Ал Гор, с една разлика. В този случай, накрая на байпас операцията, ще видите стволовите клетки от пациента, отстранени в началото на процедурата, да се инжектират директно в сърцето на пациента. Стоя тук горе, защото в един момент ще ви покажа точно в колко ранна фаза е тази технология. Ето ги стволовите клетки, отиват право в биещото сърце на пациента. Ако гледате наистина внимателно, точно около тази точка всъщност ще видите обратна струя. Виждате клетките отново да излизат. Нужни са ни всякакви видове нови технологии, нови устройства, за да поставим клетките на правилното място в правилното време.
Now I'm going to show you cell-based regeneration. And what I'm going to show you here is stem cells being removed from the hip of a patient. Again, if you're squeamish, you don't want to watch. But this one's kind of cool. So this is a bypass operation, just like what Al Gore had, with a difference. In this case, at the end of the bypass operation, you're going to see the stem cells from the patient that were removed at the beginning of the procedure being injected directly into the heart of the patient. And I'm standing up here because at one point I'm going to show you just how early this technology is. Here go the stem cells, right into the beating heart of the patient. And if you look really carefully, it's going to be right around this point you'll actually see a back-flush. You see the cells coming back out. We need all sorts of new technology, new devices, to get the cells to the right place at the right time.
Само малко данни - съвсем мъничко данни. Това беше произволна проба. По това време това беше N 20. Сега има N около 100. По същество, ако вземеш един изключително болен пациент и му направиш байпас, при него има малко подобрение. Ако му дадеш стволови клетки, както и байпас, точно за тези пациенти, те сават асимптоматични. Тези са на две години разстояние. Най-страхотното би било, ако може да се диагностицира болестта рано и да се предотврати атаката на болестта към лошо състояние.
Just a little bit of data, a tiny bit of data. This was a randomized trial. At this time this was an N of 20. Now there's an N of about 100. Basically, if you take an extremely sick patient and you give them a bypass, they get a little bit better. If you give them stem cells as well as their bypass, for these particular patients, they became asymptomatic. These are now two years out. The coolest thing would be is if you could diagnose the disease early, and prevent the onset of the disease to a bad state.
Това е същата процедура, но сега извършена с минимална намеса, със само три дупки в тялото, където вземат сърцето и просто инжектират стволови клетки чрез лапароскопична процедура. Ето ги клетките. Нямаме време да навлизаме във всички подробности, но по същество, това също действа. Може да се взема по-малко болни пациенти и да се върнат към почти асимптоматично състояние чрез този вид терапия.
This is the same procedure, but now done minimally invasively, with only three holes in the body where they're taking the heart and simply injecting stem cells through a laparoscopic procedure. There go the cells. We don't have time to go into all of those details, but basically, that works too. You can take patients who are less sick, and bring them back to an almost asymptomatic state through that kind of therapy.
Ето още един пример за терапия със стволови клетки, която все още не е твърде клинична, но мисля, че много скоро ще бъде. Това е работата на Кейси Мара от Питсбърг, наред с ред колеги по света. Те са решили, че тази течност от липосукция, която... в Съединените щати имаме много течност от липосукция. (Смях) Това е страхотен източник на стволови клетки. Тази течност от липосукция е натъпкана със стволови клетки. Значи може да влезете, да си направите прибиране на корема. Излиза течността от липосукцията, и в този случай стволовите клетки са изолирани и превърнати в неврони. Всичко е направено в лабораторията. Мисля, че твърде скоро ще се вижда третиране на пациенти със собствените им мастно-извлечени, или тлъстинно извлечени, стволови клетки.
Here's another example of stem-cell therapy that isn't quite clinical yet, but I think very soon will be. This is the work of Kacey Marra from Pittsburgh, along with a number of colleagues around the world. They've decided that liposuction fluid, which -- in the United States, we have a lot of liposuction fluid. (Laughter) It's a great source of stem cells. Stem cells are packed in that liposuction fluid. So you could go in, you could get your tummy-tuck. Out comes the liposuction fluid, and in this case, the stem cells are isolated and turned into neurons. All done in the lab. And I think fairly soon, you will see patients being treated with their own fat-derived, or adipose-derived, stem cells.
Говорих преди за употребата на устройство за драматична промяна на начина, по който третираме болестта. Ето само един пример, преди да приключа. Това е еднакво трагично. Имаме много трайно и сърцераздирателно партньорство с колегите ни в Института за хирургически изследвания при армията на САЩ, които трябва да лекуват сега 11 000 момчета, завърнали се от Ирак. Много от тези пациенти са много жестоко обгорели.
I talked before about the use of devices to dramatically change the way we treat disease. Here's just one example before I close up. This is equally tragic. We have a very abiding and heartbreaking partnership with our colleagues at the Institute for Surgical Research in the US Army, who have to treat the now 11,000 kids that have come back from Iraq. Many of those patients are very severely burned.
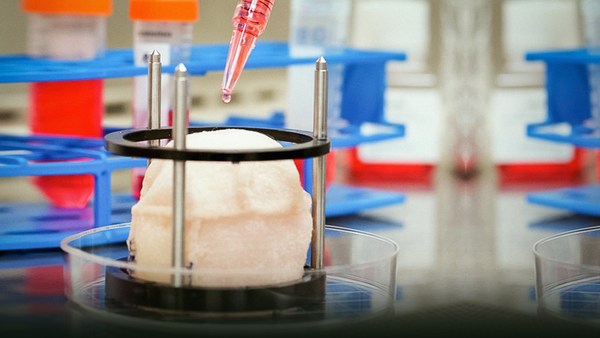
А ако има нещо, научено за изгарянето, е, че не знаем как да го третираме. Всичко, което е правено за третиране на изгаряне... по същество приемаме СОД (супероксид оксидоредуктаза) подход. Правим нещо ето тук, а после го трансплантираме на мястото на раната и се опитваме да накараме двете да се съединят. В този случай тук е бил проектиран нов, носим биореактор... трябва да бъде тестван клинично по-късно тази година в Института за системи и роботика от Йорг Герлах в Питсбърг. Този биореактор ще легне в леглото на раната. Оръдието, което виждате там, пръска клетки. То ще пръска клетки над тази област. Реакторът ще служи за оплождане на средата, в същото време и за внасяне на други неща и поради това ще засеем тази ливада, в противовес на това да опитваме СОД подход. Това е напълно различен начин да се прави.
And if there's anything that's been learned about burn, it's that we don't know how to treat it. Everything that is done to treat burn -- basically we do a sodding approach. We make something over here, and then we transplant it onto the site of the wound, and we try and get the two to take. In this case here, a new, wearable bio-reactor has been designed -- it should be tested clinically later this year at ISR -- by Joerg Gerlach in Pittsburgh. And that bio-reactor will lay down in the wound bed. The gun that you see there sprays cells. That's going to spray cells over that area. The reactor will serve to fertilize the environment, deliver other things as well at the same time, and therefore we will seed that lawn, as opposed to try the sodding approach. It's a completely different way of doing it.
Моите 18 минути изтичат. Затова, нека приключа с някои добри новини, и може би малко лоши новини. Добрата новина е, че това се случва днес. Това е много значима работа. Явно образите някак предават това. Невероятно трудно е, защото е във висша степен интердисциплинарно. Почти всяка област от науката, техниката и клиничната практика е включена в опитите да се случи това.
So my 18 minutes is up. So let me finish up with some good news, and maybe a little bit of bad news. The good news is that this is happening today. It's very powerful work. Clearly the images kind of get that across. It's incredibly difficult because it's highly inter-disciplinary. Almost every field of science engineering and clinical practice is involved in trying to get this to happen.
Ред правителства и ред региони признаха, че това е нов начин за третиране на болестта. Японското правителство вероятно бе първото, когато решиха първо да инвестират 3 милиарда, а после - още 2 милиарда в тази област. Това не е случайност. Япония е най-старата страна на Земята, по отношение на средната й възраст. Имат нужда това да сработи, или здравната им система загива. Затова влагат много стратегически инвестиции, съсредоточени в тази област. Европейският съюз - същото. Китай - същото. Китай току-що основа национален център за тъканно инженерство. Бюджетът за първата година беше 250 милиона американски долара.
A number of governments, and a number of regions, have recognized that this is a new way to treat disease. The Japanese government were perhaps the first, when they decided to invest first 3 billion, later another 2 billion in this field. It's no coincidence. Japan is the oldest country on earth in terms of its average age. They need this to work or their health system dies. So they're putting a lot of strategic investment focused in this area. The European Union, same thing. China, the same thing. China just launched a national tissue-engineering center. The first year budget was 250 million US dollars.
В Съединените щати приложихме донякъде различен подход. Ние... (Смях) ...о, за да дойде Ал Гор и да бъде в реалния свят като президент. Имахме различен подход. А подходът по същество беше просто някак да финансираме нещата при появата им. Но нямаше стратегическо инвестиране за включването на всички необходими неща и фокусирането им по внимателен начин.
In the United States we've had a somewhat different approach. (Laughter) Oh, for Al Gore to come and be in the real world as president. We've had a different approach. And the approach has basically been to just sort of fund things as they come along. But there's been no strategic investment to bring all of the necessary things to bear and focus them in a careful way.
Ще приключа с един цитат, може би малко евтин, от директора на Националния здравен институт, много чаровен мъж. С Джей Ваканти от Харвард отидохме да посетим него и ред от директорите в неговия институт преди няколко месеца, за да се опитаме да го убедим, че е време да вземе само малка част от онези 27,5 милиарда долара, които ще получи догодина, и да ги съсредоточи по стратегически начин за ускоряване на скоростта, с която тези неща стигат до пациентите. В края на една много сприхава среща, ето какво каза директорът на Националния здравен институт: "Вашата визия е по-голяма от нашия апетит". Бих искал да приключа, като кажа, че никой няма да промени нашата визия, но заедно можем да променим неговия апетит. Благодаря.
And I'm going to finish up with a quote, maybe a little cheap shot, at the director of the NIH, who's a very charming man. Myself and Jay Vacanti from Harvard went to visit with him and a number of his directors of his institute just a few months ago, to try and convince him that it was time to take just a little piece of that 27.5 billion dollars that he's going to get next year and focus it, in a strategic way, to make sure we can accelerate the pace at which these things get to patients. And at the end of a very testy meeting, what the NIH director said was, "Your vision is larger than our appetite." I'd like to close by saying that no one's going to change our vision, but together we can change his appetite. Thank you.