سأتحدث إليكم اليوم آملًا في تحويل الخوف إلى أمل. عندما نذهب إلى الطبيب اليوم وندخل إليه. توجد كلمات لا نرغب بسماعها. هناك كلمات نخاف منها بحق السكري، السرطان، الرعشة الغير إرادية، الزهايمر فشل في القلب .. فشل في الرئة أشياء نعرف أنها أمراض مستعصية لا يمكن فعل الكثير للعلاج منها
I'm going to talk to you today about hopefully converting fear into hope. When we go to the physician today -- when we go to the doctor's office and we walk in, there are words that we just don't want to hear. There are words that we're truly afraid of. Diabetes, cancer, Parkinson's, Alzheimer's, heart failure, lung failure -- things that we know are debilitating diseases, for which there's relatively little that can be done.
وما أريد أن أقدمه لكم اليوم هو طريقة مختلفة للتفكير في طريقة معالجة الأمراض المستعصية وأهميتها ولماذا بدونه -ربما- سينهار نظامنا الصحي إن كنتم ترون أنه لم ينهار بعد وأين نحن اليوم في الناحية الطبية وأين بإمكاننا أن نكون غدًا؟ وما هي العوائق التي ستقف بوجهنا؟ وسأقوم بمناقشة ذلك في 18 دقيقة. أعدكم.
And what I want to lay out for you today is a different way of thinking about how to treat debilitating disease, why it's important, why without it perhaps our health care system will melt down if you think it already hasn't, and where we are clinically today, and where we might go tomorrow, and what some of the hurdles are. And we're going to do all of that in 18 minutes, I promise.
أريد أن أبدأ بعرض تلك الشريحة لأن تلك الشريحة تخبر بشكل ما عن نظرة مجلة العلوم للأمر. هذا أحد أعداد عام 2002 وفيه نشروا العديد من المقالات المختلفة عن الإنسان الذي يستخدم الأعضاء الآلية كان موضوع العدد هو الطب التجديدي الطب التجديدي مفهوم في غاية البساطة يمكن لأي شخص أن يفهمه ببساطة، يسرّع الوتيرة التي يشفي بها الجسم نفسه في فترة زمنية مناسبة ونحن نعلم كيف نقوم بهذا بواسطة طرق عديدة معروضة هنا نحن نعلم أنه إذا كان مفصل الورك تالفًا نستطيع أن نستبدله بآخر صناعي وهذه هي الفكرة التي وضعتها مجلة "ساينس" على غلاف المجلة
I want to start with this slide, because this slide sort of tells the story the way Science Magazine thinks of it. This was an issue from 2002 that they published with a lot of different articles on the bionic human. It was basically a regenerative medicine issue. Regenerative medicine is an extraordinarily simple concept that everybody can understand. It's simply accelerating the pace at which the body heals itself to a clinically relevant timescale. So we know how to do this in many of the ways that are up there. We know that if we have a damaged hip, you can put an artificial hip in. And this is the idea that Science Magazine used on their front cover.
هذا هو النقيض للطب التجديدي. إنه ليس طباً تجديدياً الطب التجديدي هو ما طرحته مجلة "بيزنس ويك" منذ فترة ليست بالبعيدة الفكرة عبارة عن القيام بتعويض الوظيفة المفقودة للأعضاء والأنسجة التالفة بدلًا من القيام بمعالجة الأعراض بالآلات والعقاقير وما شابه –وسأعود إلى تلك النقطة عدة مرات- بدلًا من القيام بذلك، سوف نقوم بإعادة الوظيفة المفقودة للجسم عن طريق إعادة عمل الأعضاء والأنسجة التالفة فتكون النتيجة في نهاية العلاج هي أن تعود سليمًا كما كنت قبل العلاج
This is the complete antithesis of regenerative medicine. This is not regenerative medicine. Regenerative medicine is what Business Week put up when they did a story about regenerative medicine not too long ago. The idea is that instead of figuring out how to ameliorate symptoms with devices and drugs and the like -- and I'll come back to that theme a few times -- instead of doing that, we will regenerate lost function of the body by regenerating the function of organs and damaged tissue. So that at the end of the treatment, you are the same as you were at the beginning of the treatment.
يوجد القليل من الأفكار الجيدة – إذا وافقتم على أنها أفكار جيدة- أفكار قليلة جيدة وشاملة حقًا. وهذا هو نفس الشئ. إذا نظرت إلى الوراء في التاريخ. كان تشارلز ليندبيرج المعروف بقيادة الطائرات هو أول مَن فكر مع ألكسس كاريل –أحد الحائزين على جائزة نوبل- من معهد روكفلر في إمكانية زراعة الأعضاء ونشرا ذلك في كتاب عام 1937 حيث بدءا التفكير في الذي يمكن فعله في المفاعلات الحيوية لينمو العضو كاملًا؟ أمضينا وقتًا طويلًا في دراسة الوسائل والآن سأطلعكم على بعض من العمل المثمر الذي لا يزال مستمرًا
Very few good ideas -- if you agree that this is a good idea -- very few good ideas are truly novel. And this is just the same. If you look back in history, Charles Lindbergh, who was better known for flying airplanes, was actually one of the first people along with Alexis Carrel, one of the Nobel Laureates from Rockefeller, to begin to think about, could you culture organs? And they published this book in 1937, where they actually began to think about, what could you do in bio-reactors to grow whole organs? We've come a long way since then. I'm going to share with you some of the exciting work that's going on.
ولكن قبل أن أقوم بذلك, ما أحب أن أفعله الآن هو أن أشارككم حزني الشديد عن نظام العناية الصحية و الحوجة لذلك معكم. تناولت بعض المحادثات بالأمس موضوع تحسين مستوى المعيشة وتقليل الفقر مما يعني بالضرورة زيادة معدل الأعمار حول العالم. من إحدى التحديات التي نواجهها هي أننا كلما ازددنا غنى كلما عشنا فترة أطول وكلما عشنا فترة أطول كلما تطلب الأمر المزيد من المال للعناية بالأمراض التي نصاب بها كلما نكبر في السن
But before doing that, what I'd like to do is share my depression about the health care system and the need for this with you. Many of the talks yesterday talked about improving the quality of life, and reducing poverty, and essentially increasing life expectancy all around the globe. One of the challenges is that the richer we are, the longer we live. And the longer we live, the more expensive it is to take care of our diseases as we get older.
هذه ببساطة ثروة الدولة مقابل نسبة السكان الذين تزيد أعمارهم عن ال 65. ويمكنك أن ترى بوضوح أنه كلما ازدادت الدولة في الثروة المالية، كلما وجدت الناس فيها أطول أعمارًا. لماذا يعتبر ذلك الموضوع مهمًا؟ ولماذا يعتبر ذلك تحديًا هائلًا حاليًا؟ إذا كان متوسط العمر للسكان 30 سنة فستجد أن أغلب الأمراض التي عليك علاجها تكون ما بين كاحل مكسور من وقت لآخر و بعض حالات الربو أما إذا كان متوسط الأعمار في الدولة ما بين 45 إلى 55 فستكون الأمراض الذي يصاب بها الشخص العادي ما بين مرض السكر العادي أو الذي يظهر في وقت مبكر، فشل في القلب، داء شريان القلب التاجي أمراض معروف أنه يصعب الشفاء منها وأن علاجها يتطلب الكثير من المال
This is simply the wealth of a country versus the percent of population over the age of 65. And you can basically see that the richer a country is, the older the people are within it. Why is this important? And why is this a particularly dramatic challenge right now? If the average age of your population is 30, then the average kind of disease that you have to treat is maybe a broken ankle every now and again, maybe a little bit of asthma. If the average age in your country is 45 to 55, now the average person is looking at diabetes, early-onset diabetes, heart failure, coronary artery disease -- things that are inherently more difficult to treat, and much more expensive to treat.
لنلقي نظرة على الديموغرافيا في أمريكا هنا. هذه من الولايات المتحدة الأمريكية في عام 1930 كان هناك 41 عاملًا مقابل متقاعد واحد 41 كانوا غير مرضى مما يعني أن الإنفاق كان على الشخص الواحد الذي يعاني من مرض عضال في 2010 ستكون النسبة 2 إلى 1 وهذا يحدث في كل دولة صناعية وغنية كيف يمكن في الحقيقة أن توفر النقود لعلاج المرضى عندما تكون الحقائق بهذا الشكل ؟
Just have a look at the demographics in the U.S. here. This is from "The Untied States of America." In 1930, there were 41 workers per retiree. 41 people who were basically outside of being really sick, paying for the one retiree who was experiencing debilitating disease. In 2010, two workers per retiree in the U.S. And this is matched in every industrialized, wealthy country in the world. How can you actually afford to treat patients when the reality of getting old looks like this?
هذا هو العمر مقابل ثمن الرعاية الصحية وتستطيعون رؤية ذلك بوضوح عند سن ال45 من 40 إلى 45 هناك طفرة مفاجئة في تكاليف العناية الصحية إنه في الواقع على قدر كبير من الأهمية إذا تم إجراء الدراسات بشكل صحيح ستستطيع معرفة كم يتطلب علاجك كفرد للعناية بك صحيًا مناظر ل طوال حياتك وحوالي 7 سنوات قبل وفاتك. يوجد طفرة وفي الحقيقة تستطيع (ضحك ) لن ندخل في هذا الأمر (ضحك)
This is age versus cost of health care. And you can see that right around age 45, 40 to 45, there's a sudden spike in the cost of health care. It's actually quite interesting. If you do the right studies, you can look at how much you as an individual spend on your own health care, plotted over your lifetime. And about seven years before you're about to die, there's a spike. And you can actually -- (Laughter) -- we won't get into that. (Laughter)
يوجد القليل من الأشياء التي يمكنك فعلها لتغيير الطريقة التي يمكن بها معالجة ذلك النوع من الأمراض وأن تعيش –ما يمكن تسميته ب شيخوخة صحية. سوف أقوم بطرح 4 أشياء هنا ولن يكون من بينها نظام التأمين أو النظام القضائي كل ما ستقوم تلك الأشياء بفعله هو تغيير الأشخاص الذين سيقومون بالدفع ولن يغيروا السعر الحقيقي للعلاج
There are very few things, very few things that you can really do that will change the way that you can treat these kinds of diseases and experience what I would call healthy aging. I'd suggest there are four things, and none of these things include an insurance system or a legal system. All those things do is change who pays. They don't actually change what the actual cost of the treatment is.
أول شيء هو ألا تقوم بالتداوي. يمكن أن تقوم بالحد من العناية الصحية ولن نتكلم عن ذلك الأمر كثيرًا فهو أمر يسبب الاكتئاب يمكنك أن تقي نفسك ما أريد قوله هو أن من الأفضل استثمار الكثير من المال في الوقاية
One thing you can do is not treat. You can ration health care. We won't talk about that anymore. It's too depressing. You can prevent. Obviously a lot of monies should be put into prevention.
والشيء الأكثر إثارة –بالنسبة لي على كل حال- والأكثر أهمية، هي فكرة التشخيص المبكر للمرض ومن ثم التدخل لمعالجة المرض نفسه بدلًا من معالجة الأعراض فكروا فيها بالنسبة لمرض السكر على سبيل المثال اليوم عندما نكتشف المرض عند المصاب، ماذا نفعل؟ نقوم بتشخيص المرض نقوم بتشخيص المرض وبمجرد ظهور أعراضه نبدأ بمعالجة الأعراض ل 10 و 20 و 30 و 40 سنة وتكون النتيجة مُرضية فالإنسولين علاج جيد إلى حد ما ولكن تكون النتيجة أن يتوقف الجسم عن إفرازه ويكون المتوقع عند الإصابة بمرض السكر هو الإصابة بالأمراض المستعصية
But perhaps most interesting, to me anyway, and most important, is the idea of diagnosing a disease much earlier on in the progression, and then treating the disease to cure the disease instead of treating a symptom. Think of it in terms of diabetes, for instance. Today, with diabetes, what do we do? We diagnose the disease eventually, once it becomes symptomatic, and then we treat the symptom for 10, 20, 30, 40 years. And we do OK. Insulin's a pretty good therapy. But eventually it stops working, and diabetes leads to a predictable onset of debilitating disease.
لماذا لا نستطيع أن نحقن البنكرياس بشيء لإعادة تحفيز البنكرياس في بداية المرض؟ بل قبل بداية ظهور أعراضه؟ ويمكن أن يكون العلاج بتلك الطريقة أغلى في الثمن ولكن إذا تم العلاج بتلك الطريقة سنكون قادرين على عمل شيء مختلف بحق
Why couldn't we just inject the pancreas with something to regenerate the pancreas early on in the disease, perhaps even before it was symptomatic? And it might be a little bit expensive at the time that we did it, but if it worked, we would truly be able to do something different.
هذا الفيديو-في اعتقادي-يساهم في توصيل الفكرة التي أتحدث عنها بشكل كبير هذا حيوان سمندل الماء وهو يعمل على إعادة نمو طرفه إذا كان سمندل الحيوان يستطيع أن يقوم بإعادة توليد طرفه فلماذا لا نستطيع نحن أن نقوم بذلك؟ سأعرض عليكم الآن بعض الخصائص المهمة عن إعادة توليد الأطراف خلال لحظات ولكن ما نتحدث عنه في الطب التجديدي هو التجديد في كل عضو في الجسم في الأنسجة والأعضاء نفسها حقيقة اليوم هي أنه إذا مرضنا فسوف تتم معالجة الأعراض وعليك أن تقوم بتعديل نمط الحياة
This video, I think, gets across the concept that I'm talking about quite dramatically. This is a newt re-growing its limb. If a newt can do this kind of thing, why can't we? I'll actually show you some more important features about limb regeneration in a moment. But what we're talking about in regenerative medicine is doing this in every organ system of the body, for tissues and for organs themselves. So today's reality is that if we get sick, the message is we will treat your symptoms, and you need to adjust to a new way of life.
سوف أطرح عليكم ذلك الأمر بالغد وعندها نستطيع النقاش ولكنه في المستقبل المتوقع-- سنتحدث عن العلاج التجديدي هذا طرف صناعي هنا مثل هذا الذي عند الجندي الذي عاد من العراق يوجد 370 جندي رجعوا من العراق بأطراف مفقودة تخيلوا الموقف إذا استطاعوا أن يقوموا بإعادة توليد أطرافهم بدلًا من التعامل بالأطراف الصناعية إنه مفهوم صعب. سأريكم التطورات الجارية لتحقيق تلك الفكرة
I would pose to you that tomorrow -- and when tomorrow is we could debate, but it's within the foreseeable future -- we will talk about regenerative rehabilitation. There's a limb prosthetic up here, similar actually one on the soldier that's come back from Iraq. There are 370 soldiers that have come back from Iraq that have lost limbs. Imagine if instead of facing that, they could actually face the regeneration of that limb. It's a wild concept. I'll show you where we are at the moment in working towards that concept.
أؤكد لكم أنها فكرة قابلة للتنفيذ على أي عضو كيف يمكننا القيام بذلك؟ يمكننا القيام بذلك عن طريق تطوير الحوار مع الجسد نحتاج أن نتعلم لغة الجسد وأن نعيد إنشاء العمليات التي كنا نعلم كيف نقوم بها حين كنا أجنة الجنين في بداية مراحله إذا فقد أي طرف خلال أول 3 شهور من الحمل فسوف يقوم بإعادة تنميته إذًا فال DNA لديه القدرة على معالجة ذلك النوع من الجراح إنها عملية طبيعية ولكن يتم فقدانها كلما كبرنا عندما يبلغ الطفل ستة أشهر إذا فقد عقلة من أصابعه في حادث فسوف تنمو تلك العقلة ولكن عندما يكون عمر الطفل 5 أعوام يفقد تلك القدرة إلى الأبد
But it's applicable, again, to every organ system. How can we do that? The way to do that is to develop a conversation with the body. We need to learn to speak the body's language. And to switch on processes that we knew how to do when we were a fetus. A mammalian fetus, if it loses a limb during the first trimester of pregnancy, will re-grow that limb. So our DNA has the capacity to do these kinds of wound-healing mechanisms. It's a natural process, but it is lost as we age. In a child, before the age of about six months, if they lose their fingertip in an accident, they'll re-grow their fingertip. By the time they're five, they won't be able to do that anymore.
فمن أجل أن نبدأ في الحوار مع الجسد نحتاج إلى أن نتحدث لغة الجسد واليوم توجد عدة أدوات في صندوق الأدوات الخاص بنا والتي تمكننا من القيام بالحوار وسأقوم بإعطائكم مثالًا لثلاثة من تلك الأدوات التي من خلالها نستطيع التحدث مع الجسد
So to engage in that conversation with the body, we need to speak the body's language. And there are certain tools in our toolbox that allow us to do this today. I'm going to give you an example of three of these tools through which to converse with the body.
الأداة الأولى هي العلاج الخلوي وتعني بكل بساطة أن نعالج أنفسنا عن طريق عملية طبيعية باستخدام الخلايا التي تقوم بالدور الأكبر في العلاج مما يعني. إذا استطعنا أن نجد الخلايا الصحيحة وزرعهم في الجسد فإن بإمكانهم أن يقوموا بالعلاج ثانيًا: نستطيع استخدام المواد سمعنا بالأمس عن أهمية المواد إذا استطعنا اختراع وتصميم المواد أو استخراجها من البيئة الطبيعية فسيكون بإمكاننا أن نستخدمها في تحفيز الجسد لعلاج نفسه وتكون النهاية، سيكون باستطاعتنا أن نستخدم أجهزة ذكية والتي ستتولى عمل الجسد وستساعده على الشفاء.
The first is cellular therapies. Clearly, we heal ourselves in a natural process, using cells to do most of the work. Therefore, if we can find the right cells and implant them in the body, they may do the healing. Secondly, we can use materials. We heard yesterday about the importance of new materials. If we can invent materials, design materials, or extract materials from a natural environment, then we might be able to have those materials induce the body to heal itself. And finally, we may be able to use smart devices that will offload the work of the body and allow it to heal.
سأريكم الآن مثالًا على كل من هذه الأدوات وسأبدأ بتلك المواد كان لدى ستيف بادلاك –وهو في جامعة بيتسبرج- - منذ عقد مضى فكرة مميزة والفكرة عبارة عن استخدام الأمعاء الدقيقة للخنزير بعد إزالة جميع الخلايا - بطريقة تبقي الأمعاء نشطة بيولوجيًا- قد تحتوي على جميع العناصر والإشارات الكيميائية التي تعطي إشارة للجسم ليعالج نفسه وسأل سؤالًا في غاية الأهمية وهو: إذا أخذت تلك المادة الطبيعية التي تحفز العلاج في الأمعاء الدقيقة وزرعته في مكان آخر من جسد الشخص هل ستستجيب الأنسجة أو هل ستقوم بعمل أمعاء دقيقة بينما كنت أحاول أن أقوم بعمل أذن جديدة ؟
I'm going to show you an example of each of these, and I'm going to start with materials. Steve Badylak -- who's at the University of Pittsburgh -- about a decade ago had a remarkable idea. And that idea was that the small intestine of a pig, if you threw away all the cells, and if you did that in a way that allowed it to remain biologically active, may contain all of the necessary factors and signals that would signal the body to heal itself. And he asked a very important question. He asked the question, if I take that material, which is a natural material that usually induces healing in the small intestine, and I place it somewhere else on a person's body, would it give a tissue-specific response, or would it make small intestine if I tried to make a new ear?
لم أكن لأخبركم بتلك القصة لو لم تكن مقنعة الصورة التي سأقوم بعرضها عليكم (ضحك) هي صورة مقنعة. ولكن بالنسبة لأؤلئك الذين يتحسسون من أقل الأشياء -- -بالرغم من أنك قد لا تحب الاعتراف بذلك أمام أصدقائك - الأضواء خافتة . هذا وقت جيد للنظر إلى قدميك قم بفحص البلاك بيري، ، قم بعمل أي شيء غير النظر إلى الشاشة (ضحك)
I wouldn't be telling you this story if it weren't compelling. The picture I'm about to show you is a compelling picture. (Laughter) However, for those of you that are even the slightest bit squeamish -- even though you may not like to admit it in front of your friends -- the lights are down. This is a good time to look at your feet, check your Blackberry, do anything other than look at the screen. (Laughter)
ما سأقوم بعرضه الآن هي صورة لقرحة السكر من السهل الضحك قبل أن ننظر إليها هذه هي حقيقة مرض السكر أفكر كثيرًا عندما نسمع عن مرضى السكر و قرح السكر نحن لا نقوم بالربط بين القرحة والعلاج النهائي لها وهو البتر إذا لم نستطع علاجها سأقوم بوضع الشريحة الآن. ولكن ذلك لن يدوم طويلًا هذه قرحة سكر. إنها صورة مأساوية. والعلاج لتلك القرحة هو البتر هذه سيدة مسنة وهي مصابة سرطان الكبد و السكر وقررت أن تموت بجسدها كاملًا
What I'm about to show you is a diabetic ulcer. And although -- it's good to laugh before we look at this. This is the reality of diabetes. I think a lot of times we hear about diabetics, diabetic ulcers, we just don't connect the ulcer with the eventual treatment, which is amputation, if you can't heal it. So I'm going to put the slide up now. It won't be up for long. This is a diabetic ulcer. It's tragic. The treatment for this is amputation. This is an older lady. She has cancer of the liver as well as diabetes, and has decided to die with what' s left of her body intact.
وقررت تلك السيدة بعد أن جربت علاج تلك القرحة لمدة عام أن تجرب هذا العلاج الجديد الذي اخترعه ستيف هكذا كان شكل الجرح بعد 11 أسبوع من العلاج تلك المادة تحتوي على إشارات كيميائية طبيعية وتلك المادة تحفز الجسد لتعود قدرته على معالجة تلك الجراح التي كان قد فقدها من قبل
And this lady decided, after a year of attempted treatment of that ulcer, that she would try this new therapy that Steve invented. That's what the wound looked like 11 weeks later. That material contained only natural signals. And that material induced the body to switch back on a healing response that it didn't have before.
سيكون هناك بعض من الصور المخيفة للذين يخافون من تلك الصور --سأخبركم متى تستطيعون النظر ثانيًا هذا حصان لا يتألم لو كان هذا الحصان يتألم، لم أكن لأريكم ذلك المقطع لدى الحصان فتحة أنف تماثلت للشفاء وذلك كان بسبب حادث ركوب بعد عدة أسابيع من العلاج في تلك الحالة فأخذ تلك المادة سيحولها إلى مادة جيلاتينية بمعالجة ذلك الجزء ثم تكرير العلاج تلك المرات و تم شفاء الحصان وإذا تم إكمال علاجه بالموجات فوق الصوتية فسيكون ذلك رائعًا
There's going to be a couple more distressing slides for those of you -- I'll let you know when you can look again. This is a horse. The horse is not in pain. If the horse was in pain, I wouldn't show you this slide. The horse just has another nostril that's developed because of a riding accident. Just a few weeks after treatment -- in this case, taking that material, turning it into a gel, and packing that area, and then repeating the treatment a few times -- and the horse heals up. And if you took an ultrasound of that area, it would look great.
هذه هي صورة دولفين تم تضميد زعنفته يوجد الآن حوالي 400 ألف مريض حول العالم استخدموا تلك المادة لعلاج جراحهم هل تستطيع إعادة توليد عضو؟ قامت وكالة مشاريع أبحاث الدفاع المتقدم (داربا) بإعطاء ستيف 15 مليون دولار ليكون مسئولًا عن مشروع مشترك بين ثمانية مؤسسات لتبدأ عملية طرح هذا السؤال
Here's a dolphin where the fin's been re-attached. There are now 400,000 patients around the world who have used that material to heal their wounds. Could you regenerate a limb? DARPA just gave Steve 15 million dollars to lead an eight-institution project to begin the process of asking that question.
وسأريكم الآن صورة ب 15 مليون دولار هذا الرجل الذي يبلغ من العمر 78 سنة والذي فقد نهاية عقلة إصبعه تذكروا ما قلته من قبل عن الأطفال الذين يفقدون عقلة أصابعهم وتلك هي صورته بعد العلاج وهذا يحدث اليوم وخلال فترة زمنية معقولة يوجد مواد تقوم بعلاج تلك الحالات.يوجد أيضًا ترقيعات للقلب
And I'll show you the 15 million dollar picture. This is a 78 year-old man who's lost the end of his fingertip. Remember that I mentioned before the children who lose their fingertips. After treatment that's what it looks like. This is happening today. This is clinically relevant today. There are materials that do this. Here are the heart patches.
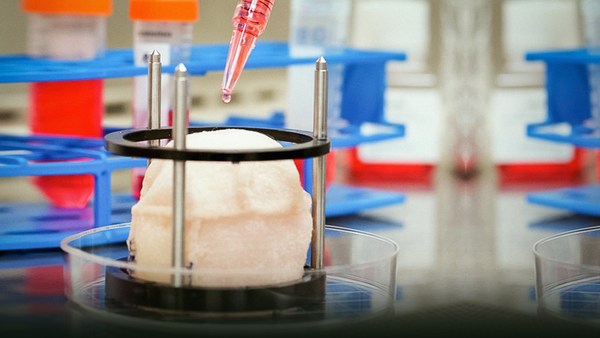
ولكن هل يمكن أن نفكر بشكل آخر بعض الشيء؟ هل تستطيع القول بدلًا من استخدام مادة هل أستطيع أن آخذ بعض الخلايا مع المادة وأزيل القطعة المتضررة من النسيج وأقوم بوضع مادة قابلة للتحلل الحيوي فيها؟ تستطيع أن ترى هنا الجزء من عضلة القلب يدق في طبق قام بفعل ذلك تورو أوكانو من مستشفى طوكيو للنساء فهو يستطيع حاليًا أن يزرع أنسجة نابضة في طبق ويقوم بتبريد الطبق فتتغير خصائص النسيج ثم يقشر هذا النسيج النابض من الطبق إنه الشيء الأكثر إمتاعًا
But could you go a little further? Could you, say, instead of using material, can I take some cells along with the material, and remove a damaged piece of tissue, put a bio-degradable material on there? You can see here a little bit of heart muscle beating in a dish. This was done by Teruo Okano at Tokyo Women's Hospital. He can actually grow beating tissue in a dish. He chills the dish, it changes its properties and he peels it right out of the dish. It's the coolest stuff.
والآن سأريكم التجديد الخلوي وما سأريه لكم هنا هي استئصال خلايا جذعية من مفصل ورك مريض وأكرر إذا كنت من الذين يخافون من تلك المظاهر ولا تريد المشاهدة فلا تنظر ولكن هذا النوع ممتع هذه عملية قلب مفتوح. مثل التي قام بها آل غور مع الفارق في هذه الحالة عند نهاية تلك العملية سوف ترون أن الخلايا الجذعية من المريض التي أزيلت في بداية العملية قد تم حقنها مباشرة في قلب المريض. ووقفت هنا لأريكم عند ذلك المشهد أن تلك التكنولوجيا لا تزال في بدايتها هنا يتم زرع الخلايا الجذعية مباشرة في قلب المريض النابض وإذا نظرتم بدقة شديدة فسوف تكون الخلايا حول تلك النقطة سوف ترون حاليًا تدفق ارتجاعي للخلايا حيث يتم لفظ الخلايا إلى الخارج مجددًا لذا فنحن نحتاج جميع أنواع التكنولوجيا الحديثة والأجهزة المتقدمة لزرع الخلايا في المكان الصحيح والوقت الصحيح
Now I'm going to show you cell-based regeneration. And what I'm going to show you here is stem cells being removed from the hip of a patient. Again, if you're squeamish, you don't want to watch. But this one's kind of cool. So this is a bypass operation, just like what Al Gore had, with a difference. In this case, at the end of the bypass operation, you're going to see the stem cells from the patient that were removed at the beginning of the procedure being injected directly into the heart of the patient. And I'm standing up here because at one point I'm going to show you just how early this technology is. Here go the stem cells, right into the beating heart of the patient. And if you look really carefully, it's going to be right around this point you'll actually see a back-flush. You see the cells coming back out. We need all sorts of new technology, new devices, to get the cells to the right place at the right time.
سأعطيكم بعض المعلومات القليلة هذه كانت تجربة عشوائية في ذلك الوقت قمنا بتجربة ذلك الدواء على 20 مريضًأ والآن نقوم بتجربته على حوالي 100 مريض ما أود قوله بشكل أساسي، إذا عالجت شخصًا مرضه شديد وقمت بعمل عملية قلب مفتوح سوف يتعافى قليلًا. وإذا أعطيتهم خلايا جذعية مع عملية القلب المفتوح لهؤلاء المرضى خاصة، زالت الأعراض. كان ذلك منذ عامين الأفضل هو أن تستطيع تشخيص المرض مبكرًا وأن تمنع بوادر المرض التي ستؤدي إلى تدهور الحالة الصحية
Just a little bit of data, a tiny bit of data. This was a randomized trial. At this time this was an N of 20. Now there's an N of about 100. Basically, if you take an extremely sick patient and you give them a bypass, they get a little bit better. If you give them stem cells as well as their bypass, for these particular patients, they became asymptomatic. These are now two years out. The coolest thing would be is if you could diagnose the disease early, and prevent the onset of the disease to a bad state.
هذه هي نفس الطريقة ولكن الآن بشكل محدود جراحيًا فعن طريق 3 ثقوب في الجسد موصلة إلى القلب ثم حقن الخلايا الجذعية بكل بساطة عن طريق المنظار هنا يتم زرع الخلايا ليس لدينا الوقت للتطرق إلى جميع التفاصيل ولكن المهم أنها طريقة جيدة نستطيع معالجة المرضى في الحالات الأقل مرضاً، وأن تجعلهم مرة أخرى بلا أعراض عن طريق هذا النوع من العلاج
This is the same procedure, but now done minimally invasively, with only three holes in the body where they're taking the heart and simply injecting stem cells through a laparoscopic procedure. There go the cells. We don't have time to go into all of those details, but basically, that works too. You can take patients who are less sick, and bring them back to an almost asymptomatic state through that kind of therapy.
هذا مثال آخر على العلاج بواسطة الخلايا الجذعية والذي لم يدخل عالم الطب إلى حد ما ولكني أعتقد أنه سيدخل عما قريب هذا من عمل كاسي مارا من جامعة بيتسبرج مع عدد من الزملاء حول العالم وقرروا أن شفط الدهون من الجسم والذي لدينا الكثير منه في الولايات المتحدة (ضحك) إنه مصدر كبير للخلايا الجذعية الكثير من الخلايا الجذعية موجود في شفط تلك الدهون تستطيع أن تقوم بعملية تجميلية لشد البطن وهنا يتم شفط الدهون وفي تلك الحالة ستكون الخلايا الجذعية معزولة وستتحول إلى أعصاب كل هذا يتم القيام به في المعمل وأعتقد أنه في القريب سوف ترى المرضى يعالجون بواسطة خلاياهم الجذعية المستخرجة من الدهون أو المستخرجة من الحيوانات
Here's another example of stem-cell therapy that isn't quite clinical yet, but I think very soon will be. This is the work of Kacey Marra from Pittsburgh, along with a number of colleagues around the world. They've decided that liposuction fluid, which -- in the United States, we have a lot of liposuction fluid. (Laughter) It's a great source of stem cells. Stem cells are packed in that liposuction fluid. So you could go in, you could get your tummy-tuck. Out comes the liposuction fluid, and in this case, the stem cells are isolated and turned into neurons. All done in the lab. And I think fairly soon, you will see patients being treated with their own fat-derived, or adipose-derived, stem cells.
تحدثت من قبل عن استخدام الأجهزة الذي من شأنه أن يغير الطريقة التي نعالج بها المرض بشكل كبير قبل أن أنتهي من الحوار هذه صورة مأساوية كسابقتها لدينا شراكة منذ فترة طويلة ومفجعة مع زملائنا في معهد الجيش الأمريكي لأبحاث الجراحة والذي عليه أن يعالج 11 ألف رجل عادوا من العراق بعض هؤلاء المرضى لديهم حروق شديدة الخطورة
I talked before about the use of devices to dramatically change the way we treat disease. Here's just one example before I close up. This is equally tragic. We have a very abiding and heartbreaking partnership with our colleagues at the Institute for Surgical Research in the US Army, who have to treat the now 11,000 kids that have come back from Iraq. Many of those patients are very severely burned.
ولو كان هناك شيء يجب أن تعلموه عن الحرق فهو أننا لا نعلم كيف نعالجه كل ما نقوم به لعلاج حالات الحرق هو عمل جراحة تجميلية حيث نقوم بعمل شيء ما هنا ثم نقوم بزرعه على مكان الجرح حتى يتم التئامهما في تلك الحالة ، تم تصميم مفاعل إحيائي حديث قابل للارتداء وسوف يتم اختباره طبيًا في وقت لاحق من هذا العام في ال ..بواسطة يورج جرلاك من جامعة بيتسبرج وذلك .....سوف يتم تصويبه إلى مكان الجرح وسوف يقوم المسدس الذي ترونه برش الخلايا حيث يقوم برش الخلايا على تلك المنطقة سيقوم المفاعل الإحيائي بتخصيب البيئة المحيطة بالخلايا وتوصيل أشياء أخرى في نفس الوقت ومن ثم نقوم بزرع تلك التربة الخصبة بدلًا من تلك الجراحة التجميلية إنها طريقة مختلفة تمامًا لمعالجة الجرح
And if there's anything that's been learned about burn, it's that we don't know how to treat it. Everything that is done to treat burn -- basically we do a sodding approach. We make something over here, and then we transplant it onto the site of the wound, and we try and get the two to take. In this case here, a new, wearable bio-reactor has been designed -- it should be tested clinically later this year at ISR -- by Joerg Gerlach in Pittsburgh. And that bio-reactor will lay down in the wound bed. The gun that you see there sprays cells. That's going to spray cells over that area. The reactor will serve to fertilize the environment, deliver other things as well at the same time, and therefore we will seed that lawn, as opposed to try the sodding approach. It's a completely different way of doing it.
انتهت ال 18 دقيقة المخصصة لي اسمحوا لي أن أنهي كلامي ببعض الأخبار الجيدة والقليل من الأخبار التي يمكن أن تكون السيئة الأخبار الجيدة هي أن ذلك العلاج يحدث اليوم إنه عمل رائع ذلك الذي عبرت عنه تلك الصور بشكل واضح ولكنه في غاية الصعوبة لأنه يحتاج إلى العديد من التخصصات بشكل كبير حتى يتم نجاحه كما أن كل مجال في الهندسة العلمية والممارسة الطبية يبذلون جهدهم من أجل أن يتحقق هذا النوع من العلاج
So my 18 minutes is up. So let me finish up with some good news, and maybe a little bit of bad news. The good news is that this is happening today. It's very powerful work. Clearly the images kind of get that across. It's incredibly difficult because it's highly inter-disciplinary. Almost every field of science engineering and clinical practice is involved in trying to get this to happen.
كما أن العديد من الحكومات والمناطق قد أقرت هذه الطريقة لعلاج الأمراض وكانت الحكومة اليابانية تقريبًا هي أول من قرر أن يستثمر أول 3 مليارات ثم 2 مليار في ذلك المجال أنها ليست مصادفة. فاليابان هي أكبر دولة على الأرض بالنسبة لمتوسط عمر الفرد وعليهم العمل بجد وإلا فسينهار النظام الصحي ولذا فهم يركزون على الاستثمار في هذا المجال وكذلك الاتحاد الأوروبي والصين وقد أنشأت الصين مركزًا قوميًا لهندسة النسيج البشري وكانت الميزانية لأول عام هي 250 مليون دولار أمريكي
A number of governments, and a number of regions, have recognized that this is a new way to treat disease. The Japanese government were perhaps the first, when they decided to invest first 3 billion, later another 2 billion in this field. It's no coincidence. Japan is the oldest country on earth in terms of its average age. They need this to work or their health system dies. So they're putting a lot of strategic investment focused in this area. The European Union, same thing. China, the same thing. China just launched a national tissue-engineering center. The first year budget was 250 million US dollars.
في الولايات المتحدة لدينا نظرة مختلفة إلى حد ما. نحن (ضحك) أن يأتي آل غور للعالم الحقيقي ويصبح رئيسا. لدينا نظرة مختلفة وتلك النظرة عبارة عن أن نمول الدراسات حتى تصبح في حيز الوجود ولكن لا يوجد استثمار استراتيجي لوضع كل الأشياء الضرورية معًا ليتم التركيز عليها بكل حرص.
In the United States we've had a somewhat different approach. (Laughter) Oh, for Al Gore to come and be in the real world as president. We've had a different approach. And the approach has basically been to just sort of fund things as they come along. But there's been no strategic investment to bring all of the necessary things to bear and focus them in a careful way.
وسأنهي كلامي بمقولة وهي إلى حد ما مقولة لا تتلاءم مع ما كنا نتحدث عنه أوجهها إلى مدير معاهد الصحة الوطنية وهو رجل جذاب إلى حد كبير ذهبت إليه مع جاي فاكنتي من جامعة هارفارد وعدد من مديري معهده لزيارته منذ عدة أشهر ولمحاولة إقناعه أننا نحتاج جزء صغير من ال27.5 مليار دولار الذي سيحصل عليها العام القادم وأخذ هذا الموضوع بطريقة استراتيجية للتأكد من أننا نستطيع تسريع وصول هذا العلاج للمرضى وفي نهاية تلك المقابلة المثيرة للأعصاب كان ما قاله المدير هو: رؤيتك أكبر بكثير من حاجتنا أحب أن أنهي بالقول أنه لن يغير رؤيتنا أحد ولكننا نستطيع مع بعضنا أن نغير نزعته. شكرًا لكم
And I'm going to finish up with a quote, maybe a little cheap shot, at the director of the NIH, who's a very charming man. Myself and Jay Vacanti from Harvard went to visit with him and a number of his directors of his institute just a few months ago, to try and convince him that it was time to take just a little piece of that 27.5 billion dollars that he's going to get next year and focus it, in a strategic way, to make sure we can accelerate the pace at which these things get to patients. And at the end of a very testy meeting, what the NIH director said was, "Your vision is larger than our appetite." I'd like to close by saying that no one's going to change our vision, but together we can change his appetite. Thank you.